Fuente: Hannah L. Cebull1, Arvin H. Soepriatna1, John J. Boyle2 y Craig J. Goergen1
1 Weldon School of Biomedical Engineering, Universidad Purdue, West Lafayette, Indiana
2 Ingeniería Mecánica y Ciencia de los Materiales, Universidad de Washington en St. Louis, St Louis, Missouri
El comportamiento mecánico de los tejidos blandos, como los vasos sanguíneos, la piel, los tendones y otros órganos, está fuertemente influenciado por su composición de elastina y colágeno, que proporcionan elasticidad y fuerza. La orientación de la fibra de estas proteínas depende del tipo de tejido blando y puede variar desde una sola dirección preferida hasta intrincadas redes malladas, que pueden alterarse en el tejido enfermo. Por lo tanto, los tejidos blandos a menudo se comportan anisotrópicamente a nivel celular y de órganos, creando una necesidad de caracterización tridimensional. Desarrollar un método para estimar de forma fiable los campos de deformación unitaria dentro de tejidos o estructuras biológicas complejas es importante para caracterizar y comprender mecánicamente la enfermedad. La tensión representa cómo el tejido blando se deforma relativamente con el tiempo, y se puede describir matemáticamente a través de varias estimaciones.
La adquisición de datos de imagen a lo largo del tiempo permite estimar la deformación y la tensión. Sin embargo, todas las modalidades de imágenes médicas contienen cierta cantidad de ruido, lo que aumenta la dificultad de estimar con precisión la tensión in vivo. La técnica descrita aquí supera con éxito estos problemas mediante el uso de un método de estimación de deformación directa (DDE) para calcular campos de deformación unitaria 3D que varían espacialmente a partir de datos de imagen volumétrica.
Los métodos actuales de estimación de deformación unitaria incluyen correlación de imágenes digitales (DIC) y correlación de volumen digital. Desafortunadamente, DIC sólo puede estimar con precisión la tensión de un plano 2D, limitando severamente la aplicación de este método. Si bien son útiles, los métodos 2D como DIC tienen dificultadpara cuantificar la tensión en regiones que se someten a deformación 3D. Esto se debe a que el movimiento fuera del plano crea errores de deformación. La correlación de volumen digital es un método más aplicable que divide los datos de volumen inicialen regiones y encuentra la región más similar del volumen deformado, lo que reduce el error fuera del plano. Sin embargo, este método demuestra ser sensible al ruido y requiere suposiciones sobre las propiedades mecánicas del material.
La técnica que se muestra aquí elimina estos problemas mediante el uso de un método DDE, por lo que es muy útil en el análisis de datos de imágenes médicas. Además, es robusta a cepa alta o localizada. Aquí describimos la adquisición de datos de ultrasonido 4D cerrados y volumétricos, su conversión en un formato analizable y el uso de un código Matlab personalizado para estimar la deformación 3D y las cepas de Green-Lagrange correspondientes, un parámetro que describe mejor las grandes deformaciones. El tensor de cepa Green-Lagrange se implementa en muchos métodos de estimación de deformación unitaria 3D porque permite calcular F a partir de un ajuste de mínimos cuadrados (LSF) de los desplazamientos. La ecuación siguiente representa el tensor de cepa Green-Lagrange, E, donde F y I representan el gradiente de deformación y el tensor de identidad de segundo orden, respectivamente.
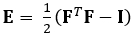 (1)
(1)
Biomedical Engineering
