Overview
Fuente: Laboratorio del Dr. Michael Evans, Georgia Institute of Technology
La constante de equilibrio, K, para un sistema químico es la relación de las concentraciones de producto de las concentraciones de reactivo en el equilibrio, cada una elevada a la potencia de sus respectivos coeficientes estequiométricos. Medición de K implica la determinación de estas concentraciones para los sistemas en equilibrio químico.
Sistemas de reacción que contienen un solo componente coloreado pueden ser estudiados mediante espectrofotometría. La relación entre absorbancia y concentración para el componente de color es medida y utilizada para determinar su concentración en el sistema de reacción de interés. Las concentraciones de los componentes incoloros pueden calcularse utilizando la ecuación química balanceada y la concentración medida de la componente de color.
En este video, curva de la ley de la cerveza para Fe(SCN)2 + es determinada empíricamente y aplicada a la medición de K para la reacción siguiente:
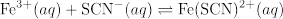
Cuatro sistemas de reacción con diferentes concentraciones iniciales de reactantes se investigan para ilustrar que K se mantiene constante independientemente de las concentraciones iniciales.
Principles
Cada reacción química está asociada con una constante de equilibrio K, que refleja la relación de las concentraciones de producto de las concentraciones de reactivo en el equilibrio químico. Para la reacción genérica una A + b B  c C + d D, la constante de equilibrio se define como
c C + d D, la constante de equilibrio se define como

donde las concentraciones en el lado derecho de la ecuación son molaridad en equilibrio. Esta ecuación se conoce como la expresión de equilibrio para la reacción. En sistemas químicos que no están en equilibrio, las reacciones de avance y retroceso ocurren a diferentes velocidades hasta las concentraciones de reactantes y productos satisfacen la expresión de equilibrio.
Para medir el valor de K para un sistema en equilibrio químico, es necesario determinar las concentraciones de reactivos y productos directa o indirectamente. Los métodos espectrofotométricos para la determinación de K implican la medición directa de la concentración de un componente de color y medición indirecta de los demás. Espectroscopía visible del componente coloreado en concentraciones conocidas revela a la relación entre absorbancia y concentración de este componente. Según la ley de Beer, esta relación tiene la forma

donde e es la absortividad molar del componente en mol/L-cm, l es la longitud del camino de la luz a través de la muestra en cm, c es la molaridad del componente en mol/L, y A es la absorbancia.
Curva de ley de la cerveza para el componente de color se puede aplicar a un sistema de reacción en equilibrio para determinar la concentración de este componente de las mediciones de absorbancia (figura 1). Entonces se pueden calcular las concentraciones de los reactantes y productos restantes ajustando las concentraciones iniciales basadas en la molaridad medido de las especies coloreadas.
El sistema estudiado aquí es la reacción del catión hierro (III) con anión tiocianato para formar un complejo de tiocianato de hierro (III).

La expresión de equilibrio para este sistema de reacción es

donde el subíndice eq denota las concentraciones de equilibrio. El producto de tiocianato de hierro (III) es de color naranja, pero ambos reactantes son incoloros en solución acuosa. Por lo tanto, [Fe(SCN)2 +]eq puede ser determinado directamente de las mediciones de absorbancia.

Las concentraciones de equilibrio de los reactivos pueden calcularse restando la concentración de equilibrio del producto de las concentraciones iniciales de los reactantes. Una tabla inicial cambio de equilibrio (ICE) ilustra cómo se relacionan las concentraciones inicial y equilibrio (tabla 1).

Repetidos ensayos de este experimento con diferentes concentraciones iniciales de reactantes deben producir el mismo valor de K, como el valor de K es independiente de la concentración.

Figura 1. Curva de ley de la cerveza para el tiocianato de hierro (III).
| Fe3 + | SCN– | Fe(SCN)2 + | |
| Inicial | [Fe3 +] me | [SCN–] me | 0 |
| Cambio | –[Fe(SCN)2 +]eq | –[Fe(SCN)2 +]eq | +[Fe(SCN)2 +]eq |
| Equilibrio | [Fe3 +] yo – [Fe(SCN)2 +]eq | [SCN–] yo – [Fe(SCN)2 +]eq | [Fe(SCN)2 +] EQ |
Tabla 1. Una tabla inicial cambio de equilibrio (hielo) que ilustra cómo se relacionan las concentraciones iniciales y de equilibrio.
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. determinar la curva de ley de la cerveza para Fe(SCN)2 +
- Calibrar un espectrofotómetro visible utilizando agua destilada como un blanco.
- Añadir 1,0 mL de 1,0 × 10-4 M Fe(NO3)3 solución a un tubo de ensayo.
- Al mismo tubo de ensayo, agregar 5,0 mL de solución de KSCN al de 0,50 M.
- Al mismo tubo de ensayo, añadir 4,0 mL de solución de 0,10 M HNO3 . Cubra el tubo con un dedo enguantado y agitar suavemente para mezclar.
- Utilice una pipeta Pasteur transferir una pequeña cantidad de la solución en una cubeta. Asegúrese de que el nivel de líquido está por encima de la trayectoria del haz luminoso en el espectrofotómetro.
- Coloque la cubeta en el espectrofotómetro, para que la luz pasa a través de los lados transparentes.
- Adquirir un espectro y registre el valormáximo de λ y la absorbancia a λmax.
- Para construir la curva de ley de la cerveza, otras soluciones con concentraciones conocidas de Fe(SCN)2 + deben ser preparadas y medidas. Repita los pasos 2 a 7 con los volúmenes de Fe (NO3)3, KSCN, al HNO3 soluciones y en la tabla 2.
- Represente la absorbancia medida versus las concentraciones de Fe(SCN)2 + en cada tubo de ensayo y determinar la línea de mejor ajuste para los datos. La pendiente de esta línea es la absortividad molar y la longitud del camino es 1 cm.
2. medición de K para el sistema de tiocianato de hierro (III)
- Preparar 4 tubos de ensayo medianos que contiene los volúmenes indicados de 0,0025 M Fe (NO3)3, 0.0025 M KSCN al y 0,10 M HNO3 soluciones en la tabla 3.
- Tapar cada tubo con un dedo y agitar suavemente para mezclar. Déjelo reposar durante al menos 10 minutos. Este descanso periodo asegura que las soluciones estén en equilibrio químico.
- Utilice una pipeta Pasteur transferir una pequeña cantidad de solución 6 a una cubeta. Asegúrese de que el nivel de líquido está por encima de la trayectoria del haz luminoso en el espectrofotómetro.
- Adquirir un espectro y registre el valormáximo de λ y la absorbancia a λmax.
- Reacciones múltiples con diferentes concentraciones iniciales de reactantes pueden ser estudiadas para ilustrar que K depende de la concentración. Para determinar K para diferentes condiciones iniciales, repita los pasos 3 y 4 para soluciones de 7 – 9.
| Número de tubo | Volumen 1.0 x 10-4 M de Fe (NO3)3 (mL) |
Volumen 0,50 M KSCN al (mL) |
Volumen 0,10 M HNO3 (mL) |
| 1 | 1.0 | 5.0 | 4.0 |
| 2 | 2.0 | 5.0 | 3.0 |
| 3 | 3.0 | 5.0 | 2.0 |
| 4 | 4.0 | 5.0 | 1.0 |
| 5 | 5.0 | 5.0 | 0.0 |
Tabla 2. Adecuados volúmenes de Fe (NO3)3KSCN al y HNO3 soluciones para ser colocados en tubos de 2-5.
| Número de tubo | Volumen 0,0025 M Fe (NO3)3 (mL) |
Volumen 0,0025 M KSCN al (mL) |
Volumen 0,10 M HNO3 (mL) |
| 6 | 1.0 | 1.0 | 5.0 |
| 7 | 1.0 | 2.0 | 4.0 |
| 8 | 2.0 | 2.0 | 3.0 |
| 9 | 2.0 | 3.0 | 2.0 |
Tabla 3. Volúmenes adecuados de 0,0025 M Fe (NO3)3, 0.0025 M KSCN al y 0,10 M HNO3 soluciones.
Determinar la constante de equilibrio de una reacción química puede proporcionar información importante acerca de la magnitud a la que se forman productos con el tiempo.
Cada reacción química está asociada con una constante de equilibrio, K, que refleja la relación de las concentraciones de los productos y reactivos, cuando la reacción ha dejado de progresar. Para medir K, estas concentraciones deben ser determinadas.
Si una reacción contiene un único componente coloreado, se puede medir su interacción con la luz para discernir su concentración. Las concentraciones de los componentes incoloros entonces se pueden calcular utilizando la ecuación química balanceada. Este video ilustra el uso de un espectrofotómetro para determinar empíricamente la constante de equilibrio para una reacción de thiocyanante de hierro.
Reacciones químicas más proceden en direcciones hacia adelante y reversas. Conforme avanza la reacción, llega a un punto donde se producen las reacciones hacia adelantadas y hacia atrás a la misma velocidad. Esto se conoce como equilibrio químico. En este estado estable, el cociente de las concentraciones de producto de las concentraciones del reactivo, cada una elevada a la potencia de sus coeficientes estequiométricos, corresponde a la constante de equilibrio, K. A medida K para un sistema de interés, los coeficientes deben conocerse, y deben determinarse las concentraciones, ya sea directa o indirectamente. Según la ley de Beer-Lambert, la concentración de una especie de color es proporcional a la absorbancia, que es la cantidad de energía que absorbe a una longitud de onda específica de luz. Esto puede expresarse matemáticamente, donde A es absorbancia, epsilon es el coeficiente de atenuación molar, que es específico del compuesto, l es la longitud del camino a través de la muestra y c es la concentración. Una curva de calibración se crea por múltiples soluciones de concentración conocida y trazar los valores de absorbancia obtenidos. Con esta curva de calibración, se pueden estudiar soluciones de concentración desconocida. Las mediciones de absorbancia se utilizan para determinar la concentración de las especies coloreadas. Entonces, se pueden calcular las concentraciones de los reactantes y productos restantes. El procedimiento siguiente estudiará la reacción de hierro tres con tiocianato para formar un complejo de tiocianato de hierro.
Una vez que las concentraciones han sido determinadas, el valor de K puede ser calculado con un inicial cambio de equilibrio, o con hielo, mesa que será explicado más lejos en los resultados.
Ahora que usted comprende cómo los métodos espectrofotométricos se pueden utilizar para determinar la constante de equilibrio, usted está listo para comenzar el procedimiento.
Antes de medir la muestra, se debe generar una curva de calibración.
Para comenzar, cero un espectrofotómetro de UV-vis utilizando agua destilada como blanco para no representar la absorbancia. Cuando se inserta una cubeta en el espectrofotómetro, asegurarse de que está orientada para que la luz pasa a través de los lados transparentes, y que el nivel de líquido está por encima de la trayectoria del haz.
Entonces, prepare 5 tubos de ensayo que contiene los volúmenes indicados de cada solución de reactivo, como se muestra en el protocolo del texto, que producirá concentraciones variables del producto. Cubrir cada tubo con un dedo enguantado y agitar suavemente para mezclar. Permita que los tubos reposar 10 min uso un Pasteur pipeta para transferir una pequeña cantidad de solución 1 en una cubeta y coloque en el espectrofotómetro. Adquirir un espectro y registrar el λmáximo y su absorbancia. Repita este proceso para soluciones de 2 a 5, usando una cubeta nueva para cada serie.
Represente la medida absorbancia versus concentración de tiocianato de hierro para cada solución. Determinar la línea de mejor ajuste para los datos. La pendiente de esta recta es el coeficiente de atenuación molar.
Ahora que se ha adquirido los datos para las soluciones estándar, prepare cuatro tubos de ensayo medianos que contiene los volúmenes indicados de soluciones como se indica en el protocolo de texto.
Tapar cada tubo con un dedo y agitar suavemente para mezclar. Déjelo reposar durante al menos 10 minutos. Este período de descanso permite que las soluciones alcanzar el equilibrio químico.
Utilice una pipeta Pasteur transferir una pequeña cantidad de solución 6 a una cubeta y coloque en el espectrofotómetro. Adquirir un espectro y registrar el valor λmáximo y la absorbancia medida en el λmáximo. Repita este proceso para soluciones de 7 – 9.
Una vez que todas las muestras han sido medidos, se pueden analizar los datos de molaridad y absorbancia para soluciones de 1 – 5. Un exceso de tiocianato se utilizó para asegurarse de que todo el hierro ha reaccionado, que simplifica el análisis.
Los datos se trazan para crear una curva de calibración. La longitud del camino de la luz, l, es típicamente 1 cm y puede tenerse fuera de los cálculos. La pendiente de la línea, que se calculó en 7600, es por lo tanto el coeficiente de atenuación. Las soluciones de ensayo 6 – 9, este valor y la absorbancia se utilizan para calcular las concentraciones de tiocianato de hierro en el equilibrio. Con estos datos, entonces podría utilizarse la tabla de hielo.
Las concentraciones de reactivo inicial se basan en la molaridad conocida de hierro y tiocianato añadido a la solución y el volumen total de la reacción. Porque el producto está formado por la reacción 1:1 de hierro y tiocianato, la concentración de equilibrio de cada uno disminuye en la cantidad de producto formado. Ahora se conoce la concentración de equilibrio de cada especie. Estos valores se utilizan para calcular la constante de equilibrio para cada solución. Los valores son más o menos constantes sobre el rango de concentraciones estudiado.
El concepto de la constante de equilibrio es importante para una amplia gama de campos científicos. La constante de equilibrio puede utilizarse para proporcionar información útil sobre la medida en que una reacción se forma productos con el tiempo. En este ejemplo, se observaron dos reacciones que contiene cristal violeta.
La primera solución fue compuesta de violeta cristal e hidróxido de sodio. El color fue observado para cambiar rápidamente de púrpura a incoloro. Esta reacción tiene un valor muy grande de K, que indica que los productos de forman casi totalmente con el tiempo.
Violeta cristal entonces fue reaccionada con acetato de sodio. Esta solución permanecía púrpura indefinidamente. Esta reacción tiene un valor muy bajo de K, por lo que no procede avanzar a un grado significativo.
Por último, la constante de disociación: un tipo específico de constante de equilibrio, puede ser utilizado para describir el comportamiento de la proteína. En este ejemplo, cambios en la estructura del ARN fueron supervisados en almacenadores intermediarios de la reacción de magnesio.
RNA purificado fue había mezclado en solución con concentraciones conocidas de magnesio y permite alcanzar el equilibrio. Entonces, la estructura resultante del RNA fue trazada.
En este caso, altas concentraciones de magnesio causaron sitios reactivos en ARN para protegerse menos, produciendo un Kd que era la mitad del valor.
Sólo ha visto la introducción de Zeus para determinación espectrofotométrica de la constante de equilibrio. Ahora debe comprender la relación definida por la ley de Beer-Lambert, cómo determinar la concentración de absorbancia con un espectrofotómetro y cómo calcular una constante de equilibrio con las concentraciones de equilibrio.
¡Gracias por ver!
Subscription Required. Please recommend JoVE to your librarian.
Results
La tabla 4 muestra los datos de absorbancia y concentración para soluciones de 1 – 5. Se determinaron las concentraciones de Fe(SCN)2 + de las concentraciones iniciales de Fe3 + bajo la suposición de que todo el Fe3 + se convierte en Fe(SCN)2 +. Un exceso de SCN– fue utilizado en los tubos 1 – 5 para asegurarse de que este supuesto es válido.
La molaridad [Fe(SCN)2 +] y la absorbancia se representan gráficamente en la figura 2. La absorbancia medida de acuerdo con ley de Beer.
Tabla 5 lista de absorbancia medido y calculado los valores de K para tubos de 6 – 9. Valores de K se determinan usando el método de tabla de hielo. Las concentraciones de los reactivo iniciales se basaron en la molaridad conocida de Fe3 + y SCN– en las soluciones de reactivo y el volumen total de la reacción (10 mL). La concentración de equilibrio de Fe(SCN)2 + fue determinada por absorbancia medida divisoria por la absorbencia molar de Fe(SCN)2 +. Porque todo el producto fue formado de la reacción 1:1 de Fe3 + y SCN–, la concentración de equilibrio de Fe(SCN)2 + corresponde a la disminución en la concentración de los reactantes. Tabla 6 muestra el proceso para tubo de ensayo 6.
Se calcula la constante de equilibrio de las concentraciones en la fila de equilibrio. Para tubo de ensayo 6,

La media el valor de K fue de 147 ± 11, ilustrando que K es aproximadamente constante sobre el rango de concentraciones estudiado.

Figura 2. Línea gráfico de absorbancia versus concentración para Fe(SCN)2 +.
| Tubo | [Fe(SCN)2 +] (mol/L) | Absorbancia |
| 1 | 1.00 x 10-5 | 0.10 |
| 2 | 2.00 x 10-5 | 0.20 |
| 3 | 3.00 x 10-5 | 0.25 |
| 4 | 4.00 x 10-5 | 0.32 |
| 5 | 5,00 x 10-5 | 0.42 |
Tabla 4. Absorbancia versus concentración de datos de Fe(SCN)2 +.
| Tubo | Absorbancia | K |
| 6 | 0.120 | 136 |
| 7 | 0.268 | 161 |
| 8 | 0.461 | 142 |
| 9 | 0.695 | 150 |
Tabla 5. Mide absorbancia y calculado K para la reacción de hierro (III) con tiocianato.
| [Fe3 +] (mol/L) | [SCN–] (mol/L) | [Fe(SCN)2 +] (mol/L) | |
| Inicial | 3.57 x 10– 4 | 3.57 x 10– 4 | 0 |
| Cambio | –1.58 x 10-5 | –1.58 x 10-5 | +1.58 x 10-5 |
| Equilibrio | 3.41 x 10– 4 | 3.41 x 10– 4 | 1,58 x 10-5 |
Tabla 6. La tabla de hielo que ilustra el proceso utilizado para tubo de ensayo 6.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
La constante de equilibrio proporciona información útil sobre la medida en que una reacción procederá a productos de forma con el tiempo. Reacciones con un valor grande de K, mucho más grande que 1, forman productos casi completa de tiempo (figura 3). Reacciones con un valor de K menor que 1 no procederá hacia adelante a un grado significativo. La constante de equilibrio por lo tanto sirve como una medida de la viabilidad de una reacción química.

Figura 3. La constante de equilibrio de esta reacción es mayor que 1. Una cantidad importante de producto coloreado se forma en cada caso, aun cuando las concentraciones iniciales de reactantes difieren.
La constante de equilibrio también proporciona información termodinámica útil acerca de los cambios en energía libre, entalpía y entropía en el curso de una reacción química. La constante de equilibrio se relaciona con el cambio de energía libre de reacción:

El cambio de energía libre de reacción a su vez se relaciona con los cambios de entalpía y entropía de la reacción:

Medidas de la dependencia de la temperatura de K pueden revelar que el Δ de cambio de la entalpiaH y la entropía cambian ΔS para una reacción. Además de proveer químicos con conocimiento en patrones de comportamiento molecular, tablas de datos termodinámicos pueden utilizarse para identificar reacciones con propiedades termodinámicas favorables. Por ejemplo, las reacciones redox que liberan grandes cantidades de energía (asociado con los valores deG Δ negativos) son candidatos atractivos para las baterías.
Valores de K para las reacciones de disociación del ácido(Kpor valores) son útiles para predecir los resultados de las reacciones ácido-base, que termodinámicamente son controlados. Ácidos fuertes se asocian con grandes Kun valores y débil ácidos con Ka valores pequeño. indicadores de pH son ácidos débiles con diferente colores formas ácidas y básicas, y el pKuna (el logaritmo negativo de base 10 de Kun) de un indicador que representa el pH en el cual se produce un cambio de color como un ácido o base se agrega a una solución del indicador.
Del mismo modo, Kun valores se utilizan en la preparación de soluciones tampón para lograr un valor del pH objetivo. La pKuna de un ácido débil representa el pH en el cual el ácido y su base conjugado están presentes en la solución en concentraciones iguales. Cuando igual cantidad de un ácido débil y su base conjugada son disueltos en una solución, el pH de la solución es igual a la pK del ácido débil.
Subscription Required. Please recommend JoVE to your librarian.




