Overview
Fuente: Laboratorio de Jeff Salacup - Universidad de Massachusetts Amherst
El producto de una extracción con disolvente orgánico, un extracto total de lípidos (TLE), es a menudo una mezcla compleja de cientos, si no miles, de diferentes compuestos. El investigador a menudo sólo está interesado en un puñado de compuestos o, si está interesado en muchos, puede necesitar eliminar a componentes no deseados que se encuentran "en el camino" o co liberador. Por ejemplo, las concentraciones de compuestos individuales en una muestra se determinan a menudo en un cromatógrafo de gases acoplado a un detector de ionización de llama (GC-FID), porque la relación entre la respuesta de la FID (en pA) y la cantidad de compuesto en una muestra (p. ej., ng/μL) es lineal y sensible. La porción de GC del instrumento separa diferentes compuestos en una muestra basada en su punto de ebullición, estructura química y afinidad con una fase sólida que puede cambiar según la aplicación. El resultado es un cromatograma (Figure 1), mostrando la separación de componentes químicos diferentes en tiempo, así como su concentración relativa (calculado como el área bajo la curva). Sin embargo, a veces más de uno compuesto elutes de la GC en un tiempo (Figure 1). En este caso, purificación de las muestras es necesario antes de compuestos pueden ser cuantificados con confianza.
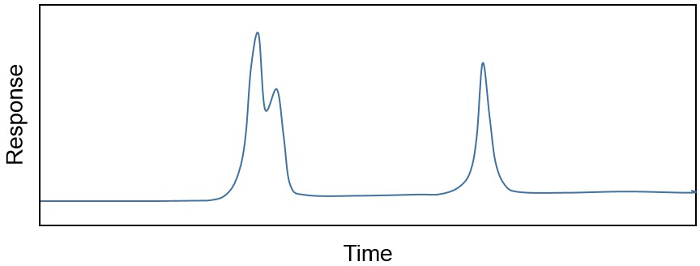
Figura 1. Un cromatograma que muestra la separación de componentes químicos diferentes en el tiempo y su concentración relativa (área bajo la curva). Se muestran picos de co liberador y separados.
Principles
Famas (ésteres metílicos de ácidos grasos) son importantes componentes de los microbios marinos y terrestres y son de uso frecuente, conjuntamente con técnicas genéticas, para describir la diversidad microbiana del ecosistema en sistemas modernos y antiguos. Sin embargo, la presencia de famas en una muestra no siempre es útil. Debido a su tamaño y química similar, FAMAS llamados alkenonatescommonly Co fin de eluir con cetonas de alquilo de cadena larga, llamadas alkenones (figura 2). La distribución de alkenones en una muestra relaciona información sobre temperatura superficial del mar en el tiempo y el lugar fue tomada la muestra, y así su caracterización exacta y precisa es importante.
Saponificación es una técnica de purificación común utilizada para convertir famas en ácidos grasos, cambiando así sus características químicas lo suficiente para eliminarlos de la elución con alkenones (figura 3). Saponificationis una forma de hidrólisis. En hidrólisis, el agua se utiliza para dividir moléculas. Saponificación es una hidrólisis que se acelera en presencia de una base como hidróxido de potasio (KOH). KOH se disuelve en K+ y OH– en el agua. El anión hidróxido (OH-, ion con carga negativa) se agrega al átomo de carbón terciario un poco, positivamente cargado en el corazón de la fama (figura 3, arriba). Sin embargo, esta configuración química es inestable, (carbono se enlaza a muchos otros átomos) y el alcóxido (ROH–) es expulsado. Pero el H del conjugado base esta forma de expulsión rápidamente se traslada al alcóxido para formar el alcohol metanol y sal de potasio de ácidos grasos (figura 3, medio). En este punto, el ofender la fama (alkenoate) ha sido transformada en un producto químico que ya no elutes conjuntamente con él. Sin embargo, si se desea también analizar la química de la fama, ellos pueden ser reclamados por la adición de ácido (HCl) a la solución, hasta que llegue a pH ~ 2. A este pH, la sal de potasio del ácido graso se divide para formar un ácido carboxílico y una sal iónica (KCl; En la figura 3, abajo).

Figura 2 . Las estructuras químicas de un Alkenone con 37 átomos de carbono y 2 enlaces dobles (parte superior) y sus asociados alkenoate Fama (parte inferior).

Figura 3 . Un esquema de la saponificación del ácido palmítico con hidróxido de potasio (KOH) para aumentar la tasa de hidrólisis (http://www.mpbio.com/).
Saponificación es una técnica comúnmente utilizada para eliminar ésteres metílicos de ácidos grasos de una mezcla orgánica compleja.
Muestras orgánicas complejas son a menudo analizadas por cromatografía de gases, que se utiliza para determinar las concentraciones relativas de componentes individuales.
Sin embargo, los compuestos que son similares en tamaño y estructura no se pueden distinguir por el instrumento, sesgando los resultados. Por lo tanto, los compuestos no deseados que producen señales superpuestas deben eliminarse para obtener resultados precisos.
Este video explica el uso de saponificación para purificar alkenones de paleoclimatología. Es la primera de una serie de detalles de la purificación de las muestras complejas biomarcadores. Cubrirá el procedimiento, así como algunos otros usos de la técnica.
Cetonas de alquilo de cadena larga poliinsaturados, llamadas alkenones, han demostrado para proporcionar información útil sobre temperatura superficial del mar pasado.
Sin embargo, los organismos que producen alkenones a menudo crean ácidos grasos ésteres de metilo que son similares en tamaño y estructura química, llamado alkenoates. Debido a estas similitudes, alkenoates deben eliminarse antes de que se puede obtener un análisis preciso.
Saponificación es una técnica común utilizada para evitar la elución de estas moléculas. Saponificación utiliza agua para dividir el enlace molecular de un éster. Una base se une al carbono en el corazón de la alkenoate. Esta reacción de adición crea un intermediario inestable y el alcóxido es expulsado.
El hidrógeno a partir de los movimientos ácidos recién formados el alcóxido expulsado, y el anión carboxilato resultante forma un enlace iónico con el catión de la base. El resultado es un alcohol y una sal de ácido graso. Adición de un ácido fuerte se vuelva a generar el ácido carboxílico. En este punto, el alkenoate que se ha convertido a una forma que ya no elutes conjuntamente con la alkenone de interés.
Ahora que usted entiende cómo la saponificación se puede utilizar para purificar una mezcla orgánica, estás listo para comenzar el procedimiento.
En primer lugar, adquirir un extracto seco total de lípidos - o TLE - que fue obtenida usando un método de extracción por solvente. A continuación, preparar las soluciones de saponificación como se indica en el protocolo de texto. Asegúrese de que todos los componentes son puros y libres de hidrocarburos. Una vez que están preparadas las soluciones, añadir el TLE seco a un frasco de vidrio de borosilicato de 60 mL. Añadir 2 mL de hidróxido de potasio normal 2 y sellar el frasco. A continuación, calentar el frasco a 60 ° C durante 2,5 h hender el enlace de éster. Cuando esto termine, deje que la muestra se enfríe a temperatura ambiente. Una vez enfriada la muestra, agregar 2 mL de solución al 5% cloruro de sodio al frasco. Tapa el frasco y agitar brevemente. Añadir gota a gota ácido de clorhídrico 6 N hasta alcanzar un pH de 2 - utilizando papel de pH para probar. La adición de este ácido serán protonate el anión de carboxilato para formar el producto final - el ácido carboxílico estable.
Ahora que la solución acidificada es libre de ester, añadir 5 mL de hexano. La tapa y agitar vigorosamente por 5 segundos extraer los compuestos orgánicos del agua. Deje que la solución a descansar hasta las fases orgánicas y acuosas separan completamente. Sales, iones y ácido clorhídrico permanecerá en la fase acuosa, mientras que los compuestos orgánicos se separan en el hexano. Cuando las fases se han separado completamente, quite aproximadamente el 75% de hexano con una pipeta y dispensar en otro frasco de 40 mL. Repita este proceso de extracción adicional de dos horas, añadir 5 mL de hexano cada vez. Una vez este finalizado, deseche la solución acuosa sobrante en un recipiente de desechos adecuado. Etiqueta el frasco que contenía la fase orgánica recién saponificada. Los ácidos carboxílicos producidos no se inyecta en los instrumentos utilizados para el análisis de alkenone sin una posterior purificación. Ácidos carboxílicos inyectados en un cromatógrafo de gases rápidamente se acumulan y arruinar las entradas, trazadores de líneas de entrada y la parte delantera de las columnas. Para eliminar estos ácidos, la muestra debe primero someterse a una técnica de purificación: separación mediante cromatografía en columna.
Saponificación tiene varias aplicaciones en la extracción y purificación de moléculas orgánicas.
Saponificación puede utilizarse no sólo para separar biomarcadores, sino también para extraer los componentes individuales para el uso en productos comerciales. En este ejemplo, compuestos del árbol del tabaco - Nicotiana glauca - fueron aislados y analizados para investigar su potencial como materia prima para una gran variedad de productos de base biológica, como combustible, calor y una gran variedad de compuestos químicos.
Las hojas fueron homogeneizadas primero centrifugadas, para concentrar las moléculas de interés. El material vegetal concentrado entonces fue saponificado. El material extraído se analizó con líquido cromatografía de espectrometría de masas, para determinar la concentración de tocoferol - una familia de compuestos de vitamina E se encuentra típicamente en las plantas.
El material extraído también puede ser reconstituido en vitro a su composición original. En este ejemplo, la saponificación se utilizó para extraer carotenoides de las plantas de espinaca, para más tarde ser reconstituido en vitro. La espinaca fue homogeneizada primero centrifugada, para cosechar las moléculas de pigmento. Estas moléculas entonces fueron suspendidas en una solución de hidróxido de potasio en un matraz, iniciar la saponificación. Los carotenoides saponificados separan en una capa de éter, que fue recopilada y secada. Utilizando una serie de solución buffers, los carotenoides y otras moléculas de pigmentación - eran más adelante reconstituida in vitro. Esta purificación permitida para el análisis de estos pigmentos sin la interferencia de compuestos orgánicos semejantemente estructurados.
Debido a su capacidad de hidrolizar ésteres, saponificación puede utilizarse para "libre" de compuestos que de lo contrario van a macromoléculas. En este ejemplo, un paso de saponificación anhidro se utiliza para convertir etilo 4-fluorobenzoate a la sal de ácido carboxílico de potassium4-fluorobenzoate. Esta desprotección mediante saponificación permite la producción de crudo SFB - una reacción que no sería posible la molécula permaneció "pegados".
Sólo ha visto la introducción de Zeus a la purificación de Uk'37 muestras mediante saponificación. Ahora debe entender cómo funciona la saponificación y cómo usarlo para purificar alkenones en un extracto total de lípidos. Otros procesos de purificación serán demostrados en videos posteriores.
¡Gracias por ver!
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. configuración y preparación de materiales
- Obtener un total de lípidos extracto (TLE) utilizando un método de extracción por solvente (sonicación, Soxhlet o extracción acelerada de disolvente (ASE)).
- Preparar una solución de KOH 2 N 5% H2O metanol.
- KOH y metanol pueden adquirirse en tiendas de productos químicos. Estos productos químicos deben ser puro y libre de hidrocarburos.
- La masa molar de KOH es 56 uma produciendo 1 mol de OH– por cada mol de KOH. Por lo tanto, para lograr una concentración de N 2, disolver 112 g de KOH en 0,95 L de agua pura y 0,05 L de metanol.
- Tenga en cuenta que la disolución de KOH en agua es exotérmica y genera una gran cantidad de calor. Tenga cuidado de agregar a los pellets KOH en el agua lentamente para evitar una reacción violenta.
- Se disuelven 112 g de pellets KOH en 0,95 litros de agua pura en una placa de agitación automática.
- Añadir 0,05 L de metanol una vez todo el KOH se disuelve para ayudar en la disolución de los biomarcadores orgánicos en la solución acuosa.
- KOH y metanol pueden adquirirse en tiendas de productos químicos. Estos productos químicos deben ser puro y libre de hidrocarburos.
- Preparar una solución de ácido de clorhídrico 6 N (HCl) en H2O.
- Ácido clorhídrico puede adquirirse en tiendas de productos químicos. Este producto químico debe ser puro y libre de hidrocarburos.
- Viene generalmente ácido clorhídrico concentrado como 13 N. Así, una mezcla 1:1 de HCl y agua pura produce una mezcla de N 6.5 de HCl, que es cerca de 6 N para los propósitos de este experimento.
- Asegúrese de agregar el ácido clorhídrico al agua y no al revés, como añadir agua al ácido clorhídrico concentrado es exotérmico y genera calor. Esto puede causar ácido clorhídrico para chapotear.
- Suavemente y lentamente vierta 100 mL de ácido clorhídrico en un vaso de precipitados con 100 mL agua pura, la mezcla entre las adiciones de ácido clorhídrico se arremolinan.
- Preparar una solución de 5% NaCl (sal de mesa) en H2O.
- NaCl se puede comprar en tiendas de productos químicos. Este producto químico debe ser puro y libre de hidrocarburos.
- Calcular y pesar la masa de sal para hacer ~ 1 L de solución al 5% (w/w). 1 L de agua pesa ~ 1 kg o 1.000 g. Así, 50 g de NaCl disuelto en 950 mL da una solución al 5% (50 g + 950 g = 1.000 g, 1.000 g/50 g = 0.05 o 5%).
- Añadir 50 g de NaCl en agua pura en una placa de agitación automática y esperar a que se disuelva.
- Obtener los siguientes materiales: 2 limpio y quemado (550 ° c por 6 h) viales de vidrio borosilicato de 40 mL con tapa forrada de PTFE; un horno de calentamiento o calentamiento bloques; pipetas de vidrio de borosilicato de combustión (550 ° c por 6 h) y bulbos; cinta de pH (rango ácido); Hexano (hexano puede adquirirse en tiendas de productos químicos. Este producto químico debe Optima grado o equivalente).
2. métodos
- Comience con el TLE seco (que contienen ésteres) en uno de los viales de borosilicato vidrio 40 mL.
- Añadir aproximadamente 10 mL de KOH N 2 a la TLE y la tapa.
- Calentar en el horno o en un bloque de calentamiento a 60 ° c por 2,5 h para hender el enlace éster (figura 3).
- Retirar la muestra del fuego y deje que se enfríe a temperatura ambiente.
- Añadir aproximadamente 10 mL de la solución de NaCl al 5% a la TLE (figura 3). Esto ayuda a mantener la interfase entre la fase acuosa y orgánica (a) de formación de espuma. La tapa y agítela brevemente.
- Añadir 6 N HCl a la TLE salada gota a gota hasta alcanzar pH 2 al protonate O– y formar el producto final, un ácido carboxílico estable (figura 3; uso papel de pH para probar). Si el TLE fue coloreado, puede haber un cambio de color coincidiendo con pH 2.
- Añadir aproximadamente 20 mL de hexano a la solución acidificada, que es ahora libre de ester. La tapa y agitar vigorosamente durante 5 s para extraer compuestos orgánicos del agua.
- Permite establecer hasta las fases acuosas y orgánicas completamente separada. Sales, iones, agua y HCl permanecen en la fase acuosa. Los compuestos orgánicos son ahora en el hexano.
- Eliminar aproximadamente el 75% del hexano sobrenadante con una pipeta y dispensar en el otro frasco de vidrio de borosilicato de 40 mL.
- Repetición de 2.7-2.9 dos veces, agregar aproximadamente 10 mL de hexano cada vez.
- Deseche la mezcla acuosa sobrante en un recipiente de residuos adecuado.
- Etiqueta el frasco que contiene hexane y materia orgánica libre de ester «TLE - saponificado.»
Subscription Required. Please recommend JoVE to your librarian.
Results
Esta purificación produce un ELT de ésteres que pueden ser co liberador con el alkenones. Sin embargo, la purificación produce ácidos carboxílicos, que no puede ser inyectados en instrumentos comúnmente utilizados para analizar las muestras para las concentraciones de alkenone debido a su baja volatilidad. Por ejemplo, el punto de ebullición del hexano, un hidrocarburo de 6 carbonos, es 68 ° c, pero el punto de ebullición de su ácido hexanoico es 205 ° c. Más marcadores biológicos susceptibles de GC tienen de 20 a 35 átomos de carbono (punto de ebullición aumenta generalmente con un número creciente de átomos), y programas de temperatura GC mayoría parada alrededor de 300 ° c. Ácidos carboxílicos inyectados rápidamente un GC se acumulan y arruinar las entradas, trazadores de líneas de entrada y la parte delantera de las columnas. Para eliminar estos ácidos, la muestra debe primero someterse a otra separación técnica de purificación mediante cromatografía en columna.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Como se mencionó anteriormente, saponificación se utiliza comúnmente en los laboratorios de geoquímica orgánica para eliminar ésteres metílicos del ácido graso (famas) de alkenones, llamado alkenoates, que co fin de eluir con alkenones en Cromatógrafos de gases (Figure 1). Saponificación se utiliza también para ácidos grasos "libres" "obligados" a los sedimentos o macromoléculas. La degradación y la preservación de materia orgánica en los sedimentos y consiste en la remoción de grupos funcionales (N, O y S) y la polimerización final de biomarcadores individuales en macromoléculas o la adsorción de macromoléculas en superficies minerales y. Biomarcadores no todos en un límite de ajuste que se convierten y la relación entre biomarcadores bound gratis pueden cambiar al ajuste y la edad de sedimentos por razones aún no totalmente explicado. Saponificación, a veces a temperaturas superiores a los aquí expuestos (> 200 ° c), se utiliza para liberar a estos biomarcadores consolidados en el esfuerzo para describir a ellos, su origen y los mecanismos responsables de su naturaleza consolidado.
Subscription Required. Please recommend JoVE to your librarian.




