Overview
Source : Laboratoires du Dr Ian poivre et Dr Charles Gerba - Université de l’Arizona
Démonstration d’auteur : Alex Wassimi
Les virus sont un groupe unique d’entités biologiques qui infectent les organismes tant procaryotes et eucaryotes. Ils sont des parasites qui n’ont aucune capacité métabolique et afin de reproduire, s’appuient sur le métabolisme de l’hôte pour produire des pièces virales qui s’assemblent à l’intérieur des cellules de l’hôte.
Les virus sont ultramicroscopiques — trop petit pour être vu au microscope photonique, visible seulement avec la plus grande résolution du microscope électronique. Une particule virale se compose d’un génome d’acide nucléique, ADN ou ARN, entouré d’un manteau de protéine, appelé une capside, composée de sous-unités protéiques ou capsomères. Dans certains virus plus complexes, la capside est entourée d’une enveloppe lipidique supplémentaires, et certains ont des appendices surfaces spike ou queues.
Les virus qui infectent le tractus intestinal des animaux et les humains sont connus comme des virus entériques. Ils sont excrétés dans les selles et peuvent être isolés des eaux usées domestiques. Les virus qui infectent les bactéries sont appelés bactériophages, et ceux qui infectent les bactéries coliformes sont appelés les coliphages (Figure 1). Les phages de bactéries coliformes sont trouvent n’importe où sont trouvent les bactéries coliformes.
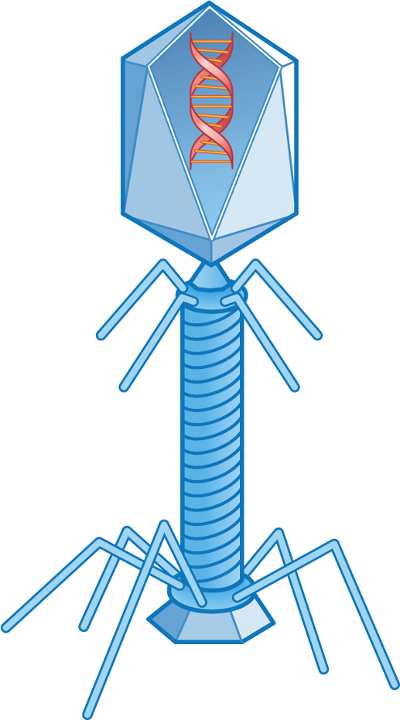
La figure 1. Coliphages T2.
Principles
Les bactériophages sont étudiés en sciences de l’environnement parce qu’ils sont un élément essentiel des systèmes biologiques. Ils sont l’entité biologique plus abondante sur terre et sont importants car ils aident à maîtriser les populations bactériennes, les processus trophique, les cycles biogéochimiques, ainsi que renforcer la diversité procaryote par transfert horizontal de gènes. Il semble également que les phages sont des indicateurs de substitution fiable pour virus entériques pathogènes qui sont aussi matières fécales-transmis mais difficile à doser. La disponibilité des méthodes relativement rapides et peu coûteuses pour énumérer les bactériophages rend un outil intéressant pour l’évaluation de la contamination fécale dans les échantillons environnementaux.
Coliphages dans l’eau sont dosés par addition d’un échantillon à molle ou une gélose de recouvrement ainsi qu’une culture d’Escherichia coli dans la phase logarithmique de croissance. Le phage attachent à la cellule bactérienne et lyse des bactéries. Les bactéries produisent une pelouse confluente de la croissance, à l’exception des zones où le phage a grandi et lysent les bactéries. Ces zones claires qui en résultent sont connues sous forme de plaques. Une superposition de gélose molle est utilisée pour limiter la diffusion physique des virus afin que, lors de la lyse d’une bactérie, elles peuvent se propager seulement voisines des cellules bactériennes.
Pour obtenir la formation de plaques optimale, il est important que la bactérie hôte est en phase de croissance journal. Ceci garantit que tous les phages attacher pour vivre des bactéries et produire la progéniture. Cela exige qu’une culture de la bactérie hôte prête chaque jour qu’un test est effectué. Habituellement, une culture est incubée le jour avant le dosage, afin qu’il soit dans la phase stationnaire. Le jour du test, la culture sert à ensemencer un bouillon, qui est incubé à obtenir assez bactéries dans la phase de log pour le dosage (cela nécessite généralement 2-3 h d’incubation dans un bain d’eau secouer à 35-37 ° C).
Subscription Required. Please recommend JoVE to your librarian.
Procedure
- Obtenir un échantillon d’eaux usées ou de l’eau contenant les coliphages.
- Diluer l’échantillon 01:10 et 1/100 à l’aide d’un tampon Tris. Ce faire transférer 1,0 mL de la culture dans 9 mL de tampon Tris et puis faire une deuxième facteur 10 dilution.
- Faire fondre les trois tubes de gélose molle (0,7 % Gélose nutritive ou gélose trypticase-soja par tube de 3 mL) en les plaçant dans un bain de vapeur ou autoclave.
- Placer l’agar dans un bain d’eau à 45-48 ° C pendant 15 minutes pour permettre à la température de l’agar pour s’adapter à 45 ° C.
- Dans le premier tube, ajouter 1 mL d’un bouillon de culture phase de journal d’e. coli1 et 1 mL d’échantillon non dilué.
- Retirer le tube du bain-marie et doucement rock entre les mains de mélanger la suspension pendant 2-3 s.
- L’eau du tube avec une serviette en papier avec un chiffon et versez l’agar sur une boîte de Pétri préalablement préparée contenant des géloses de fond (Gélose nutritive ordinaire ou gélose trypticase-soja).
- Rapidement, faire pivoter la plaque pour répandre l’agar en haut de la page. Veillez à ce que l’agar couvre toute la surface.
- Répétez les étapes 5 à 8 avec les deux autres tubes de gélose molle, en utilisant 1 mL de bactéries et 1 mL de chaque dilution de l’échantillon (Figure 2).
- Après que l’agar a solidifié, inverser les boîtes de Pétri et incuber à 37 ° C pendant 48 h. frapper toute trace d’humidité sur le couvercle de la boîte de Pétri. Si une goutte d’eau tombe sur une plaque, il causera le virus de se propager sur toute la surface de la gélose.
- Après l’incubation, compter le nombre de plaques sur chaque dilution (Figure 3) et calculer la concentration du bactériophage dans l’échantillon original. Enregistrer des différences majeures dans la taille ou l’apparence des plaques.

La figure 2. Procédure pour la préparation d’une pelouse bactérienne utilisant agar supérieur pour le dénombrement de coliphages.

La figure 3. Plaques de phage sur une pelouse bactérienne.
1 La souche e. coli ATCC 15597 généralement produira le plus grand nombre de plaques d’échantillons d’eaux usées. Il doit être cultivé pendant la nuit dans un erlenmeyer de 250 mL contenant 100 mL de nutriment ou trypticase soja bouillon et couvés sous agitation conditions à 35 ° C. 3 h avant le dosage du phage ensemencer un mL de cette culture dans un douce flacon contenant 100 mL de bouillon de soja nutriment ou trypticase et le placer dans un bain d’eau secouer à 35-37 ° C. Cela garantira que les bactéries sont dans la phase logarithmique de croissance.
Les virus sont des particules biologiques infectieux qui sont responsables de beaucoup de maladies, de froid et de grippe, l’hépatite et le VIH.
Les virus sont des particules biologiques consistant en un ADN ou ARN génome, enveloppé dans un manteau de protéine appelé une capside, parfois doté d’une enveloppe lipidique supplémentaire. Virus n’ont aucune capacité métabolique ou reproductive sur leurs propres et doivent envahir les cellules vivantes et détourner leur machinerie cellulaire afin de rendre plus de copies d’eux-mêmes.
Fois, comme les bactéries, les cellules procaryotes et cellules eucaryotes, comme celles des humains, peuvent être infectées par des classes spécifiques du virus. Plus précisément, les bactériophages sont les virus qui infectent les bactéries. Par exemple, les coliphages sont ces phages infectant Escherichia coli, une bactérie intestinale commune, certaines souches qui peuvent causer un empoisonnement alimentaire, et qui est une indication de contamination fécale de l’eau.
Tandis que les phages eux-mêmes ne sont pas généralement connues pour être pathogènes chez l’homme, il y a des preuves qu’ils sont des indicateurs fiables de substitution pour les pathogènes entérovirus aussi matières fécales-transmis mais difficile à doser. La disponibilité des méthodes relativement rapides et peu coûteuses pour énumérer les bactériophages rend un outil intéressant pour l’évaluation de la contamination fécale dans les échantillons environnementaux.
Cette vidéo mettra en place les principes qui sous-tendent l’énumération phage ; démontrer un protocole de quantification des phages, connus comme le test de la plaque ; et enfin, explorer plusieurs applications de la science de l’environnement pour la détection et le comptage des phages et autres virus.
Bactériophages, comme tous les virus, doivent parasiter les cellules vivantes, dans ce cas les bactéries, afin de reproduire.
Phages faire atterrir et fixation à la surface de la cellule bactérienne et injecter leur matériel génétique dans la cellule. Une fois à l’intérieur de la cellule, le génome viral est répliqué et les composants de protéine de la capside virale sont fabriqués, tous deux à l’aide de mécanismes biochimiques de la cellule hôte. Une fois que les particules phagiques sont assemblés, ils sont libérées par les bactéries, souvent par la lyse de l’hôte et éclate, tuant la cellule-hôte dans le processus.
Une méthode largement utilisée pour déterminer la concentration de phage dans un échantillon profite de cette activité lytique. Dans cette technique, le phage de l’échantillon est mélangé avec des bactéries et d’agar mou. Ce mélange est coulé sur boîtes de Pétri avec la gélose ordinaire comme un substrat et les formes de la couche supérieure une superposition.
Les bactéries sont à une forte concentration qu’elles forment une pelouse continue. Les bactéries doivent provenir de culture qui est dans la phase logarithmique de croissance, pour s’assurer que chaque bactérie qui infectent les phages est vivant et permet le phage produire la progéniture.
Quand une particule de phage infecte et lyse une bactérie, la descendance de phage est répartis à proximité des cellules bactériennes et continuer l’infection. L’agar mou limite la diffusion des particules phagiques. Finalement, une zone de compensation, connue comme une plaque, sera formée.
Si le phage est dilué à une concentration suffisamment faible, discrets, des plaques peuvent être observées sur la pelouse bactérienne. Ceux-ci peuvent être comptés et utilisés pour calculer le nombre d’unités de formation de plaques ou PFUs, du phage par mL de l’échantillon original.
Maintenant que vous comprenez comment les phages infectent des bactéries et comment cette activité peut être utilisée pour mesurer la concentration de phage, Let ' s go via un protocole permettant d’utiliser un essai de plaque pour énumérer des phages dans les échantillons d’eau de l’environnement.
Un jour avant la réalisation de l’essai, inoculer une colonie de la souche e. coli ATCC 15597 dans 100 mL de bouillon trypticase soja dans un erlenmeyer de 250 mL. Il incuber sous agitation à 35 ° C pendant la nuit.
3 h avant le dosage, ensemencer 1 mL de la culture d’e. coli une nuit ou plus dans une fraîche 100 mL de bouillon. Placez cette nouvelle culture dans un agitation bain-marie à une température comprise entre 35 et 37 ° C. Cela garantit que les bactéries sont dans la phase logarithmique de croissance lorsque le test commence.
Pour commencer le test de la plaque, faites 10 et 100 fois des dilutions de l’échantillon d’eau, 9 mL de tampon Tris.
À l’aide d’un bain de vapeur, fondre trois tubes de 5 mL de gélose albums 0,7 %, soit gélose trypticase de soja ou des éléments nutritifs. Une fois fondu, placer dans un bain-marie à 45 à 48 ° C pendant au moins 15 min pour la température de la gélose tombant à 45 ° C.
Dans le premier tube de gélose molle, ajouter 1 mL de la phase logarithmique préalablement préparée la culture d’e. coli et 1 mL de l’échantillon d’eau non dilué. Retirer le tube du bain-marie et doucement rock entre vos mains pendant 2-3 s de mélanger la suspension.
Verser l’agar mou sur Pétri préalablement préparée avec la gélose de trypticase soja ou en éléments nutritifs. Rapidement, faites tourner la plaque à se répandre, en vous assurant qu’elle couvre toute la surface.
Répétez l’inoculation et le placage pour les deux autres tubes, en utilisant 1 mL de chaque échantillon dilué.
Une fois l’agar albums a solidifié, inverser les plats et les incuber à 37 ° C pendant 48 h.
Après l’incubation, compter le nombre de fléaux sur chaque plaque. Le comte, calculer la concentration de bactériophage dans l’échantillon original
Par exemple, si 9 plaques ont été extraites de la plaque de dilution de 10 fois, puis il y a 9 fois 10 divisé par 1 mL, ou 90 PFUs/mL de coliphages dans l’échantillon d’eau originale.
Maintenant que vous avez vu comment phage plaque analyses, nous allons étudier comment des essais de plaque peuvent être utilisés pour énumérer les phages et autres types de virus à partir de sources diverses.
Plaque analyse axée sur les méthodes peuvent être utilisées pour isoler le bactériophage de différents échantillons environnementaux tels que les sols. Dans cet exemple, chercheurs ont recueilli tout d’abord le phage du sol, par filtration. Le phage fut ensuite utilisé pour infecter les bactéries du sol commun Arthrobacter lors d’un essai de plaque. Phages ont été cueillies sur des plaques individuelles et striées sur les nouvelles plaques d’agar et puis recouvert de gélose albums contenant des bactéries. Phage concentration diminue le long de la séquence, afin que les plaques discrètes, probablement formés par un seul type de phage, pourraient être obtenues. Ces plaques individuelles pourraient ensuite être choisis d’analyser davantage les phages au sein.
En plus des bactériophages, des essais de plaque est possible également avec d’autres virus qui infectent les mammifères, y compris ceux qui, comme la grippe. Pour ce faire, les cellules de mammifères sont d’abord grandis comme monocouches en culture de tissus plats. Des milieux contenant les virus sont ensuite ajoutés aux cellules pour permettre l’infection de se produire, avant que les cellules sont recouvertes d’un milieu immobilisation comme l’agarose gélatineuse. Après une période d’incubation qui peut durer jusqu'à deux semaines, les cellules infectées sont fixées et colorées pour permettre les plaques être visualisées et comptées.
Enfin, en plus des échantillons prélevés dans l’environnement, des essais de plaque sont utiles pour la détection et l’énumération des virus dans des échantillons de tissus chez les sujets infectés. Ici, chercheurs ont obtenu, et le poumon homogénéisé les tissus des souris infectées par gamma-virus de l’herpès. Cette homogénat contenant le virus fut ensuite utilisé pour infecter la culture de cellules de mammifères. Le nombre de plaques pourrait alors être compté pour fournir une estimation pour le titre viral dans les tissus des poumons infectés.
Vous avez juste regardé les vidéo de JoVE sur la détection des bactériophages dans des échantillons environnementaux. Vous devez maintenant comprendre la biologie fondamentale des phages, comment effectuer un essai de plaque pour doser des phages dans un échantillon d’environnement, et comment des essais de plaque peuvent être utilisés pour étudier les phages et autres virus dans des échantillons environnementaux ou cliniques. Comme toujours, Merci pour regarder !
Subscription Required. Please recommend JoVE to your librarian.
Results
Dilution de l’échantillon d’eaux usées = 10-1
Nombre de plaques obtenues = 9
Par conséquent, phage concentration en échantillon d’eaux usées
= 10 x 9 ÷ 1 mL
= 90 unités formatrices / mL
Eaux d’égout brute contient généralement 103 – 104 coliphage / mL, avec une gamme de 102 – 108 / mL.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Il y a beaucoup d’applications potentielles de coliphages comme indicateurs de l’environnement. Ceux-ci incluent leur utilisation comme indicateurs de contamination des eaux usées, l’efficacité de l’eau et de traitement des eaux usées et la survie des virus entériques et des bactéries dans l’environnement. L’utilisation des bactériophages comme indicateurs de la présence et le comportement de bactéries entériques et virus animaux a toujours été attrayante en raison de la facilité de détection et faible coût associé de phage dosages. En outre, elles peuvent être quantifiées dans des échantillons environnementaux dans les 24h par rapport à des jours ou des semaines pour les virus entériques.
1 La souche e. coli ATCC 15597 généralement produira le plus grand nombre de plaques d’échantillons d’eaux usées. Il doit être cultivé pendant la nuit dans un erlenmeyer de 250 mL contenant 100 mL de nutriment ou trypticase soja bouillon et couvés sous agitation conditions à 35 ° C. 3 h avant le dosage du phage ensemencer un mL de cette culture dans un douce flacon contenant 100 mL de bouillon de soja nutriment ou trypticase et le placer dans un bain d’eau secouer à 35-37 ° C. Cela garantira que les bactéries sont dans la phase logarithmique de croissance.
Subscription Required. Please recommend JoVE to your librarian.




