Overview
Quelle: Vy M. Dong und Zhiwei Chen, Department of Chemistry, University of California, Irvine, CA
Dieses Experiment zeigt ein Beispiel einer Ozonolyse Reaktion zur Synthese von Vanillin aus Ligninsulfonsäure (Abbildung 1). Ozonolyse von Alkenen, eine Oxidationsreaktion zwischen Ozon und ein Alken ist eine gängige Methode, Aldehyde, Ketone und Carbonsäuren vorzubereiten. Dieses Experiment zeigt auch den Einsatz von Ozon-Generator und eine niedrige Temperatur (−78 ° C) Reaktion.
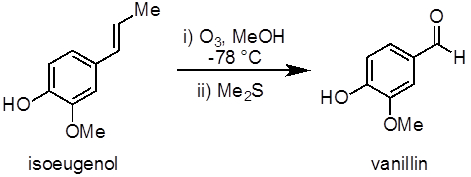
Abbildung 1. Das Diagramm zeigt die Ozonolyse von Ligninsulfonsäure, Vanillin.
Principles
Die oxidative Spaltung von Alkenen zu zwei Carbonyl-Gruppe-haltigen Verbindungen nennt man eine Ozonolyse Reaktion (Abbildung 2). Der vorgeschlagene Mechanismus (Abbildung 3) beginnt mit einem [3 + 2]-Cycloaddition zwischen Alken 1 mit Ozon, die Molozonide zwischen Azu generieren. A ist instabil und ordnet in stabiler Ozonide C über die experimentellen B. C zersetzt sich in Gegenwart von einem Reduktionsmittel wie Dimethyl Sulfid, die zwei Carbonyl-Produkte (2, 3) und Dimethyl Sulfoxid einzurichten. Wenn ein nukleophilen Lösungsmittel verwendet (z.B. Methanol), die Nucleophile Angriffe intermediate B um ein Hydroperoxid E, bilden das Produkt 3 zerfällt, wenn Dimethyl Sulfide (Abbildung 4) hinzugefügt wird. Die Reaktion erfolgt in der Regel bei −78 ° C um Nebenreaktionen zu vermeiden und in der Gegenwart einen Indikator zu bestimmen, wann die Reaktion abgeschlossen ist. Sudan III ist eine häufig verwendete Indikator. Zu Beginn die Reaktionsmischung ist rot und lila/blau wenn abwechselnd alle die Alken ist verbraucht. Wenn alle die Alken hat reagiert, reagiert die Anzeige, die eine N-N-Doppelbindung, mit dem Ozon, wodurch die Farbe zu ändern.

Abbildung 2. Das Diagramm zeigt die allgemeine Ozonolyse Reaktion ein Alken mit eine reduktive Aufarbeitung.

Abbildung 3. Das Diagramm zeigt den allgemeinen Mechanismus der Ozonolyse Alken.

Abbildung 4. Das Diagramm zeigt die Bildung von einem Hydroperoxid von intermediate B.
Subscription Required. Please recommend JoVE to your librarian.
Procedure
- Fügen Sie 200 mg Ligninsulfonsäure, 15 mL MeOH, und ~ 2 mg des Sudan III in einem 3-necked 50 mL Rundboden-Kolben ausgestattet mit einer magnetischen Stir Bar.
- Schließen Sie den Reaktionskolben an eine Sauerstoffflasche und ein Bubbler.
- Schalten Sie die Zufuhr von Sauerstoff.
- Das Reaktionsgemisch mit Trockeneis/Aceton Bad abkühlen.
- Schalten Sie den Ozon-Generator, der den Sauerstoff aus dem Tank zu Ozon umwandelt, die in der Reaktionskolben geht. Der Generator wird zwischen die Sauerstoffflasche und der Reaktionskolben sein. Lassen Sie das Reaktionsgemisch zu rühren, bis sich die rote Farbe ändert, lila/blau.
- Ausschalten der Ozon-Generator, und Sauerstoff, das Reaktionsgemisch von Ozon für 5 min zu bereinigen.
- Entfernen Sie das kühlende Bad und 0,2 mL Dimethyl Sulfid.
- Rühren Sie das Reaktionsgemisch während Erwärmung um 1 h bei Raumtemperatur.
- Entfernen Sie durch rotierende Verdunstung der Lösungsmittel. Machen Sie eine Kieselsäure Stecker durch die Platzierung von Kieselgel in einen Büchner-Trichter. Lösen Sie den Rückstand in 10 % Ethylacetat in Hexanes auf und fahren Sie die Lösung durch die Silica-Stecker unter Vakuum, um Verunreinigungen zu entfernen. Waschen Sie die Kieselsäure Stecker 2 weitere Male mit 10 % Ethylacetat in Hexanes. Sammeln Sie das Filtrat zu und entfernen Sie das Lösungsmittel durch rotary Verdampfung, Vanillin als weißer Feststoff zu erhalten.
- Berechnen Sie die prozentuale Ausbeute von Vanillin gewonnen und seine Reinheit und Identität durch Schmelzpunkt (m.p.) und 1H NMR zu etablieren.
Ozonolyse ist die Oxidation der ungesättigten Bindungen in organische Verbindungen durch Ozon.
Ozonolyse wird am häufigsten verwendet, um Spalten Alkenen um zwei Carbonyl-Produkte zu erhalten. Ozon reagiert auch mit Alkinen und Hydrazonen. Ozonolyse wird in der organischen Chemie Forschung, besonders Naturprodukt Synthese und in der industriellen Synthese von Pharmazeutika verwendet.
Dieses Video wird zeigen das Verfahren für die Ozonolyse von Alkenen und einige Anwendungen der Ozonolyse Chemie einführen.
Ozonolyse von einem Alken beginnt mit Cycloaddition von Ozon über die Kohlenstoff-Kohlenstoff-Doppelbindung, instabiles Zwischenprodukt namens ein Molozonidezu bilden. Die Molozonide distanziert sich dann in einer Carbonyl-Oxid und eine Carbonylgruppe. Diese Fragmente neu anordnen, um die Carbonyl-Sauerstoff vom Carbonyl-Oxid Sauerstoffatome zu verschieben. Die Fragmente rekombinieren dann durch Cycloaddition in eine stabilere Ozonide, in denen die Carbonyl-Sauerstoff an die Kohlenstoffatome gebunden ist.
Die Ozonide ist aufgearbeitet , um den Ring in die Carbonyl-Produkte zu Spalten. Wenn beide Substituenten auf einer Seite CO2-Gruppen sind, entsteht ein Keton unabhängig von den Bedingungen der Aufarbeitung. Angesichts einer Wasserstoff-Substituent, wird oxidativer Aufarbeitung mit einem Wasserstoffperoxid eine Carbonsäure produzieren. Reduktive Aufarbeitung mit Zink in Essigsäure oder Dimethyl Sulfid wird ein Aldehyd produzieren.
Alken Ozonolyse erfolgt in der Regel in der Gegenwart ein Indikator Reaktion verfolgen. Ein Indikator ist eine Verbindung mit eine andere visuelle Darstellung in verschiedenen Phasen der Reaktion. Beispielsweise ändern Ozonolyse des Indikators, den Sudan III ergibt sich eine Farbe aus leuchtend rot bis blau oder violett. Alkenen unterziehen Ozonolyse schneller als Sudan III, so dass die Farbe zu ändern bedeutet, dass die Alken Ozonolyse Reaktion abgeschlossen hat.
Nun, da Sie die Prinzipien der Ozonolyse von Alkenen verstehen, gehen Sie wir durch ein Verfahren für die Ozonolyse von Ligninsulfonsäure in eine der bahnbrechenden Reaktionen für kommerzielle Vanillin-Synthese.
Um den Vorgang zu starten, kombinieren Sie 200 mg Ligninsulfonsäure, 15 mL Methanol und etwa 2 mg des Indikators Sudan III in einem 3-necked Rundboden-Kolben ausgestattet mit Stir Bar.
Sichern Sie die Flasche in einer Dampfhaube über eine Platte rühren. Sicherzustellen Sie, dass der Ozon-Generator ausgeschaltet ist, und schließen Sie dann den Kolben an den Generator und ein Öl-Wäscher.
Schalten Sie die mitreißende Motor um die Lösung zu mischen. Stellen Sie sicher, dass die rote Anzeige der Reaktionsmischung gleichmäßig verteilt ist. Dann bereiten Sie ein kühlendes Bad von Trockeneis in Aceton.
Starten Sie die Sauerstoffzufuhr über den Ozongenerator. Legen Sie das kühlende Bad auf einen Labor-Buben und erhöhen Sie das Bad, das Reaktionsgemisch zu kühlen. Sobald die Mischung abgekühlt ist, beginnen Sie die Ozon-Generator.
Das Reaktionsgemisch zu überwachen, wie es rührt, bis die Mischung blau bis violett in Erscheinung. Schalten Sie die Ozon-Generator, und bereinigen Sie das Reaktionsgemisch mit zweiatomiges Sauerstoff für 5 min.
Sobald die Reinigung abgeschlossen ist, schalten Sie die Sauerstoffzufuhr und senken Sie kühlende Bad heraus unter den Kolben zu. Fügen Sie zunächst die reduktive Aufarbeitung 0,2 mL Dimethyl Sulfide in den Kolben. Lassen Sie die Mischung auf Raumtemperatur unter ständigem Rühren 1 h.
Dann entfernen Sie überschüssiges Lösungsmittel mit einem Drehverdampfer. Sobald dies erledigt ist, lösen sich die Rückstände in 10 mL 10 % Ethylacetat in Hexanes.
Verbinden Sie ein Vakuumfiltration Fläschchen mit einer Vakuumleitung. Sichern Sie einen Büchner-Trichter in die Flasche zu und laden Sie den Trichter mit Silica-Gel.
Reinigen Sie die Produkt-Gemisch durch Vakuumfiltration. Waschen Sie das Produkt durch die Silica-Gel mit zwei Portionen 10 % Ethylacetat in Hexanes.
Übertragen Sie das Filtrat auf eine Runde Talsohle Kolben. Wieder entfernen des Lösungsmittels mit Drehverdampfer, Vanillin als gelbe bis weiße kristalline Nadeln zu erhalten.
Berechnen Sie die Prozent Ausbeute, den Schmelzpunkt zu bestimmen und erhalten eine Protonen-NMR-Spektrum des Produkts.
Vanillin ist als ein weißer kristalliner Feststoff erhalten. Der Schmelzpunkt in der Literatur ist 81 bis 83 Grad. Protonen-NMR-Spektren können zu früheren Literatur Berichten verglichen werden.
Ozonolyse ist weit verbreitet in der Chemie und Biologie. Schauen wir uns ein paar Beispiele.
Ozonolyse ist ein Schritt von vielen industriellen Synthese von Pharmazeutika. Beispielsweise sind die Antibiotika Ceftibuten und Medikament aus einer gemeinsamen Zwischenprodukt Zugriff durch Ozonolyse von einem terminal Alken, ein Keton hergestellt. Das Zwischenprodukt Keton Produkt kann mit einem Enol Form interconvert. Die Enol-hydroxy-Gruppe durchläuft dann verschiedene Reaktionen in den verbleibenden Schritten gegen die zwei Antibiotika.
Ozonolyse kann der letzte Schritt einer Technik für Stereoselectively Alkylantien des alpha Kohlenstoffs der Aldehyde und Ketone. In dieser Reaktion steuert ein Pyrrolidine Reagenz der Stereoselektivität der Kohlenstoff-Kohlenstoff-Bindung-Bildung durch die Bildung einer sterisch sperrige Hydrazone. Nach Alkylierung von alpha Kohlenstoff kann der Kohlenstoff-Stickstoff-Doppelbindung von der Hydrazone durch Ozonolyse, Keton oder Aldehyd nach reduktiver Aufarbeitung zu regenerieren abgespalten.
Sie habe nur Jupiters Einführung in die Ozonolyse beobachtet.
Subscription Required. Please recommend JoVE to your librarian.
Results
Vanillin erhielt als weißer Feststoff (150 mg, 76 % Ausbeute); m.p. 76-79 ° C; 1 H NMR (400 MHz, CDCl3) δ 9,82 (Br s, 1 H), 7.43-7.41 (m, 2 H), 7.04 (d, J = 8,8 Hz, 1 H), 6.30 (s, 1 H), 3,96 (s, 3 H).
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
In diesem Experiment haben wir die Synthese von Vanillin aus Ligninsulfonsäure mit der Ozonolyse Reaktion gezeigt. Auch verwenden einen Ozon-Generator, während der Durchführung einer Niedertemperatur-Reaktion gezeigt wurde.
Ozonolyse ist eine nützliche Reaktion, Aldehyde, Ketone und Carbonsäuren von Alkenen vorzubereiten. Es wurde in Naturprodukt Synthese und industrielle Herstellung von Arzneimitteln angewendet. Artemisinin ist ein potenter Malaria Agent und gehörte zu den Naturprodukten in 2015 den Nobelpreis für Medizin anerkannt. In einer 10-stufigen Synthese von (R)-(+) - Pulegon Ozonolyse im letzten Schritt diente um das Naturprodukt (Abbildung 5) zu machen. Ceftibuten und fort sind Cephalosporin-Antibiotika im industriellen Maßstab produziert. Eine Handelsroute greift Ozonolyse auf einen gemeinsamen Schlüssel Mittelstufe, die auf beide Verbindungen (Abbildung 6) erarbeitet werden können.

Abbildung 5 . Schematische Darstellung der Ozonolyse als letzter Schritt in einer Synthese von Artemisinin.

Abbildung 6 . Diagramm, Ozonolyse, bereiten Sie einen Schlüssel Zwischenprodukt bei der divergierenden Synthese von Medikament und Ceftibuten.
Subscription Required. Please recommend JoVE to your librarian.




