Overview
Source : Vy M. Dong et Zhiwei Chen, Department of Chemistry, University of California, Irvine, CA
Cette expérience fera la démonstration de l’hydrogénation de la chalcone à titre d’exemple d’une réaction d’hydrogénation alcène (Figure 1). Dans cette expérience, palladium sur carbone (Pd/C) servira de catalyseur hétérogène pour le processus. Un ballon servira à fournir l’atmosphère d’hydrogène.
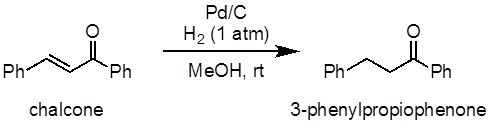
Figure 1 : Schéma montrant l’hydrogénation de la chalcone à 3-phénylpropiophénone.
Principles
L’ajout d’hydrogène dans une unité d’insaturation s’appelle une réaction d’hydrogénation. Depuis sa découverte en 1897 par Paul Sabatier, l’hydrogénation catalysée par des métaux de liaisons π, comme les alcènes (Figure 2), est devenu un processus important dans la chimie. Au cours des années, nouvelles et plus robustes des catalyseurs ont été développés, qui a élargi la portée de ce processus et activé l’hydrogénation d’être asymétrique. Lorsqu’on utilise un catalyseur hétérogène, le mécanisme accepté (Figure 3) commence par l’adsorption d’hydrogène à la surface du catalyseur Pd/C. Ensuite, la liaison de l’alcène se produit suivie de deux transferts d’hydrure séquentielle qui fournissent les alcanes saturés. Sous un catalyseur homogène, le mécanisme est différent ; Notez que la fonctionnalité de cétone peut aussi subir une réduction. Toutefois, l’hydrogénation catalytique est chimiosélective vers le groupement alcène.

Figure 2 : Diagramme montrant la réaction d’hydrogénation des alcènes générales.

Figure 3 : Diagramme montrant le mécanisme de l’hydrogénation catalytique d’alcène.
Subscription Required. Please recommend JoVE to your librarian.
Procedure
- Ajouter 210 mg de chalcone, 12 mg de 5 % Pd/C et 8 mL de MeOH dans un ballon à fond rond 25 mL équipé d’une barre d’agitation magnétique.
- Sceller le ballon à fond rond avec un septum en caoutchouc et commencer à remuer le mélange réactionnel.
- Obtenir un ballon d’hydrogène de la bouteille de gaz hydrogène et mettre de côté.
- Avec une aiguille, appliquer un vide au milieu réactionnel jusqu'à ce que bouillonnant est observée.
- Arrêter le vide et insérez le ballon à hydrogène.
- Après 30 s, enlever le ballon à hydrogène.
- Répétez les étapes 4-6, trois fois plus.
- Insérez le ballon à hydrogène et laisser le mélange réactionnel à remuer pendant 30 min.
- Enlever le ballon à hydrogène et le septum. Filtre à vide le mélange réactionnel par une plaquette de Célite dans un ballon à fond rond taré.
- Éliminer le solvant évaporateur rotatif pour obtenir le produit 3-phénylpropiophénone sous forme de solide blanc.
- Calculer le pourcentage céder et établir son identité par le point de fusion et 1H RMN et la pureté.
Depuis sa découverte en 1897 par Paul Sabatier, métal hydrogénation catalysée par des liaisons π, comme les alcènes, est devenu un processus important en chimie organique.
L’hydrogénation est une réaction chimique qui ajoute de l’hydrogène à travers des liaisons non saturées dans un composé organique.
L’utilisation de réactions d’hydrogénation s’étend au-delà de la synthèse organique en laboratoire, et il a des applications importantes dans l’énergie, industries alimentaires et pharmaceutiques.
Cette vidéo illustre les principes de l’hydrogénation, une procédure pour hydrogénation chalcone et certaines applications de laboratoire.
L’hydrogénation d’une liaison carbone-carbone doublé est une réaction de réduction, avec une molécule d’hydrogène ajoutant à travers la liaison. Un catalyseur hétérogène contenant du palladium, de platine ou de nickel est généralement nécessaire pour le processus de se produire.
La réaction est généralement réalisée à température ambiante avec le composé insaturé dissous dans un solvant approprié, tel qu’un alcool ou d’acide acétique. Une petite quantité de catalyseur est ajoutée à cette solution, qui est alors secouée et agitée en présence d’hydrogène gazeux.
L’hydrogénation est initiée en absorbant le gaz d’hydrogène sur la surface du catalyseur métallique. Cela se traduit par la dissociation des deux atomes d’hydrogène.
Ensuite, les composés organiques insaturés se fixe sur le catalyseur via sa liaison π, qui autorise deux transferts d’hydrure séquentielle sur la paire de carbone. Enfin, la liaison simple carbone-carbone hydrogéné est libérée du catalyseur et le processus se répète jusqu'à ce que la limitation des réactifs sont épuisé.
Maintenant que nous avons discuté des principes de l’hydrogénation, regardons l’hydrogénation de la chalcone utilisant un catalyseur hétérogène.
Pour commencer la procédure, recueillir les réactifs et les produits de verre et les amener sur le banc de laboratoire. Ajouter 210 mg de chalcone, 12 mg de palladium-carbone de 10 %, 1 mL d’acétate d’éthyle et 8 mL de méthanol à un ballon à fond rond 25 mL équipé d’une barre d’agitation magnétique.
Puis, sceller la fiole avec un septum en caoutchouc et commencer à remuer la réaction sur une plaque de remuer. Même si le mélange est remuant, remplir un ballon avec une aiguille et d’une soupape joint, à l’aide d’hydrogène à partir d’un cylindre.
Maintenant, avec la vanne fermée, introduire l’aiguille dans le bouchon en caoutchouc sur la fiole et appliquer un vide à l’autre ouverture sur le flacon. Quand bouillonnant est observée dans le mélange, couper le vide.
Maintenant, ouvrez le robinet et permettre à hydrogène s’écouler dans la fiole. Après 30 secondes, enlever le ballon à hydrogène et fermez-le hermétiquement. Répétez les étapes d’infusion sous vide et de l’hydrogène trois fois plus.
Le dernier cycle, laisser le ballon à hydrogène attaché au ballon et laisser le mélange réactionnel remuer pendant 30 minutes.
Pour collecter les produits de réaction, commencez par retirer le ballon à hydrogène et le septum. Vide puis filtrer le mélange réactionnel par une plaquette de Célite dans un ballon à fond rond taré.
Enfin, enlever le solvant évaporateur rotatif pour obtenir le produit, qui devrait être un solide blanc dans l’aspect. Rendement est déterminé par la pesée du contenu de la fiole de taré. L’identité de ce composé peut être ensuite confirmée via le point de fusion 1H et analyse NMR.
Dans cette procédure, un rendement de 72 % provient de l’hydrogénation de la chalcone. Une gamme de point de fusion de 65-70 ° C a été mesurée pour l’échantillon obtenu, qui concorde avec les données publiées pour le 3-phénylpropiophénone. De plus, les pics obtient 1H NMR matches les environnements hydrogène prévu pour le composé saturé.
Maintenant que nous avons regardé une procédure pour hydrogénation, nous allons jeter un oeil à certaines applications.
Dans l’industrie de l’énergie, des combustibles synthétiques sont produits provenant de sources autres que des hydrocarbures, comme le charbon et la biomasse. Friedrich Bergius, qui a remporté le prix Nobel en 1931 pour sa découverte, invente un procédé pour traiter le charbon avec de l’hydrogène et un catalyseur métallique sous haute température et la pression aux hydrocarbures de la forme.
Bio-carburant, une source d’énergie chimique dérivée du bois, l’herbe, les déchets agricoles et autres biomasses, on élabore une durable et carbone neutre alternative aux combustibles fossiles. Dans cette application, hydrogénation catalysée de ruthénium et cobalt, molybdène médiée hydrodésoxygénation servent à enlever des groupements réactifs de vinyle et de l’oxygène. Hydrotraitée combustibles sont moins corrosifs et ont une plus grande stabilité thermique.
Vous avez juste regardé les vidéo de JoVE sur l’hydrogénation. Vous devez maintenant comprendre les concepts de cette réaction, comment elle est réalisée en laboratoire et certaines de ses applications. Merci de regarder !
Subscription Required. Please recommend JoVE to your librarian.
Results
3-phénylpropiophénone a été obtenue sous forme de solide blanc (150 mg, 71 % de rendement) ; député de 65-70 ° C ; 1 H RMN (400 MHz, CDCl3) δ 8,00 (d, J = 7,2 Hz, 2 H), 7.59 (t, J = 7,2 Hz, 1 H), 7,49 (t, J = 7,6 Hz, 2 H), 7.37-7.26 (m, 5 H), 3.35 (t, J = 7,2 Hz, 2 H), 3.12 (t, J = 7,6 Hz, 2 H)
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Dans cette expérience, nous avons démontré une réaction d’hydrogénation catalytique d’un alcène. Chalcone est hydrogénée pour former le 3-phénylpropiophénone.
L’hydrogénation est une réaction exothermique (libère la chaleur) car l’alcane produit est plus stable que l’alcène de réactif. Le montant si la chaleur dégagée par la réaction peut servir d’indicateur de la stabilité de l’alcène. Dans l’industrie alimentaire, hydrogénation est utilisé pour le traitement des huiles végétales, qui sont triglycérides portant plusieurs unités de l’alcène. Variant les conditions de réaction contrôle le degré d’hydrogénation. L’hydrogénation est utilisée pour la synthèse industrielle d’hydrocarbures à partir du charbon. Ceci est connu comme le procédé Bergius et sert au traitement du charbon (carbone élémentaire) à haute pression d’hydrogène et un catalyseur métallique sous haute température. Son inventeur, Friedrich Bergius a reçu le prix Nobel de chimie en 1931.
Subscription Required. Please recommend JoVE to your librarian.




