4.9: 沉淀反应
在沉淀反应中,可溶性盐的水溶液反应以产生不溶性离子化合物— 沉淀物。当溶液中带相反电荷的离子克服其对水的吸引力并相互结合,形成从溶液中分离出来的沉淀时,就会发生反应。由于这样的反应涉及水溶液中离子化合物之间的离子交换,因此它们也被称为双重置换,双重置换,交换反应或复分解反应(希腊语为“转置”)。沉淀反应用作分析技术,以鉴定化合物中的金属离子,并采用重量分析法确定物质的组成。   
物质在水中或任何溶剂中的溶解程度定量表示为其溶解度,定义为在特定条件下可以达到的最大物质浓度。溶解度相对较大的物质据说是可溶的。当溶液的浓度超过其溶解度时,该物质将沉淀出来。溶解度相对较低的物质据说是不溶的,这些物质很容易从溶液中沉淀出来。
例如,当碘化钾和硝酸铅的溶液混合时会观察到沉淀,导致形成固体碘化铅:

此观察结果与溶解度指南一致:在所有相关化合物中,唯一不溶的化合物是碘化铅,这是碘盐一般溶解度的例外之一。
代表该反应的净离子方程为:
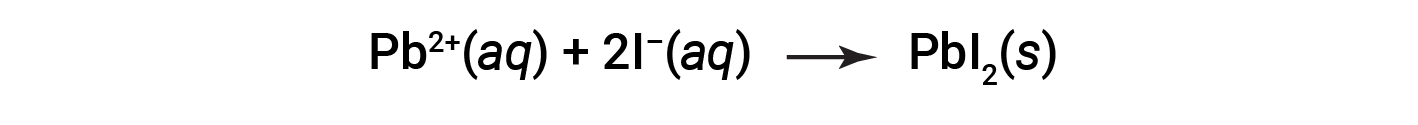
例如,硝酸银和氟化钠的混合溶液将产生包含Ag + ,NO 3 &minus; ,Na < sup> + 和F &minus; 离子。除了最初存在于溶液中的两种离子化合物AgNO 3 和NaF外,还可以从该离子集合中衍生出另外两种离子化合物:NaNO 3 和AgF。溶解度准则表明所有硝酸盐都是可溶的,但AgF是氟化物盐一般溶解度的例外之一。因此,预计会发生沉淀反应,如以下等式所述:
本文改编自 OpenStax 化学2e,第4.2节:对化学反应进行分类。


Tags
Precipitation Reactions
Ionic Solids
Water-soluble
Water-insoluble
Dissociation
Aqueous Solution
Insoluble Ionic Solid
Precipitate
Filtration
Sodium Chloride
Silver Nitrate
Ions
Cations
Anions
Solubility Rules


