11.7: 相变:汽化和凝结
物质的物理形式随温度的变化而变化。 例如,提高液体温度会导致液体汽化 (转化为蒸汽)。 这一过程称为汽化—一种表面现象。 当分子的热运动克服了分子间作用力,而分子 (在表面) 进入气态时,就会发生汽化。 当液体在封闭容器中蒸发时,气体分子就无法逸出。 随着这些气相分子随机移动,它们偶尔会与凝相表面发生碰撞,在某些情况下,这些碰撞会导致分子重新进入凝相。 从气体相向液体的变化称为凝结。
汽化是一个内置治疗过程。 游泳或淋浴后,冷却效果明显。 当皮肤上的水蒸发时,它会除去皮肤的热量并冷却皮肤。 与汽化进程相关的能量更改是汽化的焓, ΔHvap。 例如,标准温度下的水汽化由以下项表示:

同发性过程相反的是放热。 因此,气体的凝结释放热量:
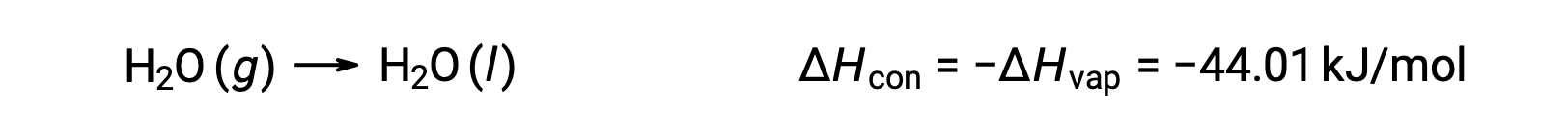
汽化和凝结是相反的过程;因此,它们的焓值与相反。 虽然汽化的焓为正,但凝结的焓为负。
不同的物质会蒸发到不同的范围 (取决于其 分子间力(IMFs) 的强度) ,因此会显示不同的汽化值焓。 分子之间相对较强的分子间有吸引力的力会导致汽化值的焓更高。 弱分子间吸引力对汽化的障碍较小,导致汽化的焓值相对较低。
本文改编自 Openstax, 化学 2e, 第10.3节:相变。


