12.7: 溶液濃度の表現
溶質とは、溶液中に含まれる成分のうち、通常は溶媒よりもはるかに低い濃度で存在するものを指します。溶質の濃度は、希薄(比較的低濃度)や濃厚(比較的高濃度)といった定性的な言葉で表現されることが多いです。
濃度を定量的に評価するには、用途に応じてさまざまな測定単位を用いることができます。モル濃度(M)は、化学の多くの応用に役立つ濃度単位です。モル濃度は、溶質の量(モル数)を溶液の体積(リットル)で割ったものと定義されています。

溶液の体積は温度によって変化するため、モル濃度も同様に変化します。モル濃度で表すと、溶質種と溶媒種の数が同じである溶液の濃度は、溶液の収縮・膨張により、温度が異なると異なる値になります。多くの束一的性質を含む計算には、値が温度に依存しないモルベースの濃度単位がより適しています。そのような単位として、モル分率(前章の気体の章で紹介した)とモル濃度があります。
モル分率とは、溶液の全成分のモル数に対する、その成分のモル量の割合です。χA
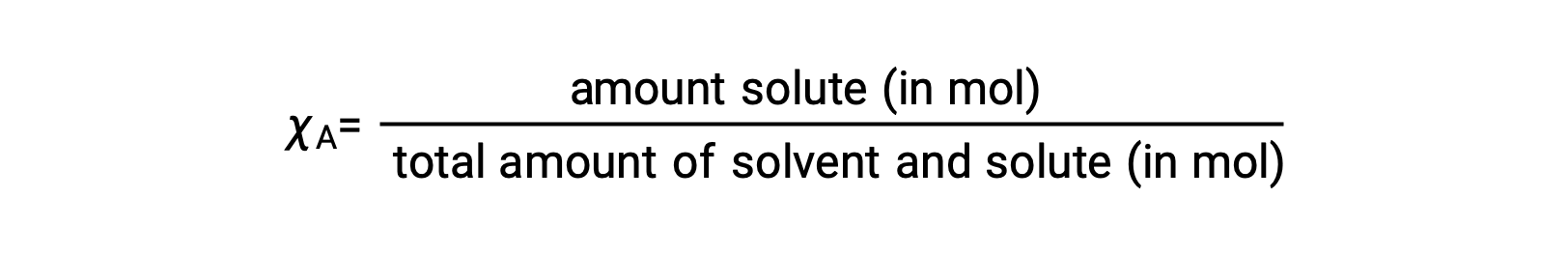
この定義では、すべての溶液成分(溶媒とすべての溶質)のモル分率の合計は1になります。
モル濃度とは、溶媒の質量(キログラム)に対する溶質のモル数の比として定義される濃度の単位です。
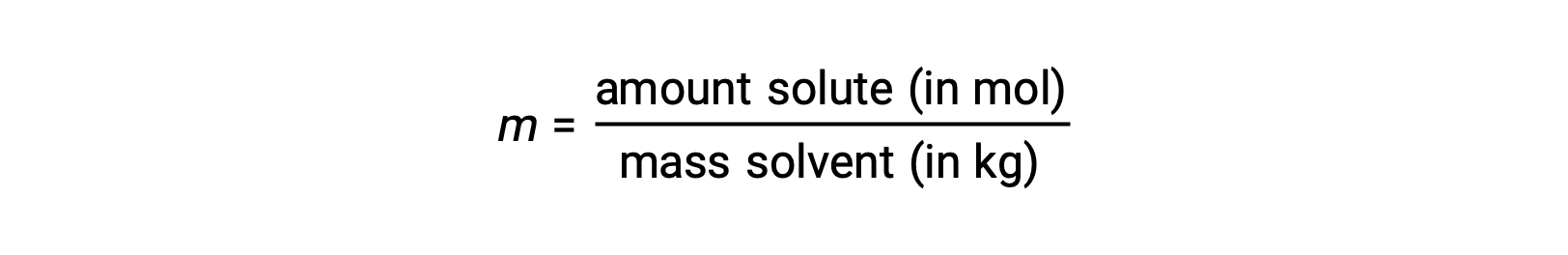
これらの単位は、質量とモル量のみで計算されるため、温度による変化がなく、温度に依存しない濃度を必要とする用途に適しています。
上記の文章は以下から引用しました。Openstax, Chemistry 2e, Section 11.4: Colligative Properties.


