Summary
本明細書では、高分子のX線結晶構造解析を用いた構造決定に使用するための脂質中間相における膜タンパク質のハイスループット結晶化ロボットのアプローチを説明しています。メソッドに不可欠な粘性及び粘着性のタンパク質を含んだ中間相を扱うことができる3つのロボットが導入される。
Abstract
膜タンパク質の構造と機能の研究は大いに高分子X線結晶構造解析(MX)を介して提供タイプの使用可能な高解像度の3次元構造を持っていることから恩恵を受ける。 MXの必須成分は、理想的には回折品質結晶の安定供給である。膜タンパク質の結晶化のメソまたは脂質立方相(LCP)メソッドの中で膜タンパク質を結晶化させるためのいくつかの方法の一つです。これは、結晶を成長するための共連続メソフェーズを利用しています。方法としては、後半のいくつかの壮観な成功を収めており、現在、それを使うことに興味を持って多くの研究グループと注目を集めている。メソッドに関連付けられている課題の一つは、ホスティングメソフェーズが厚い歯磨き粉を彷彿とさせる、非常に粘性と粘着性であるということです。このように、結晶化ウェルに少量で再現可能な方法でそれを手動で調剤することはスキル、忍耐と着実に手を必要とします。柱を行うためのプロトコル膜の構造·機能生物学(MS&FB)グループ1-3に開発されたstの。方法を説明するJoveのビデオの記事が入手できる1,4です。
メソ試験で設定するための手動のアプローチは、このような結晶の最適化および誘導体化などの特殊なアプリケーションとの明確な利点を持っています。しかしそれは低スループット法であることに苦しむん。ここでは、ロボットメソ結晶化試験で行うためのプロトコルを示しています。ロボットは、スピード、正確性、精度、小型化、還元雰囲気中または低温下、または高温下で、そのような暗闇の中でのように敵対的な条件とみなすことができるもので、長期間にわたって継続的に働くことができるという利点があります。 メソロボットで 、適切に使用すれば、大幅で遅いステップの一つである結晶化を促進することにより、膜タンパク質構造の生 産性と機能の研究を向上させることができます全体的な構造決定のパイプライン。
このビデオの記事では、我々は、 メソ crystallogenesis 内に不可欠粘性及び粘着性メソフェーズを免ずることができる3つの市販のロボットの使用例を示します。最初のロボットは、MS&FBのグループ5,6で開発されました。他の二つは、最近利用可能になっていると、完全を期すためにここに含まれています。
この記事で取り上げたプロトコルの概要を図1に示されている。すべての操作は室温(約20℃)周囲条件下で行った。
Protocol
1。結晶化プレートの準備
ロボット結晶化実験を行うように設定すると、参考文献2に詳細に記載のガラスサンドイッチ結晶化プレート( 図2)のベース·プレートの準備から始まります。ベースプレートは最初シランや井戸を作成あき両面スペーサープレートに適用する必要がありますする必要があります。このために必要な原材料及び貯蔵品は、材料の下に箇条書きされています。
- ペーパータオル上でプレートを置き、ソリューションをシラン数滴を適用し、ティッシュペーパーでプレートの表面に均等に配布します。
- 水の入ったビーカーにプレートを浸漬することにより、過剰なシラン溶液を除去します。
- ビーカーのプレートを取り出し、乾いたペーパータオル、シラン化側にそれを置き、ペーパータオルで軽く拭いて、その露出面を乾燥させてください。
- あき、両面スペーサーの上に保護カバーを剥がしそしてガラス板の乾燥、シラン化表面に、スペーサー、粘着面を下に適用します。一致し、スペーサーは、左上隅とスペーサーとプレートの2つの隣接した側面と、ベース板の上に適切に配置されていることを確認します。
- ベースプレート上にスペーサを平らにし、それらの間の緊密なシールを作成するためにローラーやbrayerを使用しています。
予め組み立てられたプレートは(; MD11-55-100、分子寸法、およびLCP96T-UVP70U、Swissci HR3-151、ハンプトンリサーチ)市販されている。コスト上の理由から、我々は上記のプロトコルに従って、我々自身の板を組み立てることを好む。
2 メソロボット1
このビデオの記事で紹介されるメソロボットの最初のは、現在、MS&FBのグループ( 図3)で使用されているものです。ロボットの完全な詳細は、材料の下およびリファレンス第5節で見つけることができます。材料とequipmeロボットを用いた結晶化試験を設定するために必要なNTは材料の下に箇条書きされています。
- ロボットのデッキの上のセクション1で調製したスペーサーをベース·プレートを置きます。それは、ベースプレートの位置合わせの目的のためだけでなく位置でマークされた独自のプラットフォームを持っている。プレートは、識別のためにラベルを付ける必要があります。
- 結晶化プレートの隣にあるロボットの甲板上の独自のプラットフォームで96ウェル沈殿ブロックを固定します。
- プラスチック製のシーリングキャップを剥離することで慎重にブロックを開きます。
- 加湿器の電源をオンにして、ロボットの甲板上のベースプレート上と向こう側に湿った空気の流れを導く。加湿器は、沈殿剤溶液の蒸発を低減するために、結晶化プレート5越えて再現性を向上することが示されている。それは、メソフェーズの分配が始まる直前に、そうでなければ周囲の相対湿度が低いときに領域を事前に加湿する、または前にONに設定されてアップにすることができます。
- 製造元の指示に従ってロボットを初期化します。正確な手順は、時間の経過とともに変化するので、楽器の具体的な手順は、どのここでは詳細に説明されない。本質的に、どのような初期化中に発生するとロボットに腕を分配メソフェーズは3つの直交する方向のX、Y、Zの基準位置が設けられていることである
- ロボットのアーム1( 図3)には、針を分配するとの完全な、ハミルトンシリンジ内のタンパク質を含んだ中間相を取り付けます。注射器にロードする方法と、中間相を準備する方法の完全な詳細は参考資料3,7-10に記載されている。
- 結晶ベースプレート上にスペーサから上部保護カバーを取り外し、ベースプレートプラットフォーム上の基点とプレート上のウェルの位置を合わせます。なお、このビデオの目的のために、保護カバーは、アライメント·ステップ中にビューアを支援するための場所に残っていた。
- 調剤syringの針先の位置を合わせます結晶化プレート(ウェルA1)の左上隅にある井戸最上の底を持つe。これは、針の先端がウェルの底に来るどれだけ近いかを見ながら分注アームの高さまたはZ座標を調整して目によって行われます。先端はちょうど井戸の底に触れていることを、ほんの少し分注アームの高さを調整しながらのプラットフォーム上で左右にプレートを移動することによって判断することができる。
- コンピュータチップの接点プレート分注アームのZ座標に入力します。調剤は、ベース板の表面に対応する、この参照Z位置から針の先端80マイクロメートルで行われるようにプログラムされている。
- 眼による位置まあ、A1の中央に針の先端。制御用コンピュータで保管基準X、先端が中心に分注アームのY座標。この座標は、板の上に残りのウェルの中心を定義するために使用されます。
- PRその新鮮なメソフェーズを確保するために、ロボットのコンピュータ上で適切なコマンドを使用してIMEシリンジ分注針と初回と後続の井戸はメソフェーズの彼らの完全な補完を受けることを塗りつぶします。組織と針先端に押し出されたメソフェーズを拭き取ってください。
- ロボットのアーム2の沈殿剤調剤先端が洗浄され、沈殿剤ブロックからソリューションを吸引するために用意されている手順をフラッシングのラウンドを開始するために実行ロボット(X-AP)プログラムを起動します。
- タンパク質を含んだ中間相(通常は50 NL)、最初沈殿剤溶液(通常は800 nl)で続いて一度に8ウェルの列と動きで井戸のシーケンシャルな読み込みを設定するには、ロボットに機能を分配アクティブにします。列をロードする間、針の端に配置されているが駐車位置にアームリターンを分配するメソフェーズは乾燥から先端にメソフェーズを防ぐために湿らせたスポンジ。調剤メソフェーズおよび沈殿のプロセスが繰り返されますプレートがいっぱいになるまでプレートを横切る11倍。メソフェーズと沈殿と96ウェルプレートのローディングが完了するまで5分かかります。
- プレートがいっぱいになると、ロボットアームがその公園の位置に戻っているとすぐに、ロボットのデッキからプレートを取り外し、平らな固体表面上に置きます。
- 直ちに、よく物の経時変化を最小限に抑えるためにカバーガラスでプレートをシールします。これは、カバーガラスがベースプレートの方形整列し、カバーガラスのどれもベースプレートのフットプリントを超えて拡張されていないことを、すべての96ウェルが完全に覆われていることを確認することが重要です。ローラまたはbrayer、カバーガラスとスペーサーの間に緊密な、均一なシールを作成するために使用されます。
- それが必要としてセットが上がったことを確認するためにプレートを点検します。何1が探していると、各ウェル中の外観 "皿の上に目玉焼き 'です。目玉焼きの黄身は、メソフェーズに対応しています。卵の白身は、沈殿剤solutiですで、パンの縁はよく結晶の境界線です。理想的には、3つの同心である。
- 結晶成長のために温度制御された記憶領域にプレートを置きます。
- もうプレートが設定されていない場合は、ロボットのデッキから沈殿ブロックを削除し、しっかりとそれを封印し、それを記憶に戻す。
- ロボットの分注アームからメソフェーズを含むシリンジを取り外し、それを解体し、次回の使用に備えて、メタノールとドライで慎重に調剤針、フェルールを含めた部品を洗浄してください。
3 メソロボット2。蚊LCP
モスキートLCPのロボット( 図4)は、ロボット1で使用されているものと同様のメソフェーズディスペンサーを搭載しています。ロボット1とは対照的に、それは使い捨てチップを用いて沈殿分注します。プログラミングソフトウェアは、特定の結晶化プレートとprecipitで作業するための機器を設定するために使用されアリブロック、および指定された順序でメソフェーズと沈殿のユーザー定義のボリュームを分配する。そのような詳細は製造業者によって提供されており、ここでは説明しない。
- 針で完全かつタンパク質を含んだメソフェーズで満たさハミルトンシリンジ、ロボット1で上述とJoveの記事1712年1のように準備をします。
- ロボットの分注アーム上の位置にシリンジをクランプします。
- デッキを使用して、Xと吐出シリンジの針のY座標値を確立するために、レーザーセンサーを搭載。これは、メソフェーズはプレート上の各ウェルの中央に正確に分配されることを保証するために必要な重要なステップです。
- コントロールパネル上のボタンを押すだけで、プライムシリンジは針からメソフェーズを追放する。井戸をロードするためにロボットを使用するための準備として、組織と針の先端から押し出さメソフェーズを削除します。
- ロボット湿っのデッキで結晶化プレートを配置する前に、毛細管現象によって所定の位置にプレートを保持するのを助けるために数滴の水でプラットフォームの表面専用。
- ガラスベース板上にスペーサから保護カバーを取り外し、良好な接着性を確保するため、しっかりと、そのプラットフォームの上に置きます。それによって調剤針先端に関してプレート上のウェルの適切な配置を確保する3コーナー井戸を揃えるために、プラットフォーム上の3つの基準点を使用します。楽器は、現在調剤サイクルに入ることを命じている。
- サイクルは、メソフェーズが新鮮メソフェーズをウェルロードに移る直前に小さなガラスプレート上に分配された第2のプライミング工程から始まる。ロボット板上のメソと最初にロード8ウェルの縦の列をしてから、メソフェーズボーラスの上に沈殿剤溶液を分配するために使い捨てチップを使用しています。すべてのウェルが充填されるまでのプロセスは、板の長さに沿って11回繰り返される。全体のプロセスは、完了までに約5分かかります。
- 削除するロボットのプラットフォームから埋めプレートとロボット1の下に上記のようにカバーガラスをしっかり閉めてください。
- 結晶成長のための温度制御された環境で、適切に標識されたプレートを置きます。
4 メソロボット3 で 。グリフォンLCP
グリフォンLCPのロボット( 図5)は、ロボット1と2について上述と類似メソフェーズ分配システムが組み込まれています。何が他の二つとそれを区別すると、すべての96沈殿剤溶液は同時に分配されていることである。
- タンパク質を含んだ中間相を準備して、ロボット1と2の下で、上述したように、吐出シリンジにロードして、Joveの記事で1712年1。
- ロボットの分注アーム上の位置にシリンジをクランプします。
- ロボットのデッキで沈殿剤溶液ブロックと結晶化プレートを置きます。
- 96先端ょんを読み込む沈殿ソリューションとD。ユーザ定義の遅延時間は、粘性の沈殿を吸引容易にするために提供されています。
- 分配サイクルを入力するように楽器を命じる。サイクルが完了するまでに約1分かかり過程で96ウェルに順次分配されるメソフェーズから始まる。 96先端ヘッドは、結晶化の井戸でメソフェーズボーラスの上に、一度にすべての96沈殿ソリューションを分配します。プレート全体の読み込み処理が2分で終了します。
- ロボットのプラットフォームから充填プレートを取り外し、ロボット1の下に上記のようにカバーガラスをしっかり閉めてください。
- 結晶成長のための温度制御された環境で、適切に標識されたプレートを置きます。
5。代表的な結果
このビデオの記事の目的は、膜タンパク質を含んだガラスsandwicでメソフェーズ、粘性で自動的に結晶化試験を設定する方法を説明することですhは、96ウェル結晶化プレート。重点は、最小限の手動介入を必要とする特殊なロボットを使用することにより自動化にあります。ロボットを使用した場合の再現性と精度は、メソフェーズおよび沈殿注し、ウェル内の両方の配置のボリュームの点では、期待されています。これらはcrystallogenesisを支える条件の有効なスクリーニングの観点から重要である。彼らはまた、イメージング機器で頻繁に行わ結晶成長を評価することを目的とする解析パイプラインの次のステップのために重要です。ドロップまたはボーラス場所はイメージングプロセスの鍵であり、ウェル内ボーラスの不規則と不適切な配置は通常のために修正するためにユーザーの介入を必要とし、時間がかかります。例示の目的のために、適切かつ不適切にロードされたプレートの例を図6に示す。
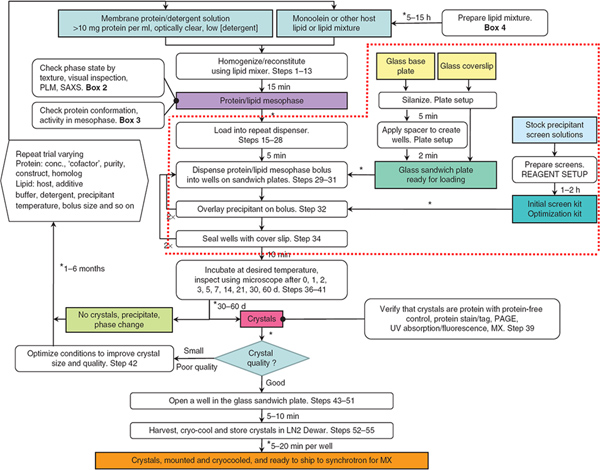
図1:フローチャートはメソ成長膜タンパク質結晶中の生産、収穫やクライオ冷却に必要な手順をまとめたものです。赤い点線で囲まれた手順では、このJoveの記事の焦点である。ロボットは、ステップ29から32にメソフェーズと沈殿ソリューションを分配するために使用されていました。参考資料3から。 拡大図を表示するにはここをクリック 。

図2:完全にロードされ、密封された96ウェルガラスサンドイッチ結晶化プレート。各ウェルには、50 nlの立方相及び1μlの沈殿剤溶液を含んでいます。明確にするために、立方晶相はスーダンレッドで染色し、沈殿剤溶液は、メチレンブルーが含まれています。資料5から。
_upload/4000/4000fig3.jpgの "alt ="図3 "/>
図3 メソロボット(ロボット1)。ロボットは二本の腕を持っています。アーム1はタンパク質を含んだ脂質メソフェーズを分配します。アーム2は沈殿ソリューションを分配します。充填中、96ウェルプレートは、それ自体が静止しているロボットの甲板上の位置に固定されたままである。二本の腕は、メソフェーズと沈殿ソリューションを提供して移動します。参考資料3から。

図4:モスキートLCPロボット(ロボット2)。ロボット1、蚊LCPのデッキとは対照的に、96ウェルプレートと沈殿剤溶液のブロックに座っている時に、充填中に水平方向に移動する。

図5グリフォンLCPロボット(ロボット3)。間にセットアップ、脂質立方相ディスペンサは、96ウェルプレートにタンパク質を多く含んだメソフェーズを提供するために移動します。デッキはその後沈殿剤溶液の先端ヘッドの下にプレートを配置するために水平に変換します。全96沈殿剤溶液は同時に分配されています。写真は、メーカーから調達( http://www.artrobbins.com/ )と標識。

図6:完全にロードされ、密封された96ウェルガラスサンドイッチプレート()と井戸適切に(B)と不適切(C、D)のメソロボット(ロボット1) に使用して充填。のプレート上のバーコードラベルをプレートインキュベーター/イメージング装置にプレートを追跡するために使用されます。パネルでは、BD、沈殿剤溶液とメソフェーズは、それぞれ、PとMのマークが付いています。予想される "皿の上に目玉焼き 'Bの井戸の外観が適切にロードされ、十分に密封さの特徴である。 C言語では、沈殿物を中心からずらした位置でうまく不適切に分注されており、スペーサーと接触して来ている。 C言語では、それは中間相の体積はそれがあるべきよりも小さいことをあまりにも見えるでしょう。沈殿剤溶液を用いて不完全ロードの例は、スケールはDに示されている、すべてのウェルの直径は6mmである。
Discussion
このビデオの記事では、我々は自動的にタンパク質を含んだ脂質メソフェーズを用いて、96ウェルガラスサンドイッチプレートにメソ結晶化試験でセットアップするロボットを使用する方法を実証した。本研究で使用したロボットは特別にもともと7に記載されているように 、粘性及び粘着性メソフェーズのナノリットルボリュームの正確で再現性の送達のための肯定的な変位のガラスシリンジを含むように設計されていました。
正確さと精度は、ロボットの重要な機能です。しかし、これらの特徴は、ロボットの性能が評価され、キャリブレーションが実行される程度と規則性と同じくらい良いです。それは個々のプレートが設定されている間、ロボットの性能が評価されるべきことは言うまでもない。それはロボットが完璧に機能し、自動で実行するロボットを残していると仮定することは適切ではない。気配りと観察オペレータがposにあるべきitionは音か何かが正常に動作していないと、すぐにそれを修正するために外観によって注意を促す必要があります。 プレートがシールされているとすぐに、それが結晶化試験のために離れて置かれる前に加えて、 各プレートを慎重によく内容の均一性のために目の検査を受けなければならない 。これは、ほんの数秒で実行するようにする必要がありますし、次のプレートをロードしている間に行うことができます。気付かは、例えば、特定のウェルが正しく入力されていないことは確か沈殿分配チップが誤動作しているという事実を強調することができる。メソフェーズの配信は不定期であると見なければならない、関連する障害のある項目は直ちに修正される必要があるでしょう。これらの問題を指摘し、セットの間の関連の調整を行うことにより、貴重な脂質や膜タンパク質など、時間と材料の節約になります。イメージャは、結晶成長、正確さと精度を追跡するために使用されている場合は、撮像中に監視することができます。ドロップまたはボーラスを持つ例えば、体系的な問題イメージャによって場所は、何かが右ではなく、プロトコルのどこか上流の是正措置が必要であることを示す。
信頼性の高い性能故にロボットの利益のために、定期的なスケジュールで校正され、必要に応じなければなりません。校正は、沈殿剤およびウェル内ボーラスと沈殿配置と同様に配信メソフェーズのボリュームを含める必要があります。明らかに、可能な限りキャリブレーションは品質管理運動の対象期間内に実施された試験で使用されるものと同様のボリュームと材料を使用して行われる必要があります。
キャリブレーションと同様に重要なのは、あまりにも在庫がロボットの部品や消耗品の適切な供給を持っているそうです。破局や予期しない障害、閉塞とクラッシュが発生するとを行うことができます。このような場合には、使用可能な交換用沈殿配信先端を有する、例えば、非常に貴重な膜タンパク質調製物は、それが必要ととして使用されていることを意味するかもしれません無駄にされていません。
ロボットの利点のいくつかは、それが本質的に連続的に動作すること、それは苦しんでいないか、または疲労 "が訴える"という事実を含む。ロボットはまた、暗闇の中でのように、制御された照明や環境条件の下で、温度の極端で、人に優しいとは見なされません条件の下で使用することができます。この記事で紹介ロボットはすべての〜20℃周囲条件下で使用されましたしかし、タンパク質および非周囲温度、制御された光11,12及び酸化剤または還元環境13を必要とするプロジェクトがあります。結晶化ロボットが使用されている場合、これらのすべては、比較的容易に、用の仕出し料理することができます。
以前Joveのビデオ記事ではメソメソッド内で結晶化試験は手動で1に設定されている方法を紹介しました。手で確実に分配することができる中間相の最小体積はb限られているyの試験を設定する人の視力と着実利き手。我々の経験では、100 nlの限り低くメソフェーズのボリュームが容易に処理されます。我々は、デフォルトのボリュームが40 NL約手動ディスペンス1研究室を知っている。しかし、かなり小さいボリュームがロボットを使って行うことができます。これとは別に、我々は550ピ コリットルという低メソフェーズボリュームがロボット14分配することができることが示されている。その作品からは、ロボットによる更なる小型化が実施されれば、結晶化実験を行うのに必要な貴重な膜タンパク質の量の大幅な削減につながる、これが可能であることは明らかでした。
このビデオの記事では、3種類の市販のロボットは脂質中間相を用いた高スループット膜タンパク質の結晶化を実証するために使用されていました。 JOVE 1712 1に記載したように、これらの最初のものは、手動で試験を設定する私たちの経験に基づいて、MS&FBのグループで開発されました。これは楽器ですリーメントは我々に最も精通していると、現在の記事の大半は、その使用に専念しています。他の二つのロボットは、記事が書かれた、関連する映像が、完全性の利益のためにここに含まれている時に、MS&FBのグループのデモにあった。すべての3つのロボットは非常に同じメソフェーズ分配システム、容積ガラスシリンジ5,7となっている本質的な機能を使用します。彼らは、沈殿剤デリバリーに関して最も大きく異なります。ロボット1と2は、8ウェル、同時に結晶化プレート上の単一の列に同時に沈殿剤を分配することができます。これとは対照的に、ロボット3は、単一のアクションですべての96沈殿ソリューションを分配します。ロボット2は使い捨ての沈殿剤調剤のヒントを持つ唯一の楽器です。特定のアプリケーションに依存する別の楽器に関連付けられている長所と短所がありますが、これらはここで詳しく説明されません。すべての3つの作業とは、私の結晶が得られたことを言えば十分メソメソッド内でmbraneタンパク質。
高分子結晶学による構造決定の全体的なプロセスの次のステップは収穫にとクライオクール結晶にこのビデオの記事で説明されるように設定するプレートから、レコード、それらからプロセスX線回折にしています。これらのトピックについては、このシリーズ1,15で個別Joveの記事で説明されています。
Disclosures
特別な利害関係は宣言されません。
Acknowledgments
この仕事に貢献し、ほとんどが膜構造·機能研究グループからのもので、過去と現在の両方のメンバーが多くの人々があります。すべての我々の暖かい感謝と感謝の意を。この作品は、アイルランド科学財団(07/IN.1/B1836)、国立衛生研究所(GM75915、P50GM073210とU54GM094599)、およびFP7 COSTのアクションCM0902からの助成金によって部分的にサポートされていました。
Materials
| Name | Company | Catalog Number | Comments |
| Brayer (roller) | Fisher Scientific | 50820937 | Tool |
| Gas-tight syringes | Hamilton | 81030 | Tool |
| Glass coverslips | Marienfeld | 01029990911 | Disposable |
| Glass plates | Marienfeld | 1527127092 | Disposable |
| Gryphon LCP Robot | Art Robbins | NA | Tool |
| In meso robot | Anachem/Gilson | NA | Tool |
| Lab notebook | Various | NA | Tool |
| Mosquito LCP Robot | TTP Labtech | NA | Tool |
| Perforated double-stick spacer tape | Saunders Corporation (hole-punched) | customized | Disposable |
| Precipitant solutions | Various | Various | Reagent |
| Purified water | Millipore | NA | Reagent |
| Rain-X | Shell Car Care | 80199200 | Reagent |
| Syringe tips | Hamilton | 7770-020 (gauge 22) | Tool |
| Tissues | Various | Various | Disposable |
| Water bottle | various | NA | Reagent |
References
- Caffrey, M., Porter, C. Crystallizing membrane proteins for structure determination using lipidic mesophases. J. Vis. Exp. (45), e1712 (2010).
- Cherezov, V., Caffrey, M. Nano-volume plates with excellent optical properties for fast, inexpensive crystallization screening of membrane proteins. J. Appl. Crystallogr. 36, 1372-1377 (2003).
- Caffrey, M., Cherezov, V. Crystallizing membrane proteins using lipidic mesophases. Nat. Protocols. 4, 706-731 (2009).
- Liu, W., Cherezov, V. Crystallization of membrane proteins in lipidic mesophases. J. Vis. Exp. (49), e2501 (2011).
- Cherezov, V., Peddi, A., Muthusubramaniam, L., Zheng, Y. F., Caffrey, M. A robotic system for crystallizing membrane and soluble proteins in lipidic mesophases. Acta Crystallogr. D Bio.l Crystallogr. 60, 1795-1807 (2004).
- Peddi, A. High-throughput automated system for crystallizing membrane proteins in lipidic mesophases. IEEE Trans. Autom. Sci. Eng. 4, 129-140 (2007).
- Cheng, A., Hummel, B., Qiu, H., Caffrey, M. A simple mechanical mixer for small viscous lipid-containing samples. Chem. Phys. Lipids. 95, 11-21 (1998).
- Caffrey, M. Crystallizing membrane proteins for structure-function studies using lipidic mesophases. Biochem. Soc. Trans. 39, 725-732 (2011).
- Caffrey, M. Crystallizing membrane proteins for structure determination: use of lipidic mesophases. Annu. Rev. Biophys. 38, 29-51 (2009).
- Caffrey, M. Membrane protein crystallization. J. Struct. Biol. 142, 108-132 (2003).
- Gushchin, I., Reshetnyak, A., Borshchevskiy, V., Ishchenko, A., Round, E., Grudinin, S., Engelhard, M., Buldt, G., Gordeliy, V. Active State of Sensory Rhodopsin II: Structural Determinants for Signal Transfer and Proton Pumping. J. Mol. Biol. 412, 591-600 (2011).
- Jordan, P., Fromme, P., Witt, H. T., Klukas, O., Saenger, W., Krauss, N. Three-dimensional structure of cyanobacterial photosystem I at 2.5 angstrom resolution. Nature. 411, 909-917 (2001).
- Grawert, T., Span, I., Eisenreich, W., Rohdich, F., Eppinger, J., Bacher, A., Groll, M. Probing the reaction mechanism of IspH protein by x-ray structure analysis. Proc. Natl. Acad. Sci. USA. 107, 1077-1081 (2010).
- Cherezov, V., Caffrey, M. Picolitre-scale crystallization of membrane proteins. J. Appl. Crystallogr. 39, 604-606 (2006).
- Li, D., Boland, C., Aragao, D., Walsh, K., Caffrey, M. Harvesting and cryo-cooling crystals of membrane proteins grown in lipidic mesophases for structure determination by macromolecular crystallography. J. Vis. Exp. (67), e4001 (2012).



