Summary
Водные двухфазных системах были использованы для одновременного картина несколько популяций клеток. Это быстрый и простой способ для сотовых паттерна использует преимущества фазового разделения водных растворов декстрана и полиэтиленгликоля и поверхностное натяжение, которое существует между двумя растворов полимеров.
Abstract
Сотовые паттерна технологий, которые являются быстрый, легкий в использовании и доступным будут необходимы для дальнейшего развития высокой пропускной способности ячейки анализы, платформы для изучения межклеточных взаимодействий и тканей инженерных систем. Это подробный протокол описывает метод для создания совместных культурах клеток с использованием биосовместимых решения декстрана (DEX) и полиэтиленгликоля (PEG), что поэтапный отдельные сочетании выше пороговых концентраций. Клетки могут быть узорными в различных конфигурациях, используя этот метод. Структурирование сотовых исключение может быть выполнена путем печати каплями DEX на подложке и покрывая их решения PEG, содержащий клетки. Поверхностного натяжения образуется между двумя растворов полимеров заставляет клетки падают вокруг внешней капли DEX и образуют круговую очистки, которые могут быть использованы для миграции анализов. Сотовые острова могут быть узорными по выдачи ячейки богатых DEX фазы в раствор ПЭГ или путем покрытия DEXкапли с раствором ПЭГ. Co-культур может быть сформирована непосредственно путем объединения ячейки исключения с структурирование DEX острова. Эти методы являются совместимыми с различными подходами обработки жидких, в том числе руководство micropipetting, и может быть использован практически с любым приверженцем типа клеток.
Introduction
Водные двухфазные системы (ATPSs) форме, когда решения двух несовместимых полимеров смешиваются при достаточно высоких концентрациях. Разделение фаз зависит от целого ряда факторов, которые включают молекулярный вес и полярности полимеры, температура решений, рН и ионной содержание водного растворителя 1, 2. Точка, в которой два полимерных растворов отдельные определяется физико-химическими свойствами выбранных фаз системы, но обычно происходит при низких концентрациях полимера (менее 20% вес / вес) в неденатурирующих условия, позволяющие ATPSs, которые будут использоваться для биотехнологии приложениям 3-9.
До сих пор наиболее широко изучены ATPS является полиэтиленгликоля (ПЭГ) / декстран (DEX) системы. ATPS, образованных этими недорогими и биосовместимых полимеров был впервые описан для очистки биомолекул путем молекулярного разбиение 2, 10. Разметкапроисходит, когда дополнительные молекулы или частицы, которые не способствуют фазная система смешивают с ПЭГ и DEX. На основе их относительного сходства либо DEX или PEG, молекул или частиц будет преимущественно находиться в одном из двух фаз или в интерфейсе. Еще одно свойство PEG / DEX ATPS является наличие поверхностного натяжения между двумя фазами полимера. ATPSs образована PEG и DEX обычно проявляют поверхностного натяжения, что значительно ниже, чем у других жидкостей двухфазных систем, таких как масло и вода, однако, поверхностное натяжение силы все еще оказывают влияние на мелкие частицы, такие как вирусы, клетки и белковых агрегатов 2 , 11-13. Наконец, с более высокой молекулярной массой ПЭГ и DEX отдельной при низких концентрациях (менее 5% вес / вес для высокого молекулярного веса полимеров сортов) в присутствии физиологических концентраций солей, есть мало, если вообще вредное воздействие на клетки млекопитающих включены в эти системы14-16.
В последнее время межфазных свойств и разделения эффектов ATPSs были применены нашей лаборатории для сотовых паттерна 14, 16-20. Это было достигнуто путем micropatterning решение плотнее DEX на подложках культуре клеток в присутствии ПЭГ. Когда клетки встраиваются в фазу PEG, они исключаются из входящих DEX капель в связи с PEG / DEX поверхностное натяжение 20. Когда клетки образцу в фазе DEX, они сохраняются на поверхности подложки культуре клеток поверхностного натяжения и перегородки 16, 17, 19.
В отличие от других методов для сотовых рисунка, ATPS ячейки паттерна проста в освоении и требует лишь элементарные знания о полимерах себя, и способность выполнять культуре клеток и использовать микропипетки. Другие методы для сотовых паттерна часто включают в себя специализированное оборудование и обучение, которые не легко переводятся в гоэлектронной науках о жизни. Например, некоторые методы (микроконтактной печати или печати на струйных принтерах) образец клеток косвенным путем применения модели биомолекулы клетки клея на подложку культуры, которые впоследствии служат в качестве объектов для прикрепления клеток 21, 22. Хотя косвенные подходы полезны для некоторых типов клеток, они требуют высокого уровня квалификации пользователя и специализированного оборудования для изготовления паттерна инструмент, и может не хватать специфику в зависимости от конкретного типа клеток / биомолекулы шаблону. Кроме того, клетки могут быть нанесены с высокой специфичностью картина путем прямого подхода паттернов, которые включают ламинарного потока рисунка, трафарету и струйной печати 23-26. Однако, эти методы также требуют опыта пользователя и специализированного оборудования, и может привести к повреждению клеток во время процесса печати. Хотя эти подходы обычно производят точные модели клетки, клетки рисунок, чтобы быть полезным инструментом в науках о жизни, оно должно быть экономически эффективнымя прост в реализации.
Здесь мы приводим подробный протокол для создания узорной использованием клеточных культур ATPSs описаны в наших ранее опубликованных приложений. Используя только micropipettors, пользователи могут создавать ячейки запретных зон или сотовый островов для миграции анализов. Это достигается путем PEG / DEX поверхностное натяжение, что либо сохраняет клетки в фазе DEX или исключает клетки на хранение в PEG фазы от DEX. По расчесывание этих двух основных методов структурирования, можно быстро генерировать совместных культурах клеток, таких как печень фибробластов со-культуры. Создание массивов методами, ATPS параметры и ожидаемые результаты описаны в деталях.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. Фазная система Характеристика: Определение пороговых значений для разделения фаз
- Подготовка растворов, содержащих ПЭГ и DEX в нужную ячейку буфера или культуральной среде, как показано на рисунке 1 (фиолетовые точки) в 15 мл или 50 мл конические пробирки. Далее, PEG и DEX будет относиться к 35 PEG кДа и 500 кДа DEX, однако, критическая концентрация будет меняться в зависимости от двух полимеров. Запись массы ПЭГ и DEX в каждом решении. Высокие концентрации растворов полимеров может занять несколько часов, чтобы раствориться. Встряхивания может быть использован для бессывороточной решений. Для сред, содержащих белки или сыворотку, поместите труб на этапе качалки, пока оба полимеров полного растворения. Запишите вес носителя, используемый для растворения полимеров и принять к сведению начальных концентрациях.
- После того, полимеры полностью растворяется, решения должны появиться облачность. Это первый признак того, что фазовое разделение произошло. Чтобы убедиться в этом, позволяющиеполимерные растворы, чтобы отдохнуть в вертикальном положении при комнатной температуре в течение 20 мин. Центрифугированием при 1000 XG может быть использован для ускорения процесса разделения фаз. Фазой плотной нижней будет DEX-богатых и верхней фазы будет PEG-богатых.
- Медленно добавить дополнительный буфер или средств массовой информации труб. Малый шаг должен быть использован, чтобы не промахиваться точки фазового разделения.
- Когда раствор станет прозрачным и не поэтапный отделяется после центрифугирования, порог для разделения фаз была достигнута. Запишите окончательный вес трубки.
- Используя предыдущие записанные весов для полимеров, наряду с конечной массы после добавления средства массовой информации, определить вес% / вес каждого из двух полимеров, при котором разделение фаз не возникает.
- Сюжет этих значений в% вес / вес PEG на оси у и% вес / вес DEX на оси х. Этот участок, известный как бинодальной кривой, может быть использована для определения пороговой концентрации для разделения фаз для различных concentratiДополнения ПЭГ / DEX в определенной среде для культивирования клеток.
2. Конфигурация 1: Исключение Создание массивов (96-а Формат плиты)
- Подготовка отдельных растворов 5,0% вес / вес PEG и 12,8% вес / вес DEX в клеточной среде культуры. Используйте ATPS решения, по крайней мере в два раза критической точки, чтобы ATPS остается после полимеров равновесия по отношению друг к другу. Существует небольшое количество потоков DEX в PEG-фазы, обогащенной и наоборот, поэтому, работая слишком близко к критической концентрации может привести к потере фазовой системы, как концентрация падает ниже критической точки. Кроме того, передача блюдо клеточной культуры для влажности и температуры контролируемой инкубатор может изменить двухфазной свойства и сделать два решения смешивается. Примечание: некоторые клетки могут работать лучше с другими составами ATPS. Приемлемые композиции могут быть выбраны на основе бинодали кривых определяется из части 1.
- Урожай клетки, которые будут использоваться для исключения Patterning. Определите общее количество / концентрация клеток в наличии. Дополнительно: маркировать клетки с CellTracker или других не-цитотоксических этикетки для флуоресцентной микроскопии.
- Осаждения клеток и ресуспендируют осадок в соответствующем объеме 5,0% PEG для достижения желаемого количества клеток для исключения. Например, в одной из лунок 96-луночный планшет требуется 37500 фибробластов быть суспендируют в 200 мкл PEG производить слияние на следующий день. Масштаб этих цифр по мере необходимости для других типов клеток и размеров культуры субстрата.
- С помощью микропипетки, не прибегает 0,5 мкл капли DEX на сухой субстрат для культивирования клеток. Увеличенная капли объемом производить большие зоны отчуждения. Капли размером от 0,1 до 1 мкл рекомендуется для исключения micropatterning. Дополнительно: DEX капли могут быть нанесены 24 часов впереди времени и позволила обезвоживают при комнатной температуре. Это может привести чистых моделей.
- Внесите 200 мкл клеточной суспензии PEG в тОн также чтобы покрыть DEX капель.
- Место в увлажненном инкубаторе в течение 12 ч при 37 ° C, 5% CO 2. Убедитесь, что антенна не наклонена в процессе обработки и что она находится на уровне полка инкубатор, чтобы избежать нарушения узоры.
- Снимите PEG раствор и вымыть три раза с 200 мкл культуральной среды.
- Добавить свежую питательную среду и возвращение в инкубаторе.
- Мониторинг культур периодически наблюдать клеточного движения в зоне отчуждения.
3. Конфигурация 2: Остров Создание массивов (96-луночный планшет формата)
- Подготовка решений 5,0% вес / вес PEG и 12,8% вес / вес DEX в культуре клеток среду, как указано выше.
- Урожай клетки будут использоваться для острова паттерна. Определите общее количество / концентрация клеток в наличии.
- Гранул и ресуспендируют клеток в соответствующем объеме на 12,8%, DEX, чтобы достичь желаемой концентрации клеток для формирования паттерна острова. Концентрации в 5000 CEООО / мкл или менее рекомендуется для высокой адгезией типов клеток. Для ячеек, которые имеют трудности присоединения или клетки, которые свободно придерживаться, концентрации до 10000 клеток / мкл может быть рассмотрен.
- Рабочие быстро, чтобы избежать высыхания, пипетка 0,5 мкл капли DEX на сухом субстрате культуры клеток, как описано выше. Не допускайте капель, чтобы высохнуть. Дополнительно: 200 мкл раствора ПЭГ могут быть добавлены к заблаговременно. DEX капли могут быть депонированы в раствор PEG, где они будут опускаться на дно и связаться с культурой поверхности. Это может привести к чистой модели острове.
- Накройте DEX капли с 200 мкл PEG.
- Место в увлажненном инкубаторе в течение 12 ч при 37 ° C, 5% CO 2. Убедитесь, что антенна не наклонена в процессе обработки и что она находится на уровне полка инкубатор, чтобы избежать нарушения узоры.
- Снимите PEG раствор и вымыть три раза с 200 мкл культуральной среды.
- Добавить свежую культурусредних и возвращение в инкубаторе.
- Мониторинг культур периодически наблюдать движение и пролиферации клеток наружу из островов.
4. Конфигурация 3: Исключение со-культур (96-луночный планшет формата)
- Подготовка решений 5,0% вес / вес PEG и 12,8% вес / вес DEX в культуре клеток среду, как указано выше.
- Урожай клетки будут использоваться для изоляции и остров паттерна. Определите общее количество / концентрация клеток доступные для каждого типа клеток. Дополнительно: Некоторые сотовые пары может появиться совершенно разные показатели распространения. Для предотвращения исключено клетки от overpopulating острова узорной клеток (особенно для долгосрочных культурах), относитесь клетки, используемые для исключения митомицином С в течение 2 часов или облучить их до уборки урожая. Это позволит предотвратить распространение. Флуоресцентные красители CellTracker могут быть использованы для различать две популяции клеток в случае необходимости.
- Осаждения клеток и ресуспендируют осадок для exclusioп паттерна в соответствующем объеме 5,0% PEG для достижения желаемого количества клеток, как указано выше. Ресуспендируют гранулы для формирования паттерна острове в соответствующем объеме 12,8% DEX для достижения желаемой концентрации клеток, как указано выше.
- С помощью микропипетки, не прибегает 0,5 мкл капли суспензии клеток DEX на сухой субстрат для культивирования клеток. Не допускайте капель, чтобы высохнуть.
- Накройте DEX капли с 200 мкл клеточной суспензии PEG.
- Место в увлажненном инкубаторе в течение 12 ч при 37 ° C, 5% CO 2. Убедитесь, что антенна не наклонена в процессе обработки и что она находится на уровне полка инкубатор, чтобы избежать нарушения узоры.
- Снимите PEG решения и мыть три раза в 200 мкл культуральной среды.
- Добавить свежую питательную среду и возвращение в инкубаторе.
- Контроль за со-культур наблюдать взаимодействие клеточных популяций. Дополнительно: Элементы управления могут быть получены путем проведения исключения или острова паттерна индивидуумыidually, путем совместного культуре клеток, которые не взаимодействуют или путем блокирования путей интерес в одной или обеих популяций клеток до и после рисунка.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Чтобы выбрать соответствующую комбинацию ПЭГ и DEX для сотовых паттерна важно для определения бинодали кривой. Эта кривая очерчивает точки, в которых ATPS могут образовываться и может варьироваться для данного набора полимеров в зависимости от температуры, рН и ионного состава. Для культивирования клеток, которые требуют настроены составы средних может быть необходимым, чтобы экспериментально определить бинодали кривой. Это достигается путем создания ряда ATPSs, которые далеки от бинодали и различного в их PEG и DEX содержимое (рис. 1, фиолетовые круги). Когда ATPS присутствует, растворы полимеров появится облачно, когда смешиваются и сравняет на отдельные фазы, если не спокойно. При добавлении дополнительного растворителя к смеси полимеров, ATPS подойдет 0% PEG / 0% DEX. В какой-то момент, смесь больше не будет поэтапно отдельно. PEG / DEX концентрация, при которой это происходит, представляет точку на кривой бинодали, а выше этой точки ATPS могут образовываться и ниже этой точки не может. Кривые на рисунке 1 представляет binodals для трех общих клеточной культуре средств массовой информации и без 10% эмбриональной телячьей сыворотки (FBS). Концентрациях, при которых ATPS образуется несколько выше, в присутствии FBS.
В наших предыдущих докладах, мы использовали ATPSs на основе критической точки (точки на бинодали, при которой равные объемы PEG и DEX форму после уравновешивания) на 2,5% ПЭГ 35% kDa/3.2 DEX 500 кДа. Результаты нашего бинодали данные находятся в непосредственной близости к этой критической точке. Мы протестировали девять фазе комбинации системы для формирования паттерна, как показано в таблице 1. С чистого решения PEG и DEX равновесие по отношению к их концентрации полимера после того, как они сочетаются, некоторые из этих решений не образуют стабильных ATPSs, и поэтому не полезно для структурирования (Таблица 1а, х знаков). Другие комбинации полимера узнаваемых моделей, Но не были достаточно равномерно для экспериментов (Таблица 1а х / ✓ знаков). Полезные составы полимера, образованного запретных зон и островов, которые были почти без клеток в не-узорные регионах (Таблица 1а, ✓ знаков).
С 10% PEG, мы заметили, что морфология клеток была аномально круглые и шпинделя, как после 24 часов, с клетками отображения уменьшенной способностью прикрепляться к поверхности культуры (Таблица 1b, х знаков). Морфология и привязанности были нормальными на 2,5% и 5% ПЭГ (Таблица 1b, ✓ знаков). Мы заметили, что сыворотка осажденного из культуральной среды при высоких концентрациях ПЭГ (таблица 1с, х баллов), что свидетельствует о ненормальной морфологии клеток и вложения в 10% ПЭГ может быть связано с проблемами с сывороткой доступа. Кроме того, PEG, как известно, нарушают плазматических мембран 27. Хотя эти эффекты наблюдаются только при высоких концентрациях низкой молecular PEG весом, то лучше использовать низкие концентрации PEG, который производит надежные паттерна.
В соответствии с нашими предыдущими докладами, мы пришли к выводу, что 5% PEG/6.4 DEX% и 5% PEG/12.8% DEX были хорошо подходят для мобильных рисунка, с 12,8% DEX производства более равномерного моделей. Ожидаемые результаты для трех паттернов форматы, используя сотовый Tracker-меченых клеток HeLa показано на рисунке 2. Следуя каждого паттерна подход, можно создать единую моделей каждого типа, с очень мало клеток вне узорные области.
Использование изоляции и остров паттерна можно оценить пролиферацию и миграцию клеток с рисунком (рис. 3). В течение трех дней, заполненных клеток HeLa запретных зон (рис. 3а-в). Остров узором клетки расширена в направлении от начальной модели (рис. 3d-е). Эти изменения могут быть количественно с помощьюстандартные ImageJ средств измерений (рис. 3, е). Важно отметить, что, когда несколько клеточных популяций являются со-культурный (рис. 2, формат 3), популяция клеток может размножаться вне и заменить другим. Структурирование отчуждения и острова паттерна могут быть полезными инструментами для оценки, если это будет проблемой. В ситуации, когда значительные различия в индекс пролиферации происходит, то рекомендуется, чтобы одна популяция клеток лечить облучением или химическими факторами для ограничения его распространения. Это особенно полезно в ситуациях, когда один тип клеток используется в качестве поддержки ячейки для медленных становится все более чувствительным типом клеток.
Мы продемонстрировали этот принцип культивирования клеток HepG2, клетки гепатоцеллюлярной карциномы линии, которая обычно используется для модели гепатоцитов биологии, с NIH 3T3 фибробласты, которые были арестованы использованием митомицина С (рис. 4). Со временем клетки HepG2 поддерживать их локализацииD колонии формы (рис. 4а). Размещая много капель в ту же пластинку и окружающие их с фибробластами можно выращивать эти клетки в формате, который является потенциально полезной для мультиплексированных исследований (рис. 4б). Сотовые острова монокультур могут быть использованы с этим форматом, как контроль за влиянием паракринной факторов (рис. 4в).
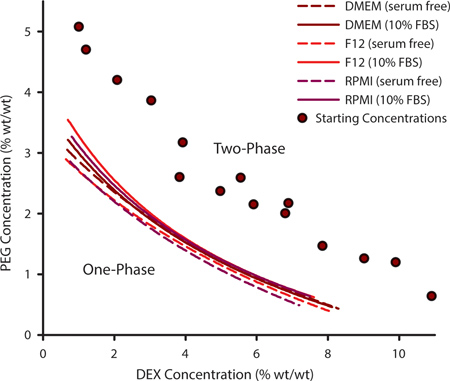
Рисунок 1. Полимер концентраций, при которых ATPS могут образовывать могут быть экстраполированы из экспериментально определенных бинодали кривые. Эта бинодали кривая была построена с использованием метода помутнения путем добавления дополнительных растворителей для измерения точек, в которых двухфазной смеси различных PEG / DEX концентрации (фиолетовая кружки) не были способны фазы separatiнг. Binodals были определены для DMEM, RPMI F12 и с и без сыворотки. Данные пункты были оснащены три параметра рациональной функции. N = 3 для каждой точки данных.

Рисунок 2. По дозирования ATPS решений на пенополистирольных плит, трех форматов для мобильных паттерна может быть произведено. Процедура начинается с помощью пипетки DEX капель), которые затем покрывают PEG б). Как только клетки приложить, ATPS решения могут быть смыты и заменена культуральной среды (C, D). Флуоресцентных изображений для монокультур окрашивали CellTracker красителей после рисунка. Для совместного культуры, клетки окрашивали отдельно с CellTracker красителей, прежде чем кучность стрельбы. HeLa клетки были использованы для создания всех трех форматов культуры. 
Рисунок 3. Структурирование отчуждения и острова паттерна может быть использован для оценки миграции и пролиферации клеток.) Исключение узорной HeLa клеток через 1 день после рисунка. Б) исключения узорной HeLa клеток через 3 дня после рисунка. С) Клетки размножаются и мигрируют, что значительно сокращает размер зона отчуждения. г) острова узором клетки HeLa 1 день после рисунка. е) острова узором HeLa клеток через 3 дня после рисунка. е) Клетки размножаются и мигрируют наружу, значительно расширяя размер острова. Изображения были количественно с использованием ImageJ программное обеспечение для измерения очистки ячейки и диапазоны ячеек острова до и после миграции. Столбики означают± SEM, по крайней мере, три независимых наблюдений.

Рисунок 4. Клеток печени / культуры фибробластов может быть создан с помощью ATPS исключения совместного культивирования паттерна.) Эти колонии сохранить свою организацию в течение 4 дней в культуре. Б) Несколько островов можно облеченные в одном блюде с потенциалом для мультиплексированных или высокой пропускной способностью анализы. с) по сравнению с не-со-культурных моделей острове, совместно культивируемых клеток отображать несколько выше уровня альбумина производства (коричневая окраска), как видно из качественного сравнения альбумина окрашенных со-культур по сравнению с монокультур. Альбумин является белок, вырабатываемый клетками печени. Таким образом, этот результат свидетельствует о том, что функция клеток печени усиливается при совместном культивировании с использованием фибробластов ATPS.
| а) структуры, образованной | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | х | х | х |
| PEG 5,0% | х / ✓ | ✓ | ✓ |
| PEG 10,0% | х / ✓ | ✓ | ✓ |
| б) морфология | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | ✓ | ✓ | ✓ |
| PEG 5,0% | ✓ | ✓ | & # Х2713; |
| PEG 10,0% | х | х | х |
| в) Сыворотка осадков | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | ✓ | ✓ | ✓ |
| PEG 5,0% | ✓ | ✓ | ✓ |
| PEG 10,0% | х | х | х |
Таблица 1.) ATPS формулировки, которые могут быть использованы для структурирования обозначены флажками, те, которые не обозначены знаками х. Б) препараты, которые сохраняют нормальную морфологию клеток и привязанности свойства указано бУ галочки, те, которые не обозначены знаками х. с) Составы, в результате осаждения белков сыворотки крови обозначаются знаками х.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Micropatterning ATPS ячейки метод требует очень мало знаний, помимо знания методов культуры клеток и могут быть быстро освоены. Преимущества этого подхода в том, что он является недорогим, быстрым и совместимы с различными типами клеток и культуры форматов. По этим причинам, наш протокол должен быть легко принята жизни ученых, особенно тех, кто изучает клеточную пролиферацию, миграцию и хемотаксис, и влияние juxtacrine и паракринной взаимодействия между клеточной популяции. Анализы, представленные здесь может быть легко количественно на уровне клеточных популяций с использованием стандартных процедур анализа изображений, доступных в программном обеспечении, таких как ImageJ.
Для создания закономерности мы рекомендуем следующие меры предосторожности. Во-первых, пипетки использоваться для дозирования раствора DEX должен быть изменен после каждой капли DEX на хранение для обеспечения более последовательного объема капли. Поскольку решение DEX относительно вязкий, Важно также, чтобы избежать сдачи на хранение избыточных DEX, которые могут присутствовать на внешней поверхности кончика пипетки и обеспечить, чтобы весь объем выхода DEX чаевых. Во-вторых, капли могут двигаться, если PEG добавляют слишком энергично или если блюдо наклонена. DEX нарушения можно свести к минимуму, сохраняя блюдо на ровную поверхность и позволяет PEG решение постепенно покрывать каплями сверху, не допуская больших сил с PEG мениска, чтобы выбить часть капли. Капля нарушение встречается чаще, с крупными каплями DEX, так что капли 0,5 мкл или менее следует использовать, если это возможно. Помимо этих технических вопросов, связанных с выдачей решения, существует очень мало подводных камней, связанных с этой техникой, при условии, что соответствующий полимер молекулярной массы и концентрации используется.
Хотя ATPS паттерна можно легко выполнить с помощью микропипетки (как показано здесь), есть множество более Sophisticated подходы, которые могут быть использованы для быстрого создания моделей более сложных геометрических массивов (например, жидкого робота обработки и акустических выброса капли), представленные в наших предыдущих исследованиях 14, 15, 20. Кроме того, можно генерировать DEX капли, которые намного меньше в объеме на пневматическим извлечения DEX через капиллярные отверстия или путем приведения отверстие в микроканале производить текущий DEX капель обшитые PEG 19. Эти подходы могут представлять интерес для тех, кто ищет для получения высокой пропускной способностью или мультиплексированных совместного культивирования или миграции анализов. Кроме того, используя микрофлюидных подхода, можно проводить эксперименты с небольшим количеством клеток, или клеток в микроканале, где влияние жидкости и просто могут быть рассмотрены. Тем не менее, эти передовые методы не являются обязательными для большинства приложений.
Водный двухфазный паттерн клеток является простой и легко адаптирована к типичным клеткикультуры обстановке. Этот метод позволяет любому исследователю доступ к типичной лаборатории клеточных культур (доступ к капот, CO 2 инкубаторе, и микропипетки) и вышеупомянутых полимеров воспроизводимо картина клеток в монокультуре и со-культуры. Наша лаборатория продемонстрировала эту возможность печати массивы ячеек для изучения миграции клеток в анализе заживления ран и для изучения последствий juxtacrine и паракринной сигнализации в дифференциации эмбриональных клеток, 16, 17, 20. Другие методы, в том числе структурирование внеклеточного матрикса 28, струйной печати 29 и структурирование по ламинарного течения в микрофлюидных устройств 25, 26 также используются для локализации клеток. Эти и другие методы эффективного подхода к достижению четко определенных моделей клеток и часто может достичь одноклеточных точностью. Однако, эти методы требуют также высоко специализированного оборудования и / или доступа к чистой комнаты объекты для изготовления печатей, используемых в PRInt белки внеклеточного матрикса или производить микрофлюидики устройств. Их подключение к источнику питания, шприцевые насосы, и другие внешние компоненты также затрудняет их реализацию за счет расходов, связанных с оборудованием и пользовательских навыков, необходимых для ее эксплуатации.
С точки зрения будущих приложений, мы ожидаем, что наш метод будет полезен для развития культуры систем, которые обеспечивают высокую пропускную анализ движения и пролиферации клеток, а также исследование межклеточных взаимодействий между несколькими клеточных популяций. До этого момента наши отчеты были сосредоточены на изучении взаимодействия только несколько видов узорной клетки сразу. Тем не менее, можно предположить, что многие субпопуляции клеток можно культивировать с общим слоем подачи исследовать влияние паракринной и juxtacrine сигнализации многих типах клеток срослись в одну установку клеточной культуры. Наконец, приложения тканевой инженерии часто требуется пространственной локализацииодин или несколько типов клеток. Это может быть возможным, чтобы адаптировать нашу технику для использования в паттерн клеток с целью получения более физиологически соответствующие ткани инженерных моделях болезни или шаблон клеток на имплантируемые материалы для клинического применения.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Авторы не конкурирующих финансовых интересов.
Acknowledgments
Эта работа была поддержана фондом Coulter, Бейстер фонда, Бакалавриат Возможности исследований (UROP) летние программы для ATA и National Science Foundation Graduate Student Research Fellowship (грант № DGE 0718128, ID:. 2010101926) для JBW.
Materials
| Name | Company | Catalog Number | Comments |
| Dextran 500,000 kDa | Pharmacosmos, Denmark | ||
| Polyethylene Glycol 35,000 kDa | Sigma-Aldrich, St. Louis, MO | ||
| Hela | ATCC, Manassas, VA | ||
| HepG2 C3A | ATCC, Manassas, VA | ||
| NIH 3T3 | ATCC, Manassas, VA | ||
| Cell Tracker | Invitrogen, Carlsbad, CA | ||
| DMEM | Gibco, Carlsbad, CA | ||
| RPMI | Gibco, Carlsbad, CA | ||
| F12 | Gibco, Carlsbad, CA | ||
| Fetal Bovine Serum | Gibco, Carlsbad, CA |
References
- Hatti-Kaul, R. Aqueous two-phase systems : methods and protocols. Methods in biotechnology. xiii, Humana Press. 440 (2000).
- Albertsson, P. A. k Partition of cell particles and macromolecules: separation and purification of biomolecules, cell organelles, membranes, and cells in aqueous polymer two-phase systems and their use in biochemical analysis and biotechnology. , 3rd ed, Wiley. 346 (1986).
- Yamada, M., et al. Continuous cell partitioning using an aqueous two-phase flow system in microfluidic devices. Biotechnol. Bioeng. 88 (4), 489-494 (2004).
- Soohoo, J. R., Walker, G. M. Microfluidic aqueous two phase system for leukocyte concentration from whole blood. Biomed. Microdevices. 11 (2), 323-329 (2009).
- Hahn, T., Hardt, S. Concentration and size separation of DNA samples at liquid-liquid interfaces. Anal. Chem. 83 (14), 5476-5479 (2011).
- Hatti-Kaul, R. Aqueous two-phase systems. A general overview. Mol. Biotechnol. 19 (3), 269-277 (2001).
- Hustedt, H., Kroner, K. H., Menge, U., Kula, M. -R. Protein recovery using two-phase systems. Trends in Biotechnology. 3 (6), 139-144 (1985).
- Keating, C. D. Aqueous Phase Separation as a Possible Route to Compartmentalization of Biological Molecules. Acc Chem. Res. 45 (12), 2114-2124 (2012).
- Helfrich, M. R., et al. Partitioning and assembly of metal particles and their bioconjugates in aqueous two-phase systems. Langmuir. 21 (18), 8478-8486 (2005).
- Diamond, A. D., Hsu, J. T. Prote. Partitioning in PEG/Dextran Aqueous Two-Phase Systems. AIChE Journal. 36 (7), 1017-1024 (1990).
- Y-T,, Zhu, Z. -Q. Modeling of interfacial tension of aqueous two-phase systems. Chemical Engineering Science. 54 (4), 433-440 (1999).
- Liu, Y., Lipowsky, R., Dimova, R. Concentration dependence of the interfacial tension for aqueous two-phase polymer solutions of dextran and polyethylene glycol. Langmuir. 28 (8), 3831-3839 (2012).
- Rha, C. Interfacial Tension of Polyethylene Glycol/Potassium Phosphate Aqueous Two-Phase Systems. Physics and Chemistry of Liquids: An International Journal. 38 (1), 25-34 (2000).
- Fang, Y., et al. Rapid Generation of Multiplexed Cell Cocultures Using Acoustic Droplet Ejection Followed by Aqueous Two-Phase Exclusion Patterning. Tissue Eng. Part C. Methods. 18 (9), 647-657 (2012).
- Tavana, H., et al. Nanolitre liquid patterning in aqueous environments for spatially defined reagent delivery to mammalian cells. Nat. Mater. 8 (9), 736-741 (2009).
- Tavana, H., Mosadegh, B., Takayama, S. Polymeric aqueous biphasic systems for non-contact cell printing on cells: engineering heterocellular embryonic stem cell niches. Adv. Mater. 22 (24), 2628-2631 (2010).
- Tavana, H., et al. Microprinted feeder cells guide embryonic stem cell fate. Biotechnol. Bioeng. , (2011).
- Tavana, H., Takayama, S. Aqueous biphasic microprinting approach to tissue engineering. Biomicrofluidics. 5 (1), 13404 (2011).
- Frampton, J. P., et al. Precisely targeted delivery of cells and biomolecules within microchannels using aqueous two-phase systems. Biomed. Microdevices. 13 (6), 1043-1051 (2011).
- Hossein Tavana, K. K., Bersano-Begey, T., Luker, K. E., Luker, G. D., Takayama, S. Rehydration of Polymeric, Aqueous, Biphasic System Facilitates High Throughput Cell Exclusion Patterning for Cell Migration Studies. Advanced Functional Materials. 21 (15), 2920-2926 (2011).
- Falconnet, D., et al. Surface engineering approaches to micropattern surfaces for cell-based assays. Biomaterials. 27 (16), 3044-3063 (2006).
- Lim, J. Y., Donahue, H. J. Cell sensing and response to micro- and nanostructured surfaces produced by chemical and topographic patterning. Tissue Eng. 13 (8), 1879-1891 (2007).
- Ringeisen, B. R., et al. Jet-based methods to print living cells. Biotechnol. J. 1 (9), 930-948 (2006).
- Wright, D., et al. Generation of static and dynamic patterned co-cultures using microfabricated parylene-C stencils. Lab Chip. 7 (10), 1272-1279 (2007).
- Takayama, S., et al. Patterning cells and their environments using multiple laminar fluid flows in capillary networks. Proc. Natl. Acad. Sci. U.S.A. 96 (10), 5545-5548 (1999).
- Berthier, E., et al. Pipette-friendly laminar flow patterning for cell-based assays. Lab Chip. 11 (12), 2060-2065 (2011).
- Davidson, R. L., O'Malley, K. A., Wheeler, T. B. Polyethylene glycol-induced mammalian cell hybridization: effect of polyethylene glycol molecular weight and concentration. Somatic Cell Genet. 2 (3), 271-280 (1976).
- Johnson, D. M., LaFranzo, N. A., Maurer, J. A. Creating Two-Dimensional Patterned Substrates for Protein and Cell Confinement. J. Vis. Exp. (55), e3164 (2011).
- Moon, S., Lin, P., Keles, H. O., Yoo, S., Demirci, U. Title Cell Encapsulation by Droplets. J. Vis. Exp. (8), e316 (2007).



