Summary
Wässriger Zweiphasensysteme wurden gleichzeitig Muster mehrere Populationen von Zellen verwendet. Dieses schnelle und einfache Methode zur Musterbildung Zelle nutzt die Phasentrennung der wässrigen Lösungen von Dextran und Polyethylenglycol und die Grenzflächenspannung zwischen den beiden Polymerlösungen besteht.
Abstract
Zelle Strukturierung Technologien, die schnell, einfach zu bedienen und erschwinglich sind, werden für die zukünftige Entwicklung von Hochdurchsatz-Zell-Assays, Plattformen zur Untersuchung von Zell-Zell-Interaktionen und Gewebe technischer Systeme benötigt werden. Diese detaillierte Protokoll beschreibt ein Verfahren zum Erzeugen von Co-Kulturen von Zellen unter Verwendung von biokompatiblen Lösungen von Dextran (Dex) und Polyethylenglykol (PEG), die Phasentrennung bei über dem Schwellenwert Konzentrationen kombiniert. Zellen können in einer Vielzahl von Konfigurationen unter Verwendung dieses Verfahrens strukturiert werden. Zellausschlussschicht Strukturierung kann durch Drucken von Tröpfchen DEX auf einem Substrat und Abdecken mit einer Lösung von PEG mit Zellen durchgeführt werden. Die Grenzflächenspannung zwischen den beiden Polymerlösungen gebildet bewirkt Zellen um die Außenseite des DEX Tröpfchens fallen und bilden eine kreisförmige Lichtung die für die Migration Assays verwendet werden kann. Zelle Inseln können durch den Verzicht auf eine Zelle reichen DEX Phase in eine PEG-Lösung oder durch Abdecken des DEX strukturiert werdenTröpfchen mit einer Lösung von PEG. Co-Kulturen können direkt durch die Kombination Zellausschlussschicht mit DEX Insel Strukturierung gebildet werden. Diese Verfahren sind mit einer Vielzahl von Liquid-Handling Ansätze, einschließlich manueller Mikropipettiervorrichtung und können mit nahezu jedem adhärenten Zelltyp eingesetzt werden.
Introduction
Wässriger Zweiphasensysteme (ATPSs) bilden, wenn Lösungen aus zwei inkompatiblen Polymeren miteinander bei ausreichend hohen Konzentrationen vermischt. Phasentrennung wird durch eine Vielzahl von Faktoren, die das Molekulargewicht und die Polarität der Polymeren, Temperatur der Lösung, pH-Wert und ionischen Gehalt der wässrigen Lösungsmittel 1, 2 umfassen beeinflusst. Der Punkt, an dem die beiden Polymerlösungen separaten von den physikochemischen Eigenschaften des ausgewählten Phasen-System bestimmt wird, sondern erfolgt in der Regel bei niedrigen Polymer Konzentrationen (weniger als 20% wt / wt) unter nicht-denaturierenden Bedingungen, wodurch ATPSs für Biotechnologie eingesetzt werden Anwendungen 3-9.
Die mit Abstand am intensivsten untersuchten ATPS ist die Polyethylenglykol (PEG) / Dextran (DEX) System. Die ATPS durch diese kostengünstig und biokompatiblen Polymeren gebildet wurde ursprünglich zur Reinigung von Biomolekülen über molekulare Partitionierung 2, 10 beschrieben. Abtrennungtritt bei zusätzlichen Molekülen oder Partikeln, die nicht dem Phasensystem beitragen mit PEG und DEX werden gemischt. Basierend auf ihren relativen Affinitäten für entweder DEX oder PEG, werden die Moleküle oder Teilchen bevorzugt in einer der beiden Phasen oder an der Schnittstelle befinden. Eine weitere Eigenschaft des PEG / DEX ATPS ist die Existenz der Grenzflächenspannung zwischen den beiden Polymer-Phasen. ATPSs von PEG und DEX gebildet zeigen im Allgemeinen Grenzflächenspannungen, die viel niedriger als in anderen Flüssig-Flüssig-Zwei-Phasen-Systeme wie Öl und Wasser, aber die Grenzflächenspannung Kräfte üben noch immer Auswirkungen auf kleine Partikel wie Viren, Zellen und Proteinaggregate 2 , 11-13. Da schließlich höhermolekularen PEG und DEX separaten bei niedrigen Konzentrationen (weniger als 5% Gewicht / Gewicht für Polymere mit hohem Molekulargewicht Sorten) in Anwesenheit von physiologischen Konzentrationen von Salzen, gibt es wenige oder gar keine schädlichen Wirkungen auf Säugetierzellen innerhalb dieser eingearbeitet Systeme14-16.
Kürzlich haben die Grenzflächeneigenschaften und Partitionierung Wirkungen ATPSs von unserem Labor für Zelle Strukturieren 14, 16-20 angewandt. Dies wurde durch Mikrostrukturierung eine dichtere Lösung auf DEX Zellkultursubstraten in Gegenwart von PEG durchgeführt. Wenn Zellen in die PEG-Phase eingearbeitet sind, werden sie aus der Eingabe der DEX Tröpfchen aufgrund PEG / DEX Grenzflächenspannung 20 ausgeschlossen. Wenn Zellen in der DEX Phase gemustert werden, werden sie an der Oberfläche des Substrats durch Zellkultur Grenzflächenspannung und Partitionierung 16, 17, 19 beibehalten.
Im Gegensatz zu anderen Verfahren zur Musterbildung Zelle ist ATPS Zelle Strukturieren einfach zu erlernen und erfordert nur rudimentäre Wissen über die Polymere selbst, und die Fähigkeit zur Zellkultur durchzuführen und eine Mikropipette. Andere Methoden zur Zelle Strukturierung beinhalten oft spezielle Ausrüstung und Ausbildung, die nicht leicht zu th übersetzte Life Sciences. Zum Beispiel können einige Methoden (Mikrokontaktdrucken oder Tintenstrahldruck)-Muster Zellen indirekt durch Aufbringen von Mustern zelladhäsive Biomoleküle an einem Kultursubstrat, das anschließend als Stellen für die Zellanheftung 21, 22 dienen. Obwohl indirekten Ansätzen nützlich für einige Zelltypen sind, erfordern sie einen hohen Grad an Geschicklichkeit und Benutzers Spezialausrüstung die Musterbildung Werkzeug herzustellen, und können Spezifität fehlt Abhängigkeit von der speziellen Zelltyp / Biomolekül Muster. Alternativ können Zellen, die mit hoher Spezifität Muster durch direkte Strukturierung Ansätze, die laminare Strömung Strukturieren, stenciling und 23-26 gehören Tintenstrahldruck abgeschieden werden. Jedoch erfordern diese Techniken auch Benutzerexpertise und Spezialausrüstung und kann Zellen während des Druckprozesses zu beschädigen. Obwohl diese Ansätze in der Regel produzieren präzise Muster der Zellen, Zell-Strukturierung ein nützliches Werkzeug in den Lebenswissenschaften zu sein, muss es kostengünstig a seinnd einfach zu implementieren.
Hier berichten wir über ein detailliertes Protokoll zur Erzeugung von strukturierten Zellkulturen mit den ATPSs in unserem zuvor veröffentlichten Anwendungen beschrieben. Mit nur Mikropipetten können Anwender Zellausschlussschicht Zonen oder Zelle Inseln Zellmigrationsassays. Dies wird mittels PEG / DEX Grenzflächenspannung, die entweder beibehält Zellen im DEX Phase oder schließt Zellen in der PEG-Phase vom abgeschiedenen DEX erreicht. Durch Kämmen diese beiden grundlegenden Strukturieren Techniken ist es möglich, schnell zu generieren Co-Kulturen von Zellen wie Leber-Fibroblastenzelle Co-Kulturen. Strukturierungsverfahren, ATPS Parametern und erwarteten Ergebnisse sind in Einzelheiten beschrieben.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
Ein. Phase-System Charakterisierung: Ermittlung Schwellenwerte für Phase Separation
- Planen Lösungen enthaltend PEG und DEX in dem gewünschten Puffer oder Zellkulturmedium, wie in Figur 1 (lila Punkte) in 15 ml oder 50 ml konischen Röhrchen gezeigt. Im Folgenden wird PEG und DEX auf 35 kDa PEG und 500 kDa DEX beziehen, aber kritischen Konzentrationen ändert sich je nach den beiden Polymeren verwendet. Notieren Sie sich die Masse von PEG und DEX in jeder Lösung. High-Konzentration Polymerlösungen kann mehrere Stunden dauern, sich aufzulösen. Vortexen für Serum-freie Lösungen verwendet werden. Für Medien, die Proteine oder Serum, legen Sie die Rohre auf einer rocken Stufe bis beide Polymere vollständig gelöst sind. Das Gewicht der verwendeten Medien, die Polymere auflösen und beachten Sie die anfänglichen Konzentrationen.
- Sobald die Polymere vollständig gelöst sind, sollten die Lösungen erscheinen möglich. Dies ist der erste Hinweis darauf, dass eine Phasentrennung erfolgt ist. Um dies zu bestätigen, damit diePolymerlösungen in vertikaler Position bei Raumtemperatur für 20 Min. ruhen. Zentrifugation bei 1000 xg kann die Phasentrennung zu beschleunigen. Je dichter untere Phase wird DEX-reich sein und die obere Phase wird PEG-reichen sein.
- Langsam fügen zusätzlichen Puffer oder Medien an den Rohren. Kleinen Schritten sollte, um nicht die Überschwingen Phasentrennungspunkt verwendet werden.
- Wenn die Lösung klar wird, und nicht mehr phasensepariert nach Zentrifugation wird der Schwellenwert für die Phasentrennung erreicht wurde. Aufzeichnen das Endgewicht des Rohres.
- Verwendung der vorherigen aufgezeichneten Gewichte für die Polymeren, zusammen mit dem Endgewicht nach Zugabe Medien bestimmen% Gew. / Gew. von jedem der beiden Polymere bei dem eine Phasentrennung nicht mehr auftritt.
- Plotten diese Werte als% Gew / Gew PEG auf der y-Achse und% wt / wt DEX auf der x-Achse. Dieser Plot, wie die binodale Kurve bekannt ist, kann verwendet werden, um den Schwellenwert-Konzentration für eine Phasentrennung für unterschiedliche concentrati bestimmenons von PEG / DEX in einer bestimmten Zellkulturmedium.
2. Konfiguration 1: Ausschluss Strukturierung (96-well Platte Format)
- Planen getrennte Lösungen von 5,0% w / w PEG und 12,8% Gew. / Gew. DEX in Zellkulturmedium. Verwenden ATPS Lösungen von mindestens dem Doppelten der kritischen Punktes, um sicherzustellen, dass ein ATPS nachdem die Polymere mit Bezug zueinander äquilibrieren bleibt. Es gibt eine kleine Menge des Flusses von DEX in die PEG-reichen Phase und umgekehrt, also arbeiten zu nahe der kritischen Konzentration kann zu einem Verlust des Phasensystems als Konzentrationen Unterschreiten kritischer Punkt führen. In ähnlicher Weise kann die Übertragung der Zellkulturschale zu einer Feuchte-und Temperatur-kontrollierten Inkubator verändern die zweiphasige Eigenschaften und stellen die beiden Lösungen mischbar. Hinweis: Einige Zellen können besser mit anderen ATPS Formulierungen. Akzeptablen Formulierungen können basierend auf den binodale Kurven aus Teil 1 bestimmt, ausgewählt werden.
- Ernten Sie die Zellen, die zur Ausgrenzung patte verwendet werdenrning. Ermitteln Sie die Gesamtzahl / Konzentration von Zellen zur Verfügung. Optional: Kennzeichnen der Zellen mit CellTracker oder andere nicht-zytotoxischen Etiketten für die Fluoreszenzmikroskopie.
- Pelletieren der Zellen und Resuspendieren des Pellets in einem geeigneten Volumen von 5,0% PEG, um die gewünschte Anzahl von Zellen für den Ausschluss erreichen. Zum Beispiel erfordert eine Vertiefung einer 96-Well-Platte 37.500 Fibroblastenzellen in 200 ul der PEG resuspendiert werden bis zur Konfluenz produzieren des folgenden Tages. Skalieren diese Zahlen als geeignet für andere Zelltypen und Kultur Substrat Größen.
- Mit einer Mikropipette, verzichten 0,5 ul Tröpfchen DEX auf ein trockenes Zellkultursubstrat. Größeres Volumen Tröpfchen größere Sperrzonen. Tröpfchen mit einer Größe von 0,1 bis 1 ul werden für den Ausschluss Mikrostrukturierung empfohlen. Optional: DEX Tröpfchen können 24 Stunden vor der Zeit abgelagert werden und bei Raumtemperatur zu entwässern. Dies kann zu saubereren Muster.
- Geben Sie 200 ul PEG Zellsuspension in ter gut zur Deckung der DEX Tröpfchen.
- In einem befeuchteten Inkubator für 12 Stunden bei 37 ° C, 5% CO 2. Stellen Sie sicher, dass das Gericht nicht bei der Handhabung und dass es auf einem Niveau Inkubator Regal gestellt zu verhindern, dass die Muster gekippt.
- Entfernen Sie die PEG-Lösung und dreimal mit 200 ul Kulturmedium.
- Fügen Sie frisches Kulturmedium und Rückkehr in den Inkubator.
- Überwachen Sie die Kulturen in regelmäßigen Abständen zu Zelle Bewegung in der Sperrzone zu beobachten.
3. Konfiguration 2: Island Strukturierung (96-well Platte Format)
- Planen Lösungen von 5,0% w / w PEG und 12,8% Gew. / Gew. DEX in Zellkulturmedium wie oben.
- Ernten Sie die Zellen, die zur Insel Strukturierung verwendet werden. Ermitteln Sie die Gesamtzahl / Konzentration von Zellen zur Verfügung.
- Pellet und Zellen in einem geeigneten Volumen von 12,8% DEX, um die gewünschte Konzentration der Zellen für die Insel Strukturierung zu erreichen. Konzentrationen von 5.000 cells / ul oder weniger sind für stark haftende Zelltypen empfohlen. Für Zellen, die Schwierigkeiten Anbringen oder Zellen, die lose anhaften haben, Konzentrationen von bis zu 10.000 Zellen / ul in Betracht.
- Arbeitet schnell zu vermeiden Trocknen Pipette 0,5 ul Tröpfchen von DEX auf ein trockenes Zellkultursubstrat, wie oben beschrieben. Lassen Sie keine Tröpfchen zu trocknen. Optional: 200 ul PEG-Lösung kann der gut aufgenommen der Zeit voraus sein. DEX Tröpfchen können dann in der PEG-Lösung, wo sie auf den Boden sinken wird, und wenden die Kultur Oberfläche abgeschieden werden. Dies kann zu saubereren Inselmuster.
- Bedecken Sie die DEX Tröpfchen mit 200 ul PEG.
- In einem befeuchteten Inkubator für 12 Stunden bei 37 ° C, 5% CO 2. Stellen Sie sicher, dass das Gericht nicht bei der Handhabung und dass es auf einem Niveau Inkubator Regal gestellt zu verhindern, dass die Muster gekippt.
- Entfernen Sie die PEG-Lösung und dreimal mit 200 ul Kulturmedium.
- Fügen Sie frisches Kulturmediummittel-und Rückkehr in den Inkubator.
- Überwachen Sie die Kulturen regelmäßig Zellbewegung und Proliferation nach außen von den Inseln zu beobachten.
4. Konfiguration 3: Ausschluss Co-Kulturen (96-well Platte Format)
- Planen Lösungen von 5,0% w / w PEG und 12,8% Gew. / Gew. DEX in Zellkulturmedium wie oben.
- Ernten Sie die Zellen, die zur Ausgrenzung und Insel Strukturierung verwendet werden. Ermitteln Sie die Gesamtzahl / Konzentration der Zellen für jeden Zelltyp. Optional: Einige Zellen Paarungen kann dramatisch anders Verbreitung Indizes anzuzeigen. Um die ausgeschlossenen Zellen aus übervölkern die Insel gemusterten Zellen (insbesondere für die langfristige Kulturen) verhindern, behandeln die Zellen für Ausschluß mit Mitomycin C für 2 Stunden oder gebraucht bestrahlen sie vor der Ernte. Dadurch wird verhindert, Proliferation. Fluorescent CellTracker Farbstoffe können verwendet werden, um die beiden Zellpopulationen unterscheiden, wenn es erforderlich ist.
- Pellet die Zellen und das Pellet für exclusion Musterbildung in einem geeigneten Volumen von 5,0% PEG zur Erzielung der gewünschten Anzahl von Zellen, wie oben beschrieben. Das Pellet für Insel Musterbildung in einem geeigneten Volumen von 12,8% DEX, um die gewünschte Konzentration der Zellen zu erreichen, wie oben.
- Mit einer Mikropipette, verzichten 0,5 ul Tröpfchen DEX Zellsuspension auf einem trockenen Zellkultursubstrat. Lassen Sie keine Tröpfchen zu trocknen.
- Bedecken Sie die DEX Tröpfchen mit 200 ul PEG Zellsuspension.
- In einem befeuchteten Inkubator für 12 Stunden bei 37 ° C, 5% CO 2. Stellen Sie sicher, dass das Gericht nicht bei der Handhabung und dass es auf einem Niveau Inkubator Regal gestellt zu verhindern, dass die Muster gekippt.
- Entfernen Sie die PEG-Lösung und dreimal in 200 ul Kulturmedium.
- Fügen Sie frisches Kulturmedium und Rückkehr in den Inkubator.
- Überwachen Sie die Co-Kulturen, die Interaktion zwischen Zellpopulationen zu beobachten. Optional: Controls kann durch Ausführen Ausschluss oder die Insel Strukturierung indiv. vorbereitet werdenidually, durch Co-Kultivierung von Zellen, die nicht interagieren oder durch Blockieren Wege des Interesses an einem oder beiden Zellpopulationen vor oder nach einem Mustern.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Um eine geeignete Kombination von PEG und DEX für Zelle Strukturieren auszuwählen, ist es wichtig, um die binodale Kurve bestimmen. Diese Kurve skizziert die Punkte, an denen ein ATPS bilden können und für einen gegebenen Satz von Polymeren auf Temperatur, pH und Ionengehalt variieren. Zum Kultivieren von Zellen, die angepasst Mediums Formulierungen erfordern kann es erforderlich sein, um experimentell die binodale Kurve. Dies wird durch Erzeugen einer Reihe von ATPSs, die weit von der binodale und Variieren in ihrer PEG und DEX contents (Abbildung 1, lila Kreise) sind bewerkstelligt. Wenn ein ATPS vorhanden ist, werden die Polymerlösungen erscheinen bedeckt, wenn sie gemischt werden und in getrennte Phasen äquilibrieren wenn sie ungestört. Durch die Zugabe von zusätzlichen Lösungsmittel, um die Polymer-Mischung werden die ATPS nähern 0% PEG / 0% DEX. An einem gewissen Punkt wird das Gemisch nicht mehr Phasentrennung. Das PEG / DEX, bei der diese auftritt repräsentiert einen Punkt am binodale Kurve; über diesem Punkt ein ATPS bilden kann und unter diesem Punkt kann es nicht. Die Kurven in Abbildung 1 stellen binodals für drei gemeinsamen Zellkulturmedien mit und ohne 10% fötalem Rinderserum (FBS). Die Konzentrationen, bei denen ein ATPS gebildet sind etwas höher in Gegenwart von FBS.
In unserer früheren Berichten, verwendeten wir ATPSs basierend auf einem kritischen Punkt (der Punkt auf der binodale an dem gleichen Volumen von PEG und DEX Form nach Äquilibrierung) von 2,5% PEG 35% kDa/3.2 DEX 500 kDa. Die Ergebnisse unserer binodale Daten sind in unmittelbarer Nähe zu diesem kritischen Punkt Wert. Wir testeten neun Phasensystem Kombinationen zum Mustern, wie in Tabelle 1 gezeigt. Da reine Lösungen von PEG und DEX bezüglich ihrer Polymerkonzentrationen äquilibrieren nachdem sie kombiniert werden, haben einige dieser Lösungen keine stabilen ATPSs und waren somit nicht brauchbar zum Mustern (Tabelle 1a, x Marken). Andere Polymer-Kombinationen hergestellt erkennbaren Mustern, Waren aber nicht gleichmäßig genug für Experimente (Tabelle 1a x / ✓ Mark). Nützliche Polymer-Formulierungen gebildet Sperrzonen oder Inseln, die fast frei von Zellen in den nicht-strukturierten Bereichen (Tabelle 1a, ✓ Mark) waren.
Mit 10% PEG, bemerkten wir, dass Zellmorphologie war ungewöhnlich runde und spindelförmige nach 24 h, mit Zellen, die eine verminderte Fähigkeit, auf die Kultur-oberfläche (Tabelle 1b, x marks) zu befestigen. Morphologie und Befestigung waren normal für 2,5% und 5% PEG (Tabelle 1b, ✓ Marken). Wir beobachteten, dass Serum gefällte aus dem Kulturmedium bei hohen PEG-Konzentrationen (Tabelle 1c, x Marken), was darauf hindeutet, dass abnorme Zellmorphologie und Befestigung in 10% PEG, um Probleme mit Serum Zugang kann bezogen werden. Zusätzlich ist bekannt, dass PEG stören Plasmamembranen 27. Obwohl diese Effekte sind nur bei hohen Konzentrationen niedrig mol beobachtetecular Gewicht PEG, ist es am besten, um die niedrigsten PEG-Konzentration, die eine zuverlässige Strukturierung produziert zu verwenden.
In Übereinstimmung mit unseren früheren Berichten schlossen wir, dass 5% PEG/6.4% DEX und 5% PEG/12.8% DEX waren gut für die Zell-Strukturierung geeignet, mit 12,8% DEX Herstellung einheitlicher Muster. Erwartete Ergebnisse für drei Strukturierung Formate mit Cell Tracker-markierten HeLa-Zellen sind in Abbildung 2 dargestellt. Durch Strukturieren nach jedem Ansatz ist es möglich, zu einheitlichen Mustern jeder Art zu schaffen, mit sehr wenigen Zellen außerhalb der strukturierten Bereiche.
Mit Ausgrenzung und Insel Strukturierung ist es möglich, die Proliferation und Migration von strukturierten Zellen (Abbildung 3) zu beurteilen. Im Laufe von drei Tagen, gefüllt HeLa-Zellen die Sperrzonen (3a-c). Insel-gemusterten Zellen expandiert nach außen von den ersten Mustern (Figuren 3d-f). Diese Veränderungen können quantifiziert Verwendung werdenStandard ImageJ Messwerkzeuge (Abb. 3 c, f). Es ist wichtig anzumerken, dass, wenn mehrere Zellpopulationen kokultivierten sind (Abb. 2, Typ 3), einer Zellpopulation kann-proliferieren und ersetzen die andere. Ausschluss Strukturierung und Insel Strukturierung kann nützliche Werkzeuge zu beurteilen, ob dies ein Problem sein wird. In Situationen, wo dramatische Unterschiede in Proliferationsindex auftreten, ist es empfehlenswert, daß man Zellpopulation durch Bestrahlung oder chemische Faktoren behandelt werden, um ihre Proliferation zu begrenzen. Dies ist insbesondere nützlich, wenn ein Zelltyp als Auflage für eine Zelle langsamer wachsende empfindlicher Zelltyp verwendet wird.
Wir haben gezeigt, dieses Prinzip durch Kultivieren HepG2-Zellen, ein hepatozelluläres Karzinom-Zelllinie, die gemeinhin Modell Hepatocyt Biologie verwendet wird, mit NIH 3T3-Fibroblasten, die Verhaftung mit Mitomycin C (Abbildung 4) wurden. Im Laufe der Zeit halten die HepG2-Zellen ihrer Lokalisation eined Kolonie Form (Abbildung 4a). Indem viele Tröpfchen in derselben Platte und sie umgebende mit Fibroblasten es ist möglich, diese Zellen in einem Format, das potentiell nützlich für multiplexte Studien (4b) ist wachsen. Zelle Insel Monokulturen kann mit diesem Format als Kontrolle für den Einfluss von Faktoren parakrine (4c) verwendet werden.
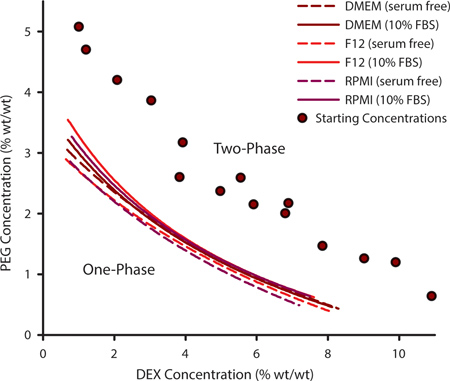
Abbildung 1. Die Polymerkonzentrationen, an dem ein ATPS bilden können aus experimentell bestimmten binodale Kurve extrapoliert werden. Diese binodale Kurve konstruiert wurde mit der Methode Trübungspunkt durch Hinzufügen zusätzlicher Lösungsmittel, um die Punkte, an denen Zweiphasengemische variierender PEG / DEX-Konzentrationen (lila messen Kreise) nicht mehr in der Lage waren phase separating. Binodals wurden DMEM, F12 und RPMI mit und ohne Serum bestimmt. Die Datenpunkte wurden mit einer Drei-Parameter-rationalen Funktion ausgestattet. N = 3 für jeden Datenpunkt.

Abbildung 2. Durch den Verzicht ATPS Lösungen auf Polystyrol-Platten können drei Formate für Zellen Strukturierung hergestellt werden. Das Verfahren beginnt durch Pipettieren DEX Tröpfchen eine), die dann mit PEG b beschichtet sind). Sobald die Zellen anzubringen, können die Lösungen ATPS weggespült und durch Kulturmedium (c, d). Fluorescence Bilder für Monokulturen wurden mit CellTracker Farbstoffe nach der Strukturierung gefärbt. Für Co-Kulturen wurden Zellen separat mit CellTracker Farbstoffe vor dem Strukturieren gefärbt. HeLa-Zellen wurden verwendet, um alle drei Kultur-Formate generieren. 
Abbildung 3. Strukturieren und Ausschluss Insel Strukturieren kann zur Zellmigration und Proliferation zu beurteilen. A) Ausschluss gemusterten HeLa-Zellen 1 Tag nach Musterung. B) Ausschluss gemusterten HeLa-Zellen 3 Tage nach Musterung. C) Zellen migrieren und proliferieren, eine deutliche Verringerung der Größe der Sperrzone. d) Insel-gemusterten HeLa-Zellen 1 Tag nach Musterung. e) Insel-gemusterten HeLa-Zellen 3 Tage nach Musterung. f) Zellen proliferieren und wandern nach außen deutlich Erweiterung der Größe der Insel. Die Bilder wurden quantifiziert mit ImageJ-Software, um die Zelle Clearing-und Zell-Insel Bereichen vor und nach der Migration zu messen. Bars stellen Mittelwerte± SEM von mindestens drei unabhängigen Beobachtungen.

Abbildung 4. Leberzelle / Fibroblastenkulturen kann mit Hilfe ATPS Ausschluss Co-Kultur Strukturierung werden. A) Diese Kolonien behalten ihre Organisation mindestens 4 Tagen in Kultur. B) Mehrere Inseln können in einem einzigen Teller mit Potenzial für Multiplex-oder High-Throughput angeordnet werden Assays. c) auf nicht-co-kultivierten Insel Mustern verglichen, zeigen die co-kultivierten Zellen geringfügig höhere Werte von Albumin Produktion (braune Färbung), wie aus qualitativen Vergleich von Albumin gebeizt Co-Kulturen im Vergleich zu Monokulturen. Albumin ist ein Protein, das von Leberzellen. Daher schlägt diese Resultat, dass die Funktion von Leberzellen verstärkt wird, wenn es mit Fibroblasten mit ATPS kokultiviert.
| a) Muster gebildet | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | x | x | x |
| PEG 5,0% | x / ✓ | ✓ | ✓ |
| PEG 10,0% | x / ✓ | ✓ | ✓ |
| b) Morphologie | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | ✓ | ✓ | ✓ |
| PEG 5,0% | ✓ | ✓ | & # X2713; |
| PEG 10,0% | x | x | x |
| c) Serum Niederschlag | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | ✓ | ✓ | ✓ |
| PEG 5,0% | ✓ | ✓ | ✓ |
| PEG 10,0% | x | x | x |
Tabelle 1. A) ATPS Formulierungen, die zur Strukturierung verwendet werden können, werden durch Markierungen, die nicht jene sind, kann durch Markierungen x angedeutet ist. B) Formulierungen, die normal Zellmorphologie und Befestigung Eigenschaften beibehalten b angedeutety Häkchen, diejenigen, die nicht durch X-Markierungen angedeutet. c) Formulierungen, die zur Ausfällung von Serumproteinen resultierten, die durch x-Noten angegeben.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Die ATPS Zelle Mikrostrukturierung Methode erfordert nur sehr wenig Know-how über Kenntnisse in Zellkultur-Techniken und kann schnell gemeistert werden. Die Vorteile dieser Vorgehensweise sind, dass sie preiswert, schnell und kompatibel mit einer Vielzahl von Zelltypen und Kultur Formaten ist. Aus diesen Gründen sollte unser Protokoll leicht Biowissenschaftler, insbesondere diejenigen, die Zellproliferation, Migration und Chemotaxis und den Einfluss der juxtacrine und parakrine Interaktionen zwischen Zellpopulationen zu studieren erlassen. Die Assays hier vorgestellten kann leicht bei der Zellpopulation Ebene mit Standard-Bildanalyse zur Verfügung stehenden Verfahren in Software wie ImageJ quantifiziert werden.
Um eine gleichbleibende Muster zu erzeugen, empfehlen wir die folgenden Vorsichtsmaßnahmen. Erstens sollte die Pipettenspitze verwendet, um die Lösung verzichten DEX geändert, nachdem jedes Tröpfchen abgeschieden DEX um einheitlichere Tropfenvolumina bereitzustellen. Da das DEX Lösung relativ viskosenEs ist auch wichtig, um zu vermeiden Abscheiden überschüssigen DEX, die auf der äußeren Oberfläche der Pipettenspitze kann und zu gewährleisten, dass das gesamte Volumen von DEX verlässt die Spitze. Zweitens können die Tröpfchen bewegen, wenn PEG ist zu stark oder hinzugefügt werden, wenn das Gericht gekippt wird. DEX Unterbrechung kann, indem sie den Spiegel auf eine ebene Oberfläche und ermöglichen die PEG-Lösung schrittweise abdecken Tröpfchen von oben, ohne daß große Kräfte von der PEG Meniskus Teil des Tröpfchens verdrängen minimiert werden. Droplet Störung tritt häufig mit großen DEX Tröpfchen, so Tröpfchen von 0,5 ul oder weniger verwendet werden, wenn möglich. Abgesehen von diesen technischen Problemen mit Abgabe der Lösungen beteiligt, gibt es sehr wenige Fallstricke mit dieser Technik verbunden sind, sofern geeignete Polymer-Molekulargewichte und Konzentrationen verwendet werden.
Obwohl ATPS Strukturieren leicht durchgeführt werden kann unter Verwendung einer Mikropipette (wie sie hier dargestellt), es gibt eine Vielzahl von mehr sophisorgfältigster Bearbeitung Ansätzen, die verwendet werden, um schnell zu generieren Mustern von komplexeren geometrischen Arrays (zB flüssige Handlingroboter und akustische Tröpfchenausstoß) kann, wie in unseren früheren Studien 14, 15, 20 dargestellt. Es ist auch möglich, DEX Tröpfchen, die viel kleiner im Volumen durch pneumatisch Ausstoßen DEX sind durch kapillare Öffnungen oder durch Betätigen einer Blende in einem Mikrokanal fließt, um Tröpfchen durch DEX PEG 19 ummantelt erzeugen erzeugen. Diese Ansätze können von Interesse für diejenigen, die mit hohem Durchsatz oder Multiplex-Co-Kultur oder Migration Assays zu produzieren. Zusätzlich können mit mikrofluidischen nähert, ist es möglich, Experimente mit einer kleinen Anzahl von Zellen durchzuführen, oder mit Zellen in einem Mikrokanal denen die Wirkung von Strömung und schiere geprüft werden kann. Jedoch sind diese Methoden nicht advanced für die meisten Anwendungen erforderlich.
Wäßrigen zweiphasigen Strukturieren von Zellen ist einfach und leicht zu einer typischen Zelle angepaßtKultur Einstellung. Diese Methode ermöglicht es jeder Forscher mit Zugang zu einer typischen Zelle culture lab (Zugang zu einer Kapuze, CO 2-Inkubator und Mikropipetten) und den genannten Polymeren reproduzierbar Muster Zellen in Monokultur und Co-Kultur. Unser Labor hat diese Fähigkeit durch Drucken Arrays von Zellen an Zellmigration in einem Assay Wundheilung zu studieren und um die Auswirkungen von juxtacrine und parakrine Signalisierung in der Differenzierung von embryonalen Zellen 16, 17, 20 prüft demonstriert. Andere Verfahren, einschließlich Strukturierung der extrazellulären Matrix 28, Tintenstrahldrucksystem 29 und Strukturierung durch laminare Strömung in mikrofluidischen Vorrichtungen 25, 26 sind auch verwendet worden, zu lokalisieren Zellen. Diese anderen Methoden sind wirksame Ansätze zur Erreichung klar definierten Muster der Zellen und können oft zu erzielen Single-Cell-Präzision. Allerdings sind diese Methoden erfordern auch hoch spezialisierte Ausrüstung und / oder den Zugang zu Reinräumen um die verwendeten Stempel pr herzustellenint extrazelluläre Matrixproteine oder produzieren Mikrofluidik-Geräte. Ihre Verbindung zu Netzteilen, Spritzenpumpen und andere externe Komponenten behindert auch deren Umsetzung aufgrund der Kosten, die mit der Anlage und Benutzerinformationen Fähigkeit erforderlich, um es zu betreiben verbunden.
Im Hinblick auf zukünftige Anwendungen erwarten wir, dass unsere Methode nützlich sein wird für die Entwicklung von Kultur-Systeme, High-Throughput-Analyse von Zell-Bewegung und Verbreitung, sowie die Untersuchung von Zell-Zell-Interaktionen zwischen mehreren Zellpopulationen ermöglichen. Bis zu diesem Punkt haben unsere Berichte über die Prüfung Zusammenspiel von nur wenigen Arten von strukturierten Zellen auf einmal konzentriert. Es ist jedoch denkbar, dass viele Subpopulationen von Zellen mit einer gemeinsamen Fütterlage um die Auswirkungen der parakrine und juxtacrine Signalisierung von vielen Zelltypen zusammen in einer einzigen Zellkultur gezüchtet Setup untersuchen könnte kultiviert werden. Schließlich Tissue Engineering-Anwendungen häufig benötigten räumlichen Lokalisierungeinem oder mehreren Zelltypen. Es kann möglich sein, um unsere Technik zur Verwendung in Strukturieren Zellen anzupassen, um mehrere physiologisch relevanten Gewebezüchtungen Krankheitsmodellen produzieren oder Muster Zellen auf implantierbare Materialien für klinische Anwendungen.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Die Autoren haben keine konkurrierenden finanziellen Interessen.
Acknowledgments
Für JBW:; Diese Arbeit wurde von der Coulter Foundation, Beyster Stiftung, der Undergraduate Research Opportunity (UROP) Sommer-Programm für ATA und einem National Science Foundation Graduate Student Research Fellowship (. 2010101926 ID gewähren keine DGE 0.718.128) unterstützt.
Materials
| Name | Company | Catalog Number | Comments |
| Dextran 500,000 kDa | Pharmacosmos, Denmark | ||
| Polyethylene Glycol 35,000 kDa | Sigma-Aldrich, St. Louis, MO | ||
| Hela | ATCC, Manassas, VA | ||
| HepG2 C3A | ATCC, Manassas, VA | ||
| NIH 3T3 | ATCC, Manassas, VA | ||
| Cell Tracker | Invitrogen, Carlsbad, CA | ||
| DMEM | Gibco, Carlsbad, CA | ||
| RPMI | Gibco, Carlsbad, CA | ||
| F12 | Gibco, Carlsbad, CA | ||
| Fetal Bovine Serum | Gibco, Carlsbad, CA |
References
- Hatti-Kaul, R. Aqueous two-phase systems : methods and protocols. Methods in biotechnology. xiii, Humana Press. 440 (2000).
- Albertsson, P. A. k Partition of cell particles and macromolecules: separation and purification of biomolecules, cell organelles, membranes, and cells in aqueous polymer two-phase systems and their use in biochemical analysis and biotechnology. , 3rd ed, Wiley. 346 (1986).
- Yamada, M., et al. Continuous cell partitioning using an aqueous two-phase flow system in microfluidic devices. Biotechnol. Bioeng. 88 (4), 489-494 (2004).
- Soohoo, J. R., Walker, G. M. Microfluidic aqueous two phase system for leukocyte concentration from whole blood. Biomed. Microdevices. 11 (2), 323-329 (2009).
- Hahn, T., Hardt, S. Concentration and size separation of DNA samples at liquid-liquid interfaces. Anal. Chem. 83 (14), 5476-5479 (2011).
- Hatti-Kaul, R. Aqueous two-phase systems. A general overview. Mol. Biotechnol. 19 (3), 269-277 (2001).
- Hustedt, H., Kroner, K. H., Menge, U., Kula, M. -R. Protein recovery using two-phase systems. Trends in Biotechnology. 3 (6), 139-144 (1985).
- Keating, C. D. Aqueous Phase Separation as a Possible Route to Compartmentalization of Biological Molecules. Acc Chem. Res. 45 (12), 2114-2124 (2012).
- Helfrich, M. R., et al. Partitioning and assembly of metal particles and their bioconjugates in aqueous two-phase systems. Langmuir. 21 (18), 8478-8486 (2005).
- Diamond, A. D., Hsu, J. T. Prote. Partitioning in PEG/Dextran Aqueous Two-Phase Systems. AIChE Journal. 36 (7), 1017-1024 (1990).
- Y-T,, Zhu, Z. -Q. Modeling of interfacial tension of aqueous two-phase systems. Chemical Engineering Science. 54 (4), 433-440 (1999).
- Liu, Y., Lipowsky, R., Dimova, R. Concentration dependence of the interfacial tension for aqueous two-phase polymer solutions of dextran and polyethylene glycol. Langmuir. 28 (8), 3831-3839 (2012).
- Rha, C. Interfacial Tension of Polyethylene Glycol/Potassium Phosphate Aqueous Two-Phase Systems. Physics and Chemistry of Liquids: An International Journal. 38 (1), 25-34 (2000).
- Fang, Y., et al. Rapid Generation of Multiplexed Cell Cocultures Using Acoustic Droplet Ejection Followed by Aqueous Two-Phase Exclusion Patterning. Tissue Eng. Part C. Methods. 18 (9), 647-657 (2012).
- Tavana, H., et al. Nanolitre liquid patterning in aqueous environments for spatially defined reagent delivery to mammalian cells. Nat. Mater. 8 (9), 736-741 (2009).
- Tavana, H., Mosadegh, B., Takayama, S. Polymeric aqueous biphasic systems for non-contact cell printing on cells: engineering heterocellular embryonic stem cell niches. Adv. Mater. 22 (24), 2628-2631 (2010).
- Tavana, H., et al. Microprinted feeder cells guide embryonic stem cell fate. Biotechnol. Bioeng. , (2011).
- Tavana, H., Takayama, S. Aqueous biphasic microprinting approach to tissue engineering. Biomicrofluidics. 5 (1), 13404 (2011).
- Frampton, J. P., et al. Precisely targeted delivery of cells and biomolecules within microchannels using aqueous two-phase systems. Biomed. Microdevices. 13 (6), 1043-1051 (2011).
- Hossein Tavana, K. K., Bersano-Begey, T., Luker, K. E., Luker, G. D., Takayama, S. Rehydration of Polymeric, Aqueous, Biphasic System Facilitates High Throughput Cell Exclusion Patterning for Cell Migration Studies. Advanced Functional Materials. 21 (15), 2920-2926 (2011).
- Falconnet, D., et al. Surface engineering approaches to micropattern surfaces for cell-based assays. Biomaterials. 27 (16), 3044-3063 (2006).
- Lim, J. Y., Donahue, H. J. Cell sensing and response to micro- and nanostructured surfaces produced by chemical and topographic patterning. Tissue Eng. 13 (8), 1879-1891 (2007).
- Ringeisen, B. R., et al. Jet-based methods to print living cells. Biotechnol. J. 1 (9), 930-948 (2006).
- Wright, D., et al. Generation of static and dynamic patterned co-cultures using microfabricated parylene-C stencils. Lab Chip. 7 (10), 1272-1279 (2007).
- Takayama, S., et al. Patterning cells and their environments using multiple laminar fluid flows in capillary networks. Proc. Natl. Acad. Sci. U.S.A. 96 (10), 5545-5548 (1999).
- Berthier, E., et al. Pipette-friendly laminar flow patterning for cell-based assays. Lab Chip. 11 (12), 2060-2065 (2011).
- Davidson, R. L., O'Malley, K. A., Wheeler, T. B. Polyethylene glycol-induced mammalian cell hybridization: effect of polyethylene glycol molecular weight and concentration. Somatic Cell Genet. 2 (3), 271-280 (1976).
- Johnson, D. M., LaFranzo, N. A., Maurer, J. A. Creating Two-Dimensional Patterned Substrates for Protein and Cell Confinement. J. Vis. Exp. (55), e3164 (2011).
- Moon, S., Lin, P., Keles, H. O., Yoo, S., Demirci, U. Title Cell Encapsulation by Droplets. J. Vis. Exp. (8), e316 (2007).



