Summary
Acuosos sistemas de dos fases se utiliza para poblaciones modelo simultáneamente múltiples de células. Este método rápido y fácil para el patrón celular se aprovecha de la separación de fases de las soluciones acuosas de glicol de polietileno y dextrano y la tensión interfacial que existe entre las dos soluciones de polímero.
Abstract
Tecnologías de células de patrones que son rápidos, fáciles de usar y asequible se requiere para el desarrollo futuro de los ensayos de rendimiento de alta celulares, plataformas para el estudio de interacciones célula-célula y sistemas de ingeniería tisular. Este protocolo detallado se describe un método para la generación de co-cultivos de células utilizando soluciones biocompatibles de dextrano (DEX) y polietilenglicol (PEG) que los de fase separada cuando se combina encima de las concentraciones umbral. Las células se pueden modelar en una variedad de configuraciones que utilizan este método. Patrón célula exclusión se puede realizar mediante la impresión de gotitas de DEX sobre un sustrato y cubriéndolos con una solución de PEG que contienen células. La tensión interfacial formada entre la dos soluciones de polímero hace que las células estén en torno al exterior de la gotita de DEX y formar un claro circular que puede ser utilizado para los ensayos de migración. Islas de células puede ser modelado por dispensación de una fase rica en células DEX en una solución de PEG, o cubriendo la DEXgota con una solución de PEG. Co-cultivos se pueden formar directamente mediante la combinación de exclusión celular con DEX patrón isla. Estos métodos son compatibles con una variedad de enfoques de manejo de líquidos, incluyendo micropipeteo manual, y se puede usar con prácticamente cualquier tipo de célula adherente.
Introduction
Acuosos sistemas de dos fases (ATPSs) forma cuando las soluciones de dos polímeros incompatibles se mezclan juntos en concentraciones suficientemente altas. La separación de fases está influenciada por una variedad de factores que incluyen el peso molecular y la polaridad de los polímeros, la temperatura de las soluciones, pH y contenido iónico del disolvente acuoso 1, 2. El punto en el que las dos soluciones de polímeros separados se determina por las propiedades fisicoquímicas de la fase del sistema elegido, pero en general se produce a bajas concentraciones de polímero (menos de 20% peso / peso) bajo condiciones no desnaturalizantes, permitiendo ATPSs que se utilizará para la biotecnología 3-9 aplicaciones.
Con mucho, los más ampliamente estudiados ATPS es el polietilenglicol (PEG) / sistema de dextrano (DEX). Los ATPS formadas por estos polímeros de bajo costo y biocompatible fue originalmente descrita para la purificación de biomoléculas por medio de partición molecular 2, 10. Particionamientose produce cuando las moléculas o partículas adicionales que no contribuyen al sistema de fase se mezclan con PEG y DEX. En base a sus afinidades relativas para ya sea DEX o PEG, las moléculas o partículas preferentemente residirá dentro de una de las dos fases o en el interfaz. Otra característica de la ATPS PEG / dex es la existencia de la tensión interfacial entre las dos fases de polímero. ATPSs formados por PEG y DEX generalmente muestran tensiones interfaciales que son mucho más bajos que otros líquido-líquido en sistemas de dos fases, tales como aceite y agua, sin embargo, las fuerzas de tensión interfacial todavía ejercen efectos sobre las pequeñas partículas tales como virus, células y agregados de proteínas 2 , 11-13. Finalmente, puesto que mayor peso molecular de PEG y DEX separado a bajas concentraciones (menos de 5% peso / peso de polímeros de alto peso molecular variedades) en presencia de concentraciones fisiológicas de sales, hay pocos o ningún efectos deletéreos sobre células de mamífero incorporado dentro de estos sistemas14-16.
Recientemente, las propiedades interfaciales y los efectos de partición de ATPSs han sido aplicadas por nuestro laboratorio para el patrón celular 14, 16-20. Esto se logró por micropatterning una solución más densa DEX sobre sustratos de cultivo de células en presencia de PEG. Cuando las células se incorporan en la fase de PEG, se excluyen la entrada de las gotitas de DEX debido a PEG / dex tensión interfacial 20. Cuando las células se modelan en la fase de DEX, que son retenidos en la superficie del sustrato de cultivo celular mediante la tensión interfacial y la partición 16, 17, 19.
En contraste con otros métodos para el patrón celular, patrón ATPS celular es fácil de aprender y sólo requiere conocimientos rudimentarios sobre los propios polímeros, y la capacidad para llevar a cabo el cultivo de células y el uso de una micropipeta. Otros métodos para modelar celular implican a menudo el equipo especializado y capacitación que no se traducen fácilmente a the las ciencias biológicas. Por ejemplo, algunos métodos (impresión por microcontacto de impresión de inyección de tinta o) células de patrón indirectamente mediante la aplicación de patrones de biomoléculas adhesivas celulares a un sustrato de cultivo que posteriormente sirven como sitios para la unión celular 21, 22. Aunque los enfoques indirectos son útiles para algunos tipos celulares, que requieren un alto grado de habilidad del usuario y equipo especializado para la fabricación de la herramienta de modelado, y puede carecer de especificidad dependiendo del tipo particular de células / biomolécula patrón. Alternativamente, las células pueden ser depositados con una especificidad alta patrón por medio de enfoques de modelado directos que incluyen patrones de flujo laminar, estarcir y la impresión de inyección de tinta 23-26. Sin embargo, estas técnicas también requieren experiencia del usuario y equipo especializado, y puede dañar las células durante el proceso de impresión. Si bien estos métodos generalmente producen patrones precisos de células, que permiten definir motivos de células a ser una herramienta útil en las ciencias de la vida, debe ser rentable unnd simple de implementar.
Aquí mostramos un protocolo detallado para la generación de patrones de cultivos celulares utilizando los ATPSs descritos en nuestras aplicaciones previamente publicados. Usando sólo Micropipetas, los usuarios pueden generar zonas de células de exclusión o islas celulares para los ensayos de migración. Esto se consigue por medio de PEG / dex tensión interfacial que o bien conserva las células en la fase de DEX o excluye las células depositadas en la fase de PEG de DEX. Por el peinado de estas dos técnicas fundamentales de dibujo, es posible generar rápidamente co-cultivos de células tales como células de hígado de fibroblastos co-cultivos. Métodos de patterning, parámetros ATPS y los resultados esperados se describen en detalle.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. Fase de caracterización del sistema: Los umbrales determinantes para la separación de fases
- Preparar soluciones que contienen PEG y DEX en el tampón deseado o medio de cultivo celular como se muestra en la Figura 1 (puntos púrpura) en 15 ml o 50 tubos cónicos ml. En lo sucesivo, PEG y DEX se refieren a PEG de 35 kDa y 500 kDa DEX, sin embargo, concentraciones críticas cambiará en función de los dos polímeros utilizados. Registrar la masa de PEG y DEX en cada solución. Alta concentración de las soluciones de polímero puede tardar varias horas para disolver. Vórtice puede ser utilizado para soluciones libres de suero. Para medios que contienen proteínas o de suero, se colocan los tubos en una etapa balanceo hasta que los dos polímeros se disuelven completamente. Anotar el peso de los medios utilizados para disolver los polímeros y tomar nota de las concentraciones iniciales.
- Una vez que los polímeros se disuelven completamente, las soluciones deben aparecer turbia. Esta es la primera indicación de que la separación de fases se ha producido. Para confirmar esto, permitir que elsoluciones de polímero a descansar en una posición vertical a temperatura ambiente durante 20 min. La centrifugación a 1.000 xg se puede usar para acelerar el proceso de separación de fases. La fase inferior densa será DEX-rica y la fase superior será PEG-rico.
- Lentamente añadir tampón adicional o medios de comunicación a los tubos. Pequeños incrementos deben utilizarse a fin de no sobrepasar el punto de separación de fases.
- Cuando la solución se vuelva clara y ya no se separa de fase después de la centrifugación, el umbral para la separación de fases se ha alcanzado. Registrar el peso final del tubo.
- Utilizando los pesos anteriores registrados para los polímeros, junto con el peso final tras la adición de medios, determinar el% en peso / peso de cada uno de los dos polímeros en el que la separación de fases ya no se produce.
- Trazar estos valores en% en peso / peso de PEG en el eje y, y% peso / peso de DEX en el eje x. Esta trama, conocida como la curva binodal, se puede utilizar para determinar el umbral de concentración para la separación de fases para diferentes concentratiComplementos de PEG / DEX en un medio de cultivo celular específica.
2. Configuración 1: Exclusión Patrones (96-así formato de placa)
- Preparar soluciones separadas de 5,0% peso / peso de PEG y 12,8% DEX peso / peso en medio de cultivo celular. Utilizar soluciones ATPS de al menos dos veces el punto crítico para garantizar que un ATPS permanece después de los polímeros equilibrar con respecto a la otra. Hay una pequeña cantidad de flujo de DEX en la fase de PEG-rico y viceversa, por lo tanto, trabajando demasiado cerca de la concentración crítica puede resultar en la pérdida del sistema de fase como la caída de las concentraciones por debajo del punto crítico. De manera similar, la transferencia de la placa de cultivo celular a una incubadora con humedad y temperatura controladas pueden alterar las propiedades de dos fases y hacer que las dos soluciones miscibles. Nota: Algunas células pueden funcionar mejor con otras formulaciones ATPS. Formulaciones aceptables pueden ser seleccionados en base a las curvas de binodal determinados a partir de la Parte 1.
- Recoger las células que se utilizarán para la exclusión patteRT ENCIA. Determinar el número total / concentración de células disponibles. Opcional: marcar las células con CellTracker u otros no citotóxicos etiquetas para microscopía de fluorescencia.
- Sedimentar las células y resuspender el sedimento en un volumen apropiado de 5,0% de PEG para lograr el número deseado de células por exclusión. Por ejemplo, un pocillo de una placa de 96 pocillos requiere 37.500 células de fibroblasto que se resuspendió en 200 l de PEG para producir confluencia el día siguiente. Escala estos números según sea apropiado para otros tipos de células y tamaños de sustrato de cultivo.
- Usando una micropipeta, dispensar gotas 0,5 l de DEX sobre un sustrato de cultivo celular seco. Las gotas más grandes producen mayores volúmenes de zonas de exclusión. Las gotitas que varían en tamaño desde 0,1 hasta 1 l se recomiendan para micropatterning exclusión. Opcional: DEX gotitas pueden depositarse 24 hr antes de tiempo y se dejó deshidratar a temperatura ambiente. Esto puede producir patrones más limpios.
- Dispensar 200 l de suspensión celular en t PEGasí que para cubrir las gotas DEX.
- Colocar en un humidificado incubadora durante 12 horas a 37 ° C, 5% de CO 2. Asegúrese de que el plato no está inclinado durante la manipulación y que se coloca en un nivel de estantería incubadora para evitar la interrupción de los patrones.
- Quitar la solución de PEG y se lava tres veces con 200 l de medio de cultivo.
- Añadir medio de cultivo fresco y el retorno a la incubadora.
- Monitorear las culturas periódicamente para observar el movimiento celular en la zona de exclusión.
3. Configuración 2: La isla Patrones (96-así formato de placa)
- Se preparan soluciones de 5,0% en peso / peso de PEG y 12,8% DEX peso / peso en medio de cultivo celular, como anteriormente.
- Recoger las células para ser utilizadas para modelar isla. Determinar el número total / concentración de células disponibles.
- Pellets y resuspender las células en un volumen apropiado de DEX 12,8% para alcanzar la concentración deseada de células para el patrón isla. Las concentraciones de 5.000 ceLLS / l o menos se recomienda para tipos de células fuertemente adherentes. Para las células que tienen dificultad para montar o células que se adhieren débilmente, concentraciones de hasta 10.000 células / l puede ser considerado.
- Trabajando con rapidez para evitar el secado, las gotitas de pipeta 0,5 l de DEX sobre un sustrato de cultivo celular seco, como se describió anteriormente. No permitir que las gotas a secar. Opcional: 200 l de solución de PEG se puede añadir a la bien delante de tiempo. Gotitas DEX entonces puede ser depositado en la solución de PEG donde se hunden hasta el fondo y en contacto con la superficie de cultivo. Esto puede producir patrones más limpios de la isla.
- Cubra las gotas de DEX con 200 l de PEG.
- Colocar en un humidificado incubadora durante 12 horas a 37 ° C, 5% de CO 2. Asegúrese de que el plato no está inclinado durante la manipulación y que se coloca en un nivel de estantería incubadora para evitar la interrupción de los patrones.
- Quitar la solución de PEG y se lava tres veces con 200 l de medio de cultivo.
- Añadir cultivo frescomedio y retorno a la incubadora.
- Monitorear las culturas periódicamente para observar el movimiento celular y proliferación hacia el exterior de las islas.
4. Configuración 3: Exclusión Co-culturas (96-así formato de placa)
- Se preparan soluciones de 5,0% en peso / peso de PEG y 12,8% DEX peso / peso en medio de cultivo celular, como anteriormente.
- Recoger las células que se utilizarán para la exclusión y el patrón isla. Determinar el número total / concentración de células disponibles para cada tipo de célula. Opcional: Algunas parejas celulares pueden mostrar índices de proliferación dramáticamente diferentes. Para evitar que las células excluidos de sobrepoblación de las células insulares patrón (especialmente para cultivos a largo plazo), el tratamiento de las células usadas para la exclusión con mitomicina C durante 2 horas o irradiar ellos antes de la cosecha. Esto evitará la proliferación. Los tintes fluorescentes CellTracker se puede utilizar para distinguir las dos poblaciones de células si es necesario.
- Pellet las células y resuspender el pellet de exclusion patrones en un volumen apropiado de 5,0% de PEG para lograr el número deseado de células, como anteriormente. Resuspender el precipitado para modelar isla en un volumen apropiado de 12,8% DEX para conseguir la concentración deseada de células, como anteriormente.
- Usando una micropipeta, dispensar gotas 0,5 l de suspensión celular DEX sobre un sustrato de cultivo celular seco. No permitir que las gotas a secar.
- Cubrir las gotitas de DEX con 200 l de suspensión celular PEG.
- Colocar en un humidificado incubadora durante 12 horas a 37 ° C, 5% de CO 2. Asegúrese de que el plato no está inclinado durante la manipulación y que se coloca en un nivel de estantería incubadora para evitar la interrupción de los patrones.
- Quitar la solución de PEG y se lava tres veces en 200 l de medio de cultivo.
- Añadir medio de cultivo fresco y el retorno a la incubadora.
- Monitorear los co-cultivos de observar la interacción entre poblaciones de células. Opcional: Los controles pueden ser preparados mediante la realización de exclusión o isla patrón individually, por las células de co-cultivo que no interactúan o bloqueando las rutas de interés en una o ambas poblaciones de células antes o después de los patrones.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Para seleccionar una combinación apropiada de PEG y DEX para el patrón de células es importante para determinar la curva binodal. Esta curva delimita los puntos en los que un ATPS pueden formar y pueden variar para un conjunto dado de polímeros basada en la temperatura, pH y contenido iónico. Para el cultivo de células que requieren formulaciones personalizadas medio puede ser necesario para determinar experimentalmente la curva binodal. Esto se logra mediante la generación de una serie de ATPSs que están lejos de la binodal y que varían en su contenido de PEG y DEX (Figura 1, los círculos de color púrpura). Cuando un ATPS está presente, las soluciones de polímero se parece turbio cuando se mezcla y se equilibrará en fases separadas si no se toca. Mediante la adición de disolvente adicional a la mezcla de polímero, los ATPS se acercará a 0% de PEG / 0% DEX. En algún momento, la mezcla ya no se separan en fases. La concentración de PEG / dex en la que esto ocurre representa un punto de la curva binodal; encima de ese punto un ATPS pueden formarse y por debajo de ese punto no se puede. Las curvas de la Figura 1 representan binodals para tres medios comunes de cultivo de células con y sin suero fetal bovino al 10% (FBS). Las concentraciones en las que se forma un ATPS son ligeramente superiores en presencia de FBS.
En nuestros informes anteriores, hemos utilizado ATPSs basa en un punto crítico (el punto de la binodal en la que volúmenes iguales de forma PEG y DEX después del equilibrio) de 2,5% de PEG 35 kDa/3.2% DEX 500 kDa. Los resultados de nuestros datos binodal están en proximidad cercana a este valor de punto crítico. Nos probó nueve combinaciones de sistema de fase para el patrón, como se muestra en la Tabla 1. Puesto que las soluciones puras de PEG y DEX equilibre con respecto a sus concentraciones de polímero después de que se combinen, algunas de estas soluciones no se formó ATPSs estables, y eran por lo tanto no es útil para el patrón (Tabla 1a, las marcas X). Otras combinaciones de polímeros producidos patrones reconocibles, Pero no eran lo suficientemente uniforme para la experimentación (Tabla 1a x / ✓ marcas). Útiles formulaciones de polímero formado zonas de exclusión o islas que eran casi carente de células en las regiones sin patrón (Tabla 1a, ✓ marcas).
Con 10% de PEG, nos dimos cuenta de que la morfología celular era anormalmente redondo y de tipo huso después de 24 hr, con células que muestran una menor capacidad para unirse a la superficie de cultivo (Tabla 1b, las marcas X). Morfología y el apego eran normales el 2,5% y el 5% de PEG (cuadro 1b ✓ marcas). Hemos observado que precipitó suero del medio de cultivo a concentraciones de PEG de alto (Tabla 1c, las marcas X), lo que sugiere que la morfología celular anormal y la fijación en 10% de PEG puede estar relacionada con problemas de acceso suero. Además, el PEG se conoce para romper las membranas plasmáticas 27. Aunque estos efectos se observaron sólo a concentraciones altas de bajo molPEG peso ecular, lo mejor es utilizar la menor concentración de PEG que produce patrones fiable.
De acuerdo con nuestros informes anteriores, llegamos a la conclusión de que el 5% PEG/6.4% DEX y el 5% PEG/12.8% DEX estaban bien adaptados para el patrón celular, con un 12,8% DEX producir patrones más uniformes. Resultados esperados para los tres formatos de modelado utilizando Cell Tracker marcados con células HeLa que se muestran en la Figura 2. Siguiendo cada enfoque patrón, es posible crear patrones uniformes de cada tipo, con muy pocas células fuera de las áreas estampadas.
Uso de exclusión y el patrón isla, es posible evaluar la proliferación y migración de células del molde (Figura 3). En el transcurso de tres días, las células HeLa llena las zonas de exclusión (Figuras 3A-C). Isla con estampado de células expandido hacia fuera desde los patrones iniciales (Figuras 3d-f). Estos cambios pueden ser cuantificados utilizandoImageJ estándar de medición de herramientas (Figuras 3 c, f). Es importante señalar que cuando múltiples poblaciones celulares son co-cultivadas (Figura 2, Formato 3), una población de células pueden proliferar fuera y sustituir a la otra. Patrones de exclusión y los patrones isla pueden ser herramientas útiles para evaluar si esto va a ser un problema. En situaciones en las dramáticas diferencias en el índice de proliferación se producen, se recomienda que una población de células de ser tratado por factores de irradiación o químicos para limitar su proliferación. Esto es especialmente útil en situaciones en las que se utiliza un tipo de célula como una célula de apoyo para un tipo más lento crecimiento celular más sensible.
Hemos demostrado este principio por cultivo de células HepG2, un carcinoma hepatocelular línea celular que se utiliza comúnmente para la biología modelo de hepatocitos, con fibroblastos NIH 3T3 que fueron detenidos usando mitomicina C (Figura 4). Con el tiempo, las células HepG2 mantener su localización unad forma colonia (Figura 4a). Al colocar muchas gotitas en la misma placa y rodeándolos con fibroblastos que es posible cultivar estas células en un formato que es potencialmente útil para los estudios multiplexados (Figura 4b). Monocultivos de células insulares se puede utilizar con este formato como un control para la influencia de los factores paracrinos (Figura 4c).
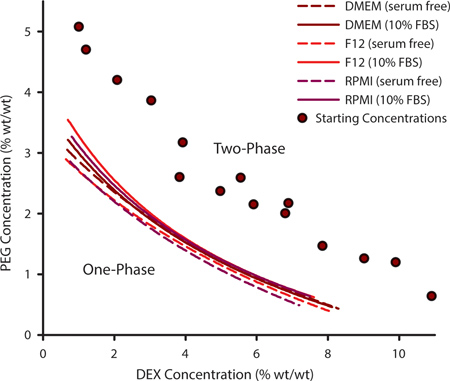
Figura 1. Las concentraciones de polímero a la que un ATPS pueden formar se pueden extrapolar a partir de curvas determinadas experimentalmente binodal. Esta curva binodal se construyó usando el método de punto de nube por adición de un disolvente adicional para medir los puntos en los que dos fases distintas mezclas de PEG / dex concentraciones (púrpura círculos) ya no eran capaces de fase separating. Binodals se determinaron por DMEM, F12 y medio RPMI con y sin suero. Los puntos de datos fueron equipados con una función de tres parámetros racional. N = 3 para cada punto de datos.

Figura 2. Al dispensar soluciones ATPS sobre placas de poliestireno, tres formatos para los patrones de células puede ser producida. El procedimiento comienza pipeteando gotas de DEX a) que se recubren a continuación con PEG b). Una vez que las células se unen, las soluciones ATPS pueden ser lavados y se reemplazó con medio de cultivo (c, d). Imágenes de fluorescencia de los monocultivos fueron teñidos con tintes CellTracker después de los patrones. Para co-cultivos, las células fueron teñidas con tintes CellTracker por separado antes de patrones. Las células HeLa se utiliza para generar los tres formatos de cultivo. 
Figura 3. Exclusión patrón y el patrón isla se puede utilizar para evaluar la migración y la proliferación celular. Una exclusión) estampadas células HeLa 1 día después de patrones. B) Exclusión estampadas células HeLa 3 días después de los patrones. C) las células proliferan y migran, reduciendo significativamente el tamaño de la zona de exclusión. d) Island con estampado de células HeLa después de 1 día patrón. e) Isla con estampado de células HeLa 3 días después de los patrones. f) Las células proliferan y migran hacia el exterior, aumentando significativamente el tamaño de la isla. Las imágenes fueron cuantificados utilizando el software ImageJ para medir el intercambio de información y de célula de células insulares antes y después de la migración. Las barras representan significar± SEM de al menos tres observaciones independientes.

Figura 4. Células de hígado / fibroblastos culturas se pueden generar utilizando exclusión ATPS co-cultivo patrón. A) Estas colonias mantener su organización durante al menos 4 días en cultivo. B) islas múltiples pueden ser dispuestos en un plato único con potencial de multiplexado o de alto rendimiento de ensayos. C) en comparación con los patrones insulares no co-cultivo, las células co-cultivadas muestran niveles ligeramente más altos de producción de albúmina (tinción marrón) como se desprende de la comparación cualitativa de albúmina manchado co-cultivos frente a los monocultivos. La albúmina es una proteína producida por las células del hígado. Por lo tanto, este resultado sugiere que la función de las células hepáticas se mejora cuando se co-cultivadas con fibroblastos utilizando ATPS.
| a) patrón formado | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | x | x | x |
| PEG 5,0% | x / ✓ | ✓ | ✓ |
| PEG 10,0% | x / ✓ | ✓ | ✓ |
| b) Morfología | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | ✓ | ✓ | ✓ |
| PEG 5,0% | ✓ | ✓ | & # X2713; |
| PEG 10,0% | x | x | x |
| c) Suero Precipitación | DEX 3,2% | DEX 6,4% | DEX 12,8% |
| PEG 2,5% | ✓ | ✓ | ✓ |
| PEG 5,0% | ✓ | ✓ | ✓ |
| PEG 10,0% | x | x | x |
Tabla 1. Unas formulaciones ATPS) que se pueden utilizar para el patrón se indican con marcas de verificación, los que no puede se indican por las marcas X. B) Las formulaciones que conservan la morfología normal de las células y las propiedades de fijación se indican bY las marcas de verificación, los que no pueden se indican con marcas de x. c) Las formulaciones que dieron lugar a la precipitación de las proteínas séricas están señaladas con marcas de x.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
La célula ATPS micropatterning método requiere conocimientos muy poco más allá de la competencia en técnicas de cultivo celular y se puede dominar rápidamente. Las ventajas de este enfoque son que es barato, rápido y compatible con una variedad de tipos de células y formatos de cultivo. Por estas razones, el protocolo debe ser fácilmente adoptada por científicos de la vida, en particular los que estudian la proliferación celular, la migración y la quimiotaxis, y la influencia de las interacciones yuxtacrina y paracrina entre las poblaciones celulares. Los ensayos presentados aquí pueden ser fácilmente cuantificados a nivel de población de células utilizando procedimientos estándar de análisis de imagen disponibles en el software como ImageJ.
Para generar patrones consistentes le recomendamos las siguientes precauciones. En primer lugar, la punta de la pipeta usada para dispensar la solución DEX debe ser cambiado después de cada gotita de DEX se deposita para proporcionar volúmenes de gotitas más consistentes. Dado que la solución DEX es relativamente viscoso, También es importante evitar depositar el exceso de DEX que podría estar presente en la superficie exterior de la punta de la pipeta y para asegurar que todo el volumen de las salidas de DEX la punta. En segundo lugar, las gotas pueden moverse si PEG se añade demasiada energía o si el plato está inclinada. DEX interrupción se puede minimizar manteniendo el plato sobre una superficie plana y dejar que la solución de PEG a cubrir gradualmente las gotitas desde arriba, sin permitir que las fuerzas grandes del menisco PEG para desalojar parte de la gotita. Interrupción gota ocurre más frecuentemente con grandes gotas de ejecución directa, por lo que las gotas de l 0,5 o menos se debe utilizar si es posible. Aparte de estas cuestiones técnicas involucradas con la dispensación de las soluciones, existen riesgos muy pocos asociados con esta técnica, siempre que apropiados pesos moleculares del polímero y las concentraciones se utilizan.
Aunque los patrones ATPS se puede realizar fácilmente utilizando una micropipeta (como se presenta aquí), hay una variedad de más sophisticated enfoques que se pueden utilizar para generar rápidamente patrones de matrices más complejas geométricas (por ejemplo, robots de manipulación de líquidos y de eyección de gotitas acústica), tal como se presenta en nuestros estudios anteriores 14, 15, 20. También es posible generar gotitas DEX que son mucho más pequeñas en volumen por neumáticamente expulsar DEX a través de orificios capilares o mediante el accionamiento de un orificio en un microcanal para producir gotitas que fluyen DEX enfundadas por PEG 19. Estos enfoques pueden ser de interés para los que buscan producir ensayos de co-cultivo o la migración de alto rendimiento o multiplexada. Además, el uso de enfoques de microfluidos, es posible llevar a cabo experimentos con un pequeño número de células, o con células en un microcanal donde los efectos de flujo de fluido y pura puede ser examinado. Sin embargo, estos métodos avanzados no son necesarios para la mayoría de aplicaciones.
Acuoso de dos fases del patrón de células es simple y de fácil adaptación a una célula típicaconfiguración de referencia cultural. Este método permite que cualquier investigador con acceso a un laboratorio de cultivo celular típico (acceso a una campana, CO 2 incubadora, y micropipetas) y los polímeros mencionados anteriormente a células de patrón reproducible en monocultivo y co-cultivo. Nuestro laboratorio ha demostrado esta capacidad mediante la impresión de matrices de células para estudiar la migración celular en un ensayo de cicatrización de la herida y para examinar los efectos de la señalización yuxtacrina y paracrinos en la diferenciación de células embrionarias 16, 17, 20. Otros métodos, incluyendo los patrones de matriz extracelular 28, impresión de chorro de tinta 29, y el patrón de flujo laminar en los dispositivos de microfluidos 25, 26 también se han utilizado para localizar células. Estos otros métodos son métodos eficaces para lograr bien definidos patrones de las células y, a menudo puede lograr una sola célula precisión. Sin embargo, estos métodos también requieren alta especialización del equipo y / o el acceso a las instalaciones de salas limpias para la fabricación de los sellos utilizados para print proteínas de la matriz extracelular o producir dispositivos de microfluidos. Su conexión a fuentes de alimentación, bombas de jeringa y otros componentes externos también dificulta su implementación debido a los costos asociados con el equipo y la habilidad del usuario para su operación.
En términos de aplicaciones futuras se espera que nuestro método será útil para el desarrollo de sistemas de cultivo que permiten análisis de alto rendimiento de movimiento y la proliferación celular, así como investigar interacciones célula-célula entre las poblaciones de células múltiples. Hasta este punto, nuestros informes se han centrado en el examen de la interacción de sólo unos pocos tipos de células a la vez estampadas. Sin embargo, es concebible que muchas subpoblaciones de células pueden ser cultivadas con una capa de alimentación común para investigar el impacto de la señalización paracrina y juxtacrine de muchos tipos de células cultivadas juntos en un medio de cultivo celular solo. Localización último, las aplicaciones de ingeniería de tejidos requiere con frecuencia espacial deuno o más tipos de células. Puede ser posible adaptar nuestra técnica para su uso en células de patrones con el fin de producir más fisiológicamente relevantes modelos de ingeniería tisular enfermedad o para células de patrón sobre materiales implantables para aplicaciones clínicas.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Los autores no tienen intereses financieros en competencia.
Acknowledgments
Este trabajo fue apoyado por la Fundación Coulter, Fundación Beyster, la Oportunidad de Investigación de Pregrado (UROP) programa de verano para ATA y la National Science Foundation Graduate Student Research Fellowship (Grant no DGE 0718128, ID:. 2010101926) para JBW.
Materials
| Name | Company | Catalog Number | Comments |
| Dextran 500,000 kDa | Pharmacosmos, Denmark | ||
| Polyethylene Glycol 35,000 kDa | Sigma-Aldrich, St. Louis, MO | ||
| Hela | ATCC, Manassas, VA | ||
| HepG2 C3A | ATCC, Manassas, VA | ||
| NIH 3T3 | ATCC, Manassas, VA | ||
| Cell Tracker | Invitrogen, Carlsbad, CA | ||
| DMEM | Gibco, Carlsbad, CA | ||
| RPMI | Gibco, Carlsbad, CA | ||
| F12 | Gibco, Carlsbad, CA | ||
| Fetal Bovine Serum | Gibco, Carlsbad, CA |
References
- Hatti-Kaul, R. Aqueous two-phase systems : methods and protocols. Methods in biotechnology. xiii, Humana Press. 440 (2000).
- Albertsson, P. A. k Partition of cell particles and macromolecules: separation and purification of biomolecules, cell organelles, membranes, and cells in aqueous polymer two-phase systems and their use in biochemical analysis and biotechnology. , 3rd ed, Wiley. 346 (1986).
- Yamada, M., et al. Continuous cell partitioning using an aqueous two-phase flow system in microfluidic devices. Biotechnol. Bioeng. 88 (4), 489-494 (2004).
- Soohoo, J. R., Walker, G. M. Microfluidic aqueous two phase system for leukocyte concentration from whole blood. Biomed. Microdevices. 11 (2), 323-329 (2009).
- Hahn, T., Hardt, S. Concentration and size separation of DNA samples at liquid-liquid interfaces. Anal. Chem. 83 (14), 5476-5479 (2011).
- Hatti-Kaul, R. Aqueous two-phase systems. A general overview. Mol. Biotechnol. 19 (3), 269-277 (2001).
- Hustedt, H., Kroner, K. H., Menge, U., Kula, M. -R. Protein recovery using two-phase systems. Trends in Biotechnology. 3 (6), 139-144 (1985).
- Keating, C. D. Aqueous Phase Separation as a Possible Route to Compartmentalization of Biological Molecules. Acc Chem. Res. 45 (12), 2114-2124 (2012).
- Helfrich, M. R., et al. Partitioning and assembly of metal particles and their bioconjugates in aqueous two-phase systems. Langmuir. 21 (18), 8478-8486 (2005).
- Diamond, A. D., Hsu, J. T. Prote. Partitioning in PEG/Dextran Aqueous Two-Phase Systems. AIChE Journal. 36 (7), 1017-1024 (1990).
- Y-T,, Zhu, Z. -Q. Modeling of interfacial tension of aqueous two-phase systems. Chemical Engineering Science. 54 (4), 433-440 (1999).
- Liu, Y., Lipowsky, R., Dimova, R. Concentration dependence of the interfacial tension for aqueous two-phase polymer solutions of dextran and polyethylene glycol. Langmuir. 28 (8), 3831-3839 (2012).
- Rha, C. Interfacial Tension of Polyethylene Glycol/Potassium Phosphate Aqueous Two-Phase Systems. Physics and Chemistry of Liquids: An International Journal. 38 (1), 25-34 (2000).
- Fang, Y., et al. Rapid Generation of Multiplexed Cell Cocultures Using Acoustic Droplet Ejection Followed by Aqueous Two-Phase Exclusion Patterning. Tissue Eng. Part C. Methods. 18 (9), 647-657 (2012).
- Tavana, H., et al. Nanolitre liquid patterning in aqueous environments for spatially defined reagent delivery to mammalian cells. Nat. Mater. 8 (9), 736-741 (2009).
- Tavana, H., Mosadegh, B., Takayama, S. Polymeric aqueous biphasic systems for non-contact cell printing on cells: engineering heterocellular embryonic stem cell niches. Adv. Mater. 22 (24), 2628-2631 (2010).
- Tavana, H., et al. Microprinted feeder cells guide embryonic stem cell fate. Biotechnol. Bioeng. , (2011).
- Tavana, H., Takayama, S. Aqueous biphasic microprinting approach to tissue engineering. Biomicrofluidics. 5 (1), 13404 (2011).
- Frampton, J. P., et al. Precisely targeted delivery of cells and biomolecules within microchannels using aqueous two-phase systems. Biomed. Microdevices. 13 (6), 1043-1051 (2011).
- Hossein Tavana, K. K., Bersano-Begey, T., Luker, K. E., Luker, G. D., Takayama, S. Rehydration of Polymeric, Aqueous, Biphasic System Facilitates High Throughput Cell Exclusion Patterning for Cell Migration Studies. Advanced Functional Materials. 21 (15), 2920-2926 (2011).
- Falconnet, D., et al. Surface engineering approaches to micropattern surfaces for cell-based assays. Biomaterials. 27 (16), 3044-3063 (2006).
- Lim, J. Y., Donahue, H. J. Cell sensing and response to micro- and nanostructured surfaces produced by chemical and topographic patterning. Tissue Eng. 13 (8), 1879-1891 (2007).
- Ringeisen, B. R., et al. Jet-based methods to print living cells. Biotechnol. J. 1 (9), 930-948 (2006).
- Wright, D., et al. Generation of static and dynamic patterned co-cultures using microfabricated parylene-C stencils. Lab Chip. 7 (10), 1272-1279 (2007).
- Takayama, S., et al. Patterning cells and their environments using multiple laminar fluid flows in capillary networks. Proc. Natl. Acad. Sci. U.S.A. 96 (10), 5545-5548 (1999).
- Berthier, E., et al. Pipette-friendly laminar flow patterning for cell-based assays. Lab Chip. 11 (12), 2060-2065 (2011).
- Davidson, R. L., O'Malley, K. A., Wheeler, T. B. Polyethylene glycol-induced mammalian cell hybridization: effect of polyethylene glycol molecular weight and concentration. Somatic Cell Genet. 2 (3), 271-280 (1976).
- Johnson, D. M., LaFranzo, N. A., Maurer, J. A. Creating Two-Dimensional Patterned Substrates for Protein and Cell Confinement. J. Vis. Exp. (55), e3164 (2011).
- Moon, S., Lin, P., Keles, H. O., Yoo, S., Demirci, U. Title Cell Encapsulation by Droplets. J. Vis. Exp. (8), e316 (2007).



