Summary
この資料に記載されている間接免疫プロトコルは、検出およびマウス乳腺中のタンパク質の局在を可能にします。完全な方法は、乳腺のサンプルを調製するために蛍光顕微鏡により画像を、組織切片の免疫組織化学を実行し、画像を再構成するために与えられています。
Abstract
間接免疫蛍光を検出し、組織中の目的のタンパク質を特定するために使用されます。ここに提示されたプロトコルは、タンパク質の免疫検出のために完全かつ簡単な方法は、乳腺泌乳マウスを例に説明しています。特にマウス乳腺腺、組織固定および凍結組織切片の解剖に関する組織サンプルの調製のためのプロトコールは、詳述されています。標準プロトコルは、任意の抗原回復工程を含む、間接免疫蛍光法を実行することも示されています。ラベルされた組織切片の観察と同様に、画像取得および後処理も記載されています。この手順は、動物組織のコレクションからのタンパク質の細胞内局在に、完全な概要を説明します。この一般的な方法は、他の組織サンプルに適用することができるが、それは、試験した各組織/一次抗体に結合するように適合されるべきです。
Introduction
乳腺は、その主な機能新生児を養うためにミルクを生産することである非定型哺乳類の外分泌器官です。乳房組織の開発は主に出生後に発生し、上皮が周囲の間質に侵入するユニークなプロセスによって特徴付けられます。この組織は、同時に生殖状態の変化( 図1)で、特に大人の寿命の間に、多くの変更(増殖、分化および回帰)を受けます。組織の全体的な形態に加えて、異なる細胞型の割合だけでなく、乳腺内での配置が劇的に発展1-5中に変化します。
胚生活の間に、乳腺上皮は、胎生10.5(E10.5)( 図1Aの周りの正中線の両側に前後と後肢の間、外胚葉のわずかな肥厚と層化によって定義されている乳房ミルクラインから派生)。E11.5で、ミルクラインが対称的に再現可能な場所で乳腺のミルクラインに沿って位置し、周囲の間充織が凝縮し始めている個々のプラコード、に分割します。プラコードは、真皮に深く沈み始め、乳腺間葉は乳腺芽(E12.5-E14.5)の周りに同心円状の層に編成されます。 E15.5の時点では、乳腺上皮は、増殖し、脂肪パッドに向けて乳腺間葉を通して押し出す主な芽を形成するために細長くを開始します。主な芽は乳首シースの形成によってマークされ、皮膚への開口部を有する中空内腔を、開発しています。 E18.5では、伸長ダクトは脂肪パッドに成長していると小さな樹状の管系に分岐した脂肪パッドに含まれます。開発は、基本的に逮捕され、基本的な乳腺は思春期までmorphogenetically静止のまま。男性の胚では、アンドロゲン受容体の活性化は消え芽の変性につながりますE15.5によって。 E18のように、乳房の発達は、思春期6-9まで停止します。
出生時に、乳腺はゆっくり伸びや枝初歩的な管系(アイソメトリック成長)を保有します。思春期の開始時に、ダクトの先端に位置する球状構造が末端芽(TEBS)が、キャップ細胞の外層と細胞の多層内部コア(体細胞)から形成されていると呼ばれます。これらの構造は非常に増殖性であり、ホルモンの合図に応答して、周囲の間質組織に潜入。乳管の伸長でTEBS結果内増殖は、分枝形態形成と相まって。このプロセスは、ニップル( 図1B、思春期)から発せられる基本的な上皮樹状のネットワークの構築につながります。上皮が全体の脂肪パッドに侵入した時に生後〜10〜12週目に、その拡張は停止し、TEBSが消えます。乳管の開発は、動的変化、 すなわち 、successiを受けます発情周期10( 図1B、成人)によると、上皮細胞の増殖と回帰しまし。
妊娠の発症から、乳房組織は、授乳の準備をするために重要な成長と形態学的変化を受けます。乳腺上皮は、広範囲に増殖し、分化する、高度に分岐した尿細管肺胞ネットワークにつながります。付随して、乳腺上皮細胞(のMEC)は、偏光と乳製品を合成し、分泌できるようになります。 MECは、収縮筋上皮細胞に囲まれており、結合および脂肪組織、血管や神経終末( 図1B、妊娠)からなる間質に組み込まれている多数の肺胞構造(腺房)に整理します。さらに、のMECの基底側は基底膜(細胞外マトリックス)に密着しており、これら2つのエンティティ間の相互作用は、しっかりと乳房の両方の形態形成および分泌機能を調節しますRY上皮11-13。
これらのプロセスはすべて最も重要なのはhormones14、パラクリン因子や細胞外マトリックスであるの様々な環境手がかりの作用に依存しています。例えば、プロゲステロンは広範側分岐15を誘導し、そのalveologenesis、プロラクチン(PRL)16,17との組み合わせで、肺胞の分化を促進し、維持します。ステロイドとPRL18、サイトカインおよび開発に関連するシグナル伝達経路に加えて、(Wntおよびシグナル伝達経路ノッチ)も乳腺系譜コミットメントと開発19-21に関与しています。妊娠の終わりには、管腔のMECは、肺胞の内腔に初乳として知られるタンパク質が豊富な牛乳を生成し始めます。また、プロゲステロンは、上皮透過性に作用し、タイトジャンクションがまだ開いているので、初乳はまた、母体血流中に見出されます。
分娩後、mammarY上皮は( 図2、乳腺上皮)ほぼすべての乳腺ボリュームのアップかかり、高度に組織化されています。乳汁産生の単位、すなわち肺胞( 図2、肺胞)は、それらの頂端細胞膜の内腔を画定して、偏乳房上皮分泌細胞(たmESC)の単層によって形成されます。肺胞は、外部環境( 図2、葉)にミルクを排出ダクトに接続されたローブにグループ化されている小葉に自分自身を配置します。母乳は、発生すなわち 、たmESCは主に胎盤ホルモンの低下(主にプロゲステロン)( 図1B、母乳)によってトリガミルクの豊富な量を分泌し始めます。乳タンパク質遺伝子は、主に授乳時に放出され、下垂体PRLに応答して、妊娠から授乳9,22,23の範囲で定義された一時的な時間経過で活性化されます。付随して、たmESCと細胞外マトリックス間の接触は、乳タンパク質SYNTを刺激両方携帯インテグリンおよびラミニン24,25の間の相互作用を介して媒介され、たmESC 26,27においてアポトーシスを抑制した信号を通じてhesis。これらのシグナル伝達経路は、特定の転写因子の活性化を介して29乳タンパク質遺伝子プロモーター28の活性化をもたらします。細胞間接触は、頂端の極性の確立と乳製品のベクトル分泌を含む分化のいくつかの側面のためにも重要です。授乳やたmESCの開始後速やかに近いタイトジャンクションは細かく新生児の栄養要求に応じて、血液からの分子の取り込みだけでなく、乳成分の合成、輸送および分泌を調整。授乳時には、肺胞を取り巻く筋上皮細胞の収縮は、オキシトシンに反応して発生し、ダクトを通って乳首に射乳につながります。ミルクはタンパク質を含む複雑な流体(主にありますカゼイン)、糖(主に乳糖)、脂質、ミネラル、ならびにそのような免疫グロブリンA(IgAの)、成長因子およびホルモンなどの生理活性分子。カゼイン、すなわち分泌経路に沿って搬送ミセル、カゼイン、超分子構造に組み立てられ、合成され、その後、エキソサイトーシスにより放出され、すなわち 、MESCの頂端細胞膜でのカゼイン含有分泌小胞の融合(のSV)( 図2)。
細胞内のトラフィックは、膜状の区画間の材料の交換に依存しており、可溶性N-エチルマレイミド感受性融合(NSF)付着タンパク質(SNAP)受容体(SNARE)30,31を含んでいます。 SNAREタンパク質ファミリーは、ターゲット膜に局在水疱性小胞膜内に存在するのSNARE(V-のSNARE)、および目標のSNARE(T-のSNARE)に細分されます。それらのコイルドコイルドメイン、VおよびTのSNAREは非常に安定な4ヘリックス束複合体を形成するために組み立てを通してジッピングによって、目と称される電子スネア複合体。この複合体は徐々に近接30,32にそれらをもたらすことによって、2つの対向する脂質二重層の融合を促進します。その後、SNARE複合体は、NSFアデノシン三リン酸によって解離され、そのアダプタータンパク質SNAPおよびSNAREタンパク質は、起源33のその区画に戻して再利用されています。興味深いことに、各SNAREタンパク質は、主に個別の細胞区画内に存在し、SNAREのペアリングは、細胞内の融合事象34の特異性に寄与することができます。以前の研究では、少なくともタンパク質23(SNAP23)および小胞関連膜タンパク質8(VAMP8)、およびシンタキシン(のStx)のシナプトソームが関連することを示唆している-7および-12カゼインエキソサイトーシス35,36における役割を果たしています。これらのタンパク質はまた、乳の脂質画分、 すなわち 、乳脂肪球(MFGs)37に関連して発見されています。現在の支配的なモデルは、細胞質脂質滴(CLDs)は中立リットルの蓄積によって形成されていることを仮定しますipids(主にトリアシルグリセロールおよびステロールエステル)および小胞体(ER)膜38〜41の2リーフレットの間の母体の食事由来のコレステロール。彼らは(直径1〜10ミクロン)MFGsとしてリリースされたmESCの頂端側に輸送されながら大CLDsはMESC頂端形質膜によって包まれて、出芽によって少なくとも部分的には、小さいCLDsの融合によって形成され、 40-42。子犬が乳離れした後に授乳を停止し、たmESCは徐々にアポトーシスによって死ぬ、バック思春期状態( 図1B、退縮)に乳房組織の回帰につながります。
免疫蛍光(IF)は、研究および臨床診断の両方で、生物学のほぼすべての面で使用される一般的な分析実験室の方法です。技術は、組織切片(免疫組織化学、IHC)または細胞(免疫細胞化学、ICC)のサンプル上で行うことができます。この強力なアプローチはfluorescent-の使用に依存しています具体的にはこのようにして、蛍光顕微鏡を通じて組織分布の可視化を可能にする、目的の抗原に(直接または間接的に)結合する標識された抗体。蛍光シグナルは、主に品質や濃度の抗体と試料の適切な処理に依存します。単純な間接免疫蛍光(IIF)プロトコルは、乳製品(カゼインとMFGs)およびマウス乳房組織( 図3)の凍結切片上の乳製品分泌(butyrophilin(BTN1)、SNAREタンパク質)に関与するタンパク質を検出するために提示されます。このプロトコルは、組織採取から画像後処理、クリティカルおよびオプションのステップだけでなく、いくつかの技術的な勧告に至るまで、完全なIHCの概要を提供していますが、また提示し、議論されています。
Subscription Required. Please recommend JoVE to your librarian.
Protocol
CD1マウスは、INRA(UE0907 IERP、ジュイ・アン・ジョザス、フランス)で飼育しました。動物のケアのすべての倫理的側面は、農業のフランスの省が定めた関連するガイドラインとライセンス要件を遵守。使用手順は、(Cometheaジュイ・アン・ジョザス/ AgroParisTechから契約12/097)ローカル倫理委員会によって承認されました。
1.乳腺サンプル調製
- マウス乳腺の解剖
- 頸椎脱臼により授乳の10日目にマウスを安楽死させると、その腹部を上に向けてダウン動物をピン。
- エタノールで腹側領域を湿らせ、ペーパータオルでそれを乾燥させます。
- 鉗子を使用して、2つの後ろ足の間に腹部の皮膚を引き上げ、鋭いハサミで約1cmの(唯一の皮膚を通して)切開を行います。この最初の切開から始めて、その後、マウスの首に皮膚をカットするはさみを使用してください。腹膜およびPIから皮膚を引き離しますnは時間の皮膚の片側の下、それは教えてストレッチ。
- 綿棒で皮膚からそれらを押し、最後に引いたり離れ腹膜からそれらを切断することにより、腹部および鼠径部乳腺を収集します。
注:このステップでカーミン染色全腺43内の乳腺上皮を可視化するために行うことができます。このアプローチは、(インビボでの治療において、生理的発達段階、疾患)は、様々な条件下での乳腺の全体的な形態を分析するのに有用であり得ます。 - 腹部の接合部と鼠径腺44にあるリンパ節を削除します。
- 乳腺組織固定
- メスで3ミリメートル3断片に乳腺組織を切断し、すぐにできるだけ多くのミルクを除去するためにリン酸緩衝生理食塩水(PBS)溶液のpH 7.4、これらの断片をすすぎます。
- すぐに紙の上に断片を乾燥タオルと氷上で10〜15分間、4%パラホルムアルデヒド(PFA、HCHO、32%ホルムアルデヒド溶液、注意)を含有する冷PBS溶液に入れて。
注:これはIIF36によっておよび/ またはin situハイブリダイゼーション45に乳腺組織切片上でその後の分析を可能にするために十分な時間です。アルデヒド固定液は、組織片(毎時〜1-3 mm)のではなく、ゆっくりと浸透するようしかし、この時間は、組織サンプルの最適な固定を確実にするために拡張することができます。また、固定液(本研究では詳述しない)で麻酔した動物を灌流することにより、in vivoで組織を固定します。
- スクロース注入
- すぐに冷PBSで乳腺の断片をすすぎ、穏やかに振盪下に4℃で16〜48時間、40%スクロース(D-サッカロース、C12H22O11、ミスター342.3グラム/モル)を含有する冷PBS溶液でそれらを浸します。
- 組織埋め込み
注:このステップでは、乳房のフラグメントは小さな断片を作るために再切断することができる(2-3 mmの3)またはその形状を調整します。- 適切にプラスチック金型にラベルを付け、OCT化合物と金型の体積の3分の1を記入し、室温で維持しました。金型ごとの乳房組織の一つの断片(2-3 mm 3で)を配置し、OCT化合物でそれをカバーしています。
- 液体窒素(アルミのシート上や金属篩を用いて)の表面に金型を置き、製品を凍結することができます。
注:これは、液体窒素中で金型を浸漬する前に、固体と白にならなければなりません。
- 組織切片が実行されるまで-80℃で凍結したサンプルを保管してください。
2.凍結組織セクショニング
注:基本的に冷凍庫内部ミクロトームでクライオスタットは、凍結組織切片を作成するのに必須です。より低い温度は、多くの場合、処女乳腺などの脂肪または脂質の多い組織のために必要とされます。
- ℃〜-26にクライオスタットの温度を調整し、それがスタビを有するまで待ちますlized。全体セクショニング手順を通して、-26℃で凍結した組織ブロックを維持します。絶対に手続き中の任意の時点で組織を解凍することは避けてください。
- 少なくとも10分間、クライオスタット内にそれらを配置することにより、C°-26にカミソリの刃、切断のサポート、アンチロール装置とブラシを冷却します。また、セクションが行われるように、ガラススライドを保存できるようにするために、クライオスタットの内側スライドボックスを配置します。
- 適切に組織切片を採取し、室温でそれらを維持するために使用されるガラススライドにラベルを付けます。そうでない場合は組織切片は、それらに付着しません。クライオスタット内部モールドからサンプルを削除します。
注:正に荷電したガラススライドを使用すると、大幅により高い静電引力に新鮮凍結組織切片の接着に有利であろう。 - (室温で維持される)10月化合物と金属組織のディスクの表面を覆い、その上に凍結サンプルを押してください。ウェットクライオスタット内部にマウント置き、共同しましょう少なくとも15分間OL。
- クライオスタットのディスクホルダに湿ったマウントを配置します。 5-6μmのカットの厚さを調整し、可能な場合は、新しい鋭い刃を使用するか、少なくともいくつかの組織はすぐに退屈なことになるので、各サンプルを切断するために使用されるブレード上の領域を変更します。
- スライスが均等にかつ正確に形成されるまで、封入剤のカットを行うことで、カミソリの刃の上にアンチロール装置の位置を調整します。理想的には、アンチロール装置は、1mm程度カミソリの刃の上にステップインします。
- 設定が正しいならば、連続的に均一な運動でホイールを回すことで、組織切片を行います。温度が理想的でない限り、組織切片は、性質上、丸くしようとします。
- 取得し、スライドガラス上に、必要に応じてそれを配置するために、ステージ全体のセクションを操縦するためにブラシを使用してください。凍結組織ブロックおよび/または剃刀の刃上に存在する可能性が残ってクリーンアップするためにブラシを使用してください。
- 引くユーザーに向けた組織切片とクライオスタットのステージにそれを押すことは避けてください。それは、ステージ上の組織切片の接着、ガラススライドでそれを回復することができないことにつながる可能性としてクライオスタットのステージに組織切片を押す避けてください。
- セクションの上にそれを保持し、組織切片に触れ、それを下に傾けることにより、スライドガラスの表面でそれらをピックアップして、組織切片を一つずつ取り出します。
注:組織切片を迅速に静電引力による温かいガラスに付着します。いくつかの組織切片は、同じスライド上に配置されている場合は、それらをオーバーラップするようにし、スペースには十分に個別に疎水性の円で囲むことができないように注意してください(3.1.1項を参照してください。)。
3.間接免疫
- セクションの検索
- スライドに取り付けられた組織の周りに疎水性の円を描くように、疎水性バリアペンを使用してください。室温で約1分間、サークル、乾燥をしてみましょう。トンの周りに線を引きます細かい黒の油性マジックでの問題のセクションだけでなく、ガラススライド側の組織切片である1と反対。
注:この円は、撥水とアセトンとアルコールに不溶です。したがって、IHC手順中に使用される水溶液に対する障壁を提供し、必要な試薬の量を減少させます。 - 室温で数分間のPBS〜250μLのドロップでそれらを覆うことにより、組織切片を再水和。 10〜15分間、PBS中の新たに調製した3%PFA溶液を〜250μlのでそれらを覆うことにより、組織切片を固定してください。
注:必要に応じて、この場合に、PBS中のアルデヒド急冷溶液(50mMの塩化アンモニウム(NH 4 Clで、氏53.5グラム/モル)を使用するか、またはPBS中の0.1Mのグリシン(C 2 H 5 NO 2、ミスター75.07グラム/モル) )固定反応を停止します。シンプルで豊かなPBS洗浄、未反応のアルデヒドを除去するために、一般的に十分です。
- スライドに取り付けられた組織の周りに疎水性の円を描くように、疎水性バリアペンを使用してください。室温で約1分間、サークル、乾燥をしてみましょう。トンの周りに線を引きます細かい黒の油性マジックでの問題のセクションだけでなく、ガラススライド側の組織切片である1と反対。
- 抗原検索(オプション)
- ビーカー内のAR溶液(100 mMトリス(C 4 H 11 NO 3、ミスター121.14)は、5%尿素(NH 2 CONH 2、ミスター60.06)は、pH 9.6)を配置します。 AR溶液の量は、完全にガラスホルダーに入れたガラススライドをカバーするのに十分なものでなければなりません。
- 温度計で温度を監視することにより95°CまでAR溶液を予熱した後、適切なラックにスライドガラスを置き、ホットバッファにラックを飛び込む、カバーは、蒸発を制限し、95℃で10分間インキュベートします。
- 水浴からビーカーを取り出して、バッファ内の別の10分間ガラススライドを残します。
- PBS(〜250μL/セクション)を組織切片をすすぎ、溶液を用いて、それらを飽和RTで少なくとも30分間、PBS中の3%ウシ血清アルブミン(BSA、〜250μL/セクション)の。
- 各組織切片上の2%BSAを含むPBSで希釈した一次抗体の30〜50μLを入れてください。
注:このボリュームは完全に組織切片をカバーするドロップを形成するのに十分です。 - 一次抗体なしのネガティブコントロールを実行するために組織切片上で単独の希釈剤(PBS中の2%BSA)の同体積を置きます。
- 系統的各IHC実験では、このネガティブコントロールが含まれており、(これは二次抗体、および/または組織の自家蛍光に非特異的標識)は、実験のバックグラウンドを推定するために使用される各二次抗体のために行います。ポジティブ又はネガティブコントロールの他のタイプは、(説明を参照)、標識の特異性を確実にするために行うことができます。
- 4℃の加湿ボックス、O / Nでガラススライドを置きます。
注:使用した一次抗体は、マウスモノクローナル抗サイトケラチンました寛大MCネビル、コロラド州保健大学が提供する8(CK8、1:50希釈)、マウスモノクローナル抗サイトケラチン14(CK14、1:50希釈)、ウサギポリクローナル抗マウスカゼイン(#7781、1:50希釈、科学総合研究センター、CO、USA)、ウサギポリクローナル抗BTN1(1:寛大IHメイザー、動物や鳥科学科、メリーランド大学、カレッジパーク、メリーランド州、米国)、ウサギポリクローナル抗Stx6(が提供する300希釈、寛大S. Tooze、癌研究イギリス、ロンドン研究所、ロンドン、英国)とウサギポリクローナル抗VAMP4(1:50希釈)により提供される1:50希釈、。 - 十分にRTで10分間、少なくとも4回、PBSで組織切片を洗浄します。
- 、2%BSAを含有するPBS中のすべての組織切片上でこの溶液の30-50μLを入れ、そして1.5時間インキュベートする。適切な二次抗体(300希釈ローダミン結合ヤギ抗ウサギIgG(H + L)、1)希釈RTで。
- 蛍光色素は、感光性分子であるので、ありません彼らの分析まで、光に組織切片を公開します。細胞膜は低い標識を妨害することができる緑色自己蛍光を発生する傾向があるので、組織切片上のIIFは、赤色蛍光体に結合された二次抗体を好みます。また、赤色の蛍光団結合二次抗体を選択すると、中性脂質(下記参照)の同時標識化を可能にします。
- 完全に室温で10分間、PBSで少なくとも4回の組織切片を洗浄します。
- いくつかの実験のために、抗原/抗体足場を安定化させるために室温で10分間、PBSで希釈した2%PFAを有する試料をインキュベートすることによって、ポスト固定を行います。しかし、この手順は、ほとんどの場合には、省略することができます。
- BODIPY 493の3μgの/ mlで含むPBS溶液の30~50μlの組織切片をインキュベートすることによってCLDsとMFGs、色中性脂質を可視化します/ RTで10分間503。急速にPBSで2回組織切片をリンス。
- RTで10分間DAPI(4-6ジアミジノ-2-フェニルインドール、5 mg / mlのストック溶液)の3μMを含むPBS溶液を30~50μlの核DNA対比。観察用のスライドをマウントする前にPBSで2回組織切片を洗浄してください。
- PBSを削除し、各組織部にメディアをマウントするのドロップを置きます。
- 液滴の外縁に接触して、スライドに対する角度でカバースリップの片側を置き、ゆっくりとカバーを下げて、気泡を避けます。液体は数分間スライドガラスとカバースリップの間に広がった後、ペーパータオルでメディアをマウントするの過剰を削除することができます。
- 観察されるまで、光への曝露を防止するために4℃でマニキュアや店舗組織切片を用いてガラススライドにカバースリップをシール。
4.蛍光観察画像の取得
注:画像取得ソフトウェアによって制御されるカメラを備えた蛍光顕微鏡をIHCの結果を観察する必要があります。
- 画像を取得する前に、ラベル付けの強度を確認し、陰性対照を見て、実験の背景を評価します。個別蛍光標識(カラーチャンネル)の写真を取得します。
- 各カラーチャンネルの同じ条件(露出と一般設定)で対応するコントロールのものを含む、すべての画像を取得します。
- 従来の顕微鏡
- 63(油浸、NA 1.3)目標とDP50撮像カメラを×20が×、標準フルオレセインイソチオシアネートのためのフィルター(FITC、緑)、ローダミン(赤)およびDAPI(青)の排出量を備えた顕微鏡と落射蛍光顕微鏡を実行します。
- 共焦点顕微鏡検査
- MICROSと共焦点顕微鏡を実行します63(油浸、NA 1.4)×する×20を使用して、ZENソフトウェアを装備した目標とレーザーの488と568 nmの励起波長を対応。
5.画像処理
注:すべての画像の後処理は、ImageJのフリーソフトウェア(http://imagej.nih.gov/ij/)を使用して実行されます。
- 画像をスーパーインポーズ(マージ)
- (ファイル/開く)結合される各チャネルで取得された画像を開きます。 8ビットグレースケール画像を扱う場合は、ルックアップテーブル(画像/ルックアップテーブル)を使用して、各チャンネルに人工の色を属性。
- (画像/カラー/チャンネルをマージ)」チャンネルを統合」コマンドを使用して、グレースケールまたはカラー画像から合成画像を生成し、各チャンネルに色を帰。
- (ファイル/開く)を結合される各チャネルで取得されたスタックを開いて、&チャンネルを統合」コマンドを使用して、イメージが同じように重畳スタックの実行#8221;各チャンネルに色を帰する(画像/カラー/チャンネルをマージ)。イメージシーケンスとして、あるいは映画(セクション5.4を参照)のような複合スタックを保存します。
- 画像スタックZ突起
- 画像平面(z軸)に垂直な軸に沿ってそれらを投影することによって画像スタックのすべての画像の2次元図を提供するために、Z投影機能(画像/スタック/ Zproject、最大強度)を使用します。 「最大強度」オプションは、各ピクセルは、スタック内のすべての画像の上に最大値が含まれていた画像を作成します。これは、特定のチャネルまたは複数のチャネルの重ね合わせ後に全体画像スタックを通して観察すべての染色の可視化を可能にする、単一の画像を生成します。
- 画像スタックの3D投影
- 平面上の回転量の突起のシーケンスを生成するために3D投影コマンド(画像/スタック/ 3Dプロジェクト、明るい点、y軸)を使用します。 SUの視覚的レンダリングrfacesと内部構造は、両方の投影法(最も近い点、ここで使用される最も明るい点()、または平均値)に依存し、可視化パラメータは、選択されました。アニメーションシーケンスの各フレームは、異なる視角から突出した結果です。
- 直交3軸(y軸は、ここで選択された)のそれぞれの周囲に作成した3D画像を回転させます。単一の画像やムービーのように製造シーケンスを保存します。
- 映画への変換画像スタック
- 画像スタック(ファイル/開く)を開き、「AVI」(ファイル/名前を付けて保存/ AVI)コマンドを使用して、.AVI形式の動画として保存します。
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
乳腺は胸部やげっ歯類における腹部の両方の腹側構造に沿って配置された皮下腺です。妊娠中のマウスの腺の5組の位置は、図4に示されている。乳腺の形態が劇的に完全授乳( 図1B)の準備をするために必要な機能の変更を反映し、その開発中に変化します。バージンまたは未経産の動物では、乳腺が見えにくいかもしれ薄い脂肪間質内に埋め込まれた疎分岐鎖状の腺管上皮で構成されています。妊娠の発症から、乳腺上皮増殖した (図4)を参照して削除することが容易になり、より大きな乳腺になり、拡大します。授乳中は、乳腺組織が厚く、による牛乳の存在に白く表示されます。腹部および鼠径部乳腺のみを頸部および胸部乳腺グランので、収集されDSが少なく簡単に筋肉との密接な関係のために削除されます。いくつかの実験のために、子犬は、たmESC 46,47によって乳汁分泌を制限するために犠牲にする前に授乳女性4~6時間から分離することができます。
乳腺筋上皮および上皮細胞の同定
肺胞を取り囲む収縮筋上皮細胞は、特にこれらの細胞型の各々により発現されるマーカーに対する抗体の使用を介して腔たmESCと区別することができます。乳腺では、現在使用されているマーカーは、サイトケラチン(CKS)です。 CKSは、上皮組織に見られる細胞骨格の中間フィラメント(平均直径10ナノメートル)を形成するために、重合の細胞質タンパク質の大きなファミリーです。中間径フィラメントは、非常に安定であり、細胞アーキテクチャの機械的支持を提供し、細胞 - 細胞接着および基底細胞の結合に寄与することにより、組織を組織組織との相互作用。上皮細胞によって発現CKSのサブセットは、主に上皮の種類、開発の段階とその分化状態に依存します。さらに、これはまた、上皮の悪性対応物に適用されます。したがって、これらのマーカーは、生理的条件下で、組織内の細胞集団を特徴付ける簡単かつ有用なツールであり、外科的病理48における腫瘍の診断及び特徴付けのために使用されます。
正常な乳腺では、筋上皮および管腔たmESCの細胞がそれぞれCK14とCK8のその差次的発現、( 図5)に基づいて区別することができます。これらの細胞質マーカーは、PFA固定とAR後の授乳中のマウスの乳房のセクションで検出されました。画像は、従来の落射蛍光顕微鏡を用いて取得しました。 CK8は管腔たmESC( 図5、CK8)の細胞質全体に分布しているように見えます。赤の背景が観察ことに注意してください核のいくつかの層( 図5、-Ig1、核)を表示する青色のDNA標識、によって示唆されるように、一次抗体なしのネガティブコントロール( 図5、-Ig1)のためのdは、組織切片の折りたたみに主に起因しています。 CK14は、具体的には、肺胞( 図5、CK14)の基部に位置平らで細長い筋上皮細胞で観察されます。これらの収縮性細胞に存在する- (SMA)(49、図4参照)筋上皮細胞を同定するための別の一般的な方法は、α-平滑筋アクチンを検出することです。
マウス乳製品の検出
分娩後、完全に分化したmESCは、牛乳の豊富な量を生産し始めます。乳成分は異なる経路40,50によって分泌されます。脂質は頂端PLの出芽によりMFGsとしてリリースされているのに対し、カゼインミセルは、ゴルジ体由来のSVのエキソサイトーシスによって分泌されますたmESCのASMA膜( 図2、乳腺上皮分泌細胞)。いくつかの実験のために、子犬は、乳汁分泌46,47を遅くするために、乳腺を収集する前に女性の4-6時間から分離されます。これらの条件下では、たmESCの頂端細胞膜および内腔の内容は容易に肺胞が収縮され、内腔が閉じているので、授乳中ではない場合である、観察することができます。などのSNAREなどの膜輸送に関与するタンパク質を研究する。また、分泌を遅くすることも不可欠です。実際、ドナーおよびアクセプター区画とその細胞内局在性との間のサイクルは、膜代謝回転が高い場合、標識は、多くの場合、拡散するため、すなわち 、授乳中に決定することは困難であるスネア。そのため、子犬を除去することにより、乳汁分泌を遅くすることは、Tとv-SNAREとは、優先的にドナーに存在する場合のSNAREの細胞内局在を調べるために、適切な条件を提供しますおよびアクセプター区画は、それぞれ(下記参照)。
図6は、子犬の存在下での授乳の10日目での授乳マウス乳腺におけるカゼインの局在、( 図6、+ P)または非存在下で( 図6、-p)を示しています。組織切片は、従来の落射蛍光顕微鏡(右の3つの列)、共焦点顕微鏡( 図6、左の列)の両方で観察されました。授乳中は、カゼインは、主に先端領域( 図6、+ P、矢印)に蓄積されているように見えます。共焦点顕微鏡は、明らかに従来の顕微鏡( 図6、カゼインで観察することはできません子犬の存在下でたmESCの基底側(図6、+ P、矢印)、で、より少ない程度にあるが、カゼインも存在することが明らかになりました)左と右のパネルを比較します。実際、広視野落射蛍光、サンプルが発する蛍光(背景のfluorescenCE)が励起されたボリュームを通過して(アウト・オブ・フォーカス蛍光)は、対物焦点面で観察されたオブジェクトの解像度を変更します。これは、厚さの試験片(2ミクロンより厚い)のために特に当てはまります。被写界深度を制御することができ、バックグラウンド蛍光は、焦点面から除外するとして共焦点顕微鏡は、落射蛍光用に調製標本から高品質の画像を得ることができます。また、子犬の存在( 図6、+ P)で、肺胞の内腔は非常に閉じており、たmESCの頂端側は子犬の不在下でより良く観察される( 図6、-p)、時のルーメン肺胞が原因乳製品の蓄積に拡張しています。乳汁分泌が遅くなる場合には、カゼインは、( 図6、-p、矢じり)頂端形質膜の下に蓄積され、明確たmESC( 図6、-p、矢印)の基底側で観測されている表示されます。主要antibのない陰性対照ODYは任意のラベル( 図6、-Ig1)を示さありませんでした。
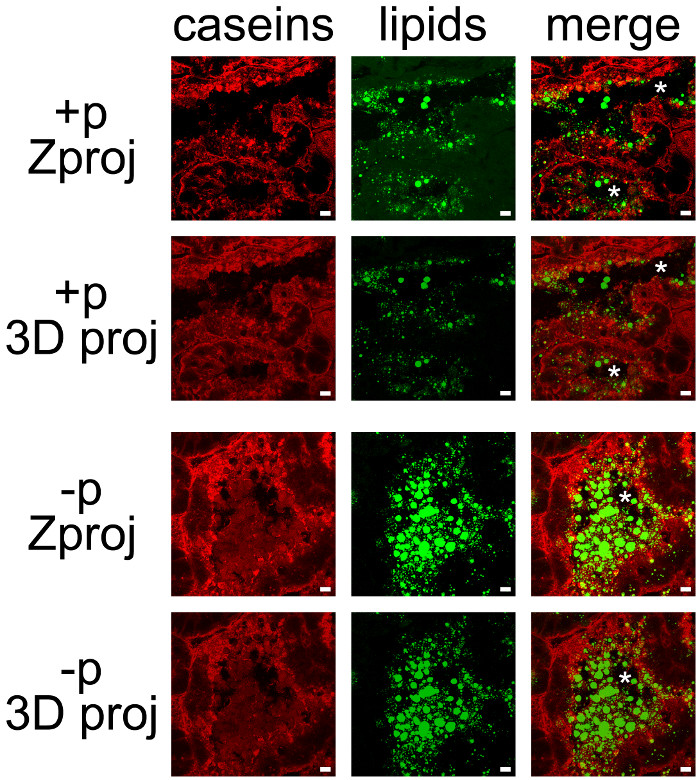
乳製品は、簡単にカゼインとCLDsとMFGs( 図7)の中性脂質の対比のためにIHCを組み合わせることにより、共同検出することができます。組織切片は、それぞれ( 図7、カゼイン、脂質)またはすべてのカラーチャンネル( 図7、マージ)はZ突起又は3D投影を生成するためにImageJので後処理した共焦点顕微鏡によりZ-スタックとして画像化しました。生成された画像シーケンスは、単一の画像( 図7、図8)や映画(補足作品を参照)として保存されています。
いくつかの標識は、その基底側に認められたが、女性が以前の仔( 図6、+ P)から分離されなかったときに、既に述べたように、カゼインは、主に、たmESCの頂端側( 図7、+ P)上に蓄積されました。 CLDsも主に大きな秘密のに対し、たmESCの先端領域に局在していますEDのMFGsは、肺胞の内腔に存在しています。 (+ pと-pを比較し、 図7)カゼインとMFGsを簡単仔の非存在下での肺胞の内腔に可視化されることに注意してください。 2カラーチャンネルの重ね合わせは、黄色のラベル( 図7、写真をマージする)を生成しないので、カゼインは、これらの条件のいずれかでCLDsまたはMFGsと共局在しないでください。ただし、画像スタックの後処理は、カゼインは、これらのタンパク質が(写真をマージし、 図7)MFGと相互作用することができることを示唆し、肺胞の内腔に分泌さMFGsを囲むことを示しています。 (各カラーチャンネルのZprojと3D PROJを比較し、 図7)を使用し、各後処理によって生成された画像の違いに注意してください。
butyrophilinの検出、MFGsのタンパク質マーカー。
BTN1はミルク51にMFGsに関連する主要なタンパク質の一つです。この膜貫通タンパク質はmainlですyがたmESCの頂端形質膜に局在し、その結果52出芽によって、そのリリース後製作所の表面で検出された。 図8は、授乳の10日目に、BTN1は主に頂端側形質膜に局在し、にしていることを示していますたmESCの先端領域でより少ない程度、。 BTN1も肺胞の内腔に存在するMFGsを囲むだけでなく、頂端CLDsの一部( 図8、3D projのマージ、矢印)。 ( 図8、3DのPROJ)上記のような結果は、取得された画像のZスタック( 図8、画像)から、またはImageJのの3D投影コマンドで生成された3Dビューとして抽出された一枚の画像として表示されます。単一のイメージは、タンパク質の頂端分布が、分泌MFGsまたは頂端CLDsのみ、Zスタックの3D再構成後に観察されるとBTN1の空間的な関連性を観察するのに十分であることに注意してください( 図8は BTN1画像を比較し、3D projのマージピクトURES)。 Zスタックはまた、タンパク質の分布のより良い空間ビューを与えるためにムービーとして再構成することができます。一人でBTN1ために取得された画像のZスタック( 補足映画1および3)または他の二つの色チャネルを重畳した(マージ、 補足映画2および4)の例として示されています。 Zスタック全体画像スタックの3D投影の( 補足映画1および2)または回転ビューとして(y軸に)上から下に画像ごとの画像を読み取ることができます( 補足映画3と4 )。
2 SNAREタンパク質の検出:Stx6とVAMP4
前述のように、のSNAREは、ドナーとアクセプターの膜の間のサイクル膜結合タンパク質です。それは勉強したときに、乳腺を収集する前に子犬から女性を分離したmESCの高い分泌活性に関連付けられている膜の代謝回転を遅くすることが良いですこれらのタンパク質。 Stx6とVAMP4は両方のトランスゴルジ網53,54に関連するものとして記載されています。しかしながら、これらのSNAREタンパク質はまた、分泌顆粒(Stx6)55,56及びゴルジ装置(VAMP4)57のような他の細胞区画のレベルで重要な役割を果たし得ます。以前の研究では、SNAREタンパク質がカゼイン分泌35,36において役割を果たすことを示唆しています。授乳中、Stx6とVAMP4がたmESCのサブ先端領域に配置されています。 Stx6は、ゴルジおよびトランスゴルジネットワーク( 図9、Stx6)に対応し、核とのMECの頂端膜の間に観察され、より少ない程度であるが、カゼイン含有のSV 36にも存在します。 VAMP4もたmESCのサブ先端領域に局在しているが、標識は、より点状であることが表示され、頂端形質膜の下に蓄積されている( 図9、VAMP4)によるCLDsとカゼインコンタ両方との関連にiningのSVの36。一次抗体なしのネガティブコントロールは、任意のラベルを生じませんでした。

図1.マウスの胚および成人期の間の乳腺発達。(A)マウスの乳腺は、(ピンク)外胚葉(水色)ミルクラインから胚10日目(E10)の周りを開発するために開始します。 E11.5では、プラコードは、乳腺の乳線に沿って対称的に形成し、周囲の間充織(ダークブルー)が凝縮し始めます。プラコードは芽(E12.5-E14.5)を形成し、E15.5に、乳腺上皮(ピンク)、増殖して脂肪パッド(ライトグリーンに向かって乳房の間葉を通して押し出す主な芽を形成するために長くする陥入します)。中空の内腔が形成され、ニップル(紫)を生じさせるために開きます。 E18.5で、乳腺上皮はrudimentaを形成外部に接続されたRY分岐構造。マクミラン出版社株式会社からの許可を得て6から適応:自然は思春期の間に(B)著作権2007年、遺伝学レビュー、乳腺上皮(紫)は大幅な成長段階(大規模な伸び、分岐部と横分岐)に入ります。妊娠、広範かつ急速な普及などに発生する分岐側の開始時に、完全に全体の乳房脂肪パッドに侵入乳腺上皮、かなりの拡大につながります。管腔たmESCはミルクを大量に分泌するときに乳腺上皮は、授乳中に高度に差別化機能状態に達します。授乳は、乳腺インボリュートを離乳後停止した場合。たmESCは、脂肪組織によって置換されるlobulo肺胞構造の消失につながる、アポトーシスおよび食作用によって除去されます。 http://brisken-lab.epfl.ch/researchのスキーム1および第2.2章から適応。 http://tvmouse.ucdavis.edu/bcancercd/22/index.htmlを。 この図の拡大版をご覧になるにはこちらをクリックしてください。
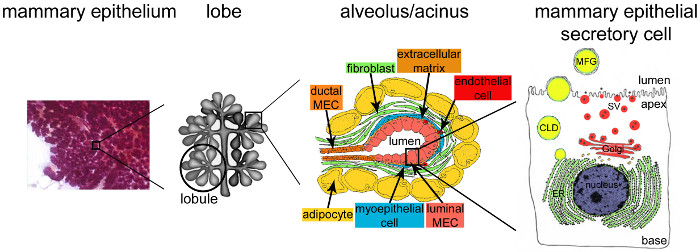
授乳中の乳腺の図2のアーキテクチャ。授乳中には、完全に開発され、高度に分岐した上皮(紫)は乳房組織の大半を占めています。上皮組織は、種々の細胞型(線維芽細胞、脂肪細胞、平滑筋細胞、血液およびリンパ管、および神経終末)を含有する基質に埋め込まれた尿細管肺胞構造によって形成されています。たmESCはローブを形成する小葉で組み立て腺房構造や肺胞に編成されています。各肺胞は、このようにミルクをDすることができるように、小葉と葉間のチャネルの高度に分岐したネットワークに接続されている機能的なミルク製造器です外に雨が降りました。各肺胞は偏光たmESCの単層で区切られている、の頂端側が中央内腔に接します。たmESCの基底側は、細胞外マトリックスと収縮筋上皮細胞に密着しています。乳製品はたmESCの頂端側で放出されます。脂質はたmESCの頂端形質膜の出芽により、乳脂肪球(MFGs)としてリリースされている間主要なミルク(カゼイン)は、ゴルジ体由来の分泌小胞(のSV)のエキソサイトーシスによってカゼインミセル(黒点)として分泌されます。 CLD:細胞質脂質滴。 ER:小胞体。 MEC:乳房上皮細胞。章2.2から適応。 http://tvmouse.ucdavis.edu/bcancercd/22/index.html。、図02 www.cellbiol.net/ste/alpHERCEPTIN1.php、図58で26から02、および50から。 この図の拡大版をご覧になるにはこちらをクリックしてください。
.withinページ= "常に"> 

図3.実験手順は、マウス乳腺の凍結切片の間接的免疫蛍光を実行します。乳腺は授乳の10日目でのCD1雌性マウスから収集されます。乳房組織をパラホルムアルデヒドで固定し、OCT化合物に包埋し、スナップ凍結される前に、スクロースに注入される小断片に切断されます。乳腺次に、サンプルを、それぞれ、プライマリおよび蛍光標識二次抗体との連続インキュベーションにより、薄凍結切片に切断し、IIFのために処理されます。マウントした後、サンプルを、続いて後処理することができる画像の取得を可能にする、蛍光顕微鏡で分析します。/53179/53179fig3large.jpg「ターゲット= "_空白">この図の拡大版をご覧になるにはこちらをクリックしてください。

図マウスの乳腺の4解剖学的位置左 :妊娠後期の段階でのマウス乳腺システムの腹ビュー。右:マウスでは妊娠後期の段階で乳腺の局在とアスペクト。授乳中、乳腺が厚いとによる肺胞における牛乳の存在のために白く見えることに注意してください。 http://ctrgenpath.net/static/atlas/mousehistology/Windows/femaleu/mousemammgldiagram.htmlとhttp://www.pathbase.net/Necropsy_of_the_Mouse/index.php?file=Chapter_3.htmlから適応。 こちらをクリックしてください。この図の拡大版を表示します。
-together.withinページ= "常に"> 
マウスの乳腺における管腔の上皮細胞および基底筋上皮細胞の図5同定腔たmESCと筋上皮細胞は、CK-8およびCK-14の発現に基づいて、授乳の10日目のマウスの乳腺にIIFによって識別されます、それぞれ。核DNAはDAPI(青)で染色しました。画像は、従来の落射蛍光顕微鏡を用いて取得しました。合成写真は、(マージ)は、それぞれ、カゼイン(赤)および核(青)に対応するラベルの重ね合わせを示しています。 -Ig1、一次抗体なしのネガティブコントロール。アスタリスクはルーメンを示しています。スケールバー=100μmである。 この図の拡大版をご覧になるにはこちらをクリックしてください。
E 6 "SRC =" /ファイル/ ftp_upload / 53179 / 53179fig6.jpg "/>
マウスの乳腺におけるカゼインの図6.細胞局在 。カゼインは、授乳の10日目のマウスの乳腺においてIIFによって検出されます。乳腺の存在(+ P)または仔の不在(-p)に雌から採取しました。画像は、従来で取得(右パネル、カゼイン、核およびマージ)または共焦点(カゼイン(赤)、左パネル)蛍光顕微鏡ました。両方の条件では、カゼイン(赤)は、先端領域(矢印)とたmESC(矢印)の基底で多かれ少なかれで検出されます。一次抗体なしのネガティブコントロールは、任意のラベル(-Ig1)が表示されません。核DNAはDAPI(青)で染色されています。合成写真は、(マージ)は、それぞれ、カゼイン(赤)および核(青)に対応するラベルの重ね合わせを示しています。アスタリスクはルーメンを示しています。スケールバー落射蛍光画像の= 100ミクロン(右パネル、カゼイン、核、マージ)および= 10µ共焦点画像(左列)のためメートル。 この図の拡大版をご覧になるにはこちらをクリックしてください。
マウス乳腺における乳製品の図7.細胞局在。カゼイン(赤)存在下での授乳の10日目のマウスの乳腺にIIFによって検出された(+ P)または仔の不在(-p)で。中性脂質(CLDsとMFGs)はBODIPY 503分の493(緑)で対比されています。複合写真(マージ)は、2つのラベル付けの重ね合わせを示します。画像は、共焦点顕微鏡を用いて、Z-スタックとして取得されました。 Z - スタックは両方のために、各チャネル(マージ)におけるZ突起(Zproj)またはスタック全体の3D投影(y軸)(立体PROJ)を生成するために、ImageJを用いて後処理しました。アスタリスクはルーメンを示しています。スケールバー=10μmである。 この図の拡大版をご覧になるにはこちらをクリックしてください。

マウスの乳腺におけるbutyrophilinおよび脂質の図8細胞局在。BTN1(赤)が仔の非存在下での授乳の10日目にマウス乳腺にIIFによって検出されます。中性脂質(CLDsとMFGs)と核DNAは、それぞれ、BODIPY 503分の493(緑)およびDAPI(青)で対比されています。画像は、画像のZスタックとして共焦点顕微鏡を用いて取得しました。結果は画像スタックから抽出された1つのイメージとして示した(画像、BTN1、脂質、核とマージ)全体画像スタックの3Dビュー(y軸)を生成したり、ImageJので後処理後にされている(3次元PROJ、BTN1 、脂質、核、マージ)。複合写真(マージ)を表示3つのカラーチャンネルの重ね合わせ。 -Ig1、一次抗体なしのネガティブコントロール。アスタリスクはルーメンを示しています。スケールバー=10μmである。 この図の拡大版をご覧になるにはこちらをクリックしてください。

図マウスの乳腺。シンタキシン6(Stx6)とVAMP4(V4) に2つのSNAREタンパク質の9細胞局在は、授乳の10日目のマウスの乳腺にIIFによって検出されます。画像は、従来の(CONV)落射蛍光または共焦点(LSM)顕微鏡を用いて取得しました。複合写真(マージ)各SNAREタンパク質(赤)のために、それぞれDAPI(偽緑色)で対比核DNAについて観察されたラベルの重ね合わせを示します。 -Ig1、一次抗体なしのネガティブコントロール。アスタリスクSは内腔を示します。共焦点画像と落射蛍光画像用= 100μmのため=10μmのスケールバー。 この図の拡大版をご覧になるにはこちらをクリックしてください。


表1免疫組織化学トラブルシューティングガイド。

補足ムービーマウス乳腺におけるbutyrophilin 1.ローカライズ。BTN1(赤)は、授乳の10日目のマウスの乳腺にIIFによって検出されます。画像は共同で取得しました Zスタックや映画を生成するために、ImageJので後処理としてnfocal顕微鏡。 Zスタックは、上から下に読み込まれます。 このビデオを見るにはこちらをクリックしてください。

補足ムービーマウス乳腺におけるbutyrophilinと中性脂質の2ローカライズ。BTN1(赤)は、授乳の10日目にマウス乳腺にIIFによって検出されます。中性脂質(CLDsとMFGs)と核DNAは、それぞれ、BODIPY 503分の493(緑)およびDAPI(青)で対比されています。画像は、各カラーチャンネルのZスタックのような共焦点顕微鏡を用いて取得され、3つのカラーチャンネルを重畳合成Zスタックを生成するためにImageJので後処理しました。得られた複合Zスタックは、上から下に読まれます。https://www.jove.com/files/ftp_upload/53179/supvid2.mp4「ターゲット= "_空白">このビデオを見るにはこちらをクリックしてください。
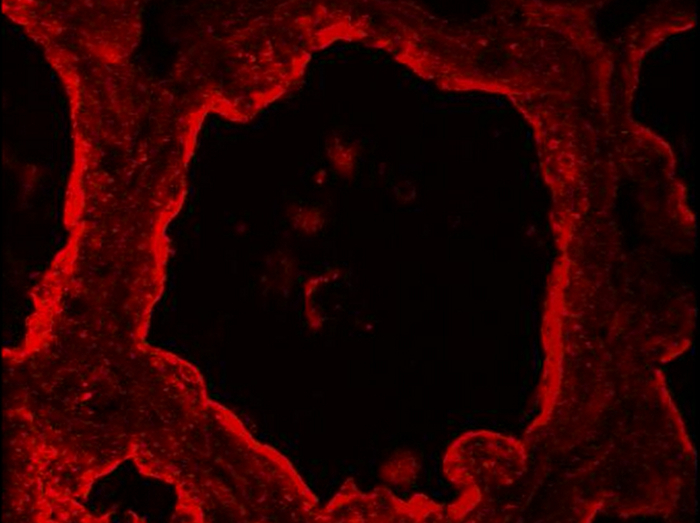
補足ムービーマウス乳腺におけるbutyrophilin 3.ローカライズ。BTN1(赤)は、授乳の10日目のマウスの乳腺にIIFによって検出されます。画像はBTN1ラベルの回転(y軸)空間ビューを生成するために、Zスタックのような共焦点顕微鏡を用いて取得し、ImageJの(3D投影)で後処理された。 このビデオを見るにはこちらをクリックしてください。

マウスマサチューセッツ州butyrophilinと中性脂質の補足映画4.ローカライズmmary腺。BTN1(赤)は授乳の10日目のマウスの乳腺においてIIFによって検出されます。中性脂質(CLDsとMFGs)と核DNAは、それぞれ、BODIPY 503分の493(緑)およびDAPI(青)で対比されています。画像は、各カラーチャンネルのZスタックのような共焦点顕微鏡を用いて取得され、3つのカラーチャンネルを重畳合成Zスタックを生成するためにImageJので後処理しました。 ImageJの(3D投影)は、さらに、複合のZスタックの空間ビューを回転(y軸)を生成するために使用された。 このビデオを見るにはこちらをクリックしてください。
Subscription Required. Please recommend JoVE to your librarian.
Discussion
IHCは、特定のエピトープ - 抗体相互作用に主に依存する組織切片中の抗原をローカライズすることは比較的単純明快な実験方法です。プロトコルの多数IIFによってタンパク質を局在化するために使用されているが、これらの手順のコアは、ほとんど同じです。しかし、強く結果に影響を与えることができるため、各個人のIHC研究のために最適化されなければならないいくつかの重要な側面があります。このアプローチの最も困難な側面、すなわち、最高の実験条件を決定することで、目的の抗原に対して強力かつ特異的なシグナルを生成するものが。実験計画と最適化のために考慮しなければならない変数は次のとおりです抗原の(1)のタイプ(種、発現レベル、細胞内位置); (2)エピトープタイプ(配列、高次構造、推定上の翻訳後修飾)。 (3)試料調製(パラフィンまたは凍結切片の埋め込み)。 (4)固定メタOD(潅流または浸漬)。 (5)(ホルムアルデヒド、アルコールまたはアセトン)を使用する固定液; (6)使用されるブロッキング試薬(正常血清、BSAまたは脱脂乳) (7)ARステップと(8)検出方法(直接または間接的に)。 (8)一次抗体(モノクローナルまたはポリクローナル)のタイプ。 (9)二次抗体(種とラベル)。 (10)counterstains(核および/または他の細胞区画標識)そして、(11)マウンティング培地(詳細は表1を参照)。固定及びブロッキングステップは、少なくとも、例えば、濃度、pH、温度、インキュベーション時間および希釈剤のような追加の因子の最適化を必要とします。
最初の重要な側面は、厳密に順番に結果の品質に影響する固定方法、にリンクされている組織サンプルの調製に関する。例えば、組織片を固定することができるか、埋め込みの前にありません。このステップは、パラフィン包埋の対すなわち選択された埋め込 み方法、OCT化合物に依存してもよいです、それ自体は時々使用した一次抗体に依存します。組織の固定は固定液で麻酔動物を灌流することによって、in vivoで行うことができます。この方法は、無傷の組織を研究する際の抗原を保存するのに有用であるが、目的の組織を固定するのに十分ではないかもしれません。この場合、(10ミリメートルを超えない、より厚い)小さな組織片を固定液中に浸漬することができます。凍結組織は、液体窒素またはイソペンタンの組織を浸漬することによって調製し、スナップ凍結をすることができ、高度にリン酸化などの翻訳後修飾のその後の検出のために推奨されます。しかしながら、パラフィン包埋組織とは異なり、凍結は細胞内の形態を変化させることができる細胞内の氷結晶の形成に起因する組織の長期保存のために十分ではありません。切断後、凍結組織切片は、最大1年間-80℃で保存することができます。いずれの場合においても、組織サンプルの調製は、組織を保存の間の妥協であります/細胞構造およびエピトープの整合性を維持します。
それは、組織の化学組成を変化させるので、不完全な(FIのxation下)及び過剰な(overfixation)のfi xation両方を回避するために、固定条件を最適化することが重要です。
実際、underfixationは、特定の抗原のタンパク質分解を促進することにより、特定の信号を減少させることができます。一方、overfixationエピトープマスキングまたは強い非特異的バックグラウンドを生成することによって、特定の標識を変更することができます。したがって、固定液の選択に加えて、インキュベーション時間などの他のパラメータは、温度およびpHは、組織固定に影響を与えます。 PFAは、IHCに使用される最も一般的な固定剤であるが、「汎用」固定剤とみなすことができません。 PFAは、タンパク質 - タンパク質およびタンパク質 - 核酸架橋を誘発し、従ってartefactuallyエピトープ(overfixation)を変更し、そのRECOを防止することができます一次抗体によってgnition。しかし、エピトープは、さらに、(下記参照)AR技術によりマスクを解除することができます。それは細胞質膜へのいくつかのリン酸化タンパク質のトランスロケーションを誘導することが示されているようにPFAはまた、特定の抗原の検出には適さないかもしれません。このような場合には、PFAはアルコールなどの適切な代替固定剤に置き換える必要があります。彼らは、組織内の水分子を置換することによって、組織の固定を可能にするので、PFAとは異なり、例えば、メタノールまたはエタノールなどのアルコールがエピトープをマスクしません。これは、タンパク質の沈殿につながり、その後によるコンフォメーション変化への抗体/エピトープ相互作用を防ぐことができます。それは広く、アルコールが浸透しないので、組織形態と同様に、PFAを維持しないと考えられています。アセトンは未固定、スナップ凍結組織切片で作業する場合、一般的に使用されている他の代替固定剤、です。しかしながら、アセトンが強力な脱水剤であり、組織タンパク質の不可逆的沈殿をもたらすことができます。
いくつかの抗原を、ARの付加的なステップは、固定剤がコンフォメーション変化を誘導またはエピトープ(エピトープのマスキング)の静電荷を変化させる場合、主に、良好な信号を得るために必要とされ得ます。 AR法は、一次抗体とエピトープの免疫反応性およびその後の相互作用を復元するために、これらのプロセスを逆にすることを目指しています。 AR法は、主に二つのアプローチに依存している:(1)プロテアーゼ誘発性エピトープ回復、 すなわち 、エピトープをマスクするペプチドを切断するようなプロテイナーゼK、トリプシンまたはペプシンなどの酵素、と。 (2)熱誘導エピトープ回復、 すなわち 、電子レンジ、圧力鍋、野菜汽船、オートクレーブまたは水浴を使用して。この後者のアプローチは、特に、タイム、温度、buffer-、およびpH感受性であり、最適な条件は、経験的に(例では、プロトコルの項に記載されている)を決定しなければなりません。あるいは、その抗原に対する抗体の親和性を向上させることができますpHまたは抗体希釈液の陽イオン濃度を変化させることによって。
透過化工程は、しばしば、特に核抗原染色のために、厚い組織切片における細胞内エピトープに良好な信号を得るために必要とされます。これは、使用して様々な方法で達成することができる:(1)固定剤などのアルコールまたはアセトン;そのようなトリトン、NP-40(0.1から0.2まで%PBSで、10分)、ジギトニン、サポニンまたはツイーン20(10〜30分間、0.2から0.5まで%)または(2)界面活性剤PFA固定後。しかし、界面活性剤の選択は、検出されたエピトープの細胞の位置に依存します。実際に、細胞膜を可溶化などのTriton-X100のような過酷な洗剤は、核エピトープ検出に適しているが、いくつかの膜性タンパク質の抽出の際に信号の変化につながることができます。穏やかな洗浄剤(サポニンおよびTween 20)を使用することは、細胞質のエピトープの検出のために適しています。
第二の重要なステップはblockinです非特異的な染色のグラム。その標的エピトープへの抗体の結合は、分子間力(例えば、疎水性及びイオン性相互作用、水素結合)によって支配されます。したがって、それらの標的抗原以外のタンパク質との一次および/または二次抗体の相互作用は、非特異的な染色を生じさせることができます。これは、目的のタンパク質(低信号対雑音比)の可視化を防止する高い蛍光バックグラウンドを生成します。試薬をブロックすると、特定の抗体/エピトープ相互作用を損なうことなく、非特異的相互作用を低減します。一般的な手順は、熱不活性化正常血清またはBSAで組織切片をインキュベートから構成されています。正常血清を用いた場合には、二次抗体の宿主動物と同じ種に由来するまたは関連のない種からのものでなければなりません。全ての場合において、選択されたブロッキング試薬はまた、一次および二次抗体のために希釈剤を添加しなければなりません。さらに、このようなトリトンX-100、Tのような非イオン性界面活性剤の使用予期する20またはサポニンは、非特異的相互作用を低減するのに役立ちます。
第三、おそらく最も重要なパラメータは、一次抗体の選択と最適化です。明らかに、最良の選択は、最小の交差反応性を有する高品質な抗体です。モノクローナル抗体は、通常、単一のエピトープに対して高い親和性および特異性を示すように、それらは、高い配列同一性を有するタンパク質ファミリーの特定のメンバーを識別するための最良のツールです。標的エピトープは、その天然のコンフォメーションの状態を失った場合またはエピトープへのアクセスが他のタンパク質、翻訳後修飾、温度、pH、固定と塩濃度との相互作用によって防止されている場合しかし、抗体/エピトープ相互作用が損なわれる可能性があります。このような場合には、ポリクローナル抗体は、同じタンパク質の複数のエピトープを認識するように、より適しています。また、それらは、しばしば、pHおよび塩濃度の広い範囲のモノクローナル抗体よりも安定です。経験のために決定されなければならない、インキュベーション時間、希釈剤および温度、予備的研究は、適切な培養条件を定義するために、すなわち 、作業希釈率(1.7から15 mg / mlの:5-25 mg / mlの、ポリクローナル抗体、モノクローナル抗体)を有しています各一次抗体。これらのパラメータは、低いバックグラウンドノイズとの最適な信号を生成する条件を決定するために最適化されなければなりません。標識化の特異性は、( すなわち 。RT対、4℃)より低い温度でより長いインキュベーション時間で愛用されています。
直接的または間接的な検出を実行するための選択肢は、多くの場合、抗原発現のレベルに依存します。例えば、高度に発現されるエピトープは、単にによる二次抗体を使用することが可能で、非特異的バックグラウンドを回避しつつ、高速かつシンプルな多色染色を可能にする、蛍光標識一次抗体を用いて検出することができます。しかし、5月には、より高いコストで低信号を生成し、できるのIFダイレクトometimes困難であること、標識抗体は市販されていません。逆に、IIFは、生成された信号が原因で一次抗体(増幅)と(一次抗体の宿主種に対して生じた)少なくとも二つの標識二次抗体との相互作用により強くなるように、下部表現エピトープを検出するために、より敏感です。さらに、様々なフルオロフォアにコンジュゲートした二次抗体の広い範囲が、比較的安価で市販されており、品質が制御されます。しかし、このアプローチは、交差反応を誘導することができるので、慎重に多重標識実験を行う際に、同じ種または異なるアイソタイプの産生されていない一次抗体を選択することが必要です。 IIFはまた時々余分なブロッキングステップを必要とします(下記参照)体系的なネガティブコントロールを含める必要があります。増幅は、さらにMOごとに結合したビオチン結合二次抗体を使用することによって達成され、蛍光アビジンまたはストレプトアビジン(4ビオチンを標識することができますlecule)。それにもかかわらず、この増幅法は、非特異的結合を防ぐために、追加のステップを必要とし、内因性ビオチンの高レベルの存在のためにいくつかの組織(肝臓、腎臓、心臓、脳、肺及び泌乳乳腺)の染色のために適合されないことが。しかしながら、内因性ビオチンは、一次抗体とのインキュベーションの前に、ビオチンとアビジン、続いて試料をプレインキュベートすることによって遮断することができます。短い波長の光で励起されたときに光を放出する特性を持つ化学小分子である共役蛍光色素の選択は、主に利用可能な顕微鏡装置の種類によって異なります。
適切に使用する蛍光色素の分光特性と抗体とのクロスオーバーの間に交差反応性の両方を制限するように設計すると、免疫蛍光ベースのIHCは、複数の細胞標的を同時に可視化を可能にします。
最後の重要なIHC実験に関する点は、染色の妥当性を支持する実験的成果物を同定するために実施し、結果を正確に解釈されなければならない陽性対照および陰性対照に関する。いくつかの組織は、結果の誤った解釈につながる可能性(自家蛍光と呼ばれる)高い蛍光バックグラウンドを示します。このように、組織切片をIHC実験を開始する前に、蛍光および明視野照明の両方で観察されなければなりません。一次抗体が体系潜在的な非特異的な二次抗体の結合ことを確実にするために、各IHC実験に含まれている必要があり省略し、陰性対照はごくわずかであり、特定の染色パターンに似あいまいか持ちません。モノクローナル一次抗体を操作する場合アイソタイプコントロールは、同じ濃度で同一のアイソタイプ( 例えばIgG1、IgG2aを、IgG2bで、IgM抗体)の非免疫抗体と交換することによって行うことができます。この制御は、ESに役立ちますサンプルと抗体の相互作用に起因する可能性が非特異的な染色を、timate。その抗原に対する抗体の特異的結合を実証するために、吸収コントロールは、一次抗体をプレインキュベートすることにより、2つの方法で達成することができる:(1)その可溶性免疫原との(10:1のモル比)O / Nで4℃で; (2)目的のエピトープを発現する細胞または組織切片を有するが、それは検討組織(例えば、59で図4Bを参照)とは異なります。どちらの場合も、一次抗体の結果としての枯渇は、ほとんど、あるいは全く染色をもたらすはずです。制御の他のタイプは、無関係な一次抗体を使用して行うことができ、すなわち 、目的のエピトープとは異なる細胞局在(細胞質対核)を示すエピトープに対する。無関係な抗体は、目的の一次抗体と同じアイソタイプと種のものでなければなりません。 IHC実験のための追加のコントロールはTISSからのサンプルの使用を含むことができます目的のエピトープを(トランスジェニック動物)を発現しないか(ノックアウト動物)ことが知られているUE。これは、有用な基準を提供し、IHC手順を最適化するのを助けることができます。
IF技術の主な限界は、それらが唯一の両方の手順では、潜在的にアーチファクトを誘発する、固定された(死んだ)に適用し、および/または細胞を透過性にすることができることです。この方法の他の制限は、試料を観察するための顕微鏡の使用によるものです。落射蛍光と共焦点顕微鏡の光学解像度が限られているように、まず、検出されたタンパク質の位置やコロケーションは解釈オーバーであってはなりません。第二に、 すなわち 、光退色。光にさらされたときに経時的な蛍光強度のフェーディング、今度は、蛍光体の光化学的破壊につながる、蛍光励起の際に、試料中の活性酸素種の発生に本質的に起因します。光退色を低減することができる:A)から保護サンプルを維持彼らの観測までのIF実験し、保存時に光; B)マウンティング培地中で退色防止剤(活性酸素種スカベンジャー)を使用しました。 C)強度および/または励起光の持続時間を減少させます。 D)蛍光体の濃度を増加させるか、高量子効率を有する蛍光色素の低濃度を使用します。およびe)( すなわち 。アレクサ蛍光体、瀬田の蛍光体、またはDyLightFluors)を光退色しにくいです堅牢な蛍光団を使用。減少したピリジンヌクレオチド(NADH:吸収、340nmで、放射、460 nm)の哺乳動物細胞において;:第三に、自己蛍光が原因フラビン補酵素(放射、515 nmの吸収を、450nmのFADとFMN)の存在下にあることが多いです。また、サンプルを固定するアルデヒド、特にグルタルアルデヒドの使用は、自己蛍光の高いレベルをもたらすことができます。これは、および/またはプローブとM個の光フィルタを選択することによって、従来の抗体のインキュベーションにPBS中の0.1%水素化ホウ素ナトリウムのサンプルを洗浄することにより最小限に抑えることができ自家蛍光の蛍光信号を相対的にaximize。彼らはしばしば非常に広い帯域幅、異なる、非対称スペクトルプロファイル、ならびに様々なピーク発光波長との数を示すように第四に、(また、ブリードスルー、クロスオーバーやクロストークと呼ばれる)の蛍光の重なりが原因で蛍光体の発光スペクトル特性に主です最大値。蛍光オーバーラップは、いくつかのフルオロフォア(多色ラベリング)で作業するときに発生すると、別の蛍光体のチャネル(フィルタ)で1フルオロフォアの発光することを特徴とします。彼らは多くの場合、結果、IFの解釈を複雑にするようブリードスルーのアーティファクトは、特に共局在または定量的研究の場合には、最小化されなければなりません。フルオロフォア発光のバランスとしてわずかしかIF手順によって改善することができる、ブリードスルー主として正しくSEPARするために最適化された蛍光フィルターセットおよび/または光電子増倍管検出器を用いて画像取得時に削減することができます蛍光体のスペクトルプロファイルを食べました。それは、特定の検出チャネルへの各信号を向けることによって、個々の蛍光体の分化の蛍光発光スペクトルを可能にするように、この点で、共焦点顕微鏡は、多色画像形成に適しています。また、共焦点顕微鏡は、標識の順次取得(同時に複数の蛍光色素分子)のための個々の検出チャネルのゲイン、光電子増倍管電圧、またはレーザパワーを調整することができます。理想的には、単一ラベルコントロールは、ブリードスルーを定量化し、最終的に計算それを除去するために行われなければなりません。二次抗体を含まない対照(バックグラウンド対照)は、信号利得の制限を設定するために調製し、最適な画像取得のための各チャンネルのオフセットすることができます。また、正確な画像背景(自己蛍光)にポスト取込み処理のために使用することができます。
結論として、記載された方法は簡単realizatiためのシンプルな標準プロトコルを提供乳腺セクションに免疫染色の上。それにもかかわらず、IHC実験の主要なステップは、特異的染色を視覚化し、非特異的バックグラウンドシグナルを最小化するために、各抗原/抗体対のために最適化されなければなりません。記載の方法はまた、得られた画像のほとんどの後処理のためのいくつかの基本的な方法を含みます。蛍光ベースの免疫検出は、診断への抗原の細胞局在から、幅広い用途を持つ強力な方法です。これらのアプローチの新展開は、生物学的構造とプロセスの画像以前に観察されない細部には、新しい蛍光団、取得装置及び顕微鏡技術の将来の発展を実現することになります。
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
著者は、彼らが競合する金融利害関係を有していないことを宣言します。
Acknowledgments
著者は、INRA MIMA2イメージングコア施設(INRA、UMR1198、ジュイ・アン・ジョザス)へと動物のケアと施設のIERPユニット(UE 0907、INRA、ジュイ・アン・ジョザス)のスタッフに感謝しています。我々はまた、非常に便利なantibodieをご提供するためのIHメイザー、MCネヴィルとS. Toozeに感謝したいと思います。
Materials
| Name | Company | Catalog Number | Comments |
| Dissection | |||
| Pins | |||
| Ethanol | |||
| Scissors | |||
| Scalpel and adapted blades | |||
| Ice | |||
| Towel paper | |||
| Tissue sample preparation | Company | Catalog Number | Comments/Description |
| Phosphate Buffered Saline (pH7.4) | Sigma | P-3813 | |
| Paraformaldehyde (PFA, 32% EM grade, 100 ml) | Electron Microscopy Sciences | 15714-S | personnal protection equipment required WARNING: this product will expose you to Formaldehyde Gas, a chemical known to cause cancer |
| OCT compound/Tissue Tek | Sakura | 4583 | |
| Sucrose (D-saccharose) | VWR | 27480.294 | |
| Plastic molds | Dominique Dutscher | 39910 | |
| Liquid nitrogen | |||
| Cryostat/sample support | Leica | CM3050S | |
| Razor blades (SEC35) | Thermo Scientific | 152200 | |
| Slide box | |||
| Glass slides Superfrost/Superfrost Ultra Plus | Thermo Scientific | 10143560W90/1014356190 | |
| Brushes | |||
| IHC | Company | Catalog Number | Comments/Description |
| Super Pap Pen | Sigma | Z377821-1EA | |
| Permanent marker (black) | |||
| 50 mM NH4Cl in PBS | Sigma | A-0171 | |
| 0.1 M glycine in PBS | VWR | 24403.367 | |
| Antigen Retrieval solution: Tris 100 mM 5% urea pH9.6 | |||
| Heater (up to 100°C) | |||
| Bovine Serum Albumin (BSA) | Sigma | A7906-100G | |
| Vectashield (anti-fading mounting medium) without DAPI/with DAPI | Vector Laboratories | H-1000/H-1200 | |
| Glass coverslips 22x50mm (microscopy grade) | VWR | CORN2980-225 | |
| Nail polish | |||
| Primary antibodies | Company | Catalog Number | Comments/Description |
| Rabbit anti-mouse caseins (#7781; 1:50 dilution) | generously gifted by M.C. Neville (University of Colorado Health Sciences Center, USA) |
||
| Mouse anti-cytokeratin 8 (CK8, clone 1E8, 1:50 dilution) | Biolegend (Covance) | MMS-162P | |
| Mouse anti-cytokeratin 14 (CK14, cloneLL002, 1:50 dilution) | Thermo Scientific | MS-115-P0/P1 | |
| Rabbit anti-butyrophilin (1:300 dilution) | generously gifted by I.H. Mather (Department of Animal and Avian Sciences University of Maryland College Park, USA) | ||
| Rabbit anti-Stx6 (1:50 dilution) | generously gifted S. Tooze (Cancer Research UK, London Research Institute, London, UK) |
||
| Rabbit anti-VAMP4 (1:50 dilution) | Abcam | ab3348 | |
| Secondary antibodies | Company | Catalog Number | Comments/Description |
| Rhodamine-conjugated goat anti-rabbit IgG (H + L) (1:300 dilution) | Jackson ImmunoResearch Laboratories | 111-025-003 | |
| Counterstains | Company | Catalog Number | Comments/Description |
| Bodipy 493/503 | Life Technologies (Molecular Probes) | D-3922 | |
| DAPI (4-6-diamidino-2-phenylindole) | Life Technologies (Molecular Probes) | D-1306 | |
| Observation/Image capture | Company | Catalog Number | Comments/Description |
| conventional fluorescence microscope | Leica Leitz DMRB microscope |
Standard filters for FITC, Rhodamine and DAPI emissions, ×63 oil-immersion objective (NA 1.3), DP50 imaging camera (Olympus), CellˆF software (Olympus) |
|
| Laser Scanning Microscope (confocal microscopy) | Zeiss LSM 510 microscope |
Plan-Apochromat ×63 oil-immersion objective (NA 1.4), CLSM 510 software, Confocal facilities, MIMA2 Platform, INRA Jouy-en-Josas, France, http://mima2.jouy.inra.fr/mima2) | |
| Image treatment | Company | Catalog Number | Comments/Description |
| ImageJ 1.49k software | Free software |
References
- Watson, C. J., Khaled, W. T. Mammary development in the embryo and adult: a journey of morphogenesis and commitment. Development. , 135-995 (2008).
- Smith, G. H. Experimental mammary epithelial morphogenesis in an in vivo model: evidence for distinct cellular progenitors of the ductal and lobular phenotype. Breast Cancer Res Treat. 39, 21-31 (1996).
- Van Keymeulen, A., et al. Distinct stem cells contribute to mammary gland development and maintenance. Nature. 479, 189-193 (2011).
- Oakes, S. R., Gallego-Ortega, D., Ormandy, C. J. The mammary cellular hierarchy and breast cancer. Cell Mol Life Sci. 71, 4301-4324 (2014).
- Visvader, J. E., Stingl, J. Mammary stem cells and the differentiation hierarchy: current status and perspectives. Genes & development. 28, 1143-1158 (2014).
- Robinson, G. W. Cooperation of signalling pathways in embryonic mammary gland development. Nat Rev Genet. 8, 963-972 (2007).
- Cowin, P., Wysolmerski, J. Molecular mechanisms guiding embryonic mammary gland development. Cold Spring Harb Perspect Biol. 2, a003251 (2010).
- Brisken, C., O'Malley, B. Hormone action in the mammary gland. Cold Spring Harb Perspect Biol. 2, a003178 (2010).
- Gjorevski, N., Nelson, C. M. Integrated morphodynamic signalling of the mammary gland. Nat Rev Mol Cell Biol. 12, 581-593 (2011).
- Daniel, C. W., Smith, G. H. The mammary gland: a model for development. J Mammary Gland Biol Neoplasia. 4, 3-8 (1999).
- Howlett, A. R., Bissell, M. J. The influence of tissue microenvironment (stroma and extracellular matrix) on the development and function of mammary epithelium. Epithelial Cell Biol. 2, 79-89 (1993).
- Edwards, G., Streuli, C. Signalling in extracellular-matrix-mediated control of epithelial cell phenotype. Biochem Soc Trans. 23, 464-468 (1995).
- Hennighausen, L., Robinson, G. W. Think globally, act locally: the making of a mouse mammary gland. Genes & development. 12, 449-455 (1998).
- Topper, Y. J., Freeman, C. S. Multiple hormone interactions in the developmental biology of the mammary gland. Physiol Rev. 60, 1049-1106 (1980).
- Brisken, C., et al. A paracrine role for the epithelial progesterone receptor in mammary gland development. Proc Natl Acad Sci U S A. 95, 5076-5081 (1998).
- Ormandy, C. J., Binart, N., Kelly, P. A. Mammary gland development in prolactin receptor knockout mice. J Mammary Gland Biol Neoplasia. 2, 355-364 (1997).
- Oakes, S. R., Rogers, R. L., Naylor, M. J., Ormandy, C. J. Prolactin regulation of mammary gland development. J Mammary Gland Biol Neoplasia. 13, 13-28 (2008).
- Hennighausen, L., Robinson, G. W. Information networks in the mammary gland. Nat Rev Mol Cell Biol. 6, 715-725 (2005).
- Kouros-Mehr, H., Werb, Z. Candidate regulators of mammary branching morphogenesis identified by genome-wide transcript analysis. Dev Dyn. 235, 3404-3412 (2006).
- Khaled, W. T., et al. The IL-4/IL-13/Stat6 signalling pathway promotes luminal mammary epithelial cell development. Development. 134, 2739-2750 (2007).
- Asselin-Labat, M. L., et al. Gata-3 is an essential regulator of mammary-gland morphogenesis and luminal-cell differentiation. Nat Cell Biol. 9, 201-209 (2007).
- Barcellos-Hoff, M. H., Aggeler, J., Ram, T. G., Bissell, M. J. Functional differentiation and alveolar morphogenesis of primary mammary cultures on reconstituted basement membrane. Development. 105, 223-235 (1989).
- Robinson, G. W., McKnight, R. A., Smith, G. H., Hennighausen, L. Mammary epithelial cells undergo secretory differentiation in cycling virgins but require pregnancy for the establishment of terminal differentiation. Development. 121, 2079-2090 (1995).
- Streuli, C. H., Bissell, M. J. Mammary epithelial cells, extracellular matrix, and gene expression. Cancer Treat Res. 53, 365-381 (1991).
- Streuli, C. H., et al. Laminin mediates tissue-specific gene expression in mammary epithelia. J Cell Biol. 129, 591-603 (1995).
- Boudreau, N., Sympson, C. J., Werb, Z., Bissell, M. J. Suppression of ICE and apoptosis in mammary epithelial cells by extracellular matrix. Science. 267, 891-893 (1995).
- Pullan, S., et al. Requirement of basement membrane for the suppression of programmed cell death in mammary epithelium. J Cell Sci. 109 (Pt 3), 631-642 (1996).
- Schmidhauser, C., Bissell, M. J., Myers, C. A., Casperson, G. F. Extracellular matrix and hormones transcriptionally regulate bovine beta-casein 5' sequences in stably transfected mouse mammary cells. Proc Natl Acad Sci U S A. 87, 9118-9122 (1990).
- Streuli, C. H., et al. Stat5 as a target for regulation by extracellular matrix. J Biol Chem. 270, 21639-21644 (1995).
- Sollner, T., et al. SNAP receptors implicated in vesicle targeting and fusion. Nature. 362, 318-324 (1993).
- Jahn, R., Scheller, R. H. SNAREs--engines for membrane fusion. Nat Rev Mol Cell Biol. 7, 631-643 (2006).
- Weber, T., et al. SNAREpins: minimal machinery for membrane fusion. Cell. 92, 759-772 (1998).
- Sollner, T., Bennett, M. K., Whiteheart, S. W., Scheller, R. H., Rothman, J. E. A protein assembly-disassembly pathway in vitro that may correspond to sequential steps of synaptic vesicle docking, activation, and fusion. Cell. 75, 409-418 (1993).
- McNew, J. A. Regulation of SNARE-mediated membrane fusion during exocytosis. Chem Rev. 108, 1669-1686 (2008).
- Wang, C. C., et al. VAMP8/endobrevin as a general vesicular SNARE for regulated exocytosis of the exocrine system. Mol Biol Cell. 18, 1056-1063 (2007).
- Chat, S., et al. Characterisation of the potential SNARE proteins relevant to milk product release by mouse mammary epithelial cells. Eur J Cell Biol. 90, 401-413 (2011).
- Reinhardt, T. A., Lippolis, J. D. Bovine milk fat globule membrane proteome. J Dairy Res. 73, 406-416 (2006).
- Robenek, H., et al. Butyrophilin controls milk fat globule secretion. Proc Natl Acad Sci U S A. 103, 10385-10390 (2006).
- Fujimoto, T., Ohsaki, Y., Cheng, J., Suzuki, M., Shinohara, Y. Lipid droplets: a classic organelle with new outfits. Histochem Cell Biol. 130, 263-279 (2008).
- Mather, I. H., Keenan, T. W. Origin and secretion of milk lipids. J Mammary Gland Biol Neoplasia. 3, 259-273 (1998).
- Heid, H. W., Keenan, T. W. Intracellular origin and secretion of milk fat globules. Eur J Cell Biol. 84, 245-258 (2005).
- McManaman, J. L., Russell, T. D., Schaack, J., Orlicky, D. J., Robenek, H. Molecular determinants of milk lipid secretion. J Mammary Gland Biol Neoplasia. 12, 259-268 (2007).
- de Assis, S., Warri, A., Cruz, M. I., Hilakivi-Clarke, L. Changes in mammary gland morphology and breast cancer risk in rats. Journal of visualized experiments : JoVE. , (2010).
- Plante, I., Stewart, M. K., Laird, D. W. Evaluation of mammary gland development and function in mouse models. Journal of visualized experiments : JoVE. , (2011).
- Galio, L., et al. MicroRNA in the ovine mammary gland during early pregnancy: spatial and temporal expression of miR-21, miR-205, and miR-200. Physiol Genomics. 45, 151-161 (2013).
- Linzell, J. L., Peaker, M. The effects of oxytocin and milk removal on milk secretion in the goat. J Physiol. 216, 717-734 (1971).
- Knight, C. H., Peaker, M., Wilde, C. J. Local control of mammary development and function. Rev Reprod. 3, 104-112 (1998).
- Walid, M. S., Osborne, T. J., Robinson, J. S. Primary brain sarcoma or metastatic carcinoma? Indian J Cancer. 46, 174-175 (2009).
- Hue-Beauvais, C., et al. Localisation of caveolin in mammary tissue depends on cell type. Cell Tissue Res. 328, 521-536 (2007).
- McManaman, J. L., Neville, M. C. Mammary physiology and milk secretion. Adv Drug Deliv Rev. 55, 629-641 (2003).
- Mather, I. H., Jack, L. J. A review of the molecular and cellular biology of butyrophilin, the major protein of bovine milk fat globule membrane. J Dairy Sci. 76, 3832-3850 (1993).
- Heid, H. W., Winter, S., Bruder, G., Keenan, T. W., Jarasch, E. D. Butyrophilin, an apical plasma membrane-associated glycoprotein characteristic of lactating mammary glands of diverse species. Biochim Biophys Acta. 728, 228-238 (1983).
- Bock, J. B., Klumperman, J., Davanger, S., Scheller, R. H. Syntaxin 6 functions in trans-Golgi network vesicle trafficking. Mol Biol Cell. 8, 1261-1271 (1997).
- Tran, T. H., Zeng, Q., Hong, W. VAMP4 cycles from the cell surface to the trans-Golgi network via sorting and recycling endosomes. J Cell Sci. 120, 1028-1041 (2007).
- Wendler, F., Page, L., Urbe, S., Tooze, S. A. Homotypic fusion of immature secretory granules during maturation requires syntaxin 6. Mol Biol Cell. 12, 1699-1709 (2001).
- Wendler, F., Tooze, S. Syntaxin 6: the promiscuous behaviour of a SNARE protein. Traffic. 2, 606-611 (2001).
- Shitara, A., et al. VAMP4 is required to maintain the ribbon structure of the Golgi apparatus. Mol Cell Biochem. 380, 11-21 (2013).
- Thibault, C., Levasseur, M. C. La reproduction chez les mammifères et l'homme. , INRA Editions. 928 (2001).
- Truchet, S., Wietzerbin, J., Debey, P. Mouse oocytes and preimplantation embryos bear the two sub-units of interferon-gamma receptor. Mol Reprod Dev. 60, 319-330 (2001).



