Summary
바이오 오일을 생산하는 목질 계 바이오 매스의 빠른 열분해 용 연료 등급 탄화수소를 생산하는 바이오 오일의 촉매 수소화를위한 실험 방법이 제시된다. 바이오 - 오일에서 미세 문자 입자 및 무기 오염 물질을 제거하는 빠른 열분해 동안 뜨거운 증기 여과도 평가 하였다.
Introduction
우리 사회는 화석 연료 (예를 들어, 석유, 천연 가스, 석탄 등)에 크게 의존한다. 이러한 리소스는 없습니다 지속 가능한 에너지 원이며, 화석 연료 자원, CO 2 배출의 환경 영향, 경제적 문제를 점차 감소에 대한 우려로 이어지는, 빠르게 증가하는 속도로 고갈되고있다. 대안과 지속 가능한 에너지 원에 대한 수요 증가가 1,2,3,4입니다. 바이오 매스는 현재 에너지 생산 및 변환 시스템의 화석 연료를 대체하는 액체 연료 (바이오) 및 탄소 계 화학 물질의 생산을위한 전용 재생 가능한 탄소 중립 리소스이다. 3,4
현재 가장 풍부하고 가장 저렴한 바이오 소스 인 목질 바이오 매스 (예, 목재, 잔디, 에너지 작물, 농업 폐기물 등), 각종 열 화학적 및 생물학적 경로를 통해 바이오 연료를 생산하는 방법으로 가장 주목 받고있다.
첫 번째 경로는 리그 노 셀룰로오스 바이오 매스의 셀룰로오스와 헤미셀룰로오스 부분을 활용할 수 있습니다. 업그레이드와 통합 열분해는 바이오 연료의 직접 생산을위한 단기 실행 가능한 기술로 간주됩니다.
열분해는 산소의 부재하에 400 내지 550 ° C 사이의 온도에서 리그 노 셀룰로오스 바이오 매스의 열분해된다. 4,5,6, 예컨대 탈 중합, 탈수, 및 C-C 결합 등의 절단 반응들을 열분해시 발생 복잡한 혼합물 O의 형성으로 이어질F 200 개 이상의 산소 화합물을들 수있다. 4,5,6 바이오 오일 (건조 사료의 75 중량 %까지) 높은 수율을 유지 바이오 매스 원료에 저장된 에너지의 최대 70 %로 제조 할 수있다. 4,5 그러나, 표준 장비의 수송 연료로 생성 된 열분해 바이오 오일을 직접 사용하기 때문에 높은 점도, 부식성, 가난한 변동성, 저와 같은 다른 물리적, 화학적 특성으로 이어질 높은 산소와 수분 함량,의 문제가 발열량 및 불량한 안정성. 따라서, 광범위한 산소 제거는 탄화수소 범위의 연료로 바이오 오일을 업그레이드하는 데 필요한 -6,7,8,9-. 수소 고체 촉매를 사용하여 촉매 수소화는 수소화 탈산 소화 및 수소 첨가 반응을 통해 산소를 제거하여 바이오 오일을 업그레이드하는 가장 일반적인 경로이다. 6,7,8,9
현재 하이드로이어서 열분해위한 주요 문제점 중 하나는 특히 대한 장기적인 안정 동작을 달성하는 것바이오 오일 바이오 오일 무기 황 잔기의 열적 불안정성 중요한 촉매 불 활성화를 야기하는 수소 제조 방법. 바이오 오일 10,11 열 불안정성 바이오 오일의 활성 종을 안정화시키는 저온 수소화에 의해 해결되었다. 바이오 오일 분획의 repolymerization을 촉진하고 증착에 의해 수소화 촉매를 비활성화 할 수있는 무기 잔류 물을 제거하여 바이오 오일 (11, 12) 정리, 도움이 될 수 있습니다. 뜨거운 증기 여과 효과적으로 열분해 동안 숯 입자를 제거하여 바이오 오일 중의 무기 함량을 감소시키는 기술이다. 13,14,15 뜨거운 증기 여과 증기의 응결 전에 고온에서 열분해 가스 / 증기 스트림으로부터 숯 미립자를 분리하는 열분해 반응기의 하류에 사용된다. 13,14,15
우리는 여기에 바이오 매스 빠른 pyrol 국립 재생 에너지 연구소 (NREL)에서 사용되는 프로토콜을보고이 Analysis와 뜨거운 증기 여과없이 모두 연속 유출 충전 층 촉매 반응기 바이오 연료 생산 바이오 오일 수소화 처리를위한 유동층 반응기 퍼시픽 노스 웨스트 국립 연구소 (PNNL)에서를 사용하는 바이오 오일을 생성한다. 반응기 시스템, 운영 방법, 처리 및 원료 바이오 오일 및 바이오 분석의 구성을 상세히 설명한다. 또는 뜨거운 증기 필터링 및 생성 된 바이오 오일의 수소 처리하지 않고 대표적인 바이오 매스 공급 원료의 열분해 처리의 결과는 또한 뜨거운 증기 여과의 영향에 대한 평가와 함께 제공됩니다.
Protocol
뜨거운 증기 여과 1. 빠른 열분해
- 바이오 매스 원료 준비
- 밀 <2mm의 입자 크기 매스. 서늘하고 건조한 장소에 보관하십시오.
- 열분해 시스템을 조립
- 열분해 반응기를 조립합니다.
- 로 내부에 장착 반응기. 반응기로 유동화 질소, 오거 질소 및 공기 라인을 연결합니다. 재킷 오거 포트에 오거를 삽입합니다. 재킷에 냉각 공기를 연결합니다.
- 마운트 및 연결 오거 모터.
- 산 30 ~ 60 cm 직접 오거 포트의 상하 개구 상기 고체 피더.
- 고체 공급 출구와 오거 포트의 수직 개구 사이 마운트 락 호퍼. 나일론 브레이드와 오거 포트에 연결하고, 25mm의 내경 비닐 튜브 강화. 호스 클램프 오거 포트에 튜브를 고정합니다. 경량, 분명, 느슨한 플라스틱 슬립 핏으로 공급기에 연결합니다.
- 사이클론과 뜨거운 필터를 조립합니다.
- 싸이 클론을 장착하고 반응기 콘센트에 사이클론 입구를 연결합니다. 사이클론에 근접 커플 수신기.
- 필터 하우징 (2 ㎛의 세공 크기를 갖는 스테인레스 제) 산 핫 필터. 핫 필터 입구에 사이클론 콘센트에 연결합니다. 사이클론 콘센트에 질소 퍼지 및 압력 릴리프를 연결합니다.
- 응축기 입구에 사이클론 입구에서 추적을 가열하는 열 테이프와 절연 담요를 사용합니다.
- 콘덴서 시스템을 조립합니다.
참고 : 실험실 잭, 링 스탠드, 실험실 클램프를 사용하여 흄 후드에서 응축기 시스템의 조각을 마운트합니다.- 제 1 콘덴서의 경우, 1.2 cm (외경) 스테인레스 스틸 튜브의 커플 15 ~ 30 cm 표준 테이퍼 조인트 튜브를 붕규산합니다. 용기 그쪽에 배치 된 500 ml의 2 구 (표준 테이퍼)에 제 1 콘덴서, 둥근 바닥 플라스크에 (수신기)를 연결t는 얼음 목욕 될 것입니다. 유리 그릇에 호스 지상 유리 관절에 클램프, 구형 관절 및 호스 미늘로 고정 9에 12 mm 명확한 비닐 튜브와이 점의 혈관 사이의 연결이 다운 스트림합니다.
- 전기 집진기 (ESP)의 하부 포트 (입구)에 제 1 콘덴서 플라스크의 출구를 연결한다.
- 드라이 아이스 트랩 (차가운 손가락 콘덴서)의 작은 상부 연결에 ESP의 상부 포트 (출구)를 연결합니다.
- ESP를하고 드라이 아이스 트랩 사이에 줄 수있는 U-튜브를 연결합니다. 물을 가득 U-튜브의 절반을 채 웁니다.
- 드라이 아이스 배스 역할을하는 용기 내에 배치 된 500㎖ 용량의 2 구 둥근 바닥 플라스크 (수신기)를 드라이 아이스 트랩을 연결한다.
- 병합 필터의 하우징의 입구 (중앙 포트)에 500 mL의 플라스크의 콘센트에 연결합니다.
- 필터 하우징의 바닥 주위에 드라이 아이스를 유지하는 용기를 배치했다.
- 필터 outle 연결건식 시험 m 및 다른 가스 분석 장치 (행 t 예컨대, 비 분산 적외선 CO 대 CO, CO 2, CH 4, 수소 열전도 검출기, 및 마이크로 가스 크로마토 그래피 (마이크로 GC)에 대한 분석 다음, 이산화탄소, 질소, 수소 및 C1-C4 탄화수소) 및 벤트.
주 : 열분해 시스템의 개략도는도 1에 도시된다. 바이오 매스 공급기, 파이로, 사이클론, 고온 증기 필터의 그림, 및 열분해 반응기 시스템의 응축은 기업 파일 S5로도 S1에 나타낸다.
- 로드 열분해 반응기
- 반응기에 모래 (330g) 200 ㎖를 붓고.
- 공급 호퍼에 지상 바이오 매스 2kg을 따르십시오.
- 누출 체크 열분해 시스템
- 응축기 입구에서 시스템을 모자.
- 0.05 MPa로 또는 예상 최고 사용 압력으로 가압 중높은 수준이다. 압력을 유지하기 위해 필요한 유동가 있음 <200 ㎖ / 분을 보장한다. 그렇지 않으면, 찾아 누수를 해결하고이 단계를 반복합니다.
- , 압력, 뚜껑을 벗기다 시스템을 완화 응축 시스템의 출구 끝 부분에 응축 시스템, 캡을 연결합니다.
- MPA는 0.01에 압력을. <200 ML의 흐름 / 분 압력을 유지하고 있는지 확인합니다. 그렇지 않으면, 찾아 누수를 해결하고이 단계를 반복합니다.
- 감압 및 악기에 응축 시스템을 다시 연결합니다.
- 반응기를 가열
- 1 표준 L / 분 3 표준 L / 분, 오거 질소 흐름 공기, 설정 유동화 질소 흐름을 냉각을 켭니다.
- 세트로 대상 500 ° C까지 온도 400-500 ℃로 다른 히터.
- 10 ° C / 분의 1의 속도로 온도를 대상으로하는 최대 램프 온도.
- 운영 준비
- 14 표준 L / 분 오거 질소 플로로 유동 질소 유량을 증대w 1.4 표준 L / min의 속도로, 0.5 표준 L / min의 유량으로 퍼지 가스를 도입. 퍼지의 대부분은 사이클론 콘센트에 파열 디스크 포트로 들어갑니다.
- 얼음과 제 1 콘덴서에서 목욕을 입력합니다. 드라이 아이스와 필터를 병합 주위에 드라이 아이스 트랩의 수신기에서 컨테이너 및 컨테이너를 입력합니다.
- 필터의 표면 상에 배치 된 열전대 유착 필터 내부 온도를 모니터하고 0 ℃ 정도로 드라이 아이스 레벨을 조정한다.
- 열분해 실험을 수행
- 록 호퍼 밸브 (사용 사초주기)와 오거를 켭니다.
- ESP를 켭니다. 5 내지 10 kV의 전압으로 설정 한 번 이상 2 초마다 호를 관찰 할 필요.
- 산소가없는 것을 확인하기 위해 마이크로 GC를 사용합니다. 오거와 락 호퍼 켜면 누출의 존재를 나타내는 것이다 출력 가스 유량의 감소를 유발하지 않았다는 것을 확인한다.
- 100g / 시간 공급 장치의 전원을 켭니다. 침대 온도를 관찰하고증가 된 열 부하를 보상하기 위해 필요한 설정 점을 증가시킨다.
- 온도는 500 ° C의 2 ° C 이내로 회복되면, 100g / 시간으로 이송 속도를 향상시킬 수 있습니다. 420g의 공급 속도 때까지이 과정을 반복 / 시간에 도달한다.
- 압력 게이지에 의해 마이크로 GC 건조 시험 m 속도 및 시스템 압력에 의해 공급 제어기, 가스 농도에 15 분마다, 기록 층의 온도, 공급 속도. ESP는 여전히 제대로 아크되어 있는지 확인합니다. 필요에 따라 이들의 임의의 변화에 응답한다. 리필 얼음과 드라이 아이스. 필요에 따라 제품 컬렉션 항아리에 ESP를 배출합니다.
- 일시 휴업
- 바이오 매스 1kg을 공급 한 후, 먹이를 중지합니다.
- 가스 수준을 한 후, 모든 히터를 끄고 1 표준 L / 분 3 표준 L / 분, 오거 흐름에 대한 흐름을 유동화 거절, 정상 상태 값의 10 % 미만으로 부패했다. ESP, lockhopper 밸브 및 오거을 끕니다.
- 시스템이 뜨거운 섹션을 열기 전에 (4 ~ 6 시간에) 식히십시오. </ OL>
- 액체 제품 및 문자를 수집합니다.
- 총 액체의 수율을 얻었다 응축기 시스템의 모든 부분을 단다. 일반적인 항아리 나 병에 콘덴서 수신기에서 액체를 부어. 또는, 유리를 청소하는 아세톤을 사용합니다.
- 항아리에 빈 문자 수신기. 고온 필터를 제거 하우징을 비우하고, 문자 항아리에 필터를 브러시. 필터를 달아. 분리 베드 재료 무게. 이 서비스에 대한 노크 아웃 용기와 HEPA 진공을 사용합니다.
- 시스템을 산화시킨다.
- 원자로, 사이클론 수신기 및 청소 고온 필터를 밀봉합니다. 1.4 절에 이와 같이 누출을 확인합니다.
- 응축 시스템을 우회하도록 유착 필터의 출구 응축기 입구에서 금속 배선을 설치한다.
- 유동 가스 등 3 표준 L / 분 질소와 1 표준 L / 분 오거 질소 흐름과 함께 550 ° C에 원자로를 가열한다.
- 유동화에 공기를 추가가스. 0.2 표준 L / 분에서 시작하여 점차 / 분 4 L로 증가. CO + CO 2 농도는 0.1 % 이하가 될 때까지 계속합니다.
- 수익률을 계산합니다.
- 응축 시스템의 질량의 전체 변경 등의 액체 수율을 계산합니다.
- 숯 침대, 고온 필터의 중량 변화의 중량 변화의 합으로 수율 사이클론 수신기 핫 필터 하우징 수집 숯을 계산한다.
주 : 추가 문자가 시스템의 산화로부터 추정하지만, 이것은 일반적으로 중요하다 할 수있다. - GC가 마른 시험 미터의 유량에서 측정 된 가스 농도의 가스의 총 질량과 같은 기체 수율을 계산한다.
바이오 오일의 2 촉매 수소 처리
주 : NREL에서 생성 된 바이오 오일 샘플은 수소 처리 시스템에서 촉매 수소화를 위해 PNNL에 제공 하였다.
- 수소 처리 시스템
- 수소 처리 시스템은 각 구성 요소를 선택하여 작동 상태에 있는지 확인합니다.
주 : 사용 된 수소 처리 반응기 시스템은 단일 패스, 병류, 연속 하향 유동 촉매 반응기로 구성된다. 1) 가스와 액체 공급 성분 2) 가열 된 반응기, 3), 가스 - 액체 생성물 분리 요소 (도 2)이 시스템은 세 개의 주요 구성 요소로 구성된다. 최대 촉매 온도 500 ° C (단 반응기 온도에서 평가)를 (최대 사용 압력 000 psig의) 시스템은 최대 13.6 MPa로 동작하도록 설계된다. - 수소 처리 모니터링 및 제어 시스템과 안전 제어 시스템이 작동 상태에 있는지 확인하십시오.
주 : 시스템 감시 부분적 각종 센서와 실내 내장 컴퓨터 프로그램에 의해 제어된다. 센서는 열전쌍, 압력 변환기 반응기뿐만 아니라 수소 환기 열차 포함원자로가있는 인클로저에 RS. 데이터는 반응기를 모니터링하기 위해 프로그램에 의해 기록된다. 출구 가스 유량은 유량계에 의해 측정되고, 데이터는 그 수반하는 소프트웨어에 의해 기록된다. 프로그램은 또한 반응기의 주요 장비의 전원을 제어한다. 실험 동안 반응기 특정 압력 변화 및 / 또는 온도 변화 또는 가연성 기체의 관점에서 작동 조건에서 원치 않는 변화를 겪게되면, 안전 한계의 존재 및 / 또는 환기 시스템이 실패하면, 프로그램이 자동 수 안전을 보장하기 위해 시스템을 종료합니다. 압력 릴리프 밸브 및 파열판은 오버 가압을 방지하기 위해 수소 처리 시스템에 설치됩니다.
- 수소 처리 시스템은 각 구성 요소를 선택하여 작동 상태에 있는지 확인합니다.
- 촉매 로딩 및 전처리
- 촉매 제조
- 모두 촉매를 분쇄,의 Ru / C, 무대-I 촉매 및 코모 / 무대-II 촉매로서 알 2 O 3 등 및0.60 mm (30 내지 60 메쉬) 입자 0.25를 유지 체.
참고의 Ru / C 촉매는 자체 제조하고 코모 / Al2O3 촉매는 상용 제품이었다.
- 모두 촉매를 분쇄,의 Ru / C, 무대-I 촉매 및 코모 / 무대-II 촉매로서 알 2 O 3 등 및0.60 mm (30 내지 60 메쉬) 입자 0.25를 유지 체.
- 반응기에 촉매 로딩
- 촉매 침대 지원 매체로 스테인리스 스틸 튜브와 스크린을 사용합니다. 반응기 외부의 "탭핑"동안 천천히 충전 촉매층을 형성하는 반응기에 순차적으로, 스테이지-II 촉매 입자 스테이지-I 촉매 입자 및 유통로 하였다 일본어 스테이지 I 촉매 압출 물을 부어 . 각 촉매의 부하 32 ml의 등온 영역에 위치한 각각의 촉매에 24 ㎖ (도 3)와 두 단계 촉매 베드를 형성한다.
- 수소 처리 시스템에 원자로를 설치
- 상기 가스와 액체에 반응기를 연결 한 다음 두 개의 히터를 설치하여 수소 처리 시스템에 배치 반응기사료 성분과 상기 기액 분리 요소.
참고 : 두 열 테이프 가열 알루미늄 피복 열을 제공하는 관형 반응기를 묶습니다. 각 가열 시스 촉매의 전처리 과정 및 하이드로 테스트 중에 반응기의 부분을 독립적으로 가열하기 위해 사용된다. 각 알루미늄 피복은 고열 및 절연 테이프로 감싸 온도 제어기를 사용하여 가열된다. 관형 고정층 촉매 반응기를 316 스테인레스 스틸, 13 mm의 내경 및 64 cm의 길이로 이루어진다. 열전대 웰 (4.7 mm 외경)는 반응기의 중심에 위치하고, 2 개의 열전대는 촉매층의 온도를 측정하는 웰에 배치된다.
- 상기 가스와 액체에 반응기를 연결 한 다음 두 개의 히터를 설치하여 수소 처리 시스템에 배치 반응기사료 성분과 상기 기액 분리 요소.
- 압력에서 시스템을 유지하고 압력 강하가 시간 당 1보다 작은 것을 보장 psig로 12.0 MPa의 질소 가스를 사용하여 누출 수소 처리 시스템의 압력을 확인한다.
- 촉매 전처리. 황화물시츄 촉매와 수소 화제 흐름 황화.
- 242 ㎖ / 분의 수소를 120 ℃ / hr의 속도로 150 ℃ 실온에서 두 촉매층을 가열한다.
- 이 242 ㎖ / 시간의 수소 시간 및 0.128 ml / 분 (a 공급 펌프에 의해 공급 데칸 35 중량 % 디 -tert- butyldisulfide)에서 에이전트를 황화 150 ℃에서 두 촉매 베드 온도를 유지한다.
- 83.3 ° C / hr의 속도로 150에서 250 ° C까지 무대-I 침대를 가열하고, 5.8 시간 동안 250 ° C로 유지한다. 같은 기간 동안 83.3 ° C / hr의 속도로 150에서 400 ° C의 단계-II 침대를 가열하고, 4 시간 동안 400 ° C로 유지한다. 절차 동안 10.3 MPa로, 0.128 ml / 분의 황화 제로 유량 242 ㎖ / 분의 수소 유속에서 반응기의 압력을 유지한다.
- 황화 에이전트 흐름을 중지하고 수소 흐름을 유지한다. 다음 원하는 반응 온도로 각각의 촉매 베드의 온도를 설정한다.
주 : 황화 에이전트 유량 사용 된 촉매의 양 및 전반적인 촉매 용액 0.12 / ㎖ 고양이 / hr의 황화 화제의 시간당 액체 공간 속도 (LHSV)에 의해 결정된다. 수소 유량은 황화 에이전트 유량 / ㎖ 황화 에이전트 액 1,890 mL의 수소에서 수소 - 대 - 황화 에이전트 유량비에 의해 결정된다. 수소 처리 장치의 기체 및 액체 공급 성분이 고압 주사기 펌프로 구성된다. 두 펌프 중 하나는 황화 제를 공급하기 위해 사용된다. 가스 및 황화 에이전트들이 반응기에서 촉매 상을 통해 아래로 통과하기 전에, 액체가 혼합되는 반응기의 전 반응 구역으로 도입된다.
- 촉매 제조
- 바이오 오일 수소
- 152 ㎖ / 분의 수소의 흐름을 조정하고 10.3 계내 압력을 유지한다. 각각 220과 400 ° C로 무대-I 촉매 침대와 무대-II 촉매층의 온도를 설정합니다.
참고 : 목즉, 수소 유량은 사용 된 촉매의 양에 의해 결정된다 0.20 ㎖ / ml의 고양이 / 각 스테이지에 대한 시간, 그리고 1900 mL의 수소 / ㎖ 바이오 오일의 수소로 바이오 오일 비 바이오 오일 LHSV . - 온도, 압력 및 수소의 흐름이 안정되어 베드 온도 및 수소 유량 기준을 기록한다.
- 바이오 오일 150 ppm의 황을 동일한 양으로 바이오 오일 피드 디 -tert- 부틸 디술 피드를 추가한다. 공급 펌프 중 하나 인 바이오 오일 공급 채우고 달성 기포가없는 액체 흐름까지 피딩 라인을 제거.
- 10.3 MPa로 인해 펌프를 가압하고, 연결 밸브를 개방하여 상기 반응기에 연결한다. / 시간 4.8 ml의 유속으로 바이오 오일을 공급하기 시작한다. 이 작업은 바이오 오일 수소 테스트를 시작합니다.
주 : 바이오 오일 유량은 사용 된 촉매의 양은 각각 0.20 ㎖의 스테이지 / ㎖ 고양이 / hr의 바이오 오일 LHSV에 의해 결정된다. 수소 가스와 바이오 오일 반응기 여기서의 사전 반응 구역으로 도입그들 반응기에서 촉매 베드를 통해 가정 트리클 흐름을 하향 통과하기 전에 기체와 액체를 혼합한다. - 반응기의 상태를 정기적으로 점검하고, 온도, 압력, 유량, 및 볼륨과 같은 파라미터를 기록한다. 상기 촉매 베드 온도는 원하는 온도의 ± 2 ℃ 이내인지 확인하여 상기 가스 및 액체 유량을 정확하게 원하는 설정과 동일하고, 반응기 압력이 소정의 압력은 0.15MPa ± 내에있다. 이다 촉매층에서 압력 강하 <0.35 MPa로 확인합니다.
주 : 시스템 감시 부분적 각종 센서와 실내 내장 컴퓨터 프로그램에 의해 제어된다. 센서는 반응기가있는 인클로저 열전쌍, 압력 변환기 반응기뿐만 아니라 수소 환기 센서를 포함한다. - 온 - 라인 마이크로 GC를 통해 배출 가스를 연출하여 배출 가스 시료마다 2 시간을 분석 할 수 있습니다.
주 : 마이크로 GC는 네 chann입니다EL 마이크로 GC 각각 수소 검사 전에 교정 가스를 이용하여 교정. - 액체 샘플을 수집 한 다음 절차를 사용하여 매 6 시간 : 질소 샘플링 트랩을 제거, 수집 바이알에 액체 시료 드레인 샘플링 트랩의 압력을 감소 우회 트랩 샘플링 트랩 전환 질소 샘플링 트랩 가압, 샘플링 트랩 생성물 흐름 리디렉션. 원하는 방향으로 가스 및 제품 전환 2 차원 및 3 방면 밸브의 일련의 동작한다.
주의 : 반응물이 촉매 상을 통과하면, 액체 생성물 및 미 반응 된 액체가 기액 분리 장치에서 가스 생성물 및 미 반응 가스로부터 분리된다. 고온 가스 원자로 시스템의 병렬 하류에 배치 된 두 개의 압축, 냉각, 액체 / 가스 냉각 트랩 (샘플 트랩 또는 바이 패스 트랩) 중 하나를 통해 전달합니다. 오프 - 가스는 압력이 감소하는 atmosp 배압 조절기를 통과heric 압력. 오프 - 가스는 그 유량을 측정하기 위해 가스 계량기를 통과한다. - 스트림에서 60 시간 동안 테스트를 실시 (스트림에 시간 [TOS]). 바이오 오일 공급을 중지하여 테스트를 종료합니다. / 분, 100 ㎖로, 100 ℃로 반응기의 온도 및 수소의 유량을 설정한다.
참고 : 시험은 수백 시간 오십에 이르기까지 던져 동안 작동 할 수있다.
- 152 ㎖ / 분의 수소의 흐름을 조정하고 10.3 계내 압력을 유지한다. 각각 220과 400 ° C로 무대-I 촉매 침대와 무대-II 촉매층의 온도를 설정합니다.
- 이후 시험 절차
- 바이오 오일을 공급하기위한 공급 펌프를 청소하는 아세톤을 사용합니다. 아세톤으로 세척 공급 펌프를로드합니다.
- 상기 촉매 베드 온도는 100 ℃로 할 때 10 내지 40 ㎖ / 분의 아세톤 유량 100 ㎖ / 분의 수소 유속 ~400 mL의 아세톤으로 촉매층을 제거.
- 반응기의 가열을 차단, 대기압 시스템을 감압하고, 적어도 24 시간 동안 반응기를 질소로 퍼지.
- 시스템에서 원자로를 제거하고 reacto에서 폐 촉매를 제거아르 자형.
- 제품 처리 및 결과 분석
- 액상 제품 가공의 경우, 두 개의 상을 분리하고 개별적으로 무게. 액체 제품은 두 단계, 가벼운 오일 상 (석유 제품)과 무거운 수상 (수성 제품)에 일반적입니다.
- 다음 오일 생성물의 분석을 실시 : 밀도를 측정하는 단계; 수분에 대한 칼 피셔 적정; 원소 분석 (D5291에 / D5373에, D5373mod 및 D1552 / D4239) 탄소, 수소, 질소, 산소 및 황 대; 총 산 번호에 대한 반 마이크로 컬러 표시 적정 (D3339); 유도 무기 콘텐츠에 대한 플라즈마 광 방출 분광법을 결합; 시뮬레이션 된 증류 (ASTM의 D2887)은 가솔린, 디젤, 제트 연료, 잔류 범위에서 연료 생성물의 상대적 양을 평가한다. 수성 제품의 다음 분석을 실시한다 : 탄소, 수소, 질소 콘 물 함량 및 원소 분석 (D5291 / D5373)에 대한 칼 피셔 적정십t 15.
- 생산 된 석유 제품, 수성 제품 및 가스 제품의 수율을 계산; 수소 소비량; 상기 유입 반응물 유량 및 밀도 입구 수소 유량, 출구 오일 제품 중량 출구 오일 생성물의 수분 함량에 기초하여 질량 균형은 수성 제품 중량 출구 가스 유량 및 배출 가스 조성을 출구.
- 유도 결합 플라즈마 발광 분광법 (15)에 의해 소모 된 촉매를 분석한다.
- 열분해 반응기를 조립합니다.
Representative Results
대표적인 초본 미생물의 빠른 열분해는 스위치 그래스, 또는 뜨거운 증기 여과 생성물 바이오 오일의 수소화 처리 촉매없이 여기에보고 된 과정에 대한 일례로서 사용된다. 이 실험의 자세한 내용은 우리의 최근의 책에서 자세히 확인할 수 있습니다. (15)
뜨거운 증기 필터링 빠른 열분해
표 1은 바이오 오일, 문자와 함께 전형적인 초본 원료에 대한 뜨거운 증기 필터없이 생성 가스 수율을 보여줍니다. 뜨거운 증기를 여과없이 대조 실험의 경우, 증기는 필터 하우징 비록 통과하지만, 상기 필터가 설치되지 않았다. 이 두 실험에서 동일한 체류 시간을 유지하므로 차이는 필터에만 기인한다. 바이오 오일 수율은 액체 인터로 바이오 매스의 주요 부분의 성공적인 전환을 나타내는, 56 %로 52 %였다테 오일. 대표적인 바이오 오일 샘플의 사진을도 4에 나타낸다. 질량 균형 폐쇄 90 %로 86 %였다. 제대로 응축 기차에서 수집되지 않은 빛 증기 질량 손실의 하나의 소스이었다. 열분해 오일을 응축하기 어려운 등 hydroxyacetaldehyde (비점 20.2 ℃)와 같은 여러 저비점 화합물을 함유. 두 번째 드라이 아이스 트랩을 추가하면 빛을 응축 화합물의 회복이 향상됩니다. 이전 응축 증기 농도를 증가시켜 빛 증기의 회복을 향상 여기에보고보다 높은 바이오 매스 공급 속도로 실험을 수행. 광 응축 화합물의 탈출 출구 가스의 가스 크로마토 그래피 - 질량 분광 분석에 의해 확인 될 수있다. 질량 균형 때문에 상대적으로 많은 양의 지팽이에서 생산 된 탈출 광 문자,의 가능성, 초본 원료 상대적으로 낮았다. 크래킹 반응에 따라서 필터에서 발생뜨거운 증기 필터의 clusion는 석유 생산량 감소 및 가스 생산량을 증가했다.
표 2 및도 5 및도 6은 초본 원료의 분석 결과 및 생성 된 바이오 오일을 나타낸다. 뜨거운 증기 필터링은 검출 한계 이하로 1.45 %에서 바이오 오일 애쉬 잔류 물을 감소시켰다. 알루미늄, 칼슘, 철, 칼륨, 마그네슘, 나트륨, 인, 규소 등의 각종 이물질은 바이오 오일에서 관찰되었으며, 이들은 주로 바이오 매스 원료에서 유래. 뜨거운 증기 필터링 상당히 뜨거운 증기 필터링 효과적으로 CHAR 화산재 입자를 제거하여 바이오 오일의 미량 원소 함량을 감소시키기위한 강력한 프로토콜임을 나타내는 바이오 오일 무기 내용을 감소시켰다. 뜨거운 증기 필터링은 또한 탄소 함량을 감소 바이오 오일의 산소 농도는 증가 하였다. 우디의 공급 원료에 비해 낮은 회분 함량이초본 원료 및 바이오 오일 애쉬 낮은 감소 무기 내용이 관찰된다. (15)
바이오 오일의 촉매 수소화
제조 된 바이오 오일의 분석 결과는 공정으로부터 제조 된 바이오 오일이 내연 기관에 직접 사용하기에 충분한 품질이 아닌 사실과 일치했다. 따라서, 바이오 - 오일의 업그레이드가 필요합니다. 두 바이오 오일 샘플을 상술 한 조건 하에서 수소 처리 시스템의 수소 처리 촉매로 업그레이드되었다.
바이오 오일은 촉매층에 축적 문자 또는 바이오 - 오일의 활성 종의 중합 제품과 수소 원자로를 연결하는 것으로 알려져있다. 따라서, 수소 시험 중에 촉매 상을 가로 지르는 압력 강하는 문자 또는 중합 제품을 축적하는 중요한 지표이다. 뜨거운 증기 여과 나IO-오일은 수소 시험에서 60시간 TOS에 대해 거의 완벽하게 수행했다. 그러나, 비 여과 바이오 오일 펌프에서 분리하고, 처리되지 않은 ~ 5 중량 %의 불용 고형분을 가졌다. 비록 이러한 치료 고형분으로 충전 촉매층을 밀봉 TOS 아마 때문에 비 여과 바이오 오일의 잔류 고형물의 50 시간 후 압력 강하 축적 여전히 있었다.
표 3 및 4, 5 및 7에서 서로 다른 토스에서 바이오 오일 수소화 처리 용 제품의 수율을 도시한다. CH 4, C 2 H 6, C 3 H (8)를 포함하는 업그레이드 오일 상과 수성 상 및 기체 생성물을 포함한 액상 제품, 위상 - 분리, C (4) H (10), CO 및 CO 2를 제작했다. 도 4는 수복 업그레이드 오일 샘플의 사진을 보여준다. 표 5업그레이드 된 오일의 분석 결과를 나타내고,도 5는 바이오 오일 및 업그레이드 된 오일의 원소 분석 결과를 비교한다. 수소화 처리는 산소, 황 및 질소를 감소시키고 생체 송유 크게 수소 첨가에 아주 효과적이었다. 업그레이드 된 오일의 산소 함량은 바이오 오일 공급 산소의 40 중량 %보다 훨씬 낮은 35이었다 ~2.0 중량 %이었다. 업그레이드 된 오일의 수소 대 탄소 비율은 바이오 오일 피드 ~1.3 비교 ~1.7이었다. 0.81에서 0.83로 증가 업그레이드 된 오일의 밀도의 추세 g / 시험 기간 동안, 60 시간 이상 TOS 온화한 촉매 불 활성화를 제안 용액.
도 7에 도시 된 바와 같이, 필터링 된 고온 증기를 필터링되지 않은 바이오 오일 사이의 수소 처리 제품의 비교는 뜨거운 증기 여과 바이오 오일 consi이다 약간 높은 물을 업그레이드 오일 비율로 이끄는 것으로 나타났다뜨거운 증기 여과 바이오 오일 피드의 높은 산소 함량 스텐트. 두 바이오 오일 업그레이드 된 기름의 특성은 매우 유사 하였다. 뜨거운 증기를 필터링 및 필터링되지 않은 바이오 오일의 수소화 처리 사이의 큰 차이는 고온 증기 여과 바이오 오일의 사용 촉매층 비 여과에 사용되는 촉매 상에 비해 이물질의 덜 증착 하였다이었다 바이오 오일.

5 cm 유동층 열분해 시스템도 1 회로도. 뜨거운 증기 필터, 축합 시스템, 및 가스 - 측정 시스템이있다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.


미니 수소 처리 반응기에서 베드 촉매의 그림 3. 도식. 촉매층의 온도 프로필은 좌측에 도시되어 있고, 각 스테이지의 촉매의 위치는 우측에 나타나있다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
S / ftp_upload / 54088 / 54088fig4.jpg "/>
대표적인 바이오 오일 샘플 (왼쪽)와 대표 업그레이드 오일 샘플 (오른쪽) 4. 사진을 그림. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

도 초본 원료 (지팽이), 고온 증기를 여과하여 생성 된 바이오 오일 및 오일의 업그레이드 원소 분석 결과 5. 비교. 탄소, 수소 및 산소 함량은 바이오 매스의 빠른 열분해 후 많이 변화하지 않았다 그러나, 산소 함량은 현저하게 감소하고, 수소 함량은 바이오 오일 수소화 처리 후 증가 하였다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
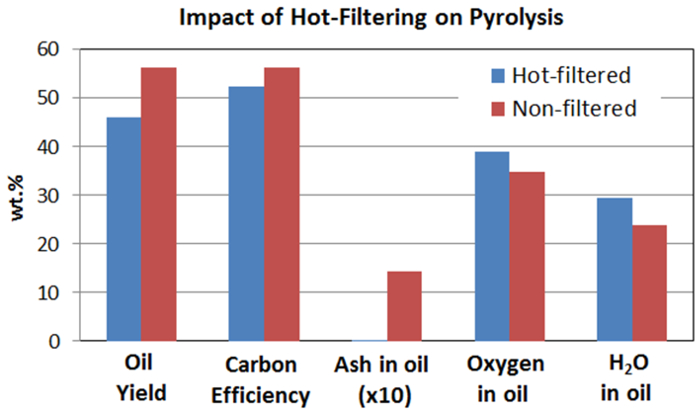
6. 오일 수율, 탄소 효율의 비교, 여과 뜨거운 증기 및 비 여과 열분해에서 바이오 오일의 일부 속성을 그림. 이 축합 전에 열분해 증기의 고온 가스를 여과의 영향을 보여준다. 고온 가스를 여과 무기 잔류 물을 제거하지만, 또한 열분해 오일 수율 [3- LM] 및 오일, 산소 농도 등의 오일 특성에 영향을 미친다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

여과 뜨거운 증기 및 필터링되지 않은 열분해로부터 바이오 오일의 수소화 처리 결과의 비교를도 7. 뜨거운 증기 여과 바이오 오일 약간 높은 물 대 리드 공연비 두 바이오 오일 업그레이드 연료의 특성은 매우 비슷하다. 두 열분해 오일의 수소 사이의 큰 차이는 뜨거운 증기 필터링 바이오 오일의 침대 촉매가 미네랄 훨씬 덜 증착을 보였다는 것이다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

표와 뜨거운 증기 여과없이 주요 열분해 제품 (바이오 오일, 숯, 가스)와 초본 원료 (지팽이)의 열분해에 대한 물질 수지 폐쇄 1. 산출한다.

로 뜨거운 증기 여과없이 생성되는 대표적인 초본 원료 (지팽이), 바이오 - 오일의 표 2. 분석.
088table3.jpg "/>
표 여과 뜨거운 증기 및 비 여과 대표 바이오 오일의 다른 토스에서 주요 수소 제품의 3. 수율.

표 4는 대표적인 바이오 오일의 수소화 처리 중에 가스 조성물을 만들었다.

대표적인 바이오 오일의 수소에서 업그레이드 된 석유 제품의 표 5. 분석.
Discussion
본 논문에서는 빠른 열분해 및 촉매 수소화를 통해 연료 범위의 탄화수소 리그 노 셀룰로오스 바이오 매스를 변환하는 자세한 절차를 설명했다. 5 cm, 내경 유동층 반응기 및 1.3 cm의 내경 고정층 촉매 반응기 및 그 동작 방법과 PNNL 수소 처리 시스템과 NREL 열분해 반응기 시스템이 상세히 설명된다. 이 반응기 시스템은 효율적이고 안전한 방식으로 수소화 열분해 테스트를 수행하는데 사용될 수있다. 우리는 열분해 반응기 시스템에서 액체 바이오 오일을 생산하는 대표적인 초본 원료를 사용하고, 상기 바이오 오일은 두 단계 촉매 베드의 Ru / C 및 코모 / 알루미늄 2 O 3 등을 황화 포함한 수소 처리 시스템에서 처리 된 촉매는 연료 범위 액체 탄화수소를 생성한다. 이 과정은 또한 목재, 잔디, 옥수수 여물 포함한 바이오 매스 원료의 광범위한 적용 열분해 된 후 생성 된 업그레이드바이오 오일은 바이오 연료를 생산합니다. 또한 바이오 매스 목재, 조류와 같은 액화 석유 (바이오 원유)과 같은 다른 바이오 매스에서 생성 된 중간체를 업그레이드에 사용될 수 16 수소 처리 및 수소 처리.
열분해시 바이오 오일 수율을 극대화 바이오 매스의 최대 휘발을 달성하기에 충분한 온도로 빠르게 바이오 매스를 가열이 필요합니다. 대부분의 미생물, 이는 500-600 ℃의 온도를 의미한다. 유동층은 높은 가열 속도를 제공하고, 바이오 매스를 모래로부터 빠른 열 전달을 제공한다. 작은 입자의 사용은 높은 가열 속도를 제공한다. 일반적으로 몇 % 더 높은 바이오 오일 수율은 <2mm 바이오 매스 지상보다 0.5 mm <바이오 매스 지상으로 달성된다. 극대화 수율은 낮은 온도 (1 ~ 2 초)의 체류 시간을 유지하여 증기의 열 균열을 최소화하는 것을 의미한다. 열분해 증기 끓는 점의 넓은 범위의 화합물이 포함되어 있습니다. 따라서, H오티 배관은 액체, repolymerized 증기 및 문자로 오염 될 경향이있다. 이러한 상황을 피하기 위해, 100 ° C 이하 오거 온도 및 오염을 방지하기 위해 400 ℃ 이상의 반응기 축합 열차 사이의 모든 표면을 유지하지만, 500 ° C 이하 열분해를 최소화. 열 테이프 철저한 커버리지 냉점을 방지하고 균일 한 온도를 제공 할 필요가있다. 그들에 폐쇄와 수 놓은 절연 패드는 일반적으로하여보다 균일 한 온도의 결과로,보다 균일 한 커버리지를 제공한다. 이는 온도가 응축기 입구 막힘을 초래할 수있는 고비 점 물질의 repolymerization 기회를 최소화하기위한 제 1 콘덴서 급격히 강하하는 것이 중요하다. 또한, 액체 회수를 최대화하고 가스 측정 및 분석 기기의 손상을 방지하기 위해 2 응축기에서 드라이 아이스를 사용하는 것이 필요하다.
일부 고급 기능은 기본 빠른 열분해 과정에서 언급되지 않았다. 나는t는 반응기 입구 근처 압력계 송신기가 유용하다. 또한, 반응기 사이클론에 걸쳐 압력 차를 측정하고 건조한 시험 미터의 최종 압력 및 온도 (정확한 부피 계산을 사용하는)을 측정하는 것이 유용하다. 또한 침대가 균일하게 충분히 균일 한 온도를 제공하기 위해 유동화되어 있는지 확인하는 열분해 침대에서 추가 열전대를하는 것이 도움이된다. 일반적으로, <5 ° C의 확산은 베드를 통해 수직으로 볼 수있다. 또한 반응기에 중첩 루프 온도 제어를하는 것이 유용하다. 오일 다량 필요하면 다시 느슨하게 장착 된 항아리와 하단에 밸브를 갖는다 아래 보조 숯 수신기 숯 수신기의 저면에 밸브를 설치하여 실장하는 것이 도움이된다. 이것은 연속 운전이 장시간 동안 유지 될 수 있도록하는 것이 가능 항아리에 마침내 보조 수신기로 숯 수신기를 비우고 할 수있다. 진동 도움이됩니다작동에 FUL. 파이프 수동 타격 사용할 수 있지만, 자동 진동자는보다 안정 교반을 제공한다. 이들은 공급기 원활한 공급 흐름을 유지하도록 로크 호퍼 오거 포트에서 연속적으로 작동 될 수있다. 또한, 문자 배수 동안 보조 문자 수신기에 자동 진동기를 사용하면 해당 작업이 훨씬 더 신뢰할 수 있습니다. 뜨거운 증기 여과 균열 및 위와 같이 바이오 오일 수율을 감소 향상시킵니다. 여전히 낮은 응축 온도 (> 400 °의 C) 상기 필터의 온도를 유지하는 균열 최소화한다. 필터에 불활성 표면은 균열을 감소시킬 수있다. 필터 면적은 압력 강하를 감소시키는 클 필요가있다.
빠른 열분해 공정의 주요 제한은 제조 된 바이오 오일은 직접적인 이용을 제한하고 지속 몇 가지 문제가 발생 고점도, 부식성 불량 휘발성 저 발열량 화학적 불안정성과 같은 몇 가지 큰 문제가 특성을 가지고 있다는자신의 업그레이드를 보내고. -6,7,8,9- 빠른 열분해는 H 2와 같은 반응성 가스의 존재 하에서 수행 항 빠른 열분해 촉매 열분해 빠르고 신속 열분해 열분해 기상 업그레이드하는 촉매 공정에 통합되고, 그리고 수소 첨가 열분해의 변형 더 높은 품질의 바이오 오일로 이어질하지만 높은 운영의 복잡성과 낮은 제품 수율을 고통을 수 있습니다. 4,8
두 단계 촉매 적 수소화 처리는 탄화수소 범위의 연료로 바이오 오일 변환하는 양호한 처리 결과를 보였다. 바이오 오일은 탄소 재료 및 이에 따른 촉매 비활성화를 형성하고 심지어 플러깅 대한 높은 경향을 초래하기 때문에 이러한 저온 repolymerization 축합을 겪을 수 보닐 페놀 화합물 등의 활성 종의 존재 화학적으로 불안정한 것으로 알려져 촉매층. 따라서, 제 1 단계 수소 첨가 단계는 프로세스에 대한 중요한이고, 이중 안정 하였다적당한 수소화 촉매를 사용하여 비교적 낮은 온도에서 카르 보닐 및 페놀의 수소화 O 오일. 수소화 촉매의 성능은 프로세스의 장기적 안정성 및 동 작성의 핵심이다. 수소화 탈산 소화에 의해 산소를 제거하여 황화물 계 수소화 촉매에 의해 제 2 단계에서 발생 하였다. 생산 수율 및 최종 오일 생성물의 특성은 두 번째 단계에서 사용 된 촉매 및 조건에 의존한다. 액체 연료의 최종 수율을 최대화하는 것은, 반응 온도, 압력, 및 공간 속도를 포함하여 이러한 알킬화 함수 CC 결합을 발생시킬 수있는 촉매 및 반응에 최적화 된 파라미터를 사용하여 달성 될 수있다. 수소화 공정의 주요 제한 때문에 화학적 불안정성 및 오염 물질 (17)의 존재하에, 수소화 촉매의 수명, 특히 첫번째 단계 수소화 촉매로서 바이오 오일의 일부 문제 성질 여전히 제한되어 있다는전체 공정 비용이 많이 드는하게 에디션. 보다 강력한 촉매를 사용함으로써 달성 될 수있는 사용 된 촉매의 수명을 최대화; 반응 온도, 압력 및 공간 속도를 포함하여 최적의 반응 매개 변수; 또는 전처리 바이오 오일 피드의 활성 종 또는 오염 물질의 함유량을 저하한다.
수소 처리가 포함 된 가연성 가스와 액체와 높은 압력과 반응기 온도에서 작동했다. 따라서, 안전 규칙과 절차를 엄격하게 따라야한다.
Disclosures
저자는 더 경쟁 재정적 이해 관계가 없음을 선언합니다.
Acknowledgments
이 작품은 PNNL의 NREL에서 계약 DE-AC36-08 - GO28308에서 미국 에너지 부 (DOE)와 계약 DE-AC05-76RL01830에 의해 지원되었다. 저자는 기꺼이 DOE의 바이오 에너지 기술 사무소의 지원을 인정합니다.
Materials
| Name | Company | Catalog Number | Comments |
| Pyrolysis system | |||
| Feedstock | Mill to pass 2 mm screen | ||
| Sand for bed material | Black Rock | Screen to 300-500 microns | |
| Furnace | Thermcraft | TSP-3.75-0-24-3C-J13667/1A | Split tube furnace 3.75 ID X 24 L |
| Pyrolysis reactor | Custom-built at NREL | 2" diameter, height 17", dual staggered plate distributor, 316SS, Auger port is 2.5 cm above distributor and is cooled with air or water, there is a coiled 1/4" 304 SS tube below the distributor to pre-heat the gas | |
| Cyclone | Custom-built at NREL | 1" diameter | |
| Cyclone receiver | Custom-built at NREL | 1 L capacity | |
| Cyclone secondary receiver | Custom-built at NREL | 1 L capacity | |
| Hot vapor filter | Serv-A-Pure | SC2-0P10B34-X | 316SS, 10 inches long, 2.0 micron |
| 2-neck round-bottomed flasks | 500 ml | ||
| Electrostatic precipitator | Allen Scientific Glassware, NREL-built electrodes | Custom built | 2" diameter 10" long ground electrode, glass enclosed, stop-cock on bottom |
| High-voltage power supply | Spellman High Voltage | Bertan 803C-300P | 30 kV max, 0.5 mA |
| Cold-finger condenser | Aldrich | Z164038 | |
| Coalescing filter | Finite | 10C15-060 | |
| Dry test meter | American Meter | DTM-200A | with IMAC counter |
| Gas chromatograph | Varian | CP-4900 | MS5A, PBQ, CP-Sil columns |
| Hydrogen detector | Gerhard Wagner | TCM-4 | thermal conductivity detector |
| Non-Dispersive Infrared Spectrometer | California Analytical | Model 300 | Carbon monoxide 0-5%, 0-25%, carbon dioxide 0-5%, 0-20%, methane 0-5,000 ppmv, 0-3% |
| Mass flow controller | Celerity (now Tylan) | Unit 7301 | 0-20 SLM reactor bottom, 0-10 SLM auger, 0-2 slm purges, 0-5 slm air |
| Auger | Auger Manufacturing Specialists | 110520 | 3/8" Dia SS RH Auger 18" |
| Motor for Auger | Leeson | Gearmotor-Parallel Shaft, 94 rpm, 1/15 HP, TEFC, 115 VAC | |
| Feeding system: Motor for hopper | Lenze | VDE0530 | 7KB4-7-100H Motor Ac Helical Gearbox 3PH 0.25 kW 1.4/0.82 A |
| Feeding system: Hopper and Loss in weight feeder | K-TRON Soder | KCL24T20 | with K10S controller |
| Feeding system: Valves | Swagelok | SS-65TS16 | 151 bar at 37 °C and 6.8 bar at 232 °C |
| Control system | Opto22 | SNAP-PAC parts | |
| Heat cables | McMaster-Carr | 4550T152 and similar | Extreme-Temperature (1,400 °F), heavy insulation for use on metal |
| Ball Vibrator | Vibtec | K 8 | |
| U-tube | Custom-built at NREL | 1/4" PFA and stainless steel tubing, 1.4 m tall | |
| Hydrotreating system | |||
| Ru on carbon catalyst | Fabricated at PNNL | 7.6 wt% Ru on carbon | |
| 3% Co and 9% Mo on Al2O3 catalyst | Alfa-Aesar | 45579 | Cobalt oxide, typically 3.4-4.5%, Molybdenum oxide typically 11.5-14.5% on alumina |
| Feeding pumps | ISCO | 500D | Syringe pump, 500 ml cylinder capacity |
| Mass flow controller | Brooks | SLA5850S1BAF4B1A1 | |
| Temperatrue controller | Cole-Parmer | WU-89000-10 | Digi-Sense Advanced Temperature Controller, 115 V |
| Thermocouples | Omega | K-type thermocouples | |
| Pressure transducer | Omega | PX309-3KG5V | |
| Heat tapes | Cole-Parmer | EW-03106-27 | Dual element heating tape, 1/2 in x 12 ft, 936 watts, 120 VAC w/ 2-prong plug |
| Digital pressure gauge | Omega | DPG4000-3K | High Accuracy Digital Pressure Gauge, with Data Logging Capability |
| Back pressure regulator | Mity-Mite | ||
| Gas flow meter | Mesa Labs | 200-220L | Dry Cal, Definer 220 Low Flow |
| Hydrotreating reactor, cross, tee, fittings | Parker, Autoclave | ||
| Combustible gas sensor | SMC | 5100-02-IT-S1-01-00-0-0 | Combustible gas detection sensor, 24 VDC power, analog 4-20 MADC output with modbus, no relays |
| H2S sensor | SMC | 5100-05-IT-S1-01-00-0-0 | H2S toxic gas sensor module, 24 VDC power, analog 4-20 MADC output with modbus, no relays |
| Ventilation sensor | TSI | FHM10 | Fume Hood Monitor FHM10 |
| Micro-Gas chromatograph | Inficon | Inficon 3000 | Four-channel micro-GC with molecular sieve, Plot U, Alumina, and Stabilwax columns |
| Lab-view based monitering and controlling system | Custom-built at PNNL | Using National Instruments parts and Labview software |
References
- BP. Statistical Review of World Energy. , http://www.bp.com/content/dam/bp/pdf/Energy-economics/statistical-review-2014/BP-statistical-review-of-world-energy-2014-full-report.pdf. (2014).
- U.S. Energy Information Administration. International Energy Outlook 2014. , http://www.eia.gov/forecasts/ieo/pdf/0484%282014%29.pdf (2014).
- Bioenergy Technologies Office. Replacing the Whole Barrel. , http://www1.eere.energy.gov/bioenergy/pdfs/replacing_barrel_overview.pdf. (2013).
- Huber, G. W., Iborra, S., Corma, A. Synthesis of transportation fuels from biomass: Chemistry, catalysts, and engineering. Chem. Rev. 106 (9), 4044-4098 (2006).
- Mohan, D., Pittman, C. U. J., Steele, P. H. Pyrolysis of wood/biomass for bio-oil: A critical review. Energy Fuels. 20 (3), 848-889 (2006).
- Bridgewater, A. V. Review of fast pyrolysis of biomass and product upgrading. Biomass Bioenergy. 29, 68-94 (2012).
- Elliott, D. C. Historical developments in hydroprocessing bio-oils. Energy Fuels. 21 (3), 1792-1815 (2007).
- Wang, H., Male, J., Wang, Y. Recent advances in hydrotreating of pyrolysis bio-oil and its oxygen-containing model compounds. ACS Catal. 3 (5), 1047-1070 (2013).
- Zacher, A. H., Olarte, M. V., Santosa, D. M., Elliott, D. C., Jones, S. B. A review and perspective of recent bio-oil hydrotreating research. Green Chem. 16, 491-515 (2014).
- Elliott, D. C., et al. Catalytic Hydroprocessing of Fast pyrolysis bio-oil from pine sawdust. Energy Fuels. 26 (6), 3891-3896 (2012).
- Venderbosch, R. H., Ardiyanti, A. R., Wildschut, J., Oasmaa, A., Heeresb, H. J. J. Stabilization of biomass-derived pyrolysis oils. Chem. Technol. Biotechnol. 85 (5), 674-686 (2010).
- Olarte, M. V., et al. Towards long-term fast pyrolysis oil catalytic upgrading. Prepr. Pap. Am. Chem. Soc., Div. Fuel Chem. 58 (2), 230-231 (2013).
- Scahill, J., Diebold, J. P., Feik, C. Removal of residual char fines from pyrolysis vapors by hot gas filtration. Developments in Thermochemical Biomass. Bridgwater, A. V., Boocock, D. G. B. , Blackie Academic and Professional. London, U.K. (1996).
- Hoekstra, E., Hogendoorn, K. J. A., Wang, X., Westerhof, R. J. M., Kersten, S. R. A., van Swaaij, W. P. M. Fast pyrolysis of biomass in a fluidized bed reactor: In situ filtering of the vapors. Ind. Eng. Chem. Res. 48 (10), 4744-4756 (2009).
- Elliott, D. C., Wang, H., French, R., Deutch, S., Iisa, K. Hydrocarbon liquid production from biomass via hot-vapor-filtered fast pyrolysis and catalytic hydroprocessing of the bio-oil. Energy Fuels. 28 (9), 5909-5917 (2014).
- Howe, D., et al. Field-to-Fuel Performance Testing of Lignocellulosic Feedstocks: An Integrated Study of the Fast Pyrolysis/Hydrotreating Pathway. Energy Fuels. 29 (5), 3188-3197 (2015).
- Wang, H., Wang, Y. Characterization of Deactivated Bio-oil Hydrotreating Catalysts. Topics in Catalysis. 59, 65-72 (2015).



