Summary
生物油を生産するリグノセルロース系バイオマスの速い熱分解および燃料範囲の炭化水素を生成するためのバイオ油の接触水素化処理のための実験方法が提示されています。バイオオイルから微粒子チャー粒子及び無機汚染物質を除去するために、高速熱分解中に高温蒸気の濾過も評価しました。
Introduction
私たちの社会は、化石燃料( 例えば 、石油、天然ガス、石炭など )に大きく依存します。これらのリソースは、持続可能なエネルギー源ではなく、化石燃料資源の先細り懸念、CO 2排出量の環境への影響、および経済的な問題につながる、急速に増加率で枯渇されています。 1,2,3,4代替と持続可能なエネルギー源の需要が高まっています。バイオマスは、現在のエネルギー生産と変換システムで化石燃料を代替するための液体燃料(バイオ燃料)と炭素系化学物質の生産のためのみ再生可能とカーボンニュートラルな資源です。 3,4
現在、最も豊富で最も安価なバイオマス源であるリグノセルロース系バイオマス( 例えば 、森、草、エネルギー作物、農業廃棄物など )は、様々な熱化学および生物学的経路を介してバイオ燃料を生産するための方法として最も注目を集めています。
最初のルートは唯一のリグノセルロース系バイオマスのセルロースやヘミセルロース部分を利用することができます。アップグレードと統合熱分解は、バイオ燃料の直接生産のための短期的な実行可能な技術であると考えられています。
熱分解は、酸素の非存在下で400〜550℃の間の温度で、リグノセルロース系バイオマスの熱分解です。 4,5,6は 、そのような解重合、脱水、及びC-C結合の切断などの反応の数を熱分解中に発生し、複雑な混合物Oの形成をもたらしますF 200以上の含酸素化合物。 4,5,6バイオオイル(乾燥飼料の75重量%まで)高収率では保持さバイオマス原料に蓄積されたエネルギーの最大70%で製造することができました。 4,5しかし、標準装備で輸送用燃料として製造した熱分解バイオオイルの直接の使用は、このような高粘度、腐食性、貧しい揮発性、低など、さまざまな物理的および化学的性質につながる高酸素や水分含有量、の問題があります発熱量、および安定性が悪いです。 6,7,8,9したがって、大規模な酸素除去は、燃料範囲の炭化水素をバイオオイルをアップグレードするために必要です。水素中で固体触媒を用いた接触水素化処理は、水素化脱酸素と水素化反応を介して酸素を除去することによってバイオオイルをアップグレードするための最も一般的な経路です。 6,7,8,9
現在、水素化処理に続いて熱分解するための主要な課題の一つは、特にため、長期安定運転を達成することですバイオ油中のバイオオイルおよび無機硫黄残基の熱的不安定性は、重要な触媒の失活を引き起こすで水素化処理を行います。 10,11バイオオイルの熱的不安定性は、バイオオイル中の活性種を安定化するために、低温水素化によって対処されてきました。バイオ油留分の再重合を触媒し、蒸着により水素化処理触媒を不活性化可能性無機残渣を除去することにより、バイオオイルの11,12クリーンアップは、価値があります。熱い蒸気濾過が効果的に熱分解中にチャー粒子を除去することによりバイオオイル中の無機含量を減少させる技術の一つです。 13,14,15ホット蒸気ろ過は、蒸気の凝縮前に高温で熱分解ガス/蒸気流からchar型微粉を分離するために、熱分解反応器の下流で使用されています。 13,14,15
ここでは、バイオマスの高速ピロールのための国立再生可能エネルギー研究所(NREL)で使用されるプロトコルを報告しますysis付きとなしの流動床反応器を用いたバイオオイルを生成するために、ホット蒸気濾過およびパシフィック・ノースウェスト国立研究所(PNNL)の両方で連続流充填層触媒反応器内のバイオ燃料を生産するバイオオイルの水素化処理のために。反応器システム、操作手順、処理、および原料、バイオ油およびバイオ燃料の分析の構成について詳細に説明します。とやホット蒸気フィルタリングおよび生産バイオオイルの水素化処理せずに代表バイオマス原料の熱分解処理の結果は、ホット蒸気ろ過の影響の評価と一緒に提示されています。
Protocol
熱い蒸気濾過1.高速熱分解
- バイオマス原料の準備
- ミル<2mmの粒子サイズにバイオマス。涼しく乾燥した場所で保管してください。
- 熱分解システムを組み立て
- 熱分解反応器を組み立てます。
- 炉内の反応器をマウントします。反応器に窒素、オーガ窒素、および空気ラインを流動接続します。ジャケットオーガポートにオーガーを挿入します。ジャケットに冷却空気を接続します。
- マウントと接続オーガーモーター。
- マウント30〜60センチ直接オーガポートの垂直開口部上記固体フィーダー。
- 固体フィーダー出口とオーガポートの垂直開口部との間のロックホッパーをマウントします。ナイロン編組とオーガーポートに接続し、内径25mmのにビニールチューブを強化。ホースクランプ付きオーガーポートにチューブを固定します。軽量、明確な、緩いプラスチックスリップフィットとフィーダに接続します。
- サイクロンとホットフィルターを組み立てます。
- サイクロンをマウントし、反応器出口にサイクロン入口を接続します。サイクロンに近いカップル受信機。
- フィルタハウジング(2ミクロンの孔サイズを有するステンレス鋼製)マウントホットフィルタ。ホットフィルタ入口にサイクロンコンセントを接続します。サイクロン出口に窒素パージと圧力リリーフを接続します。
- 凝縮器入口にサイクロン入口からトレースを加熱する熱テープと絶縁毛布を使用してください。
- コンデンサーシステムを組み立てます。
注:実験室ジャッキ、リングスタンド、実験にクランプを使用して、ドラフト内で凝縮系の作品をマウントします。- 第一凝縮のために、1.2センチ(外径)ステンレス鋼管のカップル15〜30センチ、標準的なテーパージョイントにチューブをホウケイ酸します。コンテナ股関節に配置された500ミリリットル、2口(標準テーパー)に第一凝縮、丸底フラスコ(受信機)を接続tは氷浴として機能します。ガラス製品のホースすり合わせ上のクランプ、球状関節、及びホースバーブで固定9〜12 mmの明確なビニールチューブを下流のこの点の容器間の接続を行います。
- 電気集塵装置(ESP)の下側ポート(入口)に第1の集フラスコの出口を接続します。
- ドライアイストラップ(コールドフィンガーコンデンサー)の小さな上側接続にESPの上側ポート(コンセント)を接続します。
- ESPとドライアイストラップとの間で整列するU字管を接続します。水との完全なU字管の半分を埋めます。
- ドライアイス浴となる容器に入れ、500ミリリットル、2口丸底フラスコ(受信機)にドライアイストラップを接続します。
- 合体フィルタのハウジングの入口(中央口)に500mlのフラスコの出口を接続します。
- フィルターハウジングの底部の周りにドライアイスを保持するための容器を置きます。
- フィルタを接続outle乾燥試験メーターやその他のガス分析器(のT 例えば、非分散赤外線COためのCO、CO 2、CH 4、水素を熱伝導度検出器、及びマイクロガスクロマトグラフィー(マイクロGC)用アナライザ、CO 2、窒素、水素、及びC 1 -C 4炭化水素)と通気します。
注:熱分解反応器システムの概略を図1に示されています。バイオマス供給装置、熱分解、サイクロン、ホット蒸気フィルタの写真、および熱分解反応器システムのコンデンサは、補助ファイルにS5に図S1に示されています。
- 負荷熱分解反応器
- 反応器に砂(330グラム)の200ミリリットルを注ぎます。
- 供給ホッパーに地上バイオマスの2キロを注ぎます。
- リークチェックの熱分解システム
- 凝縮器入口でシステムを締めくくります。
- 、0.05 MPaのまたは予想される最大作動圧力に加圧し方高くなっています。圧力を維持するために必要な流れは<200ミリリットル/分であることを確認してください。ない場合は、検索してリークを修正して、この手順を繰り返します。
- 圧力を開放し、キャップを取るシステム、凝縮系の出口端部で凝縮系、キャップを接続してください。
- 0.01 MPaのに加圧し。 <200ミリリットルの流れ/分、圧力を維持していることを確認してください。ない場合は、検索してリークを修正して、この手順を繰り返します。
- 商品に凝縮系を減圧し、再接続します。
- 原子炉を加熱
- 冷却空気をオンにします、1標準L /分3標準リットル/分とオーガ窒素流に窒素流を流動化設定。
- セット炉ターゲット500°Cの温度400まで500℃まで、他のヒータ。
- 1〜10℃/分の速度で温度を標的とするランプ温度アップ。
- 動作させるために準備
- 14標準リットル/分、窒素流量を流動増加、オーガ窒素FLOW 1.4標準L /分の速度、および0.5標準L /分の流量でパージガスを導入します。パージのほとんどは、サイクロンコンセントに破裂ディスクポートになります。
- 氷で第一凝縮下で風呂を埋めます。ドライアイスでフィルターを合体の周りにドライアイストラップ、その受信機の下の容器、および容器を満たします。
- 熱電対を用いてフィルタを合体の内部モニター温度がフィルタの表面上に配置され、それは0°Cになるようにドライアイスレベルを調整します。
- 熱分解実験を行います
- ロックホッパー弁(4秒のサイクルを使用)し、オーガーをオンにします。
- ESPの電源をオンにします。 5〜10キロボルトに設定された電圧は、少なくとも一回ごとに2秒アークを観察するために、必要に応じて。
- 酸素が存在しないことを確認するために、マイクロGCを使用してください。オーガとロックホッパーをオンにすると、リークの存在を示す出力ガス流量の減少を、引き起こさなかったことを確認します。
- 100グラム/ hrでフィーダーをオンにします。床の温度を確認し、増加した熱負荷を補償するために必要なセットポイントを増加させます。
- 温度が500°Cの2°C以内に回復した場合には100グラム/時間によって供給速度を増加させます。 420グラム/時間の供給速度に到達するまでこれを繰り返します。
- 圧力計により、すべてのマイクロGC、乾燥試験メーター速度で15分、レコード床温度、フィーダコントローラ上の送り速度、ガス濃度、およびシステム圧力。 ESPはまだ正常にアーク放電されていることを確認します。必要に応じてこれらのいずれかの変化に対応。氷とドライアイスを補充します。必要に応じて、生成物収集ジャーにESPを排出します。
- シャットダウン
- バイオマスの1キロを供給した後、供給を停止します。
- ガスレベルの後、すべてのヒーターをオフにする1標準L / minに3標準リットル/分とオーガーの流れへの流れを流動化下げ、定常値の10%未満に減衰しています。 ESP、ロックホッパバルブ、オーガをオフにします。
- システムがホットセクションを開く前(4〜6時間)を冷却することができます。 </ OL>
- 液体製品とチャーを収集します。
- 全液体収率を得るために、コンデンサ系のすべての部分を秤量します。共通の瓶やボトルに凝縮受信機から液体を注ぎます。また、ガラス製品をきれいにするために、アセトンを使用しています。
- 瓶に空のchar型の受信機。 、ホットフィルターを取り外し筐体を空にし、チャージャーにフィルタをはねのけます。フィルタを秤量します。取り外し、床物質の重量を量ります。このサービスのノックアウト容器とHEPAの真空を使用してください。
- システムを酸化します。
- リアクトル、サイクロンレシーバを密封し、高温のフィルターを掃除しました。 1.4節で前述したように漏れがないか確認してください。
- 凝縮系をバイパスする凝集フィルタの出口に凝縮器入口から金属線をインストールします。
- 流動化ガスとして3標準リットル/分の窒素及び1標準L /分オーガ窒素流で550°Cに原子炉を加熱します。
- 流動化に空気を追加ガス。 0.2標準L /分で開始し、徐々に/分で4 Lに増加します。 CO + CO 2濃度が0.1%未満になるまで続けます。
- 利回りを計算します。
- 凝縮系の質量の変化量などの液体の収率を計算します。
- ベッドでの重量変化、熱いフィルタの重量変化、およびサイクロンレシーバおよびホットフィルターハウジングから集めチャーの和としてチャー収率を計算します。
注:追加の文字は、システムの酸化から推定することができたが、これは通常は重要ではありません。 - GC及び乾燥試験メーターの流量で測定したガス濃度のガス状生成物の総重量のガス収率を計算します。
バイオオイルの2触媒水素化処理
注:NRELで生産バイオオイルのサンプルは、水素化処理システム上の触媒水素化処理のためPNNLに出荷されました。
- 水素化処理システム
- 水素化処理システムは、各コンポーネントをチェックすることにより、動作状態にあることを確認してください。
注:使用される水素化処理反応器システムは、単一パス、並流、連続的な、ダウンフロー触媒反応器として構成されています。 1)ガスと液体搬送素子、2)加熱反応装置、および3)気液生成物の分離・コンポーネント( 図2):システムは、3つの主要コンポーネントで構成されています。最大触媒温度500°C(のみ反応器をこの温度で評価されて)で、システムは、最大13.6メガパスカル(最高使用圧力2000 PSIG)で動作するように設計されています。 - 水素処理監視制御システムや安全制御システムが動作状態にあることを確認してください。
注:システムは、監視され、部分的に、様々なセンサと社内組み込まれているコンピュータプログラムによって制御されます。センサーは熱電対と圧力変換器原子炉用としてだけでなく、水素と換気戦争を含みます原子炉が配置されているエンクロージャ内のRS。データは、原子炉を監視するために、プログラムによって記録されています。出口ガスの流量は、流量計によって測定され、データがそれに付随するソフトウェアによって記録されます。プログラムは、原子炉の主要機器の電源を制御します。実験中、反応器は、特定の圧力変化及び/又は温度変化の観点から運転状態における望ましくない変化、または可燃性ガスを受ける場合には、安全限界の上に存在し、および/または換気システムに障害が発生した場合、プログラムが自動的に可能性安全性を確保するためにシステムをシャットダウンします。圧力逃がし弁及び破裂板はまた、過加圧から保護するために水素化処理システムにインストールされています。
- 水素化処理システムは、各コンポーネントをチェックすることにより、動作状態にあることを確認してください。
- 触媒充填と前処理
- 触媒調製
- 両方の触媒を粉砕、ルテニウム/ C、ステージIの触媒とのCoMo /ステージIIの触媒としてのAl 2 O 3、などと0.60ミリメートル(30〜60メッシュ)の粒子に0.25を維持するためにふるいです。
注:のRu / C触媒は、社内で調製したコモ/のAl 2 O 3触媒は、市販品でした。
- 両方の触媒を粉砕、ルテニウム/ C、ステージIの触媒とのCoMo /ステージIIの触媒としてのAl 2 O 3、などと0.60ミリメートル(30〜60メッシュ)の粒子に0.25を維持するためにふるいです。
- 反応器への触媒充填
- 触媒床のための支持媒体としてステンレス鋼管と画面を使用してください。反応器の外側に「タップ」しながら、ゆっくりと充填された触媒床を形成するために原子炉を順次に、ステージIIの触媒粒子、ステージIの触媒粒子、およびディストリビューターとして使用したオリジナルステージIの触媒押出物を、注ぎます。各触媒の負荷32 mlの等温ゾーン内に位置する各触媒24mlの( 図3)との二段階触媒床を形成します。
- 水素化処理システムに原子炉をインストールします
- 2ヒーターを設置した後、気体と液体にリアクトルを接続することにより、水素化処理システムに原子炉を置きます飼料成分と気液分離コンポーネント。
注:2つの熱テープ加熱アルミニウム製シースは、熱を提供するための管状反応器を囲みます。それぞれの加熱されたシースは、触媒の前処理中および水素化処理試験中に原子炉の部分を加熱するために独立して使用されます。各アルミニウムシースは、高温耐熱テープ及び断熱材で包み、温度コントローラを使用して加熱されます。管状の固定床触媒反応器は、316ステンレス鋼から13ミリメートル、内径64センチの長さで作られています。熱電対ウエル(外径4.7 mm)を、反応器の中心に配置され、2つの熱電対を触媒床の温度を測定するウェルに配置されています。
- 2ヒーターを設置した後、気体と液体にリアクトルを接続することにより、水素化処理システムに原子炉を置きます飼料成分と気液分離コンポーネント。
- 圧力でシステムを維持し、圧力の低下が毎時1のpsig未満であることを保証することにより、12.0 MPaの窒素ガスを使用して漏れを水素化処理システムの圧力を確認してください。
- 触媒前処理。硫化物水素と硫化剤の流れでその場で触媒。
- 242ミリリットル/分で水素中で120℃/ hrの速度で150℃まで室温から両方の触媒床を加熱します。
- 0.128ミリリットル/分(送液ポンプによって供給されたデカン中35重量%のジ-tert- butyldisulfide)で242ミリリットル/時と硫化剤で水素中で2時間150℃で両方の触媒床温度を維持します。
- 83.3℃/ hrの速度で150〜250°CにステージIベッドを加熱し、5.8時間250℃で維持します。同期間中、83.3℃/ hrの速度で150〜400℃のステージIIのベッドを加熱し、4時間400℃で維持します。処置中に、10.3 MPaで、0.128 ml /分での硫化剤の流量、および242 ml /分の水素流量で反応器の圧力を維持します。
- 硫化剤の流れを停止し、水素流を維持します。その後、所望の反応温度に各触媒床の温度を設定します。
注:硫化剤流量は、全体的な触媒0.12ミリリットル/ mlの-CAT / hrの触媒の使用量と硫化剤液空間速度(LHSV)で決定されます。水素流量は、硫化剤の流速及び/ mlの硫化剤液1,890 mlの水素で水素への硫化剤の流量比によって決定されます。水素化処理システムの気体と液体給コンポーネントは2高圧シリンジポンプで構成されています。 2つのポンプの一方は、硫化剤を供給するために使用されます。ガスと硫化剤は、それらが反応器内の触媒床を通って下方に通過する前に液体が混合され、反応器の予備反応器ゾーンに導入されます。
- 触媒調製
- バイオ油の水素化処理
- 152ミリリットル/分に水素流量を調整し、10.3 MPaでのシステム圧力を維持します。それぞれ、220および400℃にステージIの触媒床とステージII触媒床の温度を設定します。
注:番目E水素流量は、使用される触媒の量は、各段0.20ミリリットル/ mlの-CAT / hrのバイオオイルのLHSV、1900 mlの水素/ mlのバイオオイルの水素へのバイオオイルの比によって決定されます。 - 温度、圧力、および水素流量が安定したときに床の温度及び水素流ベースラインを記録します。
- バイオ油中の150ppmの硫黄に相当する量でバイオ油原料にジ-tert-ブチルジスルフィドを追加します。送りポンプのいずれかでバイオ油原料を充填し、気泡のない液体の流れが達成されるまで、供給ラインをパージします。
- 10.3 MPaのにポンプを加圧し、その後、接続バルブを開くことによって反応器に接続します。 4.8ミリリットル/ hrの流速でバイオオイルを供給開始します。このアクションは、バイオオイルの水素化処理のテストを開始します。
注:バイオオイル流量は、使用される触媒の量は、各段0.20ミリリットル/ mlの-CAT / hrのバイオオイルのLHSVで決定されます。水素ガスとバイオオイルはここで、反応器の予備反応器ゾーンに導入され彼らは反応器内の触媒床を通る想定細流に下向きに渡す前に、気体と液体が混在しています。 - 原子炉の状態を確認し、定期的に、例えば、温度、圧力、流量、およびボリュームなどのパラメータを記録します。触媒床の温度が所望の温度の±2℃以内であることを確認し、気体と液体の流量は、正確に目的の設定と同じであり、原子炉圧力が所望の圧力の±0.15 MPaの範囲内です。触媒床全体での圧力降下を確認してください<0.35 MPaです。
注:システムは、監視され、部分的に、様々なセンサと社内組み込まれているコンピュータプログラムによって制御されます。センサーは反応器が配置されているエンクロージャ内の熱電対と圧力変換器原子炉用としてだけでなく、水素と換気センサを含みます。 - オンラインのマイクロGCを介してオフガスを向けることによって、出口ガスサンプルごとに2時間を分析します。
注:マイクロGCは、4-channですエルマイクロGCと各水素化処理試験の前に校正ガスを用いて較正。 - 液体試料を収集し、次の手順を使用して、6時間ごとに:、窒素でサンプリングトラップをパージ、収集バイアルに液体試料を排出、サンプリングトラップの圧力を低下させる、バイパストラップにサンプリングトラップを切り替える窒素でサンプリングトラップを加圧し、サンプリングトラップへの製品の流れをリダイレクトします。所望の方向でのガスや製品をそらす二次元及び三方弁のシリーズを操作します。
注:反応物が触媒床を通過した後、液体生成物および未反応の液体が気液分離装置中のガス状生成物および未反応ガスから分離されます。高温ガスは、反応器システムの並列下流に配置された2つの加圧、冷却された、液体/ガス冷却トラップ(サンプルトラップまたはバイパストラップ)の1を通過します。オフガスは、次いで、圧力がatmospに低減される背圧調整器を通過しますheric圧力。オフガスは、次いで、流量を測定するガスメータを通過します。 - ストリーム上で60時間、試験を行う(オンストリーム時間[TOS])。バイオオイル供給を停止することによって、テストを終了します。 100ml /分、100℃、水素流量に反応器温度を設定します。
注:テストは50から数百時間に及ぶトスのために動作させることができました。
- 152ミリリットル/分に水素流量を調整し、10.3 MPaでのシステム圧力を維持します。それぞれ、220および400℃にステージIの触媒床とステージII触媒床の温度を設定します。
- 後の試験手順
- バイオオイルを供給するための供給ポンプをきれいにするために、アセトンを使用してください。アセトンで洗浄供給ポンプをロードします。
- 触媒床の温度は100℃であるときに10〜40 ml /分および100ml /分の水素流量のアセトン流速で約400 mlのアセトンで触媒床をパージします。
- 原子炉のヒーターの電源を切り、周囲圧力にシステムを減圧し、少なくとも24時間、反応器を窒素でパージします。
- システムから原子炉を取り外し、reactoから過ごした触媒を除去しますrを。
- 製品の処理および結果分析
- 液体製品の処理のために、二相を分離し、個別に秤量します。液体製品は、2つのフェーズ、軽油相(石油製品)と重い水相(水性生成物)で、通常です。
- 石油製品の以下の分析行う:密度測定を、含水量のためにカールフィッシャー滴定。炭素、水素、窒素、酸素、および硫黄元素分析(D5291 / D5373、D5373mod、およびD1552 / D4239)。全酸価のためのセミミクロ色表示滴定(D3339);無機コンテンツの誘導結合プラズマ発光分光法;模擬蒸留(ASTMのD2887)は、ガソリン、ディーゼル、ジェット燃料、残留範囲で燃料生成物の相対量を評価します。炭素、水素、窒素詐欺のための水分含有量および元素分析のためのカールフィッシャー滴定(D5291 / D5373):水性製品の次の分析を行います10トン15。
- 生成油製品、水性製品、およびガス状生成物の収率を計算します。水素消費量。入口反応体流量及び密度、入口水素流量、出口油製品重量、出口油製品の含水量、出口水性製品重量、排出ガス流量、及び出口ガス組成に基づいて、物質収支。
- 誘導結合プラズマ発光分光法15によって使用済み触媒を分析します。
- 熱分解反応器を組み立てます。
Representative Results
代表的な草本系バイオマスの急速熱分解は、スイッチグラス、またはホット蒸気濾過および製品のバイオ油の接触水素化処理することなく、ここで報告されたプロセスのための例として使用されています。これらの実験の詳細は、当社の最近の刊行物に詳細に記載されています。 15
高温蒸気濾過高速熱分解
表1は、典型的な草本原料用のホット蒸気フィルタととせずに製造バイオオイル、チャー、及びガス収率を示しています。ホット蒸気ろ過なしの対照実験のために、蒸気がフィルタハウジングかかわらず渡されたが、フィルタがインストールされていません。これは、二つの実験で同じ滞留時間を保つように、任意の違いは、フィルタのみによるものです。バイオオイルの収量は、液体インターメディアへのバイオマスの大部分の正常な変換を示し、56%〜52%でしたTE油。代表的なバイオオイルのサンプルの写真を図4に示されています。マスバランスの閉鎖は、90%、86%でした。適切に凝縮電車の中で収集されなかった光の蒸気は質量損失の一つのソースでした。熱分解油は凝縮することが困難であるようなヒドロキシアセトアルデヒド(沸点20.2℃)などのいくつかの低沸点化合物を含有します。第2のドライアイストラップを追加すると、光凝縮化合物の回収を改善します。ここで報告さよりも高いバイオマス供給速度で実験を実施する前に凝縮する蒸気濃度を増加させることによって光蒸気の回収を改善します。光凝縮性化合物の脱出は、出口ガスのガスクロマトグラフィー - 質量分光分析によって確認することができます。物質収支が原因比較的大量にスイッチグラスから製造した逃げる光のchar、の可能性が高い、草本原料には比較的低かったです。分解反応がでそうフィルターで発生しますホット蒸気フィルタのclusionは、油の収量を減少させ、ガスの収量を増加させました。
表2と5及び図 6は、草本原料の分析結果と生産バイオオイルを示します。熱い蒸気フィルタは、検出限界以下の1.45%から、バイオ油中の灰残留物を減少させました。アルミニウム、カルシウム、鉄、カリウム、マグネシウム、ナトリウム、リン、及びケイ素などの種々の無機物は、バイオ油で観察され、それらは主にバイオマス原料に由来します。ホット蒸気フィルタリングはかなり熱い蒸気のフィルタリングを効果的にchar型と灰粒子を除去することにより、バイオ油中の微量元素の含有量を減少させるための強力なプロトコルであったことを示し、バイオオイル中の無機内容を減少させました。熱い蒸気フィルタリングはまた、炭素含有量が減少し、バイオ油中の酸素含有量を増加させました。木質原料はと比較して低い灰分含量を有します草本原料、およびバイオオイルの灰で低い削減と無機内容が観察されます。 15
バイオ油の水素化処理触媒
生成バイオオイルの分析結果は、そのようなプロセスから製造されたバイオ油は、内燃エンジンで直接使用するのに十分な品質ではないという事実と一致していました。したがって、バイオ油のアップグレードが必要となります。 2バイオオイルのサンプルは、上述の条件下での水素化処理システムにおける触媒水素化処理することによりアップグレードされました。
バイオ油は、生物油中の活性種の文字または重合生成物が触媒床に蓄積するように水素化処理反応器を接続することが知られています。したがって、水素化処理試験中の触媒床を横切る圧力降下は、文字または重合生成物を蓄積する重要な指標です。ホット蒸気フィルタリングBIO-油は水素化処理試験において、60時間TOSのために、ほぼ完璧に動作しました。しかしながら、非濾過バイオオイルポンプで分離し、処理しなかった約5重量%の未溶解固形分を有していました。でもこれらの未処理の固体と、充填された触媒床を差し込むTOS、おそらく非フィルタリングバイオオイル中の残留固形物の50時間後の圧力損失の蓄積はまだありました。
表3および4と5と7のリストに別のトスでのバイオオイルの水素化処理のための製品の歩留まりを図 。 CH 4を含むアップグレード油相と水相とを含む相分離された液体生成物、およびガス状生成物、C 2 H 6、C 3 H 8、C 4 H 10、CO、及びCO 2を製造しました。 図4は、修復、アップグレード油試料の写真を示しています。 表5アップグレードされた油の分析結果を示し、 図5は、バイオオイル、アップグレード油の元素分析結果を比較します。水素化処理は、酸素、硫黄、および窒素を低減し、バイオ油原料から著しく水素を添加することで非常に有効でした。アップグレードされた油中の酸素含有量は約2.0バイオ油原料中の酸素の35〜40重量%よりも有意に低かった重量%でした。アップグレードされた油の水素対炭素比は、バイオ油原料のための〜1.3に比べて、約1.7でした。テストの期間にわたって0.81から0.83グラム/ mlに増加したアップグレード油の密度の傾向は、60時間のTOSにわたる穏やかな触媒の不活性化を示唆しています。
図7に示すように、高温蒸気濾過および非濾過バイオオイルとの間の水素化処理生成物の比較は、バイオオイルろ過熱蒸気はconsiでわずかに高い水対アップグレード油比をもたらすことが示されましたホット蒸気フィルタリングバイオ油原料で高い酸素含有量を有するステント。 2つの生理油のアップグレードされた油の特性は非常に類似していました。ホット蒸気濾過し、非フィルタリングバイオオイルの水素化処理の大きな違いは、高温蒸気ろ過バイオオイルの使用の触媒床が非濾過し使用する触媒床に比べ無機物のはるかに少ない堆積を示したことでしたバイオオイル。

5cmの流動層熱分解反応器システムのための図1の回路図。熱い蒸気フィルタ、凝縮装置、及びガス測定システムがあります。 この図の拡大版をご覧になるにはこちらをクリックしてください。


ミニ水素化処理反応器内の触媒床の図3の回路図。触媒床の温度プロファイルは、左側に示され、各段の触媒の位置は右側に示されています。 この図の拡大版をご覧になるにはこちらをクリックしてください。
S / ftp_upload / 54088 / 54088fig4.jpg "/>
図代表的なバイオオイルサンプル(左)と代表的なアップグレードされた油試料の4写真(右)。 この図の拡大版をご覧になるにはこちらをクリックしてください。

草本原料(スイッチグラス)の元素分析結果の図5の比較、ホット蒸気ろ過を用いて製造バイオオイル、およびアップグレードされた油。炭素、水素、及び酸素含有量は、バイオマスの速い熱分解後にあまり変化しなかった、しかし、酸素含有量が大幅に減少し、水素含有量は、バイオ油の水素化処理の後に増加しました。 この図の拡大版をご覧になるにはこちらをクリックしてください。
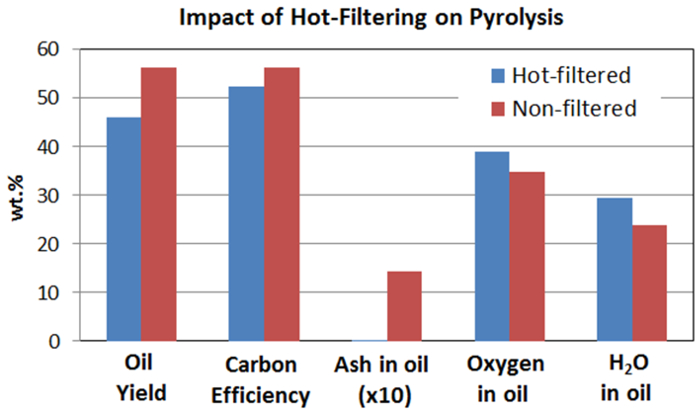
油収量、炭素効率、およびホット蒸気濾過し、非フィルタリング熱分解からのバイオオイルのいくつかのプロパティの図6の比較。これは、従来凝縮熱分解蒸気の高温ガスろ過の影響を示しています。高温ガスろ過、無機残渣を排除するが、それはまた、熱分解油の収率[3-LM]、オイル酸素含有量などの油特性に影響を与えます。 この図の拡大版をご覧になるにはこちらをクリックしてください。

ホット蒸気濾過し、非フィルタリング熱分解からバイオ油の水素化処理結果の図7の比較。ホット蒸気フィルタリングバイオオイルは、わずかに高い水対につながります燃料比と2バイオ油のアップグレード燃料の特性は非常に類似しています。 2熱分解油の水素化処理の大きな違いは、バイオオイル高温蒸気ろ過の触媒床は、ミネラルのはるかに少ない堆積を示したことです。 この図の拡大版をご覧になるにはこちらをクリックしてください。

ホット蒸気ろ過とない表1主要な熱分解生成物の収率(バイオオイル、チャー、およびガス)と草本原料(スイッチグラス)の熱分解のためのマスバランスの閉鎖を。

ホット蒸気ろ過ととせずに製造代表草本原料(スイッチグラス)の表2分析とバイオオイル。
088table3.jpg "/>
ホット蒸気濾過し、非フィルタリング代表バイオオイルのための別のトスでの主要な水素化処理製品の表3収量。

表4は、代表的なバイオ油の水素化処理時のガス組成をプロデュース。

代表的なバイオ油の水素化処理からアップグレードされた石油製品の表5.分析。
Discussion
本稿では、高速熱分解し、触媒水素化処理を介して燃料範囲の炭化水素をリグノセルロース系バイオマスを変換するための詳細な手順を説明しました。 5cmの内径流動床反応器および1.3 cmの内径固定床触媒反応器およびその操作手順とPNNLの水素化処理システムとNREL熱分解反応器システムについて詳細に説明します。これらの反応器システムは、効率的かつ安全な方法で熱分解及び水素化処理試験を行うために使用することができます。我々は、のように2 O 3硫化のRu / CとのCoMo / Alを含む熱分解反応器システム内の液体バイオオイルを生成するための代表的な草本原料を使用し、その後、バイオ油は二段階触媒床を有する水素化処理システムで処理しました。燃料範囲液体炭化水素を生成する触媒。プロセスはまた、木、草、およびトウモロコシ茎葉などのバイオマス原料の広い範囲の熱分解に適用され、その後、生産のアップグレードバイオオイルは、バイオ燃料を生成します。 16水素化処理および水素化プロセスはまた、木材や藻類などのバイオマスから、このような液化油(バイオ、粗)のような他のバイオマス生成された中間体をアップグレードするために使用することができます。
熱分解の間にバイオ油の収率を最大にすることは、バイオマスの最大の揮発を達成するのに十分な温度に急速にバイオマスを加熱することが必要です。ほとんどのバイオマスの場合、これは500〜600℃の温度を意味します。流動床は、高い加熱速度を提供し、バイオマスの砂からの迅速な熱伝達を提供します。小粒子の使用は、より高い加熱速度を提供します。典型的には数パーセント高いバイオオイルの収率は<2ミリメートルにバイオマス地面と比べて0.5ミリメートル<にバイオマスグラウンドで達成されます。最大化収率は、また、低温(1~2秒)での滞留時間を維持することによって蒸気の熱分解を最小限に抑えることを意味します。熱分解蒸気の沸点の広い範囲の化合物を含みます。このように、時間OT配管は、液体、再重合蒸気とチャーと汚れになる傾向があります。この状況を回避するために、100℃以下のオーガ温度及びファウリングを避けるために400℃以上の反応器と凝縮列車間の全ての表面を維持するが、500℃以下で熱分解を最小限にすること。加熱テープで完全なカバレッジは、コールドスポットを防止し、均一な温度を提供することが必要です。それらの上にクロージャとカットソー絶縁パッドは、一般的に、それによって、より均一な温度が得られ、より均一なカバレッジを提供します。温度が凝縮器入口の閉塞につながる可能性高沸点物質の再重合の機会を最小限に抑えるために、第1凝縮器で急速に低下することが重要です。また、液体回収を最大にし、ガス測定および分析機器への損傷を防止するために、第2の凝縮器にドライアイスを使用することが必要です。
いくつかの拡張機能は、基本的な高速熱分解の手順で言及されていませんでした。私tは反応器入口付近の圧力計または送信機を有することが有用です。また、反応器サイクロンの前後差圧を測定し、(正確な量の計算を可能にするために)乾燥試験メーターで最終圧力と温度を測定するのに有用です。また、床は均一な温度を提供するために均一に十分に流動化されていることを確認するために、熱分解ベッドで追加の熱電対を持っていると便利です。典型的には、<5℃の広がりは、床を通って垂直に見られます。また、原子炉にネストされたループ温度制御を有することが有用です。油のより大きな量が必要とされている場合、順番に緩く、それに取り付けられた瓶と下部のバルブを有し、char型の受信機の底部にバルブを設置し、その下の二次char型の受信機をマウントすると便利です。これは、連続運転を長時間維持することができるように、二次受信し、最終的にダウンジャーに内チャー受信機を空にすることができます。振動が助けです動作にFUL。パイプの手動ドキドキを使用することができるが、自動振動をより確実に攪拌を提供します。これらは、フィーダを介して円滑な供給流を維持するために、ロックホッパーおよびオーガポートに連続的に動作させることができます。また、char型の排水中の二次char型の受信機に自動バイブレータを使用すると、その操作ははるかに信頼性の高いことができます。ホット蒸気濾過は割れ向上し、上記のようにバイオオイルの収量を減少させます。 (> 400℃)、低フィルタの温度を維持するが、それでも凝縮温度以上にすると、割れ最小限に抑えることができます。フィルター上の不活性表面も割れ減少させることができます。フィルタ領域は、圧力降下を減少させるために大きくする必要があります。
高速熱分解プロセスの主な制限は、生産バイオオイルは、その直接の利用を制限し、DURいくつかの問題が発生し、高粘度、腐食性、貧しい揮発性、低発熱量、および化学的不安定性、などいくつかの主要な問題の性質を有することです彼らのアップグレードをる。 6,7,8,9高速熱分解は、H 2等の反応性ガスの存在下で行う、請求急速熱分解、触媒急速熱分解、高速熱分解は熱分解蒸気をアップグレードする触媒プロセスと統合され、かつhydropyrolysis、の変異体、高品質のバイオオイルにつながるが、より高い運用の複雑さと低い製品歩留まりを受けることができます。 4,8
二段階触媒水素化は、燃料範囲の炭化水素へのバイオオイルを変換するための良好な加工結果を示しました。バイオ油は、炭素質材料およびその結果として触媒の失活を形成し、偶数の目詰まりのために高い傾向をもたらすので、このような低温で再重合および縮合を受けることができ、カルボニル及びフェノール化合物などの活性種の存在下で化学的に不安定であることが知られています触媒床。したがって、第1段階の水素化工程は、プロセスのために重要であり、BIを安定化するために使用しました。適切な水素化触媒を用いて比較的低い温度でカルボニル及びフェノールの水素化により、O-オイル。水素化触媒の性能は、プロセスの長期安定性と操作性の鍵でした。水素化脱酸素による酸素の除去は、硫化物系水素化処理触媒により、第2段階で起こりました。製造された最終油生成物の収率及び特性は、第二段階で使用される触媒および条件に依存します。液体の最終燃料の収率を最大にするようなアルキル化関数としてのC-C結合、反応温度、圧力及び空間速度などの最適化された反応パラメータを生成することができる触媒を使用することによって達成することができます。水素化処理方法の主な制限は、ため、このような化学的不安定性と汚染物質17の存在、水素化処理触媒の寿命、特に最初のステップの水素化触媒としてのバイオオイルでいくつかの問題の性質のため、まだ制限されている、ということです全体のプロセスは高価になり編、。より堅牢な触媒を使用することによって達成することができる使用される触媒の寿命を最大化します。反応温度、圧力及び空間速度などの最適化された反応パラメーター。またはバイオオイルフィードに活性種または汚染物質の含有量を低下させるために前処理。
水素化処理は、関係する可燃性ガスと液体と高い圧力及び反応器温度で操作しました。したがって、安全規則や手順が厳密に従うべきです。
Disclosures
著者は、彼らが競合する金融利害関係を持たないことを宣言します。
Acknowledgments
この作品は、NRELとPNNLで契約DE-AC05-76RL01830で契約DE-AC36-08-GO28308の下で米国エネルギー省(DOE)によってサポートされていました。作者は感謝してDOEのバイオエネルギー技術のOfficeのサポートを認めます。
Materials
| Name | Company | Catalog Number | Comments |
| Pyrolysis system | |||
| Feedstock | Mill to pass 2 mm screen | ||
| Sand for bed material | Black Rock | Screen to 300-500 microns | |
| Furnace | Thermcraft | TSP-3.75-0-24-3C-J13667/1A | Split tube furnace 3.75 ID X 24 L |
| Pyrolysis reactor | Custom-built at NREL | 2" diameter, height 17", dual staggered plate distributor, 316SS, Auger port is 2.5 cm above distributor and is cooled with air or water, there is a coiled 1/4" 304 SS tube below the distributor to pre-heat the gas | |
| Cyclone | Custom-built at NREL | 1" diameter | |
| Cyclone receiver | Custom-built at NREL | 1 L capacity | |
| Cyclone secondary receiver | Custom-built at NREL | 1 L capacity | |
| Hot vapor filter | Serv-A-Pure | SC2-0P10B34-X | 316SS, 10 inches long, 2.0 micron |
| 2-neck round-bottomed flasks | 500 ml | ||
| Electrostatic precipitator | Allen Scientific Glassware, NREL-built electrodes | Custom built | 2" diameter 10" long ground electrode, glass enclosed, stop-cock on bottom |
| High-voltage power supply | Spellman High Voltage | Bertan 803C-300P | 30 kV max, 0.5 mA |
| Cold-finger condenser | Aldrich | Z164038 | |
| Coalescing filter | Finite | 10C15-060 | |
| Dry test meter | American Meter | DTM-200A | with IMAC counter |
| Gas chromatograph | Varian | CP-4900 | MS5A, PBQ, CP-Sil columns |
| Hydrogen detector | Gerhard Wagner | TCM-4 | thermal conductivity detector |
| Non-Dispersive Infrared Spectrometer | California Analytical | Model 300 | Carbon monoxide 0-5%, 0-25%, carbon dioxide 0-5%, 0-20%, methane 0-5,000 ppmv, 0-3% |
| Mass flow controller | Celerity (now Tylan) | Unit 7301 | 0-20 SLM reactor bottom, 0-10 SLM auger, 0-2 slm purges, 0-5 slm air |
| Auger | Auger Manufacturing Specialists | 110520 | 3/8" Dia SS RH Auger 18" |
| Motor for Auger | Leeson | Gearmotor-Parallel Shaft, 94 rpm, 1/15 HP, TEFC, 115 VAC | |
| Feeding system: Motor for hopper | Lenze | VDE0530 | 7KB4-7-100H Motor Ac Helical Gearbox 3PH 0.25 kW 1.4/0.82 A |
| Feeding system: Hopper and Loss in weight feeder | K-TRON Soder | KCL24T20 | with K10S controller |
| Feeding system: Valves | Swagelok | SS-65TS16 | 151 bar at 37 °C and 6.8 bar at 232 °C |
| Control system | Opto22 | SNAP-PAC parts | |
| Heat cables | McMaster-Carr | 4550T152 and similar | Extreme-Temperature (1,400 °F), heavy insulation for use on metal |
| Ball Vibrator | Vibtec | K 8 | |
| U-tube | Custom-built at NREL | 1/4" PFA and stainless steel tubing, 1.4 m tall | |
| Hydrotreating system | |||
| Ru on carbon catalyst | Fabricated at PNNL | 7.6 wt% Ru on carbon | |
| 3% Co and 9% Mo on Al2O3 catalyst | Alfa-Aesar | 45579 | Cobalt oxide, typically 3.4-4.5%, Molybdenum oxide typically 11.5-14.5% on alumina |
| Feeding pumps | ISCO | 500D | Syringe pump, 500 ml cylinder capacity |
| Mass flow controller | Brooks | SLA5850S1BAF4B1A1 | |
| Temperatrue controller | Cole-Parmer | WU-89000-10 | Digi-Sense Advanced Temperature Controller, 115 V |
| Thermocouples | Omega | K-type thermocouples | |
| Pressure transducer | Omega | PX309-3KG5V | |
| Heat tapes | Cole-Parmer | EW-03106-27 | Dual element heating tape, 1/2 in x 12 ft, 936 watts, 120 VAC w/ 2-prong plug |
| Digital pressure gauge | Omega | DPG4000-3K | High Accuracy Digital Pressure Gauge, with Data Logging Capability |
| Back pressure regulator | Mity-Mite | ||
| Gas flow meter | Mesa Labs | 200-220L | Dry Cal, Definer 220 Low Flow |
| Hydrotreating reactor, cross, tee, fittings | Parker, Autoclave | ||
| Combustible gas sensor | SMC | 5100-02-IT-S1-01-00-0-0 | Combustible gas detection sensor, 24 VDC power, analog 4-20 MADC output with modbus, no relays |
| H2S sensor | SMC | 5100-05-IT-S1-01-00-0-0 | H2S toxic gas sensor module, 24 VDC power, analog 4-20 MADC output with modbus, no relays |
| Ventilation sensor | TSI | FHM10 | Fume Hood Monitor FHM10 |
| Micro-Gas chromatograph | Inficon | Inficon 3000 | Four-channel micro-GC with molecular sieve, Plot U, Alumina, and Stabilwax columns |
| Lab-view based monitering and controlling system | Custom-built at PNNL | Using National Instruments parts and Labview software |
References
- BP. Statistical Review of World Energy. , http://www.bp.com/content/dam/bp/pdf/Energy-economics/statistical-review-2014/BP-statistical-review-of-world-energy-2014-full-report.pdf. (2014).
- U.S. Energy Information Administration. International Energy Outlook 2014. , http://www.eia.gov/forecasts/ieo/pdf/0484%282014%29.pdf (2014).
- Bioenergy Technologies Office. Replacing the Whole Barrel. , http://www1.eere.energy.gov/bioenergy/pdfs/replacing_barrel_overview.pdf. (2013).
- Huber, G. W., Iborra, S., Corma, A. Synthesis of transportation fuels from biomass: Chemistry, catalysts, and engineering. Chem. Rev. 106 (9), 4044-4098 (2006).
- Mohan, D., Pittman, C. U. J., Steele, P. H. Pyrolysis of wood/biomass for bio-oil: A critical review. Energy Fuels. 20 (3), 848-889 (2006).
- Bridgewater, A. V. Review of fast pyrolysis of biomass and product upgrading. Biomass Bioenergy. 29, 68-94 (2012).
- Elliott, D. C. Historical developments in hydroprocessing bio-oils. Energy Fuels. 21 (3), 1792-1815 (2007).
- Wang, H., Male, J., Wang, Y. Recent advances in hydrotreating of pyrolysis bio-oil and its oxygen-containing model compounds. ACS Catal. 3 (5), 1047-1070 (2013).
- Zacher, A. H., Olarte, M. V., Santosa, D. M., Elliott, D. C., Jones, S. B. A review and perspective of recent bio-oil hydrotreating research. Green Chem. 16, 491-515 (2014).
- Elliott, D. C., et al. Catalytic Hydroprocessing of Fast pyrolysis bio-oil from pine sawdust. Energy Fuels. 26 (6), 3891-3896 (2012).
- Venderbosch, R. H., Ardiyanti, A. R., Wildschut, J., Oasmaa, A., Heeresb, H. J. J. Stabilization of biomass-derived pyrolysis oils. Chem. Technol. Biotechnol. 85 (5), 674-686 (2010).
- Olarte, M. V., et al. Towards long-term fast pyrolysis oil catalytic upgrading. Prepr. Pap. Am. Chem. Soc., Div. Fuel Chem. 58 (2), 230-231 (2013).
- Scahill, J., Diebold, J. P., Feik, C. Removal of residual char fines from pyrolysis vapors by hot gas filtration. Developments in Thermochemical Biomass. Bridgwater, A. V., Boocock, D. G. B. , Blackie Academic and Professional. London, U.K. (1996).
- Hoekstra, E., Hogendoorn, K. J. A., Wang, X., Westerhof, R. J. M., Kersten, S. R. A., van Swaaij, W. P. M. Fast pyrolysis of biomass in a fluidized bed reactor: In situ filtering of the vapors. Ind. Eng. Chem. Res. 48 (10), 4744-4756 (2009).
- Elliott, D. C., Wang, H., French, R., Deutch, S., Iisa, K. Hydrocarbon liquid production from biomass via hot-vapor-filtered fast pyrolysis and catalytic hydroprocessing of the bio-oil. Energy Fuels. 28 (9), 5909-5917 (2014).
- Howe, D., et al. Field-to-Fuel Performance Testing of Lignocellulosic Feedstocks: An Integrated Study of the Fast Pyrolysis/Hydrotreating Pathway. Energy Fuels. 29 (5), 3188-3197 (2015).
- Wang, H., Wang, Y. Characterization of Deactivated Bio-oil Hydrotreating Catalysts. Topics in Catalysis. 59, 65-72 (2015).



