Summary
ここでは、従来のタバコの煙、電子たばこエアロゾルの抽出物を作成するためのプログラマブル試験装置について述べる。このメソッドは、従来のタバコと電子タバコの間の直接比較を行うための便利なツールを提供し、電子タバコ研究へアクセスできるエントリ ポイントです。
Abstract
電子タバコ中、高校生の間で最も人気のあるタバコ製品、大人の間で最も人気のある代替タバコ製品。高品質の電子タバコの使用の結果に再現性のある研究は公衆衛生の懸念を新興国や証拠をクラフト基づく規制政策の理解に不可欠です。論文数の成長は、電子タバコを議論しながら少し一貫性にあるメソッド グループ、結果にほとんどコンセンサス。ここでは、従来のタバコの煙、電子たばこエアロゾルの抽出物を作成するためのプログラマブル試験装置について述べる。このプロトコルのアセンブリおよび当該装置の操作のための指示の詳細し、2 つのサンプル アプリケーションで生成された抽出物の使用方法を示します:体外セル実行可能性の試金およびガスクロマトグラフィー質量分析法。このメソッドは、従来のタバコと電子タバコの間の直接比較を行うためのツールを提供し、電子タバコ研究へアクセスできるエントリ ポイントです。
Introduction
医療機関での集中的な努力にもかかわらずタバコ製品の使用タバコ喫煙1に帰因するこれらの死の大半の世界、予防可能な死の主要な原因のまま。2003 年に市場に入り、電子タバコは、タバコ製品のユーザーの間で人気の高まっています。現在、電子タバコはアメリカ大人 (~ 5%)2の間で慣習的なタバコ ・中間 (〜 5.3%) と高校生 (~ 16%)3の中で最も人気のあるニコチン配信システムに最も普及した代わりであります。現在の傾向が続けば場合、は、将来の世代のための慣習的なタバコを交換する電子タバコを期待できます。しかし、電子タバコの使用の健康への影響は不明します。
電子タバコの人気が増加 2013年3,4まで電子タバコに関する研究が本格的に開始されませんでした。それ以来、異なるモデルの数は、彼らの毒性の問題に対処するため採用されています。しかし、多くの研究結果が競合していると、電子タバコは、一般的にある慣習的なタバコより毒性が少ないと思える電子タバコの健康影響に関する現在のコンセンサスは5,を使わない6,7. 私たちの以前の研究は、電子タバコが大幅 DNA 損傷と酸化ストレスと細胞死8 の誘導を引き起こす能力にもかかわらず、従来のタバコよりも血管の内皮細胞に毒性を示します.しかしより多くの研究は、電子タバコの使用の健康への影響についての確固たる結論を描くことができます前に必要です。
慣習的なタバコは予防血管疾患9の主要な原因であるとは、電子タバコの血管の健康リスクの関心の高まりは、10、11,12を使用しています。電子タバコの血管系に及ぼす影響を研究するために私たちの研究室は8の作動マイコン喫煙/vaping デバイス (図 1) を開発しました。このデバイスは、水溶液や有機溶剤のいずれか従来のタバコの煙や電子タバコ エアロゾルの液体抽出物の生成が可能です。調節可能なレギュレーター フローと PBASIC タイミングのプログラムの組み合わせによる空気の流れを制御、デバイスが任意の数のユーザー定義のプロトコルによるとエキスを生成するのに使用できます。ここではアセンブリ、2 つの潜在的なアプリケーションと同様に、このデバイスの操作詳細:体外細胞生存率評価とガスクロマトグラフィー質量分析法。
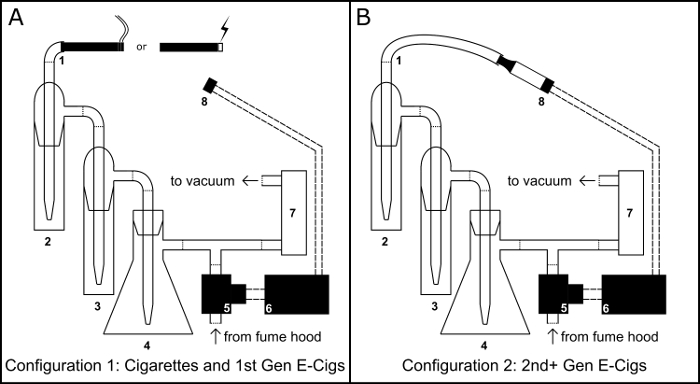
図 1: 喫煙/Vaping デバイス。たばこ/たばこ電子タバコ (電子セエグ) 構成 (A) のようなタンク電子タバコ構成 (B) で喫煙/vaping デバイスの物理的な組み立ての模式図。コンポーネント キー: 1) 吸入ポート;2) プライマリ コレクション インピン;3) オーバーフロー インピン;4) Buchner フラスコ真空トラップ5) 通常開電磁弁;6) BS1 マイクロ コント ローラー;7) 空気流量制御;8) 510 電子タバコ戦車ベースのスレッド。この図の拡大版を表示するのにはここをクリックしてください。
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. デバイスの組立
- Buchner フラスコ (図 1#4) 鋼のリングに立つし、乾燥剤として塩化カルシウムの 50 g でそれを充填して真空トラップを作成 100 mL を保護します。ゴム貫通穴栓付けフラスコを密封、パラフィン フィルムとストッパーの接合部をラップし、スルーホール ピペットを実行します。
- ビニール チューブを使用すると、t 字路のホース コネクタ ストッパーから延びるピペットを接続します。
- ビニール チューブを使用すると、互いに 2 つインピン (図 1#2 & #3) を接続し、2 番目のインピンの出力を t 字のホース コネクタに接続します。
- ビニール チューブを使用して、吸入ポート (図 1#1) として最初のインピンの入力ポートに接続します。
- ビニール チューブを使用して空気レギュレータ (図 1#7) の入力ポートに Buchner フラスコのサイドアームを接続し、真空ポンプに空気レギュレータの出口ポート。
- 図 2 aの回路図によると回路を組み立てます。
- シリアル アダプターと製造元のソフトウェアを使って BS1 マイクロ コント ローラー (図 1#6) に PBASIC プログラム SVL.bs1 (図 2 b、また https://github.com/ChastainAnderson/SVL で入手可能) をアップロードします。
- リングの場所、510 スレッド ベース (図 1 #8) スタンド クランプです。
- ビニール チューブを使用すると、t 字路のホース コネクタの自由端にソレノイド バルブ (図 1#5) に接続します。
注: デバイスする必要があります完全な操作の準備ができて、タイトな空気が、ホースク ランプおよび必要に応じて真空グリースを適用ことを確認するすべての関節をチェックします。

図 2: 電気回路図と PBASIC コード。図 2 aは両方通常開電磁弁をアクティブ化に必要な電気回路を組み立てるための電気回路図を表示し、ボタンの加熱コイルは、電子タバコを活性化 (、510 をスレッド電子タバコ タンク基本)。加熱コイル (p: 電源の電気的パラメーターR: 抵抗;i: 電流) 投影され、デジタルマルチメータ ポスト アセンブリを実証する必要があります。図 2 bには、図 2 a (https://github.com/ChastainAnderson/SVL も入手可能) に回路を制御するために必要な PBASIC タイミングのプログラムが表示されます。SVT ・ IPT (#5 & #6) タイミング定数は、ms の単位と活性化時間は 2 秒と 28 のダウンタイムを提供するために設定されて s.この図の拡大版を表示するのにはここをクリックしてください。
2. サンプルの調製及び保存
- 室温で気密のポリ袋で暗闇の中ですべて未開封従来と電子タバコのサンプルを格納します。
- 開くと、余分な水分を吸収する紙タオルで 4 ° C で、気密のポリ袋でサンプルを格納します。
- 前 ~ 60% 湿度室温ヒュミドールのすべてのサンプルを平衡させ、使用前に少なくとも 30 分間。
3. 一般的なタバコ煙/電子タバコ エアロゾル抽出装置の操作
- 各電子タバコ cartomizer/タンク前-vaping 分析用天秤を使用して量を決定します。プレ/ポスト ポスト vaping 重量の差は、適切な投与量を決定する使用されます。
注: 3R4F 参照タバコは、ニコチン 0.7 mg 含まれていると見なされます、商業たばこブランドのニコチン含有量は、従来の分析法13によって定めることが。 - サンプル アプリケーション 1 の血管内皮細胞培養培地の 4.3 ml プライマリ インピンの貯水池を入力します。サンプル アプリケーション 2、アセトン 5 mL でタンクを埋めます。
-
電子タバコや抽出のためタバコの従来を準備します。
- 従来のタバコを使用して、フィルター周りにクリアのテープの一部を適用、シガレット ペーパーがフィルターを結合容易に目に見える印を置きます。
- 電子タバコのようなタバコを使用している場合も充電がバッテリーに堅くねじで締まる、cartomizer いることを確認します。
- 電子タバコ タンクを使用する場合は、電子タバコの液体の適切な量がタンクに読み込まれているかどうかを確認し、510 スレッド ベースの上にタンクのネジします。
- 吸入ポート (図 1#1) に従来または電子タバコの先端を挿入し、ホースをクランプで固定します。
- 真空ポンプをオンにします。
- プル 1.65 リットル/分 55 mL パフ 2 秒以上を確保するためにフロー メーターを調整します。
- マイクロ コント ローラーをオンにします。従来のタバコを使用している場合は、最初のパフにタバコを点灯します。
- 投影まで実行希望濃度 (百万または % 単位で重量/体積) を実現します。
-
分析用天秤を使用して蒸発後各電子タバコ cartomizer/タンクの質量を決定します。この測定測定は、大量消費の合計を決定するステップ 3.1 の撮影に比較します。溶剤量/消費質量濃度を計算します。製品間の正規化に消費されるニコチンのモル濃度を使用します。
- 十分な質量が消費された場合は、デバイスに電子タバコを返すし、さらに消費します。
- 十分なまたは余分な固まりが消費された場合は進みます。
4. ろ過とストレージ
- エキスの細胞培養に使用する場合は、0.22 μ m ペス シリンジ フィルターを介してフィルターします。
- すぐに抽出物を使用または-80 ° C で保存します。アンダーソン、他のための準備の一部として8、電子タバコ エアロゾルを示した、少なくとも 2 週間安定である、タバコの煙まで 2 年間の安定性は、詐欺師、らによって確立されています。13。
5. デバイスのクリーニング
- それぞれの抽出後チューブを洗い、70% エタノールと脱イオン水を防ぐためにデバイスの貯水池がサンプル間引き継ぐ。
- 次の洗浄、簡単にラインの乾燥を支援するために気流を許可する空のデバイスを実行します。
6. サンプル アプリケーション 1: 中性赤の取り込みセル実行可能性の試金
- 内皮細胞成長培地の 4.3 mL に上記のように抽出を実行します。
- 1 日前、1 x 10 の4セル/好演内皮細胞成長培地の 100 μ L の密度の 96 ウェル プレートにひと臍帯静脈内皮細胞をシードします。
- コントロールとして機能する新鮮な内皮細胞培地のいずれかの 100 μ L または 75 μ L 消費 2 mM ニコチン濃度エキス (1.4 mg を 25 μ l 添加混合内皮細胞成長培地の古い血管内皮細胞の培養液に置き換えてセルを扱う4.3 mL 内皮細胞成長培地にニコチンを消費) 治療として 500 μ M の最終的な集中に。
- 両方のタバコの煙、電子たばこエアロゾルのコンポーネントの多くは揮発性、井戸の気密を保つために箔シールを使用します。
- インキュベート プレート 18-24 h 37 ° C および 5% の CO2。
-
ニュートラルレッド染色液を準備します。
- バッファー内の塩溶液 10 mL に中立赤の染料 33 mg を溶解して 100 x 中性赤ストック溶液を作成します。
- 直前の使用、ニュートラルレッド染色液 x 1 を作成する細胞培養液の原液を 1: 100 x 100 を希釈します。
- ニュートラルレッド染色の使用、および使用する前に、少なくとも 30 分の 37 ° C で液をすぐに孵化させなさい。
メモ: それは潜伏時に析出する結晶の正常です。細胞文化の井戸にこれらの結晶を適用しないようにするには、注意が必要です。必要な場合は、中立赤在庫および染色ソリューションをフィルター処理する.22 μ m フィルターを使用できます。
- 抽出を削除し、ニュートラルレッド染色液適切な定量化のための少なくとも 3 つの空井戸を作成するまあ、超過分の使用あたりの 100 μ L を追加します。
- 37 ° C、5% CO2で 2-4 h でプレートを孵化させなさい。
- ニュートラルレッド染色液を削除し、PBS の水没で 3 x を洗ってください。
- 中立的な赤を適用解除ソリューション (50% 脱イオン水、49% エタノール, 1% 酢酸) を染色します。
- 揺れで部屋の温度で、少なくとも 10 分間、インキュベートします。
- 540 で吸光度を読み nm。
- データを分析するには、空白の井戸の平均値を引き算すること、空白の調整コントロールよく価値の平均を正規化します。
7. サンプル アプリケーション 2: ガスクロマトグラフィー質量分析法
- 上記としてアセトン 5 mL に抽出を実行します。
- 1 ~ 100 の部品の最終的な集中を達成するためにデバイスを実行百万 (e-液体消費/アセトンの量量の重量) サンプルの。
- 高精度ガラス製注射器を使用すると、1 μ L を GC-MS によるデバイスのインジェクターに注入します。250 ° C で、1:20 次のオーブン プロトコルで ZB 5 列の結合ガスクロマト/四重極分光システム分割比率注入: 50 ° C で 1 分ランプを 10 ° C/分 140 ° c;300 ° C まで 20 ° C/分と 10 分間保持します。
- エアロゾル成分を識別するために対象のライブラリに結果として得られる質量スペクトルに一致します。
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
ひと臍帯静脈の露出の 24 時間以内に従来のタバコの煙のエキス (CSE) または電子タバコ エアロゾルに内皮細胞抽出 (EAE) は重要な (CSE P対コントロール < 0.001; 対 EAE P制御< 0.01;n = 6) セル実行可能性 (図 3 a) の減少。抽出物は、2、2 秒、毎分 55 mL パフの噴き出しプロファイルで生成されて、デバイスによって消費されるニコチンのに基づいてモル濃度を正規化します。CSE の 500 μ M 消費ニコチン同等物への露出が激減、コントロールの 11.06 ± 0.28% 生菌、EAE の 500 μ M 消費ニコチン同等物への露出制御の 86.65 ± 4.60% 実行可能なセルを軽減されます。
図 3 bは、ガスクロマトグラフィーによる商業電子タバコから電子タバコ成分の揮発性に基づいて分離を示します。コンポーネントは、四重極質量分析器で識別されました。ボラティリティの順に特定のコンポーネントが含まれます: プロピレング リコール、アセチル プロピオニル、製剤、グリセリン、ニコチン、3-nitropthalic 酸。唯一プロピレング リコール、グリセロール、ニコチンの製品ラベル1に開示されました。

図 3: サンプル アプリケーション: 細胞の生存率と GC さん中性赤の取り込みアッセイの結果は 500 μ M にひと臍帯静脈内皮細胞に実行された図 3 a表示消費 3R4F 研究参照タバコ (CSE) からどちらか従来のタバコ煙のニコチン同等または市販の電子タバコ (EAE) から電子タバコ エアゾール。バーは、平均 ± 標準偏差です。定める 2 つの尾を持つ、意義、対になっていない t 検定とアスタリスクで示された結果: * * P < 0.01;P < 0.001;n = 6。図 3 bは、アセトンに可溶化電子タバコ エアロゾルのガスクロマト グラフの結果を表示します。ピークは、各化合物の保持時間 (ボラティリティ) の順を表し、四重極質量分析によって識別されました。1) プロピレング リコール;2) アセチル プロピオニル;3) 製剤。4) グリセロール;5) ニコチン;6) 3-nitropthalic 酸。この図の拡大版を表示するのにはここをクリックしてください。
Subscription Required. Please recommend JoVE to your librarian.
Discussion
このプロトコルの最も重要な要素は、デバイスがきれいなスタートを確実とそれぞれの抽出の完了し、確実にすべてのシールが保持されますので空気の流れが一定です。デバイスが適切にクリーンアップされない場合リスクがあるキャリーの上のサンプルの間です。さらに、装置は長時間時間凝縮したエアロゾルの汚れたまま、乾燥溶媒はシステムをブロックできます。注意してください、それが通常ある従来のタバコとエアフローを吹きかけるとき圧力降下をするメーターをデバイスが部屋の空気を引いている間、パフの中に必要な気流を提供するために調整する必要があります。このメソッドの主な機能は、電子タバコの技術の進歩に追いつくために適合する能力です。たとえば、多くの電子タバコ加熱コイルのボタン押して活性化が必要です。直接、このデバイスには、ユーザー プログラムの間隔でボタンを押すを模倣した (図 2 a) 制御回路に加熱コイルが組み込まれています。このメソッドの主な制限は、電子タバコ用も特徴と標準業務手順書の不足から生じる。我々 は慣習的なタバコの研究参照タバコ14国際プロトコル15,16を使用ことができます、我々 は電子タバコにこれらのメソッドを適応させるだけと適切にそれを保証することはできません。電子タバコのユーザーの動作をモデル化します。さらに、このプロトコルは、液体培地でエキスを生成します。これは適切なは特定の細胞など、内皮細胞、気道の細胞など、他のセルタイプより良い電子タバコ エアロゾルへの直接露出を学ぶことができます。
このデバイスの性質を新しい標準の運用手順を開発するを更新することができます。特定の質問に合わせてデバイスを可能にすることができる変更のいくつかのポイントが存在します。新しい電子タバコ電子タバコ17の以前のモデルよりもワット数の高い範囲を網羅します。回路図は図 2 aで提示で両方抵抗加熱コイル、加熱コイル自体に隣接してに使用される最終的な電力を調節する異なる抵抗値 (またはも可変抵抗) を持つ部品のスワップでした。電子タバコの液体をイアントします。アトマイザーの最終的な理論的な力は、従来の力の式で計算できます。
 または
または
どこ p: 電源;V: 電圧;R: 抵抗;i: 電流。
電子タバコの使用のための広く受け入れられている国際標準操作手順はありません、別のグループは、さまざまなパラメーターと噴き出しプロファイルを採用すること。ISO 3088:201215人 TobLabNet SOP 116など従来のタバコ喫煙プロトコルの変更されたバージョンを使用し続けるいくつかのグループが、一般的な電子タバコの標準は CORESTA CRM8118、です。さらに、多くの実験室は引き続き研究室および/または機関特定の政体を使用します。このインスタンスで 2、2 秒分あたり 55 mL パフから成る矩形波パフ プロファイルを採用ただし、必要に応じて他のたばこを吸うプロファイルに適応することができますデバイスのモジュール、プログラム可能な性質。パフのボリュームは、直接空気の流量を調整することによって変更できます。パフ時間と加熱コイル活性化時間は、プログラム SVL.bs1 (図 2 b5 # & #6) で SVT と IPT の定数を変更することによって変更できます。これが SVT IPT 定数、例えば SVT1を表す暖房回路の活性化、SVT2バルブ回路間の時間を分割することにより行うことができる 1 つの脱たばこを吸う時間とアクティブにする時間を同期したい場合、バルブ回路の活性化および暖房回路、SVT3暖房回路の不活性化と不活性化バルブ回路と同様に IPT の間の時間を表すの不活性化までの時間を表します。多くのタンク電子タバコで、510 のスレッド ベースが一般的ですが、ユニバーサルではありません。ユーザーが必要な場合、異なるスレッド ベースを置き換えることができます。方形波プロファイルする必要がない場合は、波のプロファイルを再構築する連続プログラマブル コンポーネントと空気流量計または電磁弁を交換してください。
電子タバコ研究進行、可用性と電子タバコのユーザー補助デバイスを喫煙ハードルのままです。タバコ喫煙マシンは 1843 として早くタバコ製品の研究の不可欠な部分をされているそして今日市販喫煙機慣習的なタバコ19,20のさまざまながあります。従来のタバコ喫煙21の複数の確立された標準操作手順書があります。しかし、多くの従来のタバコ喫煙器具正確にデザイン違い従来および電子タバコと電子タバコのブランドおよびモデル内の相違から電子タバコを喫煙の無能を証明しました。よう: 直径、PSI 要件、およびセンサーやボタンの必要性に基づいて活性化17。現在空気液体インターフェイス露出 (Borgwalt22 Vitrocellなどと同様に、直接エアロゾル抽出用に設計されたデバイスを含むデバイスが含まれている電子タバコ喫煙マシンの異種商業分野があります。22,23)。商業オプションの可用性、にもかかわらず多くのグループはエアロゾル抽出10、11,12,24、の実験室の中で作製したデバイスを使用し続ける25,26. これの動機はさまざま。いくつかのケースでより良いモデル人間の行動10研究者を求めます。他の人はタバコの煙12の以前に発行された研究との連続性を維持しようとしています。まだ他の人は直接研究室製作24での動機として商業代わりの到達不能を引用します。これらのデバイスは、多くの形態をとるし、多くの場合、実験室特定のプロトコルを使用して。残念ながら、メカニズム、効果、およびこれらのデバイスとプロトコルの機能の下で-が多い。
(図 3 a) 上記 2 つのサンプル アプリケーションの最初は、従来のタバコの煙、電子たばこエアロゾルの内皮細胞生存率に及ぼす影響を説明します。従来のタバコの煙は、引き起こす内皮細胞死と障害9に示されている、それは合理的な電子タバコを仮定するエアロゾルと同様の効果を持っています。これをテストするには、ニコチン 24 h の従来のタバコの煙のエキスまたは電子タバコ エアロゾルと同等のレベルを抽出するひと臍帯静脈内皮細胞をさらされます。電子タバコ エアロゾルによる削減の効果量は後削減中 〜 13%, 両方従来のタバコの煙、電子たばこエアロゾルは、細胞生存率の統計的に有意な減少を引き起こす、従来タバコ煙暴露 90% に近づきます。これは、電子タバコは従来のタバコよりも血管に害が少ないという考えをサポートするが、まだ安全ではないです。(図 3 b) 上記 2 つのサンプル アプリケーションの 2 つ目は、有機溶媒に抽出する電子タバコ エアロゾルを分離されてその構成と質量分析器で分析することができますを示しています。生成されたコンポーネントのリスト、電子タバコ製品のラベリングの精度についての情報を提供し、アセチル プロピオニル (2, 3-ペンタンジオン)27など特定の潜在的に有害のコンポーネントがハイライトされます。この実験で特定したコンポーネントが定量化されていませんが、一方、CORESTA CRM8428の説明など従来の分析技術は定量化を実行できます。
ここでは、私たちは従来のタバコの煙や電子タバコ エアロゾルから抽出液を生成することができるプログラム可能な試験装置を発表しました。このデバイス (電子タバコの主要な商業ブランド) などの製品設計の多様な配列に対応することができ、抽出プロセスは、ユーザーの仕様にカスタマイズできます。この特定のインスタンスで、内皮細胞生存率測定; で生成された抽出物の使用が示しました。ただし、このデバイスによって生成された抽出物は、単一のセル人口と同様、共培養、植、または他の in vitroモデルの任意の型に適用でした。これらの抽出物は活性酸素種検出、細胞増殖アッセイ、従来免疫染色など頻繁に使用される生物学的アッセイの広い数と互換性があります。また、ガスクロマトグラフィー質量分析法による電子タバコ抽出物の成分を分解する能力は、個別エアロゾル成分の詳細な研究のための出発点を提供します。全体的にみて、このデバイスは、電子タバコの研究にアクセスできるエントリ ポイントを提供します。
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
チューレーン大学によって管理されるタバコ製品規制科学研究員プログラムはアルトリア クライアント サービス規制によって資金を供給します。
Acknowledgments
著者はチューレーン大学細胞部と原稿を編集の彼の援助のための分子生物学の博士ロバート dotson さんと彼の援助のため化学のチューレーン大学科の博士ジェームズ ・ ボリンジャーの支援を認める質量分析のプロトコル設計。さらに著者は、チューレーン大学講座細胞・分子生物学化学のチューレーン大学の部門のサポートと空間や設備の使用を認めます。この作品は、チューレーン大学理学と工学から c. アンダーソンにタバコ製品規制科学研究奨学金によって支えられました。
Materials
| Name | Company | Catalog Number | Comments |
| 12 V AC/DC Wall Mount Adaptor | Digi-Key | T1099-P5P-ND | |
| 2.2 Ohm Resistors | Digi-Key | A105635-ND | Used in tandem to generate the 4.4 Ohm resistance in Figure 2A |
| 330 Ohm Resistors | Digi-Key | 330QBK-ND | |
| 510 Threaded Base | NJoy | N/A | Recovered by dismantalling a second generation NJoy electronic cigarette |
| Acetic Acid, Glacial | Sigma-Aldritch | A6283 | |
| Acetone (Chromatography Grade) | Sigma-Aldritch | 34850 | |
| Basic Stamp Project Board | Digi-Key | 27112-ND | This board contains the BS1 Microcontroller, serial adaptor, power switch, and a barrel pin connector for the AC/DC Wall Mount Adaptor |
| Basic Stamp USB to Serial Adapter | Digi-Key | 28030-ND | An optional component to allow the BS1 serial adaptor to communicate through USB |
| Buchner Flask (Vacuum Flask) 250 mL | VWR | 10545-854 | |
| Clear Tape | 3M | S-9783 | |
| Clear Vinyl Tubing, 3/8" ID | Watts | 443064 | |
| EGM-2 Endothelial Cell Culture Medium | Lonza | CC-3162 | |
| Ethanol | Pharmco-Aaper | 111000200 | |
| Flow Regulator | Dwyer | VFA-23-BV | |
| Gas Chromatograph | Varian | 450-GC | |
| Glass Syringe, 10 mL | Sigma-Aldritch | Z314552 | |
| Glass Syringe, 10 µL | Hamilton | 80300 | |
| High Vacuum Silicon Grease | Dow Corning | 146355D | |
| Hose Clamp | Precision Brand | 35125 | |
| Human Umbilical Vein Endothelial Cells | ATCC | PCS-100-013 | |
| Mass Spectrometer | Varian | 300-MS | |
| Midget Impinger | Chemglass | CG-1820-01 | |
| Neutral Red | Sigma-Aldritch | N4638 | |
| Paraffin Film | 3M | PM-992 | |
| Plate Seal Roller | BioRad | MSR0001 | |
| Plate Seal; Foil | Thermo | 276014 | |
| Ring Stand 20" | American Educational Products | 7-G15-A | |
| Solenoid Valve (normally open) | US Solid | USS2-00081 | |
| Solid State Relay | Digi-Key | CLA279-ND | |
| Stand Clamp | Eisco | CH0688 | |
| Syringe Filter, PES, 0.22 um | Millipore | SLGP033RS | |
| Syringe, 10 mL | BD Syringe | 309604 | |
| Through Hole Stopper, Size 6 | VWR | 59581-287 | |
| Vacuum Pump | KNF Neuberger | N86KTP |
References
- World Health Organization. WHO Report on the Global Tobacco Epidemic, 2011. , Italy. (2011).
- Weaver, S. R., Majeed, B. A., Pechacek, T. F., Nyman, A. L., Gregory, K. R., Eriksen, M. P. Use of electronic nicotine delivery systems and other tobacco products among USA adults, 2014: results from a national survey. Int. J. Public Health. 61 (2), 177-188 (2016).
- Singh, T., et al. Tobacco Use Among Middle and High School Students - United States, 2011–2015. MMWR Morb. Mortal. Wkly. Rep. 65 (14), 361-367 (2016).
- Corey, C. G., Ambrose, B. K., Apelberg, B. J., King, B. A. Flavored Tobacco Product Use Among Middle and High School Students--United States, 2014. MMWR Morb. Mortal. Wkly. Rep. 64 (38), 1066-1070 (2015).
- Pisinger, C., Døssing, M. A systematic review of health effects of electronic cigarettes. Prev. Med. 69, 248-260 (2014).
- Callahan-Lyon, P. Electronic cigarettes: human health effects. Tob. Control. 23 (Suppl 2), ii36-ii40 (2014).
- Dinakar, C., O'Connor, G. T. The Health Effects of Electronic Cigarettes. N. Engl. J. Med. 375 (14), 1372-1381 (2016).
- Anderson, C., Majeste, A., Hanus, J., Wang, S. E-cigarette aerosol exposure induces reactive oxygen species, DNA damage, and cell death in vascular endothelial cells. Toxicol. Sci. Off. J. Soc. Toxicol. , (2016).
- U.S. Department of Health and Human Services. The Health Consequences of Smoking: 50 Years of Progress. A Report of the Surgeon General. , Atlanta, GA. U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Center for Chronic Disease Prevention and Health Promotion, Office on Smoking and Health (2014).
- Farsalinos, K., et al. Comparison of the Cytotoxic Potential of Cigarette Smoke and Electronic Cigarette Vapour Extract on Cultured Myocardial Cells. Int. J. Environ. Res. Public. Health. 10 (10), 5146-5162 (2013).
- Schweitzer, K. S., et al. Endothelial disruptive proinflammatory effects of nicotine and e-cigarette vapor exposures. Am. J. Physiol. - Lung Cell. Mol. Physiol. 309 (2), L175-L187 (2015).
- Putzhammer, R., et al. Vapours of US and EU Market Leader Electronic Cigarette Brands and Liquids Are Cytotoxic for Human Vascular Endothelial Cells. PLOS ONE. 11 (6), e0157337 (2016).
- Crooks, I., Dillon, D. M., Scott, J. K., Ballantyne, M., Meredith, C. The effect of long term storage on tobacco smoke particulate matter in in vitro genotoxicity and cytotoxicity assays. Regul. Toxicol. Pharmacol. 65 (2), 196-200 (2013).
- Roemer, E., et al. Mainstream Smoke Chemistry and in Vitro and In Vivo Toxicity of the Reference Cigarettes 3R4F and 2R4F. Beitr. Zur Tab. Contrib. Tob. Res. 25 (1), (2014).
- International Organization for Standards. ISO 3088:2012 Routine analytical cigarette smoking machine – Definitions and standard conditions. , (2012).
- World Health Organization. Standard Operating Procedure for Intense Smoking of Cigarettes. , (2012).
- Brown, C. J., Cheng, J. M. Electronic cigarettes: product characterisation and design considerations. Tob. Control. 23 (Suppl 2), ii4-ii10 (2014).
- Cooperation Centre for Scientific Research Relative to Tobacco. CRM No. 81 - Routine Analytical Machine for E-Cigarette Aerosol Generation and Collection - Definitions and Standard Conditions. , (2015).
- Thorne, D., Adamson, J. A review of in vitro cigarette smoke exposure systems. Exp. Toxicol. Pathol. 65 (7-8), 1183-1193 (2013).
- Klus, H., Boenke-Nimphius, B., Müller, L. Cigarette Mainstream Smoke: The Evolution of Methods and Devices for Generation, Exposure and Collection. Beitr. Zur Tab. Contrib. Tob. Res. 27 (4), (2016).
- Baker, R. The Development and Significance of Standards for Smoking-Machine Methodology. Beitr. Zur Tab. Contrib. Tob. Res. 20 (1), (2014).
- Thorne, D., Crooks, I., Hollings, M., Seymour, A., Meredith, C., Gaca, M. The mutagenic assessment of an electronic-cigarette and reference cigarette smoke using the Ames assay in strains TA98 and TA100. Mutat. Res. Toxicol. Environ. Mutagen. 812, 29-38 (2016).
- Thorne, D., Larard, S., Baxter, A., Meredith, C., Gaҫa, M. The comparative in vitro assessment of e-cigarette and cigarette smoke aerosols using the γH2AX assay and applied dose measurements. Toxicol. Lett. 265, 170-178 (2017).
- Herrington, J. S., Myers, C. Electronic cigarette solutions and resultant aerosol profiles. J. Chromatogr. A. 1418, 192-199 (2015).
- Yu, V., et al. Electronic cigarettes induce DNA strand breaks and cell death independently of nicotine in cell lines. Oral Oncol. 52, 58-65 (2016).
- Ji, E. H., et al. Characterization of Electronic Cigarette Aerosol and Its Induction of Oxidative Stress Response in Oral Keratinocytes. PLOS ONE. 11 (5), e0154447 (2016).
- Morgan, D. L., et al. Chemical Reactivity and Respiratory Toxicity of the -Diketone Flavoring Agents: 2,3-Butanedione, 2,3-Pentanedione, and 2,3-Hexanedione. Toxicol. Pathol. 44 (5), 763-783 (2016).
- Cooperation Centre for Scientific Research Relative to Tobacco. CRM No. 84 - Determination of Glycerin, Propylene Glycol, Water, and Nicotine in the Aerosol of E-Cigarettes by Gas Chromatographic Analysis. , (2017).



