Summary
Hierin, rapporteren we de synthese en de kristallisatie van 3,5-lutidine N -oxide uitdrogen door een eenvoudig protocol dat van de klassieke synthese van pyridine N verschilt-oxide. Dit protocol maakt gebruik van verschillende grondstoffen en gaat minder reactietijd opleveren van een nieuwe solvated supramoleculaire structuur, die onder traag verdamping kristalliseert.
Abstract
De synthese van 3,5-lutidine N -oxide uitdrogen, 1, tot stand gekomen in de route van de synthese van 2-amino-pyridine-3,5-dicarbon zuur. De methodologie voor niet-gesubstitueerde pyridine in 1957 in een proces van 12u Ochiai eerst gebruikt, maar geen X-ray geschikt kristallen zijn verkregen. De vervangen ring gebruikt in de hier voorgestelde methodologie duidelijk beïnvloed de toevoeging van watermoleculen in de asymmetrische eenheid, die een verschillende nucleofiele sterkte in 1verleent. De X-ray geschikt crystal samengestelde 1 werd mogelijk als gevolg van de stabilisatie van de negatieve lading in de zuurstof door de aanwezigheid van twee watermoleculen waar de waterstofatomen doneren positieve lading in de ring; dergelijke watermoleculen dienen goed te bouwen een supramoleculaire interactie. De gehydrateerd moleculen mogelijk voor het alkalische systeem dat wordt bereikt door aanpassing van de pH tot en met 10. Nog belangrijker is, de dubbele methyl vervangen ring en een reactietijd van 5 h, maakt het een meer veelzijdige methode en met bredere chemische toepassingen voor toekomstige ring invoegingen.
Introduction
Tegenwoordig wetenschappers over de hele wereld hebben zijn te investeren middelen naar de ontwikkeling van nieuwe synthetische routes voor de functionalization van aromatische groepen, die staan bekend om de lage reactiviteit voorzijde aan toevoeging reacties1,2, 3. Pyridine, waar een stikstofatoom een koolstofatoom vervangt, presenteert een soortgelijke chemische reactiviteit op analoge ringen uitsluitend uit koolstof atomen3 bestaaten het meestal ondergaat een vervanging mechanisme in plaats van toevoeging. N-oxiden zijn onderscheidend door de aanwezigheid van een donor band tussen stikstof en zuurstof gevormd door de overlapping van de nonbonding elektronenpaar op stikstof met een lege orbitaal op de zuurstof atoom3. Met name, pyridine N-oxiden zijn Lewis basen, omdat hun N-O-groep als een elektrondonor fungeren kan en ze kunnen combineren met Lewis zuren vormen de overeenkomstige Lewis-zuur-base paren. Deze eigenschap heeft een essentiële chemische gevolg, omdat het kan de vergelijking van de Lewis zuren naar potentiële elektrofielen verhogen en dus te laten reageren onder omstandigheden waar normaal de reactie niet zou worden. Waarschijnlijk is de meest voorkomende gebruik van dergelijke stoffen in verschillende oxidatiereacties waar zij als oxidanten4 optreden. Pyridine N-oxiden en veel van hun ring-matiemaatschappij derivaten zijn terugkerende moleculen biologisch actieve en farmacologische agenten5, en een duidelijke ruimtelijke spreiding door verschillende spectroscopische tools is opgericht voor sommigen van hen6,7. In onderzoek naar verschillende groepen koppelen aan de pyridine-ring, hebben wetenschappers getest verschillende methoden voor de productie van een gemakkelijke en conventionele methode, aangezien isoxazolines een katalytische hoeveelheid base zoals DBU vereist in kokend xyleen aan formulier 6- vervangen-2-aminopyridine, N-oxiden8,9. Een verscheidenheid van pyridine derivaten werden omgebouwd tot hun overeenkomstige N-oxiden in aanwezigheid van een katalytische hoeveelheid mangaan tetrakis(2,6-diclorophenyl) porfyrine en ammonium acetaat in CH2Cl2/CH3 GN-8,10. Andere pyridine zijn geoxideerd tot hun stikstofoxiden H2O2 in aanwezigheid van katalytische bedragen van methyltrioxorhenium8,11, of door toevoeging van overtollige dimethyldioxirane met CH2Cl2 bij 0 ° C, wat leidt tot de overeenkomstige N-oxiden8,12,13,14. Bis (trimethylsilyl) peroxide in aanwezigheid van trioxorhenium in CH2Cl2 is gebruikt voor de synthese van pyridine N-oxiden8,11. De synthese van aminopyridine N-oxiden waarbij acylering met behulp van Caro zuur (peroxomonosulfuric zuur) ook is gemeld8. Niettemin, de methodologie hier gemeld, en die gebruikt een deel van de methode gerapporteerd door Ochiai1, biedt zeer goede resultaten met behulp van ijsazijn, goedkoper en toegankelijk reagentia en H2O2 . Deze praktijk is meer geschikt voor gebruik in grote schaal preparaten die op de tertiaire amines inwerken, produceert goede opbrengsten in een reactie die slechts 30% waterstofperoxide vereist en ijsazijn in een temperatuur tussen de 70-80 ° C, en het maakt gebruik van een zuiveringsproces dat is beschikbaar in de meeste laboratoria van de synthese zoals distillatie, zonder het gebruik van de katalysator of duurder reagentia1. De literatuur meldt dat andere methoden ook vaak termijnen van 10-24 h en temperaturen boven 100 ° C 4,8 betrekken, en de opbrengst van goed gevormde kristallen voor X-ray analyses is zelden gerapporteerd.
Reactief, worden diverse N -oxide derivaten gebruikt voor de lutidine ring, adequaat te activeren in een nucleofiele of elektrofiele bakboord. De nucleofiele of elektrofiele factor wordt beïnvloed door de substituenten. Met de pyridine-ring wordt de intrekking van de elektron-groepen, is de belangrijkste factor de nucleofiele karakteristiek1. De gratis N-oxide verbindingen zijn zelden geïsoleerd als geschikt kristallen voor x-stralen analyse als gevolg van de gedelokaliseerd lading in de aromatische ring. Echter is de Solvatatie factor cruciaal voor het stabiliseren van de negatieve dichtheid van de zuurstof-15.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. reactie
- Plaats in een zuurkast een geopende ronde 100 mL-kolf met 0,5 mol (29.8 mL) ijsazijn en Voeg 0.051 mol (5.82 mL) van 3,5-dimethylpyridine en 5 mL van de H2O2 (35%). Houd het mengsel reactie onder constante magnetische roeren, bij een innerlijke temperatuur van 80 ° C gedurende 5 uur.
- Na de reactietijd, cool de kolf tot 24 ° C met ijs (do niet bloot het azijnzuur aan het ijs gassen) en sluit deze aan een hoog vacuüm distillatie-eenheid voor 90-120 min te verwijderen overtollige azijnzuur.
Let op: Gebruik geen warm materiaal. Wacht totdat het glaswerk een beheersbare temperatuur bereikt. Dit zal ook voorkomen dat dampen invoeren van de bovenkant van de distillatie-eenheid. - Voeg gedistilleerd water (10 mL) tweemaal om ervoor te zorgen het verwijderen van elk spoor van azijnzuur en te concentreren het mengsel veel mogelijk.
2. basiciteit aanpassing en extractie
- Ontbinden in bi-distillated water het geïsoleerde viskeuze en transparant product en breng de pH op 10 met zuivere solide nb2CO3met een potentiometer.
- Breng zorgvuldig de oplossing in een scheitrechter van 250 mL en haal het 5 keer met 250 mL CHCl3 ter verbetering van het rendement. Herstellen van de organische laag en droog het zo over solide nb24 voor 30 minuten maximaal, dat het product zal bevatten. Indien nodig, opnieuw uitpakken de waterige fase met de gewenste hoeveelheid CHCl3.
Let op: CHCl3 slaperigheid en duizeligheid kunnen veroorzaken; behandelen met zorg en in een zuurkast. - Verwijder het oplosmiddel onder verminderde druk met een hoog vacuüm distillatie-eenheid, tot de vorming van een zeer hygroscopisch duidelijk beige kristallijn poeder (70%).
3. kristallisatie proces
- Los 4.3 g de kristallijn poeder in 50 mL koude hoge uitgevoerde vloeibare chromatografie (HPLC) rang diethylether. Vacuüm Filtreer de oplossing voor het verwijderen van elk spoor van solide grondstof of zelfs stof. Giet het filtraat in een glazen petrischaaltje, waarbij het te vertragen verdampen bij 4 ° C in een laboratorium koelkast.
- Ervoor zorgen dat er na twee dagen, heldere kleurloze kristallen zijn verkregen. Meet vervolgens het smeltpunt, dit in het bereik van 310-311 K. moet
4. analyse van 3,5-Lutidine N -oxide Dehydrate
- Verwijder de kristallen die worden gevormd, van prismatische vorm en kleurloos, door decanteren van de kolf van muren voor verdere x-stralen analyse. Als niet direct gebruikt, houden de kristallen in diethylether te vermijden crystal hydratatie.
- Ontbinden 0.010 g van 3,5-lutidine N -oxide uitdrogen in 0.4 mL CDCl3 NMR H1 en C13 analyse om te bewijzen de doeltreffendheid van de procedure uit te voeren.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Het protocol is in wezen een uitbreiding van de Ochiai techniek1. Echter de lagere temperatuur en minder tijd worden toegepast. Deze eenvoudige methode kan worden gebruikt voor het verkrijgen van een veelzijdige ligand, oftewel een gesubstitueerde pyridine N-oxide afgeleide. Om te bevestigen de vorming van 1, zijn NMR, 1H en 13C analyse voorkeur voor het testen van de doeltreffendheid van de procedure.
De chemische verschuiving toont de vorming van 1. Het signaal op 2,28 ppm (deeltjes per miljoen) komt overeen met de zes gelijkwaardige waterstof van de twee methylgroepen in de 3 en 5 posities, die het magnetisch veld in minder verhouding dan de permanente magnetische waarnemen. Er zijn twee soorten septuplets: men behoort tot het proton in de c positie op 7,9, welke verdubbelt de grootte van het andere signaal op 6,9 dat tot het proton in positie a. Figuur 1 behoort de chemische shifts uitgelokt door de aanwezigheid van de zuurstof atoom bonde toont d aan het stikstofatoom van de pyridine-ring. De zuurstof-atoom is electro-terug te trekken en de dichter waterstofatomen aan het zuurstofatoom (c en a) Toon verplaatsing naar een hogere frequentie dan die voor de methyl-waterstof (b).
Hetzelfde proces wordt uitgezet voor de NMR 13C spectrum, Figuur 2, waar de signalen voor de dichter koolstofatomen naar het zuurstofatoom (c en een) Toon frequentie scheiding tussen hun signalen van Δc = 1300 Hz en Δeen = 200 Hz. Nogmaals, vertonen de koolstofatomen methyl geen wijzigingen. Het IR-spectrum kan worden gebruikt om het succes van de methode ook.
Het ORTEP diagram, Figuur 4, toont de aanwezigheid van twee moleculen van water rond het asymmetrisch molecuul. Deze moleculen worden verondersteld te stabiliseren van de N-O-binding. In soortgelijke gevallen, het is beschreven voor pyridine N-oxide en verwante aromatische stikstofoxiden. Er is een significante stabiliseren π-type O→N rug-donatie, weerspiegeld in een hoger is dan 1 en een aantal eenzame elektronenparen berekende bond-volgorde op de O atom lager dan 36.
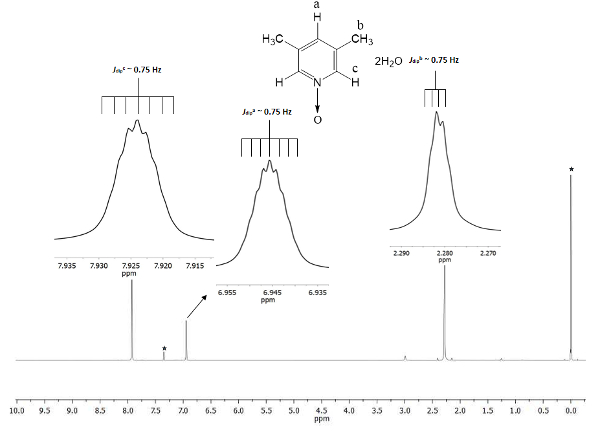
Figuur 1 . TMS verwezen CDCl3 500 MHz NMR 1H spectrum van 1. De integraties en chemische shifts van de drie signalen komen overeen met drie verschillende types van waterstofatomen die aanwezig zijn in de lutine N-oxide. Klik hier voor een grotere versie van dit cijfer.
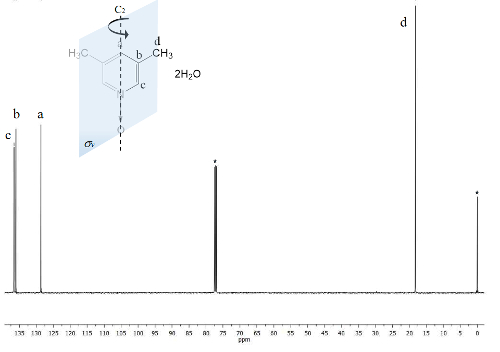
Figuur 2 . TMS verwezen CDCl3 100 MHz NMR 13C-spectrum van 1. Drie signalen worden waargenomen voor de vijf aromatische koolstofatomen en een voor de twee methylgroepen. Klik hier voor een grotere versie van dit cijfer.
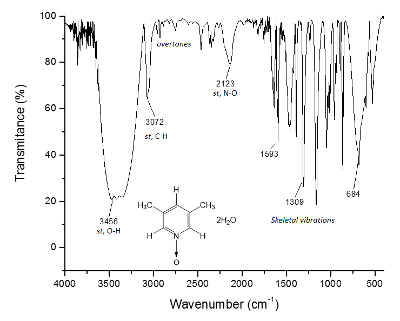
Figuur 3 . IR-spectrum van 1. De O-H obligaties, vooral van 3300 cm-1, zijn verantwoordelijk voor de vorming van supramoleculaire structuur en de vorming van kristallen. Klik hier voor een grotere versie van dit cijfer.

Figuur 4 . ORTEP diagram van 1 waar twee moleculen van H2O formulieren brug waterstofbruggen met lutidine van zuurstof, rijden hun waterstofatomen richting het zuurstofatoom. Dit cijfer is gewijzigd van Merino García et al. 12 Klik hier voor een grotere versie van dit cijfer.

Figuur 5 . Foto's van geschikte röntgendiffractie kristallen van 1 in diethylether (boven) en op open air (onderkant). Een van deze kristallen was bevestigd in de diffractometer van de X-ray en toonde een pad van de diffractie van röntgenstralen, die werd traduced en verfijnd door speciale computationele programma's in een moleculaire en kristallijne structuur24,25, 262827,,. Klik hier voor een grotere versie van dit cijfer.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Het protocol hier gepresenteerd is een conventionele methode een zuurstof-atoom te koppelen aan het stikstofatoom van de 3,5-lutidine als een functionalization methode van substraten. Deze techniek is ook goed ingeburgerd aan opbrengst X-ray geschikt gedehydrateerde kristallen (Figuur 5, foto's genomen met een Sony DSC-HX300 Cyber-schot camera). Voor zover wij hebben niet veel verslagen de productie van dergelijke kristallen16beschreven. Veel verbindingen groeien ideale kristallen voor x-stralen analyse als ze zijn in chelaatvorm door verschillende metalen17,18,19,20. Zodra de kristallijn poeder wordt gevormd, is het belangrijk om een uittreksel uit hun moederlogen met behulp van een Kitasato kolf en een Buchner trechter. Met behulp van rubberen slangen, de Kitasato kolf is verbonden met een vacuüm lijn en bovenop de Buchner trechter is geplaatst met filtreerpapier. Zodra het vacuüm is ingeschakeld, wordt het koffiefilter bevochtigd met een kleine hoeveelheid oplosmiddel waaruit het product is uitgekristalliseerd. Hiermee voorkomt u dat de kristallijn poeder druppelen in de Buchner trechter door het vacuüm effect. Na het veiligstellen van het koffiefilter, wordt de oplossing met de kristallijn poeder geschud om ervoor te zorgen dat alle de kristallijn poeder wordt gefiltreerd, en niets in de bodem van de kolf blijft. De oplossing is snel uitgegoten over de Buchner trechter. De kristallijn poeder, verkregen nog voor ongeveer 10 min aan het filtreerpapier, en vervolgens het vacuüm is uitgeschakeld en de kristallijn poeder is losgekoppeld van het papier en opgeslagen in een ondoorzichtige glazen ampul, aangeduid met de code en bewaard bij 4 ° C tot verdere analyse. De filtrated vloeistof wordt gegoten in een glazen petrischaaltje, laat het aan langzaam verdamping bij 4 ° C om de vorming van toereikende kristallen voor x-stralen analyse.
Het is belangrijk op te merken dat dit protocol maakt gebruik van oplosmiddelen en materialen die gemakkelijk verkrijgbaar en over het algemeen zijn te vinden op elk onderzoekslaboratorium. De aanpassing van de pH door toevoeging van nb2CO3 en de consistente magnetische roeren zijn cruciaal voor het rendement van het uiteindelijke product. Het is echter belangrijk aandacht te besteden extra voorzichtig zijn in alle stappen in een proces, met name in de extractie waar geen spoor van grondstof moet aanwezig zijn om de vorming van kristallijn poeder en vervolgens kristallen veroorloven. Dus, deze fase extractie/zuivering kan worden gecontroleerd door NMR of IR spectroscopie om de kwaliteit van het product.
Om ervoor te zorgen de reproduceerbaarheid van dit protocol, is NMR een uitstekend hulpmiddel. Zelfs fijne details zijn zichtbaar in het spectrum. Alle signalen worden als inzetstukken in Figuur 1weergegeven. Deze inzetstukken verbeelden duidelijk een splitsing, namelijk multipliciteit, van alle signalen. Bijvoorbeeld, de protonen b (Jduikb ~ 0,75 Hz) Toon vier pieken bij de kam van het signaal, met een scheiding onder hen (Δpiek-piek) misselijk constante van ~ 0.0075 ppm. De 0.0075 ppm kan worden omgezet naar energie met behulp van de volgende vergelijking21
 Vergelijking 1
Vergelijking 1

De transformatie wordt aanbevolen omdat de signalen ontvouwen afkomstig zijn uit de datieve ruimtelijke interactie tussen de waterstof van de drie kernen van de methylgroep, en hoewel ze verder dan de 4 single obligaties met protonen c en a, zij kunnen waarnemen hun dipolaire magnetische dynamiek interacties22. Bovendien, maakt de gratis sigma verlijmen van rotatie in de methylgroep het super hyperfine proton-proton interactie zichtbaar zijn in de veelheid van het signaal. De septuplets van protonen een en c op 6.9 en 7.9 pag/min, respectievelijk zijn afgeleid van hetzelfde fenomeen in polaire karakter. In deze gevallen, protonen een en c de protonen in de methylgroep voor dynamische dezelfde rotatie kan onderscheiden. Laatst, zoals verwacht, de berekende Jduik voor a, b en c hebben nauwelijks dezelfde waarde, ~ 0,75 Hz. Deze aantallen voor de afzonderlijke interacties bevestigen de ruimtelijke rangschikking van de kernen van waterstof in de magnetische anisotropie.
Aan de andere kant, maakt de C2v symmetrie van 1 gelijkwaardige koolstofatomen23. Het 13C-spectrum, Figuur 2, geeft de typische signaal voor methylgroepen gekoppeld aan aromatische ringen, koolstofatomen d op 18 pag/min. Bovendien een signaal op 129 ppm is zichtbaar op deze regio als gevolg van het minder elektronegatievere element beïnvloed koolstof een. Bij hoge frequenties zijn het signaal voor de meer blootgesteld koolstofatomen kernen tot het magnetisch veld gepresenteerd op 137 ppm22.
De voorgestelde methodologie is zeer nuttig voor de synthese van pyridine N-oxiden, bieden goede opbrengsten, in een redelijke tijd met zachte reactie voorwaarden en goedkoop en gemakkelijk toegankelijke reagentia, die geen extra katalysatoren vereisen. Deze voorwaarden kunnen worden gebruikt voor de wetenschappelijke en educatieve gemeenschap te verkrijgen van een breed scala van pyridine N-oxiden als precursoren voor andere moleculen van belang. De geschikte methode biedt de mogelijkheid voor het verkrijgen van experimentele en conceptuele basishulpmiddelen in educatieve laboratoria voor studenten, bewijzen van een succesvol synthese van verbindingen en het geluk dat de vorming van kristallen. Het is echter belangrijk te benadrukken dat, zoals een chemische reactie, het noodzakelijk is alle voorzorgsmaatregelen te nemen, aangezien de gebruikte reagentia in het algemeen gevaarlijk zijn.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Alle auteurs verklaren geen belangenconflict.
Acknowledgments
Het huidige werk gesteund door Vicerrectoría de Investigación y Estudios de Posgrado uit BUAP, onjuiste of Science en projecten nr. REOY-NAT14, 15, 16-G. HEAS-NAT17. RMG Bedankt CONACyT (Mexico) voor de beurs 417887.
Materials
| Name | Company | Catalog Number | Comments |
| 3,5-lutidine | Sigma-Aldrich | L4206-500ML | |
| Glacial acetic acid | Fermont | 3015 | |
| Hidrogen peroxide (35%) | Sigma-Aldrich | 349887-500ML | |
| Na2CO3 anhydrous | Productos Químicos Monterrey | 1792 | |
| Na2SO4 anhydrous | Alfa reactivos | 25051-C | |
| CHCl3 | Fermont | 6205 | |
| Ethyl eter | Mercury Chemist | QME0309 | |
| Distilled water | Comercializadora Química Poblana | not-existent |
References
- Ochiai, E. Recent Japanese work on the chemistry of pyridine 1-oxide and related compounds. J. Org. Chem. 18 (5), 534-551 (1953).
- Solomons, T. W. G. Organic Chemistry 2nd Edition. , John Wiley & Sons. 1110 (1976).
- Albini, A., Pietra, S. Heterocyclic N-Oxides. , CRC Press. ISBN: 0849345529 328 (1991).
- Koukal, P., Ulc, J., Necas, D., Kotora, Heterocyclic N.-Oxides. Topics in Heterocyclic Chemistry. 53, 29-58 (2017).
- Wen-Man, Z., Jian-Jun, D., Xu, J., Jun, X., Huan-Jian, X. Visible-Light-Induced C2 alkylation of pyridine N.-oxides. J. Org. Chem. 82 (4), 2059-2066 (2017).
- Merino García, M. R., Ríos-Merino, F. J., Bernès, S., Reyes-Ortega, Y. Crystal structure of 3,5-dimethylpyridine N-oxide dihydrate. Acta Cryst. 72 (12), 1687-1690 (2016).
- Sarma, R., Karmakar, A., Baruah, J. B. N-Oxides in Metal-Containing Multicomponent Molecular Complexes. Inorg. Chem. 47 (3), 763-765 (2008).
- Youssif, S. Recent trends in the chemistry of pyridine N-oxides. ARKIVOC. 2001, 242-268 (2001).
- Chucholowski, A. W., Uhlendorf, S. Base catalyzed rearrangement of 5-cyanomethyl-2-isoxazolines; novel pathway for the formation of 2-aminopyridine N-oxides. Tetrahedron Lett. 31 (14), 1949-1952 (1990).
- Thellend, A., Battioni, P., Sanderson, W., Mansuy, D. Oxidation of N-Heterocycles by H2O2 Catalyzed by a Mn-Porphyrin: An Easy Access to N-Oxides Under Mild Conditions. Synthesis. 1997 (12), 1387-1388 (1997).
- Copéret, C., Adolfson, H., Tinh-Alfredo, V. K. h, Yudin, A. K., Sharpless, K. B. A simple and Efficient Method for the Preparation of Pyridine N-Oxides. J. Org. Chem. 63 (5), 1740-1741 (1998).
- Ferrer, M., Sánchez-Baeza, F., Messeguer, A. On the preparation of amine N-oxides by using dioxiranes. Tetrahedron. 53 (46), 15877-15888 (1997).
- Adam, W., Briviba, K., Duschek, F., Golsch, D., Kiefer, W., Sies, H. Formation of singlet oxygen in the deoxygenation of heteroarene N-oxides by dimethyldioxirane. J. Chem. Soc. Chem. Commun. 1995 (18), 1831-1832 (1995).
- Murray, R. W., Singh, M. A Facile One-Step Synthesis of C-Arylnitrones Using Dimethyldioxirane. J.Org.Chem. 55 (9), 2954-2957 (1990).
- Kim, S. W., Um, T., Shin, S. Brønsted acid-catalyzed α-halogenation of ynamides from halogenated solvents and pyridine-N-oxides. Chem. Commun. 53 (18), 2733-2736 (2017).
- Campeau, L., Rousseaux, R., Fagnou, K. A solution to the 2-pyridyl organometallic cross-coupling problem: regioselective catalytic direct arylation of pyridine N-oxides. J. Am. Chem. Soc. 127 (51), 18020-18021 (2005).
- Gang, L., et al. Metal-free methylation of a pyridine N-oxide C-H bond by using peroxides. Org. Biomol. Chem. 13 (46), 11184-11188 (2015).
- May, D., Nyman,, Hampden-Smith, M. J., Duesler, E. N. Synthesis, characterization, and reactivity of group 12 metal thiocarboxylates M(SOCR)2Lut2[M) Cd, Zn; R ) CH3, C(CH3)3; Lut ) 3,5-Dimethylpyridine (Lutidine)]. Inorg. Chem. 36 (10), 2218-2224 (1997).
- Cho, S. H., Hwang, S. J., Chang, S. Palladium-Catalyzed C-H Functionalization of Pyridine N-Oxides: Highly Selective Alkenylation and Direct Arylation with Unactivated Arenes. J. Am. Chem. Soc. 130 (29), 9254-9256 (2008).
- Ide, Y., et al. Spin-crossover between high-spin (S = 5/2) and low-spin (S = 1/2) states in six-coordinate iron(III) porphyrin complexes having two pyridine-N. oxide derivatives. Dalton Trans. 46 (1), 242-249 (2017).
- Drago, R. S. Physical Methods in Chemistry. , Saunders College Publishing USA. 750 (1977).
- Cervantes-Mejía, V., et al. Branched Polyamines Functionalized with Proposed Reaction Pathways Based on 1H-NMR, Atomic Absorption and IR Spectroscopies. American Journal of Analytical Chemistry. 5 (16), 1090-1101 (2014).
- Huheey, J. E., Keiter, E. A., Keiter, R. L. Inorganic Chemistry: Principles of Structure and Reactivity, 4th Edition. , Oxford University Press. Mexico. ISBN: 9706131620 1023 (1997).
- Rigaku, CrysAlisPRO. , (2013).
- Sheldrick, G. M. SHELXT - Integrated space-group and crystal-structure determination. Acta Cryst. 71 (1), 3-8 (2015).
- Sheldrick, G. M. Crystal structure refinement with SHELXL. Acta Cryst. 71 (1), 3-8 (2015).
- Sheldrick, G. M. A short history of SHELX. Acta Cryst. 64 (1), 112-122 (2008).
- Macrae, C. F., et al. Mercury CSD 2.0 - new features for the visualization and investigation of crystal structures. J. Appl. Cryst. 41 (2), 466-470 (2008).
- ChemBioDraw Ultra 13. , PerkinElmer. (2013).



