Summary
Здесь, мы сообщаем, синтез и кристаллизации 3,5-lutidine N -оксида обезвоживаются путем простой протокол, который отличается от классической синтез пиридин N-оксида. Этот протокол использует различные исходного материала и включает в себя меньше время реакции на выход новой сольватированного супрамолекулярные структуры, которая кристаллизуется под медленные испарением.
Abstract
Синтез 3,5-lutidine N -оксида обезвоживать, 1, было достигнуто в синтезе маршрут 2-амино пиридин-3,5-дикарбоновых кислот. Отиай впервые использовал методологию для-замещенных пиридинов в 1957 году в 12 h процесс, но не подходит кристаллы рентгеновского были получены. Замещенных кольцо, используемые в методологии, представленные здесь явно под влиянием добавлением молекул воды в асимметричной блок, который совещается различные реакции нуклеофильного прочность в 1. Рентгеновских подходит кристалл составные 1 стало возможным благодаря стабилизации отрицательный заряд в кислороде наличием двух молекул воды где атомы водорода пожертвовать положительный заряд в кольцо; такие молекулы воды служат также построить супрамолекулярные взаимодействия. Гидратированная молекул может быть возможным для щелочных системы, что достигается корректировка pH до 10. Важно отметить, что двойной метил заменить кольцо и время реакции 5 h, делает его более универсальным методом и с более широкой химических приложениями для будущих кольцо вставок.
Introduction
В настоящее время ученые во всем мире инвестировать ресурсы в развитие новых синтетических маршрутов для функционализации ароматических групп, которые известны для низкой реакционной фронта дополнение реакции1,2, 3. Пиридина, где Атом азота заменяет атома углерода, представляет подобный химической активности в аналоговый, кольца, состоящий исключительно из атомов углерода3, и обычно подвергается механизм замены вместо сложения. N-оксидов отличительные присутствие доноров связь между азота и кислорода, образованный перекрытия nonbonding пары электронов на азота с пустой орбитального на атом кислорода3. В частности, пиридин N-оксиды являются основаниями Льюиса, потому что их N-O остаток могут выступать в качестве донора электрона, и они могут сочетать с кислотами Льюиса, формирования соответствующих пар кислотно щелочного Льюис. Это свойство имеет основные химические последствие, потому что он может увеличить nucleophilicity кислот Льюиса к потенциальным электрофилами и тем самым позволяют им реагировать в условиях, где обычно реакция не будет происходить. Вероятно наиболее частое использование таких соединений в различных реакций окисления, где они выступают в качестве окислителей4. Пиридина N-оксидов и многие из их производных, кольцо функционализированных периодических молекул биологически активных и фармакологических агентов5, и ясно пространственного распределения разными средствами спектроскопических был создан для некоторых из них6,7. В исследованиях на присоединение различных групп в кольцо пиридина Ученые испытали различные методологии для производства простым и обычным методом, поскольку isoxazolines требует каталитического количества базы таких дБу в кипящей ксилола в форме 6- заменить-2-aminopyridine N-оксиды8,9. Целый ряд производных пиридина были преобразованы в их соответствующих N-оксидов в присутствии катализатора количество марганца tetrakis(2,6-diclorophenyl) порфирина и аммония ацетат CH2Cl2/ч3 CN8,10. Другие пиридинов окисляются до их оксидов, используя H2O2 в присутствии каталитических количеств methyltrioxorhenium8,11, или путем добавления избыточных dimethyldioxirane CH2Cl2 при 0 ° C, что приводит к соответствующим N-оксиды8,12,,1314. Бис (триметилсилиловые) пероксид в присутствии trioxorhenium CH2Cl2 был использован для синтеза пиридина N-оксиды8,11. Синтез aminopyridine N-оксиды, с участием ацилирование, используя Каро кислота (peroxomonosulfuric кислота) был также сообщила8. Тем не менее методология, сообщили здесь, и которая использует частью методологии, сообщила Отиай1, дает очень хорошие результаты с использованием более дешевых и доступных реагентов, H2O2 и уксусной кислоты кристаллизированной. Эта практика является более подходящим для использования в больших масштабах препараты, которые действуют на третичных аминогрупп, она производит хорошие урожаи в реакции, которая требует только 30% перекиси водорода и уксусной кислоты кристаллизированной в температуре 70-80 ° C, и он использует процесс очистки Это доступно в большинстве лабораторий синтез как дистилляция, без использования катализатора или дороже реагенты1. Литература сообщает, что другие методологии также часто связаны сроки от 10-24 h и температурах выше 100 ° C 4,8, и доходность сформирован кристаллов для рентгеновского анализов редко сообщается.
Реактивно различные N -оксидов производных используются должным образом активировать lutidine кольцо, нуклеофильного или электрофильное способом. Реакции нуклеофильного или электрофильное фактор зависит от фторсодержащими заместителями. С кольцом пиридина, электрон снятия группы основным фактором является нуклеофильного характерные1. Бесплатные N-оксид соединений редко изолированы как подходящие кристаллы для рентгеноструктурного анализа из-за делокализованных заряд в ароматическое кольцо. Однако сольватация фактор имеет решающее значение для стабилизации негативные плотность кислорода15.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. реакция
- Место в Зонта открыт круглый 100 мл флакон с 0,5 моль (29,8 мл) Ледниковая укусная кислота и добавить 0,051 моль (5.82 мл) 3,5-dimethylpyridine и 5 мл, H2O2 (35%). Храните смесь реакции при постоянном помешивании магнитные, при внутренней температуре 80 ° c за 5 ч.
- После времени реакции прохладный колбу до 24 ° C со льдом (ДУ не подвергайте уксусной кислоты газов на лед) и подключите его к блоку высокой вакуумной дистилляции для 90-120 минут для удаления избыточных уксусной кислоты.
Предостережение: Не используйте горячего материала. Подождите, пока посуда достигает управляемой температуре. Это также позволит избежать ввода в верхней части блока перегонки паров. - Добавьте дистиллированную воду (10 мл) дважды, чтобы обеспечить удаление следов уксусной кислоты и сконцентрировать смесь много как можно скорее.
2. основности перестройки и добыча
- Растворяются в би дистиллированной воды изолированных вязкой и прозрачной продукт и использовать потенциометр для настройки pH до 10 с чисто твердых Na2CO3.
- Осторожно поместите решение в воронку разделения 250 мл и распакуйте его в 5 раз с 250 мл3 КХКЛ для повышения урожайности. Восстановить органический слой и высушить его над твердых Na2так4 за 30 минут максимум, который будет содержать продукт. В случае необходимости, повторно извлечь водяной участок с нужное количество КХКЛ3.
Предупреждение: КХКЛ3 может вызвать сонливость и головокружение; ручка с осторожностью и внутри зонта. - Удаление растворителя под пониженным давлением с высокой вакуумной дистилляции единицы, до формирования очень гигроскопичные ясно бежевый кристаллический порошок (70%).
3. кристаллизации процесс
- Растворите 4,3 г кристаллического порошка в 50 мл холодного высокой выполненных жидкостной хроматографии (ВЭЖХ) класс диэтиловом эфире. Фильтр вакуумный решение для удаления следов твердых исходного материала или даже пыль. Налейте стакан Петри фильтрата, оставляя его медленно испаряется при 4 ° C в лаборатории холодильник.
- Убедитесь, что после двух дней, были получены четкие бесцветные кристаллы. Затем измеряют плавления, которая должна быть в диапазоне от K. 310-311
4. Анализ 3,5-Lutidine N -оксид Dehydrate
- Удаление кристаллов, которые образуются, призматической формы и бесцветно, декантации от стен колбу для дальнейшего рентгеноструктурного анализа. Если используется не сразу, сохранить кристаллы в диэтиловом эфире избежать кристалл гидратации.
- Растворите 0,010 g 3,5-lutidine N -оксида обезвоживает в 0,4 мл CDCl3 для выполнения1 H ЯМР и анализа13 C, чтобы доказать эффективность процедуры.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
Протокол является по существу продолжением Отиай в метод1. Однако применяются более низкой температуры и меньше времени. Этот простой метод может использоваться для получения универсальный лиганд, который является замещенных пиридина N-оксидов производных. Чтобы подтвердить создание 1, ЯМР 1Ч и 13C анализ предпочтительны для проверки эффективности процедуры.
Химический сдвиг демонстрирует формирование 1. Сигнал на 2,28 ppm (частей на миллион) соответствует шести эквивалентных водороды две группы метила в позициях 3 и 5, которые воспринимают магнитное поле в меньше доли чем постоянного магнитного. Существует два набора septuplets: одна принадлежит к протона в положении c на 7,9, который удваивается размер сигнала на 6,9, который принадлежит протона в положение а., рис. 1 показывает химические сдвиги спровоцирован присутствием bonde атом кислорода d на атоме азота пиридина кольца. Атом кислорода-электро снятия и ближе атомы водорода с атомом кислорода (c и) шоу перемещения на более высокой частоте, чем для метил водороды (b).
Тот же процесс строится для NMR спектр 13C, рис 2, где сигналы для углей ближе к атому кислорода (c и) показывают частота разделения между их сигналы Δc = 1300 Гц и Δ = 200 Гц. Еще раз метил угли не показывают каких-либо изменений. Чтобы увидеть успех метода также может использоваться ИК спектра.
ORTEP диаграммы, Рисунок 4, демонстрирует наличие двух молекул воды, окружающие асимметричного молекулы. Считается, что эти молекулы стабилизировать N-O Бонд. В подобных случаях, он был описан для пиридина N-оксида и связанных с ними ароматических оксидов. Существует значительный стабилизации π-типа O→N обратно пожертвование, отражение в вычисляемых облигаций порядка выше, чем 1 и ряд одинокий пар электрона на O атома ниже 36.
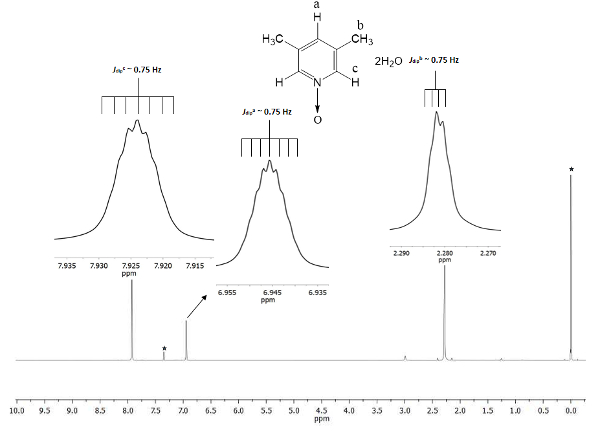
Рисунок 1 . TMS ссылки на CDCl3 в 1H 500 МГц NMR спектр 1. Интеграция и химические сдвиги трех сигналов согласны с тремя различными типами атомов водорода в lutine N-оксида. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
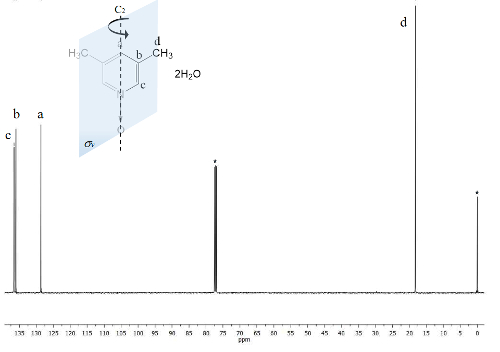
Рисунок 2 . TMS ссылки на CDCl3 13C 100 МГц NMR спектр 1. Три сигналы наблюдаются для пяти ароматических углеродов и один для двух метильных групп. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
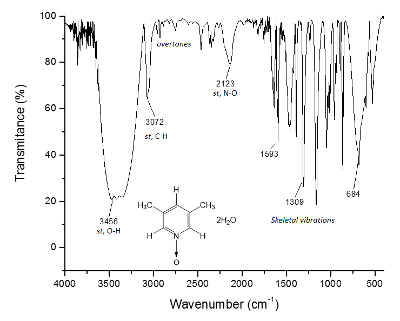
Рисунок 3 . Инфракрасный спектр 1. O-H-Облигации, выше 3300 см-1, отвечают за формирование супрамолекулярные структуры и формирования кристалла. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 4 . Диаграмма 1, где две молекулы H2O форм мост водородных связей с lutidine с кислородом, вождение их атомы водорода к атому кислорода ORTEP. Эта цифра была изменена от Мерино Гарсия и др. 12 Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.

Рисунок 5 . Картины из кристаллов подходящих рентгеновской дифракции 1 в диэтиловом эфире (вверху) и на открытом воздухе (внизу). Один из этих кристаллов был подтвержден в рентгеновский дифрактометр и показал путь дифракции рентгеновских, который был traduced и уточнены специальные вычислительные программы в молекулярной и кристаллические структуры24,25, 26,27,28. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
Протокол, представленные здесь является обычный метод, чтобы связать атом кислорода с атомом азота 3,5-lutidine как метод функционализации субстратов. Этот метод также хорошо установленных приносить рентгеновского подходит сушеные кристаллов (рис. 5, фотографии, сделанные с помощью камеры Sony DSC-HX300 Cyber-shot). Насколько мы обеспокоены тем, не во многих докладах описал производства таких кристаллов16. Многих соединений растут идеально кристаллы для рентгеноструктурного анализа, когда они хелатные различных металлов17,18,19,20. После того, как образуется кристаллический порошок, важно извлечь его из их мать ликеры с помощью Китасато колбу и воронку Buchner. С помощью резиновых шлангов, настой Китасато подключен к вакуумной линии и поверх него воронка по Buchner помещается с фильтровальной бумаги. После того, как был включен вакуум, фильтровальная бумага, смоченным небольшое количество растворителя, из которых кристаллизуется продукта. Это предотвращает сочащийся в воронку Buchner вакуумным эффектом кристаллический порошок. После обеспечения фильтровальная бумага, раствор, содержащий кристаллический порошок потрясен обеспечить все кристаллического порошка фильтруется, и никто не остается в нижней части колбы. Решение быстро поливают Buchner воронку. Кристаллический порошок получен осталось около 10 мин на фильтровальной бумаге и затем Пылесос выключен и кристаллический порошок отсоединяется от бумаги и хранится в непрозрачного стекла флакона, помечены с его кодом и хранится при температуре 4 ° C до дальнейшего анализа. Фильтрующейся жидкости наливается в стакан Петри, оставляя медленно испарения при 4 ° C для улучшения формирования адекватных кристаллов для рентгеноструктурного анализа.
Важно заметить, что этот протокол использует растворителей и материалы, которые легко достижимы и обычно встречаются в любой исследовательской лаборатории. Корректировка уровня pH путем добавления Na2CO3 и последовательного перемешивания магнитные имеют решающее значение для выхода конечного продукта. Однако важно уделять внимание осторожны всех этапов процесса, особенно в стадии добычи, где никаких следов исходный материал должен присутствовать позволить формирование кристаллический порошок и впоследствии кристаллов. Таким образом этот этап извлечения/очистки может контролироваться ЯМР или ИК спектроскопии для обеспечения качества продукции.
Чтобы обеспечить воспроизводимость этого протокола, ЯМР является отличным инструментом. В спектре видны даже мельчайшие детали. Все сигналы отображаются как вкладки на рисунке 1. Эти вставки изображают четко раскола, а именно многообразие, всех сигналов. Например, b протонов (Jdipb ~ 0.75 Гц) Показать четыре пики на гребне сигнала, с разделением среди них тошноту константа (пик пикΔ) ~ 0,0075 ppm. 0,0075 ppm могут быть преобразованы в энергии, используя следующее уравнение21
 Уравнение 1
Уравнение 1

Преобразование рекомендуется, потому что сигналы разворачивается от двухполюсные пространственного взаимодействия между тремя водороды ядра метильной группы, и даже несмотря на то, что они дальше, чем 4 одной облигации с протонами c и a, они способны воспринимать их взаимодействие двухполюсные магнитного импульса22. Кроме того свободный Сигма, склеивание вращение в метильной группы позволяет супер дескриптивное Протон протонного взаимодействия видимы в кратности сигнала. Septuplets протоны и c на 6,9 и 7.9 ppm, соответственно являются производными от же двухполюсные природный феномен. В этих случаях, протоны и c можно дифференцировать протонов в метильной группы для же динамическое вращение. Последние, как ожидается, рассчитанных Jкупанием , b, и c имеют почти одинаковые значения, ~ 0.75 Гц. Эти количества взаимодействий подтверждают spatial расположения ядер водорода на протяжении магнитной анизотропии.
С другой стороны C-2v симметрии 1 делает эквивалентные углей23. 13C спектр, Рисунок 2показывает типичный сигнал метильных групп, придает ароматических колец, d углей на 18 млн. Кроме того, сигнал на 129 ppm виден в этот регион из-за менее электроотрицательных элемент влияние углерода. На высоких частотах сигнала для более подвергаются ядер атомов углерода к магнитному полю, представлены на 137 ppm22.
Представлена методика является очень полезным для синтеза пиридина N-оксиды, обеспечивая хороший урожай, в разумные сроки с мягкой реакции условий и дешевых и легко доступных реагентов, которые не требуют дополнительных катализаторов. Эти условия могут использоваться для научных и образовательных сообщества получить широкий спектр пиридинов N-оксидов в качестве прекурсоров для других молекул интерес. Подходящей методологии дает возможность приобрести основные экспериментальные и концептуальные инструменты в учебных лабораториях для студентов, доказав успешный синтез соединений и счастье увидеть формирование кристаллов. Однако важно подчеркнуть, что, как любой химической реакции, это необходимо принимать все меры предосторожности, поскольку обычно используются реагенты являются опасными.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Все авторы заявляют никакого конфликта интересов.
Acknowledgments
Настоящая работа была поддержана Vicerrectoría де инвестигасьон и Posgrado de Estudios BUAP, разглашение науки и проектов № REOY-NAT14, 15, 16-G. HEAS-NAT17. RMG КОНАСИТ (Мексика) благодарит за стипендию 417887.
Materials
| Name | Company | Catalog Number | Comments |
| 3,5-lutidine | Sigma-Aldrich | L4206-500ML | |
| Glacial acetic acid | Fermont | 3015 | |
| Hidrogen peroxide (35%) | Sigma-Aldrich | 349887-500ML | |
| Na2CO3 anhydrous | Productos Químicos Monterrey | 1792 | |
| Na2SO4 anhydrous | Alfa reactivos | 25051-C | |
| CHCl3 | Fermont | 6205 | |
| Ethyl eter | Mercury Chemist | QME0309 | |
| Distilled water | Comercializadora Química Poblana | not-existent |
References
- Ochiai, E. Recent Japanese work on the chemistry of pyridine 1-oxide and related compounds. J. Org. Chem. 18 (5), 534-551 (1953).
- Solomons, T. W. G. Organic Chemistry 2nd Edition. , John Wiley & Sons. 1110 (1976).
- Albini, A., Pietra, S. Heterocyclic N-Oxides. , CRC Press. ISBN: 0849345529 328 (1991).
- Koukal, P., Ulc, J., Necas, D., Kotora, Heterocyclic N.-Oxides. Topics in Heterocyclic Chemistry. 53, 29-58 (2017).
- Wen-Man, Z., Jian-Jun, D., Xu, J., Jun, X., Huan-Jian, X. Visible-Light-Induced C2 alkylation of pyridine N.-oxides. J. Org. Chem. 82 (4), 2059-2066 (2017).
- Merino García, M. R., Ríos-Merino, F. J., Bernès, S., Reyes-Ortega, Y. Crystal structure of 3,5-dimethylpyridine N-oxide dihydrate. Acta Cryst. 72 (12), 1687-1690 (2016).
- Sarma, R., Karmakar, A., Baruah, J. B. N-Oxides in Metal-Containing Multicomponent Molecular Complexes. Inorg. Chem. 47 (3), 763-765 (2008).
- Youssif, S. Recent trends in the chemistry of pyridine N-oxides. ARKIVOC. 2001, 242-268 (2001).
- Chucholowski, A. W., Uhlendorf, S. Base catalyzed rearrangement of 5-cyanomethyl-2-isoxazolines; novel pathway for the formation of 2-aminopyridine N-oxides. Tetrahedron Lett. 31 (14), 1949-1952 (1990).
- Thellend, A., Battioni, P., Sanderson, W., Mansuy, D. Oxidation of N-Heterocycles by H2O2 Catalyzed by a Mn-Porphyrin: An Easy Access to N-Oxides Under Mild Conditions. Synthesis. 1997 (12), 1387-1388 (1997).
- Copéret, C., Adolfson, H., Tinh-Alfredo, V. K. h, Yudin, A. K., Sharpless, K. B. A simple and Efficient Method for the Preparation of Pyridine N-Oxides. J. Org. Chem. 63 (5), 1740-1741 (1998).
- Ferrer, M., Sánchez-Baeza, F., Messeguer, A. On the preparation of amine N-oxides by using dioxiranes. Tetrahedron. 53 (46), 15877-15888 (1997).
- Adam, W., Briviba, K., Duschek, F., Golsch, D., Kiefer, W., Sies, H. Formation of singlet oxygen in the deoxygenation of heteroarene N-oxides by dimethyldioxirane. J. Chem. Soc. Chem. Commun. 1995 (18), 1831-1832 (1995).
- Murray, R. W., Singh, M. A Facile One-Step Synthesis of C-Arylnitrones Using Dimethyldioxirane. J.Org.Chem. 55 (9), 2954-2957 (1990).
- Kim, S. W., Um, T., Shin, S. Brønsted acid-catalyzed α-halogenation of ynamides from halogenated solvents and pyridine-N-oxides. Chem. Commun. 53 (18), 2733-2736 (2017).
- Campeau, L., Rousseaux, R., Fagnou, K. A solution to the 2-pyridyl organometallic cross-coupling problem: regioselective catalytic direct arylation of pyridine N-oxides. J. Am. Chem. Soc. 127 (51), 18020-18021 (2005).
- Gang, L., et al. Metal-free methylation of a pyridine N-oxide C-H bond by using peroxides. Org. Biomol. Chem. 13 (46), 11184-11188 (2015).
- May, D., Nyman,, Hampden-Smith, M. J., Duesler, E. N. Synthesis, characterization, and reactivity of group 12 metal thiocarboxylates M(SOCR)2Lut2[M) Cd, Zn; R ) CH3, C(CH3)3; Lut ) 3,5-Dimethylpyridine (Lutidine)]. Inorg. Chem. 36 (10), 2218-2224 (1997).
- Cho, S. H., Hwang, S. J., Chang, S. Palladium-Catalyzed C-H Functionalization of Pyridine N-Oxides: Highly Selective Alkenylation and Direct Arylation with Unactivated Arenes. J. Am. Chem. Soc. 130 (29), 9254-9256 (2008).
- Ide, Y., et al. Spin-crossover between high-spin (S = 5/2) and low-spin (S = 1/2) states in six-coordinate iron(III) porphyrin complexes having two pyridine-N. oxide derivatives. Dalton Trans. 46 (1), 242-249 (2017).
- Drago, R. S. Physical Methods in Chemistry. , Saunders College Publishing USA. 750 (1977).
- Cervantes-Mejía, V., et al. Branched Polyamines Functionalized with Proposed Reaction Pathways Based on 1H-NMR, Atomic Absorption and IR Spectroscopies. American Journal of Analytical Chemistry. 5 (16), 1090-1101 (2014).
- Huheey, J. E., Keiter, E. A., Keiter, R. L. Inorganic Chemistry: Principles of Structure and Reactivity, 4th Edition. , Oxford University Press. Mexico. ISBN: 9706131620 1023 (1997).
- Rigaku, CrysAlisPRO. , (2013).
- Sheldrick, G. M. SHELXT - Integrated space-group and crystal-structure determination. Acta Cryst. 71 (1), 3-8 (2015).
- Sheldrick, G. M. Crystal structure refinement with SHELXL. Acta Cryst. 71 (1), 3-8 (2015).
- Sheldrick, G. M. A short history of SHELX. Acta Cryst. 64 (1), 112-122 (2008).
- Macrae, C. F., et al. Mercury CSD 2.0 - new features for the visualization and investigation of crystal structures. J. Appl. Cryst. 41 (2), 466-470 (2008).
- ChemBioDraw Ultra 13. , PerkinElmer. (2013).



