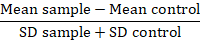Summary
단백질 집계 세포 산화 스트레스 elicits. 이 프로토콜 amyloidogenic 단백질의 세포내 주와 관련 된, cytometry 사용 하 여 산화 스트레스 모니터링 하는 방법을 설명 합니다. 접근은 아 밀 로이드 β 펩 티 드의 가용성과 집계 경향이 이체의 동작을 연구 하는 데 사용 됩니다.
Abstract
단백질 misfolding 및 녹말 체 conformations로 집계 발병 및 여러 신경 퇴행 성 질환의 진행에 관련 되어있다. 그러나, 여전히 약간의 정보는 어떻게 불용 성 단백질에 대 한 집계는 그들의 독성 효과 비보를 발휘. 단순 간결한 및 진 핵 모형 유기 체, 박테리아와 효 모, 등 세포내 녹말 체 형성, 집계 전파 및 독성 뒤에 있는 메커니즘의 우리의 현재 이해에 크게 기여 했다. 이 프로토콜에서 효를 사용 하 여 단백질의 형성 및 세포질 산화 스트레스에 미치는 영향 관계를 해 부 모델로 설명 합니다. 메서드는 amyloidogenic 단백질의 세포내 수용 성/집계 상태 감지 세포 산화 손상 cytometry (FC)을 사용 하 여 식에서 결과의 정량화 결합 합니다. 이 방법은 간단 하 고 빠르며, 양적입니다. 연구는 그들의 각각 고유한 집계 경향으로 아 밀 로이드 β 펩 티 드 이체의 큰 세트에 기인한 세포질 산화 스트레스를 연관 하 여 기법을 보여 줍니다.
Introduction
Proteostasis 셀 체력과 노화 프로세스의 근본적인 결정 이다. 셀, 네트워크는 올바른 refolding misfolded 단백질 conformers의 보호자 또는 그들의 타겟된 베이스로 몇 가지 잘 보존 메커니즘1 보장 하기 위한 정교한 단백질 품질 관리에 의해 단백질 항상성 유지 ,2,3,,45. 연구의 많은 발병과 인간의 질병의 광범위 한 범위와 proteostasis, 단백질 misfolding 및 집계의 실패의 진행 사이의 링크에 지원을 제공 합니다. 예를 들어, 단백질 예금의 존재는 많은 신경 퇴행 성 질환, 알츠하이머병, 파 킨 슨 병, 등, 헌팅턴의 질병6,7,8의 병 적인 특징을 간주 됩니다. prionogenic 질병, 고 퇴행 성 비 amyloidoses9. 그것은 집계 반응에서 초기 oligomeric 및 protofibrillar 어셈블리 붐비는 셀룰러 환경10다른 단백질 들과 탈 선 상호 작용을 설정 하는 세포 독성의 주요 elicitors는 건의 되었다. 또한, 전파 하는 그들의 독성 효과11,12셀 사이의 단백질 포함 (PI)를 전송할 수 있습니다. 따라서, PI의 대형 셀, 어디 처리 될 수 있다 또는 주요 부작용 없이 축적에서 특정 위치에 위험한 집계 된 종의 존재를 제한 하는 해독 메커니즘 구성 실제로 수 있습니다. 수 있습니다. 13 , 14.
표준 체 외에서 생 화 확 적인 접근 집계 반응와 그들의 속성15,16종에 대 한 중요 한 통찰력을 제공 했다. 그러나, 이러한 분석 실험에서 사용 하는 조건 셀 내에 발생 하는 명확 하 게 다른 있으며, 따라서 그들의 생리 적인 관련성 질문. 세포질 통로 단백질 품질 관리, autophagy, 진핵생물19,20,21 중 세포질 산화 환 원 상태17,18 의 규제 등의 주목할 만한 절약 때문에 ,,2223, 신진 효 모 Saccharomyces cerevisiae (S. cerevisiae) 단백질 집단의 분자 결정 요인 연구 특권 간단한 세포 모델 나왔다 그리고 생물학으로 관련 환경24,,2526에 관련 된 세포 독성 영향.
단백질 집계 성향 본질적으로 기본 순서로 인코딩 기능입니다. 따라서, 아 밀 로이드 같은 구조의 형성 예측할 수 있습니다 식별 및 집계 추진의 힘의 평가에 따라 지역 polypeptides27에. 그러나, 예측 단백질 시퀀스의 생체 외에서 집계 속성 bioinformatic 알고리즘의 성공에도 불구 하 고 그들은 여전히 이러한 경향 vivo에서 세포 독성 영향으로 번역 하는 어떻게 예측까지 있습니다. 체계적인 방식으로 주어진된 단백질의 집계 상태 및 그것의 관련 된 세포 손상을 사이 연결 하는 연구는 전산이 한계를 우회 하는 데 도움이 있습니다. 이 연결은 현재 연구, 아 밀 로이드 β 펩 티 드 Aβ42 단일 잔류물에만 서로 다른 하지만 집계 경향 vivo에서28의 연속 범위 표시의 이체의 큰 세트의 활용에서 해결 됩니다. 특히, 구조적 종 효 모 세포에서 집계 하기 쉬운 단백질에 의해 elicited 산화 손상에 대 한 회계를 식별 하는 FC 기반 접근 방식을 설명 합니다. 방법론에는 단순, 높은 처리 능력, 그리고 정확한 양적 측정 등 많은 이점을 제공합니다. 이 방법은 PI 놀이 산화 스트레스에 대 한 보호 역할을 확인 가능 합니다.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1. S. cerevisiae 문화와 단백질 표정
참고: Aβ 변종 전시 Aβ42 펩 티 드 (그림 1A)의 위치 19 (Phe19)에서 단일 잔류물에 돌연변이 인해 다른 상대 집계 경향. 이 펩 티 드 이체는 녹색 형광 단백질 (GFP), 집계 기자 (그림 1)29역할으로 태그 됩니다.
- 플라스 미드 BY4741 부모의 배경 (타 그의3Δ1 레이2Δ0 만난15Δ0 ura3Δ0)30효 모 세포로 20 Aβ42-GFP 변종에 대 한 인코딩 변환. 각 플라스 미드 GSSGSSG 링커에 의해 GFP를 융합 하는 Aβ42 돌연변이 인코딩합니다. 플라스 미드는 pESC(-URA) 이며 선택 가능한 마커 URA329를 포함.
- 다음 구성 요소와 uracil (사우스 캐롤라이나-우 라) 없이 합성 완전 한 매체 준비: 1.9 g/L 효 질소 uracil, 5 g/L 황산 암모늄과 900 mL ddH2O의 기본 20% (w/v) 포도 당 100ml와 결합.
- 2% 포도 당을 포함 하는 SC-우 라 중간의 20 mL로 변형 된 효 모 세포에의 한 식민지를 넣고 하룻밤 동요 210 rpm에서 30 ° C에서 문화를 성장.
- 다음 날, 신선한 SC-우 라 중간의 5 mL에 접종 100 µ L의 숙박 문화에 의해 새로운 효 모 세포 배양 성장.
- 에는 OD590 0.5, 원심 4 분 3000 x g에서 문화, 상쾌한, 삭제 고 resuspend 동일한 양의 신선한 SC-우 라 중 2% 유를 포함 하는 셀.
- 30 분 동안 210 rpm 동요에서 30 ° C에서 품 어. 그리고 4 분 3000 x g에서 세포를 원심는 상쾌한을 삭제 합니다. 재조합 형 단백질 표정 유도 2% 갈 락 토스를 포함 하는 신선한 SC-우 라 매체에 셀 resuspend
- 단백질 표정 2% 갈 락 토스를 포함 하는 사우스 캐롤라이나-우 라 중간에 유도의 16 h 후 4 분 3000 x g에서 원심 분리 하 여 살 균 microcentrifuge 관에 유도 세포의 1 mL를 수확.
참고: 가장 관련성이 높은 차이 발생 후 Aβ42 GFP 변종 표현 16 h. 유도 효 모 세포의 유도 기간 형광 현미경 검사 법 (그림 2B) 셀 안에 재조합 단백질 분포를 결정 하 여 구상 될 수 있다.
2. 세포 얼룩
참고: 신선한 비 유발 세포는 FC 분석 동안 형광 임계값을 설정 하는 부정적인 컨트롤으로 구성 해야 합니다.
- 16 h 유발 효 모 세포를가지고 고 590에서 그들의 광학 밀도 결정 nm (OD590). 0.1의 OD590 를 버퍼링 하는 멸 균 인산 염 분 (PBS)에 그들을 희석.
- 버퍼링 인산 염 분 x 1을 다음과 같이 준비: NaCl, KCl, 나2HPO4, 1.44 g의 0.2 g의 8 g을 추가 하 고 KH2포4 ddH2오의 800 mL의 0.24 g pH 7.4에 조정 후 1 L ddH2O의 솔루션 작성 HCl. 버퍼 0.2 µ m 필터를 통해 필터링.
- 레이블이 표시 된 튜브 (12 × 75 m m 라운드 하단 폴리스 티 렌)을 표현 하는 세포 정지를 전송 하 고 빛에서 그들을 보호. 그들은 비 유도 및 비-얼룩진 셀 함께 분석에 대 한 교류 cytometer에 로드할 준비가 다는 것을 확인 하십시오.
- 5 µ M의 최종 농도에 각 샘플을 (예를 들어, CellROX 딥 레드) 산화 스트레스 프로브를 추가 하 고 어둠 속에서 30 분 동안 30 ° C에 세포를 품 어.
- 부 화, 후 셀 1 x PBS로 3 회 세척 하 고 FC 그들의 분석 전에 버퍼의 동일한 볼륨에 그들을 resuspend.
3. 교류 Cytometry 분석
참고: 적절 한 레이저와 필터는 FC 설치를 사용 하 여 GFP와 산화 스트레스 프로브 형광 신호를 감지. 교류 cytometer GFP의 발견을 위한 488 nm 청색 레이저와 산화 스트레스 프로브 형광의 탐지를 위한 635 nm 빨간 레이저를 사용할 수 있습니다. GFP와 산화 스트레스 프로브 방출 형광의 인수는 각각 530/30 nm BP 필터와 660/20 BP 필터 수행 (표 1).
- 새 워크시트 패널 열기 에 클릭 하 고 다음 인수 점 플롯을 만들.
- 도구 모음에서 분산형 플롯 도구 를 선택 하 고 A를 만들기 음모 쪽 분산형-지역 변수 (SSC-)는 y 축 대 앞으로 피해 지역에 (FSC-A)는 x 축에 선형 눈금에.
- 도구 모음에서 분산형 플롯 도구 를 클릭 하 고 x 축 대에 변수 FL1 지역 (FITC)와 음모를 만들. FL3 지역 (APC)는 y 축에 로그 눈금.
- 악기 설정 아이콘을 클릭 합니다. 보상 탭을 클릭 하 고 모든 보상 수준을 설정 합니다. 인수 탭에서 클릭 하 고 기록 20000 이벤트의 총 수를 선택 합니다.
- 유량 아이콘 낮은흐름 속도 전환 하려면 클릭 합니다.
- 취득 탭 비 유도, 흠 없는 세포 실행 시작을 클릭 하 고 인구 중간 왼쪽 사분면에 배포 될 때까지 측면 분산형 및 앞으로의 악기 설정 에서 전압을 조정 합니다.
- 다각형 아이콘 세포 인구 세포 파편을 제외 하 고 주변 지역 R1 설정을 클릭 하 고이 문이 인구 p 1을 사용 하 여 모든 형광 점 플롯과 히스토그램 표시 (그림 3)에 대 한 R1 =.
- 형광 신호의 PMT 전압을 조정 하려면 셀 낮은 왼쪽된 사분면에 배포 될 때까지 튜닝 악기 설정 탭에서 이득 FL1 FL3 점 플롯에 흠 없는 셀을 실행 합니다.
- GFP 형광을 측정 하는 유도 셀에 샘플을 변경 합니다. 악기 설정 탭에서 인구 오른쪽 아래 사분면에 배포 될 때에는 FSC-A 대 FL1 (FITC) 이득을 설정 합니다. 게이트 (게이트 P2) 긍정적인 세포 인구를 정의 합니다.
- 변경 샘플 비 유발 산화 스트레스는 FSC-A 대 FL3 (APC) 도트 음모에 형광으로 표시 하려면 셀 스테인드. 튜닝 이득 셀 인구는 왼쪽 위 사분면에서 배 부 될 때까지. P3에 긍정적인 세포 인구 게이트입니다.
- 확인을 셀 형광을 나타내는 히스토그램 아이콘 두 히스토그램 플롯 합니다. 형광 강도 나타내는 FL1 (FITC) GFP 형광을 나타내는 x 축, 이며 FL3 (APC) 형광을 나타내는 y에 로그 눈금에 P2 및 P3 인구를 각각 적용 있는지 확인 합니다.
참고: 막대 그래프 오버레이 다른 Aβ 이체를 표현 하는 셀의 형광 프로필 간의 차이 설명 하기 위해 좋은 방법입니다.
4. 재조합 단백질 Immunodetection
- 단백질 표정 수준 결정, 16 h에 대 일 분, 4000 x g에서 원심 분리에 의해 유도 된 효 모 배양 수확을-80 ° c.에 셀 펠 릿 저장
- PBS에 16 h에 대 한 재조합 단백질을 표현 하는 수집 된 셀 resuspend 20의 OD590 를 각 Aβ42 GFP 돌연변이의 200 µ L 셀 정지를 준비 합니다.
- 총 단백질 분수 분석에 대 일 분 14000 x g에서 원심 분리 하 여 각 돌연변이의 100 µ L를 수확 하 고 효 모 세포의 용 해 버퍼 Y의 동일한 볼륨에 셀 펠 릿 resuspend-(50 mM Tris HCl pH 8.0, 1 %DMSO, 200 mM NaCl, 1 mM EDTA 10 mg/mL SB3-14 (myr 포함 된 당 istyl sulfobetaine) 보충 1 m m phenylmethylsulfonyl 불 (PMSF)).
- 온화한 동요에서 실 온에서 20 분에 대 한 샘플을 품 어.
- Bradford 분석 실험을 사용 하 여 단백질 추출 농도 결정 합니다. 15% 아크릴 SDS 페이지 젤 전기 이동 법에 60 분 100 V에서 polyvinylidene difluoride (PVDF) 막에 오 각 샘플의 단백질 추출의 최대 5 µ g를 로드 합니다.
- 브래드 퍼 드 Coomassie 화려한 블루 G-250의 100 밀리 그램으로 시 약 50ml 95% 에탄올에에서 용 해 하 고 85% (w/v) 인산의 100ml를 추가 준비. 다음, 염료 해산 완전히 ddH2O 1 l 혼합물을 희석 하 고 그냥 사용 하기 전에 셀 루 로스 필터 종이 통해 필터링.
참고: 브래드 퍼 드 시 해야 될 빛 갈색. - 소 혈 청 알 부 민 (BSA)의 브래드포드 시 약 1000 µ L에서 단백질의 5-100 µ g에서 배열의 표준 준비.
- 1-10 µ L 단백질의 브래드포드 시의 1 mL에 추출 하 고 품 어 5 분 동안 실내 온도에 혼합물을 추가 합니다.
- 표준과 마약595에서 단백질 추출 물 샘플의 흡 광도 측정 한다.
- 분석을 위해 표준 대에 대 한 얻은 흡 광도 값으로 음모를 확인 합니다. 단백질의 µ g입니다. 표준 곡선에 따라 달라 집니다, 있는 경우 볼륨 및 희석, 고려는 양의 단백질에서 원래 샘플의 농도 결정 합니다.
- 브래드 퍼 드 Coomassie 화려한 블루 G-250의 100 밀리 그램으로 시 약 50ml 95% 에탄올에에서 용 해 하 고 85% (w/v) 인산의 100ml를 추가 준비. 다음, 염료 해산 완전히 ddH2O 1 l 혼합물을 희석 하 고 그냥 사용 하기 전에 셀 루 로스 필터 종이 통해 필터링.
- 린스 Tris 버퍼 염 분 (TBS), x 1 막 0.1% Tween 20 (TTBS), 1 x TTBS의 5% (w/v) 무 지방 건조 우유를 사용 하 여 차단 하 고.
- 10 x TBS의 1 리터를 준비 하려면 기본 트리 스의 24 g와 H2Odd 900 mL에 NaCl의 88 g을 녹이 고 pH 7.6 조정. DdH2O l. 1의 최종 볼륨을 추가 10 x 재고 1 일부 ddH2o.의 9 부분 혼합 1 x 솔루션에 대 한
- 기본 β 아 밀 로이드 항 체 희석 6E10 1:1,000와 함께 1 시간에 대 한 막 품 어 그리고 이차 항 체 염소와 실 온에서 1 h에 대 한 반대로 마우스 IgG HRP 공액 희석 1:10, 000.
- 막 Luminata 형광 시 약의 1 mL를 사용 하 여 개발 및 단계 5.2에서에서 설명한 densitometric 분석 하 여 밴드를 계량 합니다.
5. 데이터 분석
- FC에서 얻은 데이터를 분석 하려면 표시 의미 형광 강도 (MFI) 테이블을 만듭니다와 그 해당 표준 오류 또는 GFP 형광 및 산화 스트레스 수준에 대 한 차이 (CV)의 계수 중간 형광.
- 관리자 탭 및 통계 아이콘 각 채널에 필요한 통계 데이터를 사용자 지정을 클릭 합니다.
참고: 비교할 때 단백질 이체, 접이식 배경 또는 해상도 통계 (RD)에 형광 값 데이터 변환: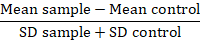
이 통계에서 평균 샘플 문제 샘플의 평균 형광, 평균 컨트롤은 컨트롤을 사용 하는 셀의 평균 형광 이며 SD는 평균 형광의 표준 편차. RD 요소 MFI 값 보다 더 정확한 인덱스는 그것 뿐만 아니라 샘플 뿐만 아니라 데이터의 확산을 위한 계정 사이의 차이 계산 합니다. 이 계산은 시간이 지남에 수행 다른 실험 데이터를 비교 하는 때 특히 적합 합니다. 일단는 RDs를 계산 통계 시험의 사용은 단백질 이체의 관찰 된 차이점의 중요성을 확인 하는 것이 좋습니다.
- 관리자 탭 및 통계 아이콘 각 채널에 필요한 통계 데이터를 사용자 지정을 클릭 합니다.
- 단백질 immunodetection에 대 한 재조합 단백질 수준 서쪽 오 점 ImageJ 소프트웨어를 사용 하 여 계량.
- Densitometry 분석 하기 전에 개발 된 막의 원래 raw 이미지를 JPEG 파일 형식와 회색조 모드 변환.
- 회색값 의미 분석 메뉴의 설정 측정 섹션을 조정 합니다.
- ImageJ에서 사각형 도구를 클릭 하 고 밴드 densitometry 분석에 대 한 일관 된 크기와 관심 (ROI)의 영역을 정의. 만든된 사각형 프레임 안에 막 이미지에 각 밴드 센터 고 측정 Ctrl + M (측정 명령)를 사용 하 여 하나 하나를 기록 합니다.
- 동일한 투자 수익 영역을 적용 하는 각 밴드에 인접 한 로컬 백그라운드를 측정 합니다. 측정 후 각각의 개별 밴드에서 해당 로컬 백그라운드를 뺍니다.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
이 프로토콜 어디 Phe19은 모든 자연 proteinogenic 아미노산28변경 되었습니다 Aβ42 펩 티 드의 20 이체의 컬렉션을 사용 하는 방법을 설명 합니다. 이 단백질의 이론적인 집계 경향 두 다른 bioinformatic 알고리즘 (AGGRESCAN와 탱고31,32)를 사용 하 여 분석할 수 있습니다. 두 경우 모두에서이 분석 집계 추세, ascribing, 일반적으로 높은 값과 가장 낮은 소수 성 잔류물을 충전 하 고 극 지 것의 진보적인 그라데이션 렌더링 (그림 1B, 1c).
실험적으로 다른 Aβ42 이체의 세포내 집계 상태를 추적 하기 위해 설명된 실험 플라스 미드, Aβ42에 대 한 인코딩 및 갈 락 토스를 유도할 수 있는 GAL1 통제 GFP (그림 1A) 융합의 변화 필요 S. cerevisiae으로. 16 h의 유도 기간 후 Aβ42 이체를 표현 하는 효 모 세포 형광 현미경으로 구상 될 수 있다. 이 시각화 분석된 컬렉션에서 20 이체에서 10에서 파이의 형성을 확인 가능 하 게. 수와 크기는 형광의 다 변형에서 variant (그림 2). 그림 2A 각각 두 개의 독립적인 문화의 500 셀의 총에서 PI 정량화를 보여줍니다. 여기, 우리는 우수한 계약 사이 예측을 관찰할 수 있다 및 집계 속성 vivo에서 .
단백질의 형성이 모델 셀 시스템에서 산화 스트레스를 실행할 수 있는지 여부를 해결 하기 위해이 프로토콜을 사용 하 여 FC 셀룰러 GFP 형광 반응 산소의 지표로 서 fluorogenic 프로브의 형광 함께 모니터링 종 (선생님) 생산입니다. 그림 3 와 균질 분산 및 PI 형성 Aβ42 이체에 각각 해당 Gln 및 Ile 돌연변이 대 한 결과 얻은 절차를 보여 줍니다.
첫째, 분석된 셀 인구는 FSC-A 대 SSC A 점에 게이트 (P1) 플롯 분석 (그림 3A)에서 암 세포를 제거 하. P1 인구의 산화 스트레스 조사 대 GFP의 형광 신호 녹색 형광 세포 P3에 문이 점 플롯 그래프에 표시 됩니다 (그림 3B). 그림 3C 와 3D 이력서 (표 2)를 포함 하 여 평균 및 각 형광 성 감 적의 메디아 형광을 측정 하기 위해서는 각 표현된 변종에 대 한 통계 데이터를 생성 하는 히스토그램을 표시 합니다.
모든 돌연변이 그들은 단일 아미노산 (Aβ42-GFP 시퀀스의 0.02%)에 차이가 있기 때문에 동일한 수준에서 표현 될 것으로 예상 된다. 그러나, proteostasis 기계는 그들의 특정 집계 경향에 차동 방식으로 응답할 수 있습니다. 따라서, 세포 추출 물에 단백질 표정 수준 Aβ 특정 항 체 (그림 4)를 사용 하 여 정량은. 우리는 일반적인 경향으로 PI 형성 Aβ42 이체는 존재는 cytosol에 균질 분산 된 나머지 그 보다 낮은 수준에서 참조 하십시오.
Aβ42 변종 간의 중요 한 차이점은 그들의 산화 스트레스 프로브 형광, 단백질 수준, 그리고 GFP 형광 속성 PI와 그들의 본질적인 집계 경향 ( 를 형성 하는 그들의 기능을 기준으로 표시 됩니다 때 관찰 될 수 있다 그림 5). 더 많은 집계-경향이 PI 형성 변형 유도 더 녹는 들 (그림 5A, 5B) 보다 훨씬 낮은 산화 긴장. 이러한 결과 크기와 개별 셀 (그림 2)와 산화 스트레스 레벨 당 집계 수 사이 분명 한 상관 관계가 있다. PI 형성 변형, 특히 돌연변이 위치 19, Trp와 페 베어링 homogenously cytosol (그림 5C, 5d)에 배포 하는 보다 낮은 수준에서 셀에 있습니다. 이 예외는 Thr 돌연변이, 세포의 10% 미만 PI를 형성 (그림 1B, 1c). 이 누 룩 품질 관리 저하 기계28에 의해 가장 집계 경향이 변종 지워집니다 선택적으로 사실와 일치 합니다. GFP 형광 단백질 수준과 상관 더 수용 성 Aβ42 형태에 대 한 잘 하지만 그 파이 (그림 5E, 5 층)을 형성. 이것은 아마도 이러한 세포 인구에 있는 형광에서 나온 두 개의 서로 다른 구획는 cytosol와 포함, 및 그들의 상대적 기여 총 형광 돌연변이34간에 차이가 있기 때문에.

그림 1 . Aβ42-GFP 융해 구성의 컬렉션에 대 한 집계 성향 분석 모든 자연적인 아미노산에 의해 위치 19 Aβ42 펩 티 드에 잔류물의 돌연변이에서 파생 된. A.이 이미지 링커 (Aβ42, 회색; 여 GFP를 wt Aβ42 융합의 3D 모델을 보여줍니다 GFP, 녹색), Aequorea 빅토리아 에서 녹색 형광 단백질에 대 한 PDB 1EMA 및 알 츠 하이 Aβ 펩 티 드 Phe19 사이드 체인 wt Aβ42의 빨간색으로 표시 됩니다에 대 한 2OTK에 따라. 모델은 Pymol 소프트웨어를 사용 하 여 만들어집니다. Aβ42 시퀀스에서 잔류물 19 중앙 소수 클러스터에서 중심 위치를 차지합니다. 두 명의 다른 bioinformatic 예언자를 사용 하 여 만든 막대 그래프: B. AGGRESCAN, C. 탱고. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 2 . 변종 Aβ42 GFP PI 형성 S. cerevisiae 문화 16 h 식의 유도. A. 막대 그래프는 PI 2 생물 복제에 각 변형에 대 한 500 형광 세포의 총에서 계산의 다른 숫자 포함 된 셀의 비율을 나타냅니다. B.이 이미지는 선택 된 Aβ42 GFP 변종 (Phe, Ile, Thr, Trp)의 대표적인 형광 현미경 이미지. 그들은 GFP (450-500 nm) 및 방출 범위 (515-560 nm) 여기 필터를 사용 하는 UV 빛에서 취득 했다. 눈금 막대를 나타냅니다 10 µ m. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 3 . 교류 cytometry (FC) 분석 o에 대 한 계획f S. cerevisiae 세포 선택한 Aβ42 GFP 이체를 표현. A. 차트 점 플롯 문이 효 모 세포 (P1)에서는 (FSC-A 대 SSC-A) 세포 암 세포 인구에서 제거 됩니다. FC 점 플롯 Gln (균질 분산) 및 일 (PI 형성) 이체의 미세한 이미지 옆에 표시 됩니다. 눈금 막대가 나타냅니다 10 µ m. B 이러한 분산형 점 작 이미지 산화 스트레스 프로브를 GFP A 대 는 문이 인구 (P3)는 배경 신호를 제외한만 형광 셀 포함을 나타냅니다. C셀 주파수 히스토그램입니다. p 1과 D에서 문이 GFP 신호 (FITC 진폭). CellROX (APC 진폭) P3에서 문이입니다. 셀 인수 교류 cytometer 수행 했다. 각 플롯 20000 이벤트를 나타냅니다. Q 고 각각 Gln 및 Ile Aβ42 돌연변이에 해당. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 4 . 세포질 단백질 수준 부 량이 고 이 그림 Aβ42 GFP 뮤턴트의 총 단백질 분수의 서쪽 오 점 S. cerevisiae에 표현의 16 h 후. PI 형성 이체는 녹색으로 표시 하 고 그 만들어진다는 cytosol에서 배포는 빛 빨강으로 표시. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.

그림 5 . 세포질 산화 스트레스, 세포내 GFP 형광, 및 세포의 단백질 레벨에서 표현의 16 h 후 결정 Aβ42-GFP 돌연변이 대 한 S. cerevisiae. X 축에 표시 하는 이체는 AGGRESCAN (왼쪽된 패널) 또는 탱고 (오른쪽 패널)에 의해 그들의 예상된 집계 경향에 따라 주문 했습니다. PI 형성 이체는 녹색으로 표시 하 고 PI 형성 비 이체는 밝은 빨강으로 표시. A. B. 바 그래프 Aβ42 GFP 돌연변이의 FC 분석 하 여 얻은 산화 스트레스 프로브 형광 값을 표시. C. D. 이러한 막대 그래프 ImageJ 소프트웨어를 사용 하 여 서쪽 오 점 densitometry 분석 하 여 정량으로 단백질 수준을 나타내는. E. F. FC 분석 후 GFP 형광 값을 표시 하는 막대 그래프. 산화 스트레스에 대 한 오차 막대 프로브 그리고 GFP 형광 값 FC 문이 셀의 차이 (CV)의 계수를 대표 한다. 단백질 표정 수준에 대 한 오차 막대 대표 ± SE (n = 3). 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
| 채널 | Fluorophore | 여기 파장 (nm) | 밴드 패스 필터 |
| FITC | GFP | 488 | 530/30 |
| APC | CellRox | 635 | 660/20 |
| PerCP | IP | 488 | 585/42 |
표 1입니다. 레이저 소스, 대역 통과 필터 및 fluorophores 교류 cytometer에서 사용.
| GFP 형광 | 이력서 | CellROX 형광 | 이력서 | |
| A | 9316 | 96.4 | 1964 | 127.5 |
| C | 9709 | 91.9 | 1275 | 172.2 |
| D | 11213 | 101.7 | 3443 | 155.8 |
| E | 12256 | 101.1 | 3220 | 152.2 |
| F | 3010 | 96.1 | 1245 | 146.4 |
| G | 11541 | 97.2 | 2947 | 158 |
| H | 7895 | 98.2 | 3582 | 120.8 |
| 난 | 7365 | 97.2 | 1416 | 141.3 |
| K | 10839 | 100.4 | 3102 | 122.1 |
| L | 7605 | 96.9 | 1401 | 161.8 |
| M | 8149 | 96 | 1308 | 170.4 |
| N | 12741 | 97.5 | 3403 | 134.9 |
| P | 9768 | 102.8 | 2629 | 143.6 |
| Q | 13066 | 91.3 | 3354 | 169.9 |
| R | 8537 | 101.3 | 2839 | 127.5 |
| S | 12053 | 99.1 | 3313 | 174.3 |
| T | 10615 | 97.7 | 2213 | 107.7 |
| V | 9169 | 96.1 | 1878 | 121.7 |
| W | 1715 | 94.7 | 1531 | 100 |
| Y | 7574 | 94.5 | 1234 | 138 |
표 2. GFP 형광 및 산화 스트레스 프로브 형광 16 헤에 대 한 Aβ42 GFP 돌연변이 표현 하는 효 모 세포의 FC 분석 하 여 얻은 값의 목록 이 표에서 평균 형광 강도 (MFI) 및 각 돌연변이 대 한 이력서.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
다양 한 질병 세포 예금6,,78,33으로 misfolded 단백질의 축적에 연결 된다. 많은 노력 계정 단백질 농도를 고려 하지 않습니다, 계산 방법을 사용 하 여 이러한 질병의 발병을 트리거하는 분자 메커니즘을 해명 되었습니다 또는 생체 외에서 접근, 어떤 단백질 농도 반응 동안 상수 남아 있습니다. 그러나, 셀, 내 단백질 지속적으로 합성 되며 혼잡과 비 균질 환경에서 저하. 이 철에, 에서 시험관 및 생체 내에서 집계 속성 사이 amyloidogenic 단백질의 빈번한 불일치를 설명합니다.
왜 간단한 휴대 전화 모델, 효 모, 합리적인 선택 집계를 공부 하 고 더 많은 생물 학적 맥락에서 신경 퇴행 성 질환 관련 단백질의 독성 관련 여러 이유가 있다. 예를 들어, 그들은 우리가 여기 구현 하는 것과 같은 빠른 분석을 사용 하 여 그대로 세포 인구에 단백질 misfolding 집계의 영향을 분석 하는 가능성을 주지. 그러나, 우리는 산화 수준을 효 모 종자 들 다를 수 있습니다 고려해 야 합니다. 따라서, 긴장, 또는 심지어 다른 단백질을 비교, oxidants와 reductants, DTT와 diamine, 사용 되어야 한다 산화/감소 규모를 설정 하.
이 문서, bioinformatic 분석, 세포 단백질 정량화에 나와 있는 예제에서 단백질 지역화 이미징 및 GFP 활동 및 산화 스트레스 레벨의 동시 FC 분석 통합 되어 있는 분자를 식별 하 종 단백질 집계 반응에 의해 elicited 산화 손상에 대 한 책임. 결과 더 수용 성 Aβ42 이체 보다는 더 많은 집계-경향이, 높은 산화 스트레스를 촉진 하는 방법을 보여 줍니다. 이 diffusible 종 되 고 더 위험한 Aβ42 종의 비보를 가리킵니다. 변종 집계의 낮은 독성 단백질 품질 기계, 그들의 가용성의 그것 보다 낮은 단백질 수준에서 발생 하 여 이러한 conformations PI로 압수는 사실 및 그들의 특혜 저하 응답 것 대조 물입니다.
설명된 방법 Aβ42 집계/수용 성 종에 의해 생성 하는 산화 스트레스의 분석에 국한 되지 않습니다 하 고 단백질 집계 장애의 다양 한 연구에 적용 될 수 있습니다. 또한, 기술 추가 임상 응용 프로그램에 대 한 산화 활성 단백질의 축적을 촉진 하는 그 분자를 삭제할 수 있도록 세포 산화 스트레스에 집계 억제제의 효과 모니터링 하는 데 유용할 수 있습니다. 마지막으로, fluorogenic 프로브를 사용할 수로 서는 방법은 정량적 데이터를 제공 하는 쉬운 방법, 빠른에서 단백질 집계에 연결 된 분자 종 다른 독성 효과 대 한 책임을 식별 하는 놀라운 기회 제공 합니다.
Subscription Required. Please recommend JoVE to your librarian.
Acknowledgments
Materials
| Name | Company | Catalog Number | Comments |
| Yeast cells BY4741 | ATCC | 201388 | Genotype: MATa his3Δ1 leu2Δ0 met15Δ0 ura3Δ0 |
| pESC(-Ura) plasmid | Agilent Genomics | 217454 | Yeast expression plasmid with a Gal promotor. Selectable marker URA3 |
| Yeast Synthetic Drop-out Medium Supplements | Sigma | Y1501 | Powder |
| Yeast Nitrogen Base Without Amino Acids | Sigma | Y0626 | Powder |
| Raffinose | Sigma | R7630 | Powder |
| Glucose | Sigma | G7021 | Powder |
| Galactose | Sigma | G0750 | Powder |
| Phosphate Buffered Saline (PBS) | Fisher Scientific | BP3991 | Solution 10X |
| CellROX Deep Red Reagent | Life Technologies | C10422 | Free radical cell-permeant fluorescent sensor, non-fluorescent while in a reduced state, and exhibits bright fluorescence upon oxidation by reactive oxygen species (ROS), with absorption/emission maxima at 644/665 nm. |
| Y-PER protein extraction reagent | Thermo Scientific | 78990 | Liquid cell lysis buffer |
| Acrylamide/Bis-acrylamide | Sigma | A6050 | Solution |
| Bradford dye reagent | Bio-Rad | 5000205 | Dye reagent for one-step determination of protein concentration |
| β-amyloid antibody 6E10 | BioLegend | 803001 | Mouse IgG1. The epitope lies within amino acids 3-8 of beta amyloid (EFRHDS). |
| Goat anti-mouse IgG-HRP conjugate | Bio-Rad | 1721011 | |
| Membrane Immobilon-P, PVDF | Millipore | IPVH00010 | |
| Luminata forte | Merk | WBLUF0100 | Premixed, ready to use chemiluminescent HRP detection reagent |
| Phenylmethanesulfonyl fluoride solution (PMSF) | Sigma | 93482 | Protease inhibitor. Dissolved at 0.1 M in ethanol |
| FACSCanto flow cytometer | BD Biosciences | 657338 | Equipped with a 488 nm blue laser for the detection of GFP, and 635 nm red laser / 530/30 nm BP filter and 660/20 BP filter |
| Mini Trans-Blot Electrophoresis Transfer cell | Bio-Rad | 1703930 | Protein transference system |
| Mini-PROTEAN Tetra Handcast Systems | Bio-Rad | 1658000FC | Electrophoresis system |
References
- Frydman, J. Folding of newly translated proteins in vivo: the role of molecular chaperones. Annual Review of Biochemistry. 70, 603-647 (2001).
- Hartl, F. U., Bracher, A., Hayer-Hartl, M. Molecular chaperones in protein folding and proteostasis. Nature. 475, 324-332 (2011).
- Wong, E., et al. Molecular determinants of selective clearance of protein inclusions by autophagy. Nature Communications. 3, (2012).
- Winkler, J., Tyedmers, J., Bukau, B., Mogk, A. Chaperone networks in protein disaggregation and prion propagation. Journal of Structural Biology. 179, 152-160 (2012).
- Glickman, M. H., Ciechanover, A. The ubiquitin-proteasome proteolytic pathway: destruction for the sake of construction. Physiological Reviews. 82, 373-428 (2002).
- Dobson, C. M. Getting out of shape. Nature. 418, 729-730 (2002).
- Chiti, F., Dobson, C. M. Protein misfolding, functional amyloid, and human disease. Annual Review of Biochemistry. 75, 333-366 (2006).
- Aguzzi, A., O'Connor, T. Protein aggregation diseases: pathogenicity and therapeutic perspectives. Nature Reviews Drug Discovery. 9, 237-248 (2010).
- Rapezzi, C., et al. Transthyretin-related amyloidoses and the heart: a clinical overview. Nature Reviews Cardiology. 7, 398-408 (2010).
- Deas, E., et al. Alpha-synuclein oligomers interact with metal ions to induce oxidative stress and neuronal death in Parkinson's disease. Antioxidants & Redox Signaling. 24, 376-391 (2016).
- Brundin, P., Melki, R., Kopito, R. Prion-like transmission of protein aggregates in neurodegenerative diseases. Nature Reviews Molecular Cell Biology. 11, 301-307 (2010).
- Frost, B., Diamond, M. I. Prion-like mechanisms in neurodegenerative diseases. Nature Reviews Neuroscience. 11, 155-159 (2009).
- Arrasate, M., Mitra, S., Schweitzer, E. S., Segal, M. R., Finkbeiner, S. Inclusion body formation reduces levels of mutant huntingtin and the risk of neuronal death. Nature. 431, 805-810 (2004).
- Ross, C. A., Poirier, M. A. Opinion: what is the role of protein aggregation in neurodegeneration? Nature Reviews Molecular Cell Biology. 6, 891-898 (2005).
- Mishra, R., Sjölander, D., Hammarström, P. Spectroscopic characterization of diverse amyloid fibrils in vitro by the fluorescent dye Nile red. Molecular BioSystems. 7, 1232-1240 (2011).
- Klunk, W. E., Jacob, R. F., Mason, R. P. Quantifying amyloid by congo red spectral shift assay. Methods in Enzymology. 309, 285-305 (1999).
- Khurana, V., Lindquist, S. Modelling neurodegeneration in Saccharomyces cerevisiae: why cook with baker's yeast? Nature Reviews Neuroscience. 11, 436-449 (2010).
- Tenreiro, S., Outeiro, T. F. Simple is good: yeast models of neurodegeneration. FEMS Yeast Research. 10, 970-979 (2010).
- Moosavi, B., Mousavi, B., Macreadie, I. G. Yeast model of amyloid-β and Tau aggregation in Alzheimer's disease. Journal of Alzheimer's Disease. 47, 9-16 (2015).
- Tenreiro, S., Munder, M. C., Alberti, S., Outeiro, T. F. Harnessing the power of yeast to unravel the molecular basis of neurodegeneration. Journal of Neurochemistry. 127, 438-452 (2013).
- Yang, J., Hao, X., Cao, X., Liu, B., Nyström, T. Spatial sequestration and detoxification of huntingtin by the ribosome quality control complex. eLife. 5, (2016).
- Braun, R. J., Büttner, S., Ring, J., Kroemer, G., Madeo, F. Nervous yeast: modeling neurotoxic cell death. Trends in Biochemical Sciences. 35, 135-144 (2010).
- Figley, M. D., Gitler, A. D. Yeast genetic screen reveals novel therapeutic strategy for ALS. Rare Diseases. 1, e24420 (2013).
- Cooper, A. A., et al. Alpha-synuclein blocks ER-Golgi traffic and Rab1 rescues neuron loss in Parkinson's models. Science. 313, 324-328 (2006).
- Johnson, B. S., McCaffery, J. M., Lindquist, S., Gitler, A. D. A yeast TDP-43 proteinopathy model: exploring the molecular determinants of TDP-43 aggregation and cellular toxicity. Proceedings of the National Academy of Sciences of the United States of America. 105, 6439-6444 (2008).
- Bharathi, V., et al. Use of ade1 and ade2 mutations for development of a versatile red/white color assay of amyloid-induced oxidative stress in saccharomyces cerevisiae. Yeast. 33, 607-620 (2016).
- Pallarès, I., Ventura, S. Advances in the prediction of protein aggregation propensity. Current Medicinal Chemistry. , (2017).
- Villar-Piqué, A., Ventura, S. Protein aggregation propensity is a crucial determinant of intracellular inclusion formation and quality control degradation. Biochimica et Biophysica Acta. 1833, 2714-2724 (2013).
- Navarro, S., Villar-Piqué, A., Ventura, S. Selection against toxic aggregation-prone protein sequences in bacteria. Biochimica et Biophysica Acta. 1843, 866-874 (2014).
- Morell, M., de Groot, N. S., Vendrell, J., Avilés, F. X., Ventura, S. Linking amyloid protein aggregation and yeast survival. Molecular BioSystems. 7, 1121-1128 (2011).
- Conchillo-Solé, O., et al. AGGRESCAN: a server for the prediction and evaluation of "hot spots" of aggregation in polypeptides. BMC Bioinformatics. 8, 65 (2007).
- Fernandez-Escamilla, A. M., Rousseau, F., Schymkowitz, J., Serrano, L. Prediction of sequence-dependent and mutational effects on the aggregation of peptides and proteins. Nature Biotechnology. 22, 1302-1306 (2004).
- Renner, M., Melki, R. Protein aggregation and prionopathies. Pathologie Biologie.(Paris). 62, 162-168 (2014).
- Carija, A., Navarro, S., de Groot, N. S., Ventura, S. Protein aggregation into insoluble deposits protects from oxidative stress. Redox Biology. 12, 699-711 (2017).