Summary
Здесь мы представляем тандем массового спектрометрирования-протокол на основе количественного определения часто используемых антибиотиков в интенсивной терапии, а именно Цефепим, меропенем, Ципрофлоксацин, Моксифлоксацин, линезолид и пиперациллин.
Abstract
Существует растущий спрос для терапевтического мониторинга лекарственных препаратов антибиотиков во многих клинических учреждениях, особенно в том, что касается реализации программ антибиотик руководством больницы.
В текущей работе мы представляем мультиплекс высокопроизводительных жидкостной хроматографии тандем масс-спектрометрии (HPCL-МС/МС) протокол для количественной оценки Цефепим, меропенем, Ципрофлоксацин, Моксифлоксацин, линезолид и пиперациллин, часто используемые антибиотики в интенсивной терапии. Этот метод был ранее всесторонне проверяются согласно рекомендации Европейского агентства лекарственных средств.
После очистки быстрой выборки разделены по столбцу ВЭЖХ реверс фаза C8 в течение 4 минут и количественно с соответствующей стабильной меченных изотопом внутренних стандартов в масс-спектрометрии электроспрей ионизации (ESI +) в нескольких реакции согласно время наблюдения (MRM). Представленный метод использует простой инструментарий с единообразных условий хроматографического, позволяя для ежедневных и надежные антибиотик терапевтического мониторинга лекарственных препаратов в клинических лабораториях. Калибровочная кривая охватывает диапазон фармакокинетические концентрации, тем самым включая антибиотик недалеко от минимальной концентрации тормозной (MIC) количества восприимчивых бактерий и пик концентрации (CМакс), которые получаются с болюсным схемы управления. Без необходимости сыворотки разбавления до очистки образца площадь под кривой для управляемых антибиотик можно получить через несколько измерений.
Introduction
Хотя Антибиотики произвели революцию в практике медицины, тяжелые бактериальные инфекции остаются основной причиной заболеваемости и смертности в критических болезней1. В этой связи скорейшего отправления подходит противоинфекционных в адекватной дозировке имеет верхней значение для болезни управления2.
Растущее количество доказательств показывает, что эмпирическое лечение с антибиотиков широкого спектра действия, становится все более проблематичным с учетом сложности популяциях пациентов. Это особенно верно для интенсивной терапии (ОРИТ), где огромные межличностная изменчивость основные фармакокинетические параметры (PK) часто наблюдается3,4. Соответственно СИС пациентов подвергаются риску неминуемой югу терапевтических уровней с опасностью недостаточно терапевтический успех5,6. Потом снова пациенты необоснованно подвергаются чрезмерно высокой концентрации антибиотиков, которые могут привести к серьезным неблагоприятных событий с не клинические преимущества7. Злоупотребление антибиотиками и недостаточности дозирование также подпитывается распространение устойчивости к антибиотикам, который становится растущей угрозой для общественного здравоохранения8.
Для улучшения использования антибиотиков и сохранения их effectivenessas как можно дольше, Всемирная организация здравоохранения запустила глобальный план действий по антибиотикорезистентности в 2015 году9. Антибиотик руководством программы являются важным краеугольным камнем разумного использования антимикробной национального здравоохранения стратегии10, помогая врачам, чтобы значительно улучшить качество ухода за пациентами11 и, в то же время, Снижение резистентности к антибиотикам12. Антимикробной дозирования в отдельных пациентов путем применения лечебного препарата мониторинг (TDM) является ключевым инструментом в этом контексте13.
На сегодняшний день, коммерчески доступных TDM анализы доступны только для гликопептидных антибиотики и аминогликозидов. Количественная оценка веществ других классов обычно требует разработки собственного метода или проверки, которая может быть громоздким. Мы, таким образом, подробно представить протокол для надежной assay массы на основе спектрометрии, который может использоваться для количественного определения наиболее актуальных антибиотиков в СИС в течение их клинических соответствующей концентрации диапазонах14. Метод был недавно создан в нашем объекте, масс-спектрометрия и с тех пор был применен для обычной TDM в СИС. В процедуре используется простой аналитического параметра с единого образца очистки, что позволяет для быстрого осуществления антибиотик TDM во многих учреждениях с возможностями масс-спектрометрии.
Протокол, описанные здесь был оптимизирован для количественной оценки Цефепим, меропенем, Ципрофлоксацин, Моксифлоксацин, линезолид и пиперациллин в сыворотке крови человека, используя изотопного разбавления жидкостной хроматографии (LC) в сочетании с тандем массы спектрометрия (МС/МС). Для изотопного разбавления LC-MS/MS методологии стабильный изотоп меченых соединений добавляются к образцу интерес с матрицей конкретным (например, сыворотка). Меченных изотопом стандартов можно отличить от их немеченого коллегой, а именно аналита интереса, из-за различных молекулярных масс Природные молекулы и продуктов их фрагментации, называют перехода родителя Ион дочь иона. Как изотоп меченых соединений имеют почти идентичные общий физико-химическими поведение, по сравнению с их немеченого коллегой, они являются идеальным внутренних стандартов для MS/MS, позволяя почти матрица независимые аналита количественной оценки с высокой степенью точность15. В настоящее время многие стабильной меченных изотопом внутренних стандартов, которые могут использоваться для количественного определения мелкомолекулярных, включая TDM противомикробных препаратов, коммерчески доступны.
Хроматографическое разделение антибиотик аналитов в протоколе описаны выполняется с аналитической реверс фаза столбец C8-длина алкильной цепи (100 мм х 2,1 мм, 3 мкм-размер частиц). Во время разработки метода внутренний стандарт нормализованных матрица факторов для всех аналитов был между 94,6% и 105,4%, с коэффициентом вариации ≤8.3%14.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
Примечание: Рекомендуется для работы в вытяжной шкаф при обработке органических растворителей, таких, как метанол. Подготовьте все буферы и подвижных фазах в объемная колбах. Если не указано иное, решения может храниться при комнатной температуре до 1 месяца после подготовки.
1. Подготовка калибраторы и контроля качества образцов
Примечание: Соответствующий лист анализа данных для подготовки запасов и Спайк решений приводится в Дополнительный файл. Для обеспечения прослеживаемости вставьте производителя, номер каталога и большое количество каждого антибиотика в соответствующих колонках. Распустить все антибиотики в холодное хранение при температуре 4 ° C и сохранить рабочее время как можно более коротким.
- Подготовка 100 мл 25% метанола в воде: заполнять объемные колбу 100 мл с 25 мл абсолютного метанола и заполнить его до 100 мл дистиллированной водой.
- Подготовка 10 мл 200 мм уксусной кислоты в воде: заполнять объемные флакон 10 мл с 9 мл воды класса ВЭЖХ, 115 мкл уксусной кислоты кристаллизированной (99,5% чистоты, 17,4 М) и Долейте дестилированную воду до 10 мл.
- Подготовка 25 мл 25% метанола в воде с 20 мм уксусной кислоты: заполнять объемные колбу 25 мл с 2,5 мл раствора уксусной кислоты водный 200 мм, добавить 6,25 мл абсолютного метанола и заполнить колбу 25 мл дистиллированной водой.
- Используйте в точности масштабе весить надлежащего количества антибиотиков в 15 мл конические трубы, как описано в Дополнительный файл в столбце начальный вес.
- Подготовка запасов решения фторхинолоны, Ципрофлоксацин и моксифлоксацина в 25% метанола воды, включая 20 мм уксусной кислоты. Для этого, добавьте соответствующий объем взвешенных величин как описано в Дополнительный файл в столбце «окончательный объем». Быстро растворяются фторхинолонов антибиотиков в ультразвуковой ванне на 2 мин и интенсивной vortexing.
- Подготовка запасов решения и Цефепим, меропенем, линезолид, пиперациллин в 25% метанола воды. Чтобы сделать это, добавьте соответствующий объем взвешенных величин, как описано в Дополнительный файл в столбце конечный объем и быстро растворяются антибиотиков по интенсивной vortexing. Растворите меропенем как последнего вещество.
- Объединяйте фондовых решения всех антибиотиков, как описано в таблице соответствующий объем запасов раствора в Дополнительный файл приносить десятикратно концентрированной Спайк решения.
- Спайк девять томов с одного тома десятикратно концентрированной Спайк решений для получения сыворотки калибраторы 0 – 7 сыворотки, свободной от наркотиков и контроль качества (КК) A-D. К примеру добавить 0,5 мл раствора Спайк в 4,5 мл сыворотки в 10-мл полипропиленовые трубы и Инкубируйте 15 мин в холодное хранение при температуре 4 ° C на Роликовый Смеситель на 50 об/мин.
- Использование повторяющихся пипетки для создания 100 мкл аликвоты калибраторы и бок в 1,5 мл полипропиленовые трубы.
- Храните калибраторы, контроль качества и антибиотик акций решения-80 ° c на срок до шести месяцев.
- Для каждого антибиотик также подготовьте изящное решение содержит 1000 мг/Л одного антибиотика. Разбавьте соответствующего Стоковый раствор с соответствующим растворителем (например, для ципрофлоксацина, использовать 25% метанола воды, включая 20 мм уксусной кислоты).
Примечание: Требуются для настройки инструмента аккуратные антибиотик решения только.
2. Подготовка внутренних стандартов микс
Примечание: Внутренние стандарты являются меченных изотопом коллегами аналитов интерес, которые добавляются к образцу во время очистки образца. Как внутренние стандарты имеют практически идентичные общий физико-химических свойств с их коллегами-без названия, они компенсировать матрица эффектов данного образца.
- Подготовка 10 мл 50% метанола в воде, добавив 5 мл абсолютного метанола в колбе 10 мл дрожания и заполнить его до 10 мл дистиллированной водой.
- Подготовка 10 мл 50% метанола в воде, включая 20 мм уксусной кислоты. Чтобы сделать это, добавьте 1 мл уксусной кислоты 200 мм флакон 10 мл, добавить 5 мл абсолютного метанола и заполнить его до 10 мл дистиллированной водой.
- Генерировать акций решения внутренних стандартов (IS) с 1000 мг/Л непосредственно во флаконах, предоставляемых производителем. Растворите Цефепим -13C12D3 сульфат в дистиллированной воде, меропенем D6, линезолид D3и5 пиперациллин D в 50% метанола водный раствор. Растворите ципрофлоксацин D8 в 50% метанола воды с 20 мм ацетат и Моксифлоксацин гидрохлорид -13C1D3 в дистиллированной воде с 20 мм ацетат.
- Комбинат является запасов решения в 1,5 мл полипропиленовые трубы для получения пятикратный сосредоточены внутренние стандартные смеси. 10 мкл Цефепим -13C12D3, 10 мкл меропенем D6, 1 мкл ципрофлоксацин D8, 2 мкл Моксифлоксацин гидрохлорид -13C1D3, 2 мкл линезолид D 3и 10 мкл пиперациллин D5 965 мкл 25% метанола-воды.
- Сохранять внутренние стандартные складе решения и пятикратный концентрированной смеси IS-80 ° c.
3. пациент выборки-хранения
Примечание: Убедитесь, что сыворотке получается максимально быстро и поддержание холодовой цепи замороженных образцов.
- Сбор цельной крови в сыворотке крови коллекции трубок.
- Пусть сгусток крови для 20-30 мин при комнатной температуре.
- Отделите сыворотку от крови центрифугированием в 2000 x g за 10 мин.
- Передать супернатант чистой полипропиленовые трубы.
- Храните сыворотки до шести месяцев при температуре-80 ° C до тех пор, пока он является анализ. Кроме того Храните образцы до 3 дней при температуре-20 ° C.
4. буфер подготовка для хроматографии
- Подготовить 1 М аммония Формиат в воды, растворяют 6.306 g Формиат аммония в 100 мл воды класса ВЭЖХ с помощью 100 мл встряхнуть флакон. Храните решение до 1 месяца при 4 ° C.
- Подготовка мобильного фазы [10 мм аммония Формиат в воды муравьиной кислоты (99.9:0.1 v/v)]. Заполнять 1000 mL объемной колбу с примерно 500 мл воды класса ВЭЖХ, добавить 1 мл раствора муравьиной кислоты и 10 мл 1 М раствора аммония Формиат и заполнить его до 1000 мл с водой класса ВЭЖХ. Передача мобильных этапа A в чистой стеклянной бутылке и подключить его к системе ВЭЖХ. Магазин мобильных этап до 2 недель при комнатной температуре.
- Подготовка этапа мобильных ВЭЖХ класса B. Передача абсолютного метанола в чистой стеклянной бутылке и подключить его к системе ВЭЖХ.
- Использование абсолютного метанола как иглы вымыть растворителем и подключите соответствующие трубки стеклянной бутылке, содержащие подвижная фаза б.
- Генерировать печатью и очистительного растворителя метанола вода муравьиной кислоты (7:92.9:0.1, v/v/v). Заполнять 1000 mL объемной колбу с приблизительно в 500 мл дистиллированной воды, добавить 70 мл абсолютного метанола, 1 мл раствора муравьиной кислоты и Долейте дестилированную воду до 1000 мл. Передача растворителя в чистой стеклянной бутылке и подключить его с системой ВЭЖХ.
Примечание: Различные системы Автоматический пробоотборник использовать как сильной, так и слабых иглы мыть растворителя. В таком случае Подготовьте Вымойте решения согласно рекомендациям изготовителя. Например сильное мыть спиртом метанола воды isopropylic (70:20:10, v/v/v) и слабых мыть с водой метанол (95:5, v/v).
5. инструмент настройки
Примечание: Этот шаг выполняется для установки метода на конкретных масс-спектрометр.
- Разбавьте аналита аккуратные 1000 мг/Л и внутренние стандартные решения 1:10 или 1: 100 в смесь мобильных этапа A и B (50: 50, v/v), в зависимости от интенсивности сигнала детектора. Настроить масс-спектрометр с функцией autotune или сделать ручной настройки для следующих переходы ионов родителей к дочь14: Цефепим (481.0 > 167.0/395.7), Цефепим -13C12D3 (485.1 > 167.1 / 400,0), меропенем (384.1 > 114.0/141.0), меропенем D6 (390.1 > 114.0/147.2), Ципрофлоксацин (332.0 > 231.0/245.0), Ципрофлоксацин D8 (340,1 > 235.1/249.3), Моксифлоксацин (402.0 > 261.0/383.9), Моксифлоксацин13 C1D3 (406.1 > 265.1/388.0), линезолид (338.0 > 235.0/296.0), линезолид D3 (341.1 > 235.1/297.1), пиперациллин (518.0 > 143.0/358.9) и5 пиперациллин D (523.1 > 142.8/364.1).
- Для инструментов с автотюнинг используйте функцию autotune для автоматической настройки напряжения и параметры входа MS через детекторы.
- Для инструментов с ручной настройки, настройки (например, столкновения напряжения и энергию столкновения) до оптимальной (обычно максимум) интенсивность сигнала получается в детектор для каждого родителя и дочь Ион. Например Подключите смешивания теэ, доставить подвижная фаза A и B (50: 50, v/v) 0,5 мл/мин и непрерывно влить аккуратно антибиотиков или внутренний стандарт с расходом 0,1 мл/мин.
6. ВЭЖХ МС/МС Set-up
Примечание: Особенности масс-спектрометр, ВЭЖХ системы (включая автоматический пробоотборник) и соответствующее программное обеспечение, зависит от производителя. Адаптировать параметры масс-спектрометр и мыть процедуры согласно рекомендациям изготовителя.
- Хранить параметры масс-спектрометр в соответствующем 'MS настроить файл '. Использование электроспрей ионизации в положительных режиме (ESI +) для всех аналитов. Адаптировать параметры источника ионов для инструмент используется (например, капиллярные напряжение 1,5 кв, источник температуре 120 ° C, desolvation температуре 400 ° C, скорость потока газа desolvation 600 Л/ч, RF объектив напряжения 0,1 V и продолжительность 80 мс).
- Укажите аналита и внутренних стандартов настройки параметров (например, капиллярные напряжения, энергию столкновения) в 'файл MS'.
- Задать условия Автоматический пробоотборник следующим в 'входного файла ': температура образца при 10 ° C с лимитом ± 5 ° C; мыть последовательности в 1 x продувка мойка червей с 600 мкл продувки объем замены.
- В вышеупомянутом 'входного файла ', набор скорости расхода 0,4 или 0,5 мл/мин, время работы до 4 мин, высокий предел давления до 345 бар и столбец температуру 30 ° C с лимитом ± 5 ° C. Добавьте имя растворителя мобильных этапов A и B и установить их на 7% B/93% A, соответственно.
- Программа хроматографического градиент в 'входного файла ' следующим: 0.00 – 0,10 мин с 7% мобильных фазы B/93% A, 0,11 – 0,60 мин с 65% мобильных фазы B/35% A, 0,61 – 2.10 мин с 95% мобильных фазы B/5% A, 2.11 – 4,00 мин с 7% мобильных фазы а. B/93%
Примечание: Вычислить объем загородный колонки, перепускные объем для инструментальной платформы и исследуемое вещество сохранение факторов, как описано в USP < 621 > хромотографии руководящего принципа16.
7. пример измерения мастер файла
Примечание: С 'пример измерения мастер-файл ', задаются пациента образцы, начал ВЭЖХ-МС/МС анализа и оценки данных выполняется. Создаются два отдельных шаблонов файлов, включая пару контроль низкого и высокого качества; один шаблон включает в себя пару КК A и C, другой один КК пары B и D.
- Создайте новый 'пример измерения мастер-файл '. Выберите вышеупомянутые 'MS настроить файл ', 'файл MS'и «входной файл» (раздел 6), вставьте их в каждой линии образца и укажите объем впрыска с 15 мкл.
- В порядке возрастания, добавьте «образец текста» для калибраторов 0 – 7 и контроля качества (КК) пара кондиционера или КК пара B/D.
- Укажите тип образца. Выберите образец типа «стандарт» для калибраторов и «QC» для контроля качества пар.
- Укажите концентрация каждого антибиотические вещества для соответствующего калибраторы и контроль качества (см. таблицу, концентрация [мкг/мл] Cal 0 7-Cal, QC/c или B/D,).
- Программа «метод оценки данных '. Используйте переходы, которые были оптимизированы в инструмент, тюнинг (раздел 5). Соответствие каждого антибиотика с соответствующим стандартом меченных изотопом (например, меропенем - меропенем D6).
8. Пример очистки и анализа ВЭЖХ МС/МС
Примечание: Для каждого образца пакета, парных контроля качества с низкой и высокой антибактериальной концентрации (КК/c или QC B/D) обрабатывается и анализируется. Между различными пакетами, парными выборками КК используются альтернативные последовательности (например, на день 1, выберите 'пример измерения мастер-файл ' включая КК пара кондиционера; на 2 день, выберите одну пару включая КК B/D. Обработка образцов сыворотки иллюстрируется на рисунке 1.
- Подготовьте агент осадков 10% метил -трет-бутилового эфира в метаноле (составлявшее, v/v) (например, объемные заполнять 25 мл флакон с 2,5 мл метил -трет-бутилового эфира и заполнить его в 25 мл абсолютного метанола).
- Место обратная фаза C8 в столбце камеру. Подключите его к ВЭЖХ и масс-спектрометр в направлении потока.
- Создать список выборки. Откройте соответствующий 'пример измерения мастер-файл ' шаблон и добавьте пациентов образцов, должны обрабатываться в список. Создавать группы до 20 пациентов образцов и фланка их с соответствующей пары контроля качества.
- Влажные премьер HPCL системы с помощью 'входного файла ' управления программное обеспечение: установить функцию «мокрой Прайм» 50% мобильных фазу A/50% B и мокрой премьер 2 мин с расходом 1 мл/мин.
- Обновите шприца. Для этого выполните 6 ударов 600 мкл в программное обеспечение управления.
- Сбалансировать столбце обратная фаза C8. С помощью программного обеспечения, включите потока в 'входного файла ' и промойте его с 7% мобильных фазы B/93% A как минимум 5 минут, используя скорость потока 0,5 мл/мин проверить столбец температуры 30 ° c.
- Оттепель пациентов образцов, один Алиготе калибраторов 0 – 7 и пара контроля качества (или A / B или c/d).
- С повторяющимся пипетки мкл 25 внутренние стандартные смеси 100 мкл калибровочных, КК образца или пациента сыворотки в 1,5 мл полипропиленовые трубы и вихревой трубе на несколько секунд.
- Инкубируйте смесь для 5 мин при комнатной температуре на benchtop шейкер (например, при 1200 об/мин).
- С повторяющимся пипетки добавьте 150 мкл Реагента осадков образца внутренний стандарт микс.
- Опять же вихревой трубки на несколько секунд и Инкубируйте 5 мин при комнатной температуре на benchtop шейкер (например, при 1200 об/мин).
- Центрифуга для подвески на 20000 x g в настольная центрифуга для 10 мин при 4 ° C.
- Разбавляют ВЭЖХ класс воды с помощью стеклянный флакон с микро Вставка супернатант 1:3 и загрузить его как обработанные образцы для Автоматический пробоотборник.
- Вручную запустить анализ ВЭЖХ-МС/МС 'пример измерения управления файла '.
Примечание: Для длительного хранения, тщательно промойте столбце аналитического согласно рекомендации производителя [например, метанол 0,5 мл/мин-воды (50: 50, v/v)], чтобы предотвратить крах фазы.

Рисунок 1: Схематическое изображение образца очистки. Белка осадков в высоких центробежных сил дает плотные гранулы и ясно супернатанта, указывающее что осадков белок была завершена. Все время обработки составляет около 30 мин, включая пример очистки, хроматографического разделения и анализа МС/МС. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
9. Оценка качества и количественная оценка
- Для обработки образцов, откройте соответствующий 'пример измерения управления файла ', выберите калибраторы, контроль качества и пациентов образцов и оценить их с 'метод количественного определения антибиотиков '.
- Проверьте ли пики для конкретных аналита были должным образом интегрированы. Осмотрите вершины для каждого калибратор, КК и пациент образец и вручную их реинтеграции в исходных условий при необходимости.
- Изучить калибровочной кривой и проанализировать ли он выполняет следующие критерии качества: линейность) за весь диапазон, b r2 > 0.995 коэффициент калибровки, c) отклонение каждой калибровки в пределах ± 15% от стандартной Номинальная стоимость, за исключением нижний предел количественного определения (LLOQ), где требуется ± 20%.
- Отклонить калибровки стандарт, не соблюдают вышеупомянутые критерии и переоценку калибровочной кривой, включая регрессионный анализ.
- Изучение качества управления и изучить ли отклонения в пределах ± 15% от номинальной стоимости.
- Если концентрация пациента выборки превышает концентрацию значения наивысшей калибровочной пробы, разбавляют образца с дистиллированной водой, вплоть до 1:5 (например, 100 мкл сыворотки плюс 400 мкл дистиллированной воды) до очистки образца. Reperform шаги 8.8 – 8.14 для этого конкретного образца и запущена его повторная обработка.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
С помощью описанных протокола, типичный Хроматограмма изображен на рисунке 2. Согласно Фармакопеи США (USP) хроматографии рекомендации16, был определен столбец объем в рамках нынешней системы с ~0.22 мл и загородный столбца объем (включая инжектор, шланги и соединители) с ~0.08 мл, давая перепускные объем ~0.30 мл. Вычисляемые удержания факторы для всех аналитов были 2.8 (для Цефепим) - 4.2 (для пиперациллин).
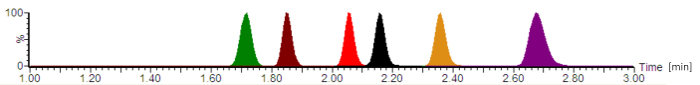
Рисунок 2: типичный аналитических хроматограммы с интенсивностью сигнал нормализованные. Антибиотики элюирующие в следующем порядке: Цефепим (зеленый), меропенем (коричневый), (красный) ципрофлоксацин, Моксифлоксацин (черный), линезолид (оранжевый) и пиперациллин (фиолетовый). Удержания раз, которые приводятся в минутах, и симметрии пик аналита варьируются в зависимости от точный состав мобильных этапов, скорость потока, хроматографии труб и аналитические колонки возраста. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
На рисунке 3A содержит список образец диаграммы для обработанных образцов, включая калибраторы 0 - 7 («Kalibrator 0» - «Kalibrator 7»), контроль качества и пациент сера, которые обозначаются номером инъекции (#); текст идентификации образец (Образец текста); Измеренная концентрация в мг/Л (высококонцентрированные); тип образца, который является пустым, стандарт, контроля качества или пациента образца (тип); Номинальная концентрация калибраторов в мг/Л (Std. Conc); аналитическая удержания время (РТ); ответ, который представляет собой отношение площади пика области аналита/пик IS (ответ); отклонение от значения номинальной концентрации (% Dev); флакон позиция (флакон); и время приобретения (Acq.Time). Параметр key используется для количественной оценки является ответ, постепенно увеличивается с концентрацией исследуемое вещество, из-за постоянное количество добавлен меченных изотопом внутреннего стандарта.
Рисунок 3B показывает калибровочной кривой. В регрессии коэффициент определения r2 должна быть > 0.995. В следующей калибровки модели используется для всех аналитов, описанные в этом методе: Кривый типа = Линейная; происхождения = включена; Вес = 1 / x; Преобразование оси = none. В данном примере, калибровочной кривой и контроль качества выполнения всех критериев качества: r2 > 0.995 для калибровочной кривой и отклонение КК образцов и калибраторы (включая LLOQ) находится в пределах ± 15% от номинальной стоимости.
Измеренной родителей к дочь Ион переходы (MRM) приведены в Рисунок 3 c, показаны четыре пики в то же время удержания: две верхние вершины изображают две переходы, которые измеряются аналита интерес, представляют собой нижней две вершины переходы для соответствующего меченных изотопом внутреннего стандарта. Для оценки качества вершины аналита в окнах времени удержания соответствующих визуально проверены и вручную реинтегрированы в начале исследования, при необходимости.
Минимально ингибирующее концентрация (MIC) является центральным компонентом антимикробной TDM, определяя фармакокинетические экспозиции, которая требуется для достижения целевой фармакокинетические/фармакодинамических (PK/KD) соотношение13,17. Соответственно уровни концентрации антибиотиков TDM цели выражаются применительно к MIC причинных патогенов. Учитывая, что действие бета лактамных антибиотиков зависит от времени, их эффективность максимизируется путем достижения терапевтических концентраций, превышающих MIC-4 x 5 x (fT > 4-5 x MIC). Когда перед неизвестным инфекционных патогенов, целевой корыта диапазон концентраций бесплатно пиперациллин (белок несвязанные) является, таким образом, 64 мг/Л, соответствующий приблизительно 90 мг/Л всего пиперациллин18.
Первый пациент (пример #11) имеет удовлетворительного высокой сыворотки через уровень пиперациллин 83,4 мг/Л, что также является достаточным для проблемы патогены, например синегнойной палочки. Вторым пациентом (пример #12) имеет концентрацию примерно 0,2 мг/л, которая находится ниже низкие калибратора (LLOQ). Возможно пациент восстановился, и администрация пиперациллин было прекращено. Таким образом, результат «< 0,5 мг / Л» сообщается в Больница информационной системы. Третий пациент (образец #13) имеет низкий пиперациллин корыта концентрации только 5,3 мг/Л, что не является достаточным для явное большинство патогенных микроорганизмов. Для эффективного антимикробной химиотерапии дозировку следует увеличить врач.
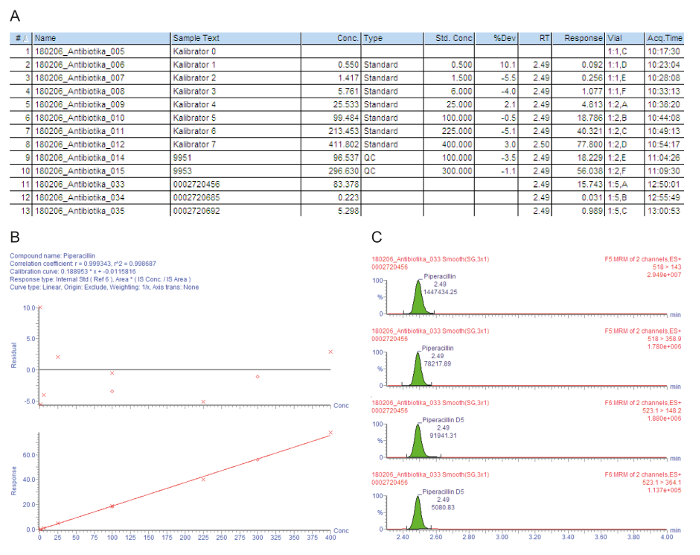
Рисунок 3: образцового качества оценки и количественного определения для аналита пиперациллин. Эти панели представляют собой анализ данных масс-спектрометрии. (A) Эта группа показывает пример списка, включая калибраторы (стандартный, образцы #1 - #8), контроля качества (QC, образцы #9 и #10) и пациент сера (образцы #11 - #13). Калибратор 0 относится к пустым без исследуемое вещество, но с добавлением внутреннего стандарта. 9951 представляет B КК, 9953 представляет КК D. (B) Эта группа показывает Калибровочная кривая для пиперациллин. Процент отклонения от номинального калибратор концентрации уступаны верхнем графике (y-ось: остаточная), нижняя графа изображает диапазон линейной калибровки. (C) Эта группа показывает несколько время реакции, мониторинг (MRM) для пиперациллин и соответствующего внутреннего стандарта пиперациллин D5 для пациента сыворотки образца #12. Двух родителей к дочь Ион переходы представлены с их время удержания и интенсивности соответствующих сигналов. Пожалуйста, нажмите здесь, чтобы посмотреть большую версию этой фигуры.
Дополнительного файла. Пожалуйста, нажмите здесь, чтобы загрузить этот файл.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
В этой рукописи, мы приводим протокол для простой и надежный тандем массы на основе спектрометрия метод количественного определения часто используемых антибиотиков в СИС19, а именно Цефепим, меропенем, Ципрофлоксацин, Моксифлоксацин, линезолид, и пиперациллин14. Таблицу сопровождает рукопись для подготовки антибиотик запасов решений, калибраторы и контроль качества, принимая во внимание чистоте антибиотиков и молекулярный вес их counterions. Учитывая, что концентрации антибиотиков являются довольно высокими, их количественная оценка должна быть не особую проблему с аналитической точки зрения. Соответственно мы уверены, что этот Протокол применяется к различным MS инструментальных платформ. Для метода передачи пользователям предлагается подсчитать объем загородный колонки и перепускные объем их хроматографические системы и адаптировать начала градиента соответственно времени16. Во время настройки метода система также должна быть оценена для переноса, и, при необходимости, пустой образец должны вводиться после высоких калибратор и пациент образцов с высокой концентрации антибиотиков. Пользователи также должны рассмотреть возможность детектор насыщенность, которая возникает, когда слишком много ионов введите тандемные масс-спектрометр. Соответствующие детектор насыщенность могут быть устранены с небольших объемов закачки, выше аналита разрежения во время очистки образца, и/или отстройка целевой исследуемое вещество (например, понижение оптимального напряжения настройки).
В отличие от других методов диапазон калибровки позволяет как количественную оценку концентрации вблизи MIC восприимчивы патогенов, а также пик концентрации (cМакс), которые получаются с болюсным администрацией. C высокийМакс-значения для взрослых сообщается в соответствующих профессиональных информационных бюллетеней на УЛХ наркотиков безопасности базы данных следующим образом: 163,9 мг/Л для Цефепим20, 112 мг/Л для меропенем21, 4,6 мг/Л для ципрофлоксацин22 , 4.1 мг/Л для Моксифлоксацин23, 21.2 мг/Л для линезолид24и 298 мг/Л для пиперациллин25. Антибиотик концентрации мониторинг в циркуляции крови пациента позволяет корректировка дозы на восприимчивость участвующих патогенов, но фармакокинетические площадь под кривой также могут быть получены через несколько проб крови с данного Протокол.
Многие антибиотики (особенно Бета лактамные меропенем) являются химически неустойчивыми раз распущен. Наиболее важным этапом в этот протокол является, таким образом, подготовка запасов решений, калибраторы и контроль качества в холодных условиях26,27. В этом отношении важно как можно быстрее заморозить пациентов образцов. Хотя сыворотки хранения при температуре-80 ° C рекомендуется26, нашей стабильности эксперименты показывают, что образцы также могут быть хранить до 3 дней при температуре-20 ° C без каких-либо значительное уменьшение концентраций антибиотиков (даже на уровне корыта).
Рекомендуется выполнять проверку пригодности системы перед анализом каждой ВЭЖХ-МС/МС пациентов образцов (например, с калибратором 3). Как правило тест пригодности системы используется для проверки воспроизводимости LC-MS/MS системы и посмотреть, если это также достаточным для анализа предстоит сделать. Таким образом например, снижение интенсивности сигнала являются причиной загрязнения конус MS развертки, который, затем, требует его очистки с органического растворителя. Чтобы источник MS в чистоте, отвлечь клапан может быть представлен после столбце хроматографии, направляя «исследуемое вещество free» части мобильных фазы для отходов, прежде чем они достигнут масс-спектрометр. С другой стороны увеличение давления можно указать столбец, засорение со временем. Для увеличения столбце долголетия экономически precolumn фильтра рекомендуется. Если давление по-прежнему является проблемой, скорость потока 0,4 мл/мин могут также использоваться с хроматографического градиент в этом протоколе.
Незначительные ограничением этой методики является, что она требует трех отдельных этапов ручной очистке образца, что приводит к общей сроки приблизительно 30 мин Добавление внутренних стандартов, меченных изотопом агенту осадков может сохранить некоторые время обработки. Однако это должно быть сделано только для высокой пропускной способности дискретизации и с осадками агента хранится в холодном виде (например, при-20 ° C), как внутренние стандарты также деградируют в пробирке при повышенных температурах.
Описывается протокол был разработан для обработки в стандартных 1,5 мл полипропиленовые трубы образца. Для антибиотиков TDM потребуется более высокий уровень пропускной способности, процедура можно обновить формат несколькими хорошо пластины, с помощью адекватных центрифуги вставок или фильтра плиты с вакуумный коллектор.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Авторы не имеют ничего сообщать.
Acknowledgments
Авторы благодарят за его помощь в создании представлен метод доктора Schütze и доктор Zoller за ценный вклад относительно правильной калибровки диапазон. Авторы также признают технический персонал Фонда масс-спектрометрии.
Materials
| Name | Company | Catalog Number | Comments |
| cefepime hydrochloride | Sigma-Aldrich | 1097636 | USP Reference Standard |
| meropenem trihydrate | Sigma-Aldrich | Y0001252 | EP Reference Standard |
| ciprofloxacin | Sigma-Aldrich | 17850 | |
| moxifloxacin hydrochloride | Sigma-Aldrich | SML1581 | |
| linezolid | Toronto Research Chemicals | L466500 | |
| piperacillin sodium salt | Sigma-Aldrich | 93129 | |
| cefepime-13C12D3 sulfate | Alsachim | C1297 | Isotope labelled internal standard for cefepime |
| meropenem-D6 | Toronto Research Chemicals | M225617 | Isotope labelled internal standard for meropenem |
| ciprofloxacin-D8 | Toronto Research Chemicals | C482501 | Isotope labelled internal standard for ciprofloxacin |
| moxifloxacin-13C1D3 hydrochloride | Toronto Research Chemicals | M745003 | Isotope labelled internal standard for moxifloxacin |
| linezolid-D3 | Toronto Research Chemicals | L466502 | Isotope labelled internal standard for linezolid |
| piperacillin-D5 | Toronto Research Chemicals | P479952 | Isotope labelled internal standard for piperacillin |
| methanol | JT Baker | 8402 | |
| HPLC grade water | JT Baker | 4218 | |
| formic acid | Biosolve | 6914132 | |
| acetic acid | Biosolve | 1070501 | |
| ammonium formate | Sigma-Aldrich | 70221-25G-F | |
| tert-Butyl methyl ether | Merck | 101845 | |
| Fortis 3 μm C8 100 * 2.1 mm | Fortis | F08-020503 | |
| Ti-PEEK-encased Prifilter (2 μm) | Chromsystems | 15011 | |
| 2795 Alliance HPLC system | Waters | 176000491 | |
| Quattro micro API Tandem Quadrupole System | Waters | 720000338 | |
| QuanLynx 4.1 software | Waters | / | Data evaluation software provided by the mass spectrometer manufacturer |
| Supplemental File | Stock Solutions |
References
- Fleischmann, C., et al. Assessment of Global Incidence and Mortality of Hospital-treated Sepsis. Current Estimates and Limitations. American Journal of Respiratory and Critical Care Medicine. 193 (3), 259-272 (2016).
- Dellinger, R. P., et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012. Intensive Care Medicine. 39 (2), 165-228 (2013).
- Lodise, T. P., Drusano, G. L. Pharmacokinetics and pharmacodynamics: optimal antimicrobial therapy in the intensive care unit. Critical Care Clinics. 27 (1), 1-18 (2011).
- Macedo, R. S., Onita, J. H., Wille, M. P., Furtado, G. H. Pharmacokinetics and pharmacodynamics of antimicrobial drugs in intensive care unit patients. Shock. 39, Suppl 1. 24-28 (2013).
- Petersson, J., Giske, C. G., Eliasson, E. Standard dosing of piperacillin and meropenem fail to achieve adequate plasma concentrations in ICU patients. Acta Anaesthesiologica Scandinavica. 60 (10), 1425-1436 (2016).
- Abdul-Aziz, M. H., Lipman, J., Mouton, J. W., Hope, W. W., Roberts, J. A. Applying pharmacokinetic/pharmacodynamic principles in critically ill patients: optimizing efficacy and reducing resistance development. Seminars in Respiratory and Critical Care Medicine. 36 (1), 136-153 (2015).
- Imani, S., Buscher, H., Marriott, D., Gentili, S., Sandaradura, I. Too much of a good thing: a retrospective study of beta-lactam concentration-toxicity relationships. Journal of Antimicrobial Chemotherapy. 72 (10), 2891-2897 (2017).
- Ventola, C. L. The antibiotic resistance crisis: part 1: causes and threats. Pharmacy & Therapeutics. 40 (4), 277-283 (2015).
- World Health Organization. Global Action Plan on Antimicrobial Resistance. , Available from: http://www.who.int/antimicrobial-resistance/global-action-plan/en (2015).
- Pulcini, C. Antibiotic stewardship: update and perspectives. Clinical Microbiology and Infection. 23 (11), 791-792 (2017).
- Cairns, K. A., et al. The impact of a multidisciplinary antimicrobial stewardship team on the timeliness of antimicrobial therapy in patients with positive blood cultures: a randomized controlled trial. Journal of Antimicrobial Chemotherapy. 71 (11), 3276-3283 (2016).
- Baur, D., et al. Effect of antibiotic stewardship on the incidence of infection and colonisation with antibiotic-resistant bacteria and Clostridium difficile infection: a systematic review and meta-analysis. Lancet Infectious Diseases. 17 (9), 990-1001 (2017).
- Roberts, J. A., Norris, R., Paterson, D. L., Martin, J. H. Therapeutic drug monitoring of antimicrobials. British Journal of Clinical Pharmacology. 73 (1), 27-36 (2012).
- Paal, M., Zoller, M., Schuster, C., Vogeser, M., Schutze, G. Simultaneous quantification of cefepime, meropenem, ciprofloxacin, moxifloxacin, linezolid and piperacillin in human serum using an isotope-dilution HPLC-MS/MS method. Journal of Pharmaceutical and Biomedical Analysis. 152, 102-110 (2018).
- Vogeser, M., Seger, C. Pitfalls associated with the use of liquid chromatography-tandem mass spectrometry in the clinical laboratory. Clinical Chemistry. 56 (8), 1234-1244 (2010).
- United States Pharmacopeia and National Formulary. Chapter <621>. CHROMATOGRAPHY (USP 37-NF 32 S1). , United Book Press, Inc. Baltimore, MD. 6376-6385 (2014).
- Wong, G., Sime, F. B., Lipman, J., Roberts, J. A. How do we use therapeutic drug monitoring to improve outcomes from severe infections in critically ill patients? BMC Infectious Diseases. 14, 288 (2014).
- EUCAST: European Committee on Antimicrobial Susceptibility Testing. Information on clinical breakpoint tables. , Available from: http://www.eucast.org/clinical_breakpoints/ (2017).
- Surveillance der Antibiotika-anwendung und der bakteriellen Resistenzen auf Intensivstationen. SARI information for antibiotic consumption 2016 of all intensive care units participating at SARI. , Available from: http://sari.eu-burden.info/auswertung/down/AD-ZEIT.pdf (2016).
- Cefepime hydrochloride: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2016/050679s040lbl.pdf (2016).
- Meropenem: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2008/050706s022lbl.pdf (2006).
- Ciprofloxacin hydrochloride: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2016/019537s086lbl.pdf (2016).
- Moxifloxacin hydrochloride: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2010/021277s038lbl.pdf (2010).
- Linezolid: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2012/021130s028lbl.pdf (2011).
- Piperacillin and Tazobactam: Highlighs of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2017/050684s88s89s90_050750s37s38s39lbl.pdf (2017).
- Zander, J., et al. Effects of biobanking conditions on six antibiotic substances in human serum assessed by a novel evaluation protocol. Clinical Chemistry and Laboratory. 54 (2), 265-274 (2016).
- Zander, J., et al. Quantification of piperacillin, tazobactam, cefepime, meropenem, ciprofloxacin and linezolid in serum using an isotope dilution UHPLC-MS/MS method with semi-automated sample preparation. Clinical Chemistry and Laboratory. 53 (5), 781-791 (2015).



