Summary
MALT1 reglerar medfödd immunitet men hur detta sker är fortfarande oklara. Vi använde den selektiva MALT1 paracaspase hämmaren MLT-827 nysta MALT1 bidrag till medfödda signalering nedströms Toll-like eller C-typen lektin-liknande receptorer, visar att MALT1 reglerar produktionen av myeloisk cytokiner, och nedströms av C-typ lektin-liknande receptorer, selektivt.
Abstract
Förutom sin funktion i lymfoida celler, som har behandlats av ett flertal studier, spelar paracaspase MALT1 också en viktig roll i medfödda celler nedströms mönster erkännande receptorer. Bäst studerade är Dectin-1 och Dectin-2 medlemmarna av familjen typ C lektin-like receptor som inducerar en SYK - och CARD9-beroende signalering kaskad leder till NF-κB aktivering, på ett sätt som MALT1-beroende. Däremot kan Toll-liknande receptorer (TLR), såsom TLR-4, sprida NF-κB aktiveringen utan signal via en MYD88/IRAK-beroende kaskad. Ändå, om MALT1 kan bidra till TLR-4 signalering har förblivit oklar. Senaste bevis med MLT-827, en potent och selektiv hämmare av MALT1 paracaspase aktivitet, indikerar att TNF-produktion nedströms av TLR-4 i mänskliga myeloida celler är oberoende av MALT1, i motsats till TNF-produktion nedströms Dectin-1, vilket är MALT1 beroende. Här tog vi upp MALT1 selektiv engagemang i mönsterigenkänning avkänning ytterligare, med hjälp av olika mänskliga och mus cellulära preparat, och stimulering av Dectin-1, MINCLE eller TLR-4 vägar. Vi gav också ytterligare insikter genom att utforska cytokiner bortom TNF-, och genom att jämföra MLT-827 till en SYK-hämmare (Cpd11) och en IKK hämmare (AFN700). Sammantaget kan informationen ytterligare bevis för MALT1-beroendet av typ C lektin-like receptor — signalering i motsats till TLR-signalering.
Introduction
Paracaspase aktiviteten av MALT1 (Mucosa-associerade lymfoida vävnad lymfom translokation protein 1) avslöjades i 20081,2. Sedan dess har har ett antal studier rapporterat sitt kritiska bidrag till antigen receptorn svaren i lymfocyter. Genetiska modeller i musen samt farmakologi data stödjer en nyckelroll i T-celler, T-cells beroende autoimmunitet och B-cells lymfom inställningar3,4. I lymfocyter, MALT1 paracaspase aktivering sker vid montering av en CARD11-BCL10-MALT1 komplexa5, som utlöses av antigen-receptor proximala signalering nedströms av T - eller B-cells receptor. Det finns också gott om bevis för att en liknande CARD9-BCL10-MALT1 komplexet är viktigt för föröknings signaler nedströms av typ C lektin-liknande receptorer (Fullmäktigeledamot), e.g., Dectin-1, Dectin-2 och MINCLE i myeloida celler6,7. Dectin-1 har studerats särskilt väl då denna väg är kritisk för värd försvar mot svampinfektioner8,9. Innebörden av MALT1 i Toll-liknande receptorer (TLR) vägar, dock förblivit kontroversiell10. Senaste rönen i mänskliga myeloida celler uteslutit en direkt roll för MALT1 paracaspase aktivitet i regleringen av TNF-produktion nedströms av TLR-411.
I den nuvarande arbetet använde vi olika experimentella inställningarna och stimulerande förhållanden i mänskliga och mus myeloida celler sond medfödda signalvägar, förlitar sig på specifika farmakologiska verktyg-hämmare och mätning av cytokin produktion.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
Experiment utfördes enligt de riktlinjer och normer av Novartis mänsklig forskning etikkommittén.
1. beredning av perifera mononukleära blodceller (PBMC) från mänskliga Buffy rockar
Obs: Vi fick buffy rockar från friska frivilliga en dag efter insamling, i 50 mL påsar. De var enligt informerat samtycke och som samlats in genom den Interregionale Blutspende Schweizeriches Rotes Kreuz. Vi hanterat dem med hjälp av proceduren nedan, vid rumstemperatur såvida inte annat anges.
- Förbereda en steril och ren par sax och en 1-litersbägare med en plastpåse (under en lamina flöde).
- Överför lättcellsskikt till bägaren och öppna det försiktigt med saxen.
- Med 25 mL pipett, tillsätt 100 mL av fosfatbuffrad saltlösning buffert/etylendiamintetraättiksyrans dinatriumsalt (PBS/EDTA: PBS 1 x pH 7,4 som innehåller inga CaCl2 och inga MgCl2, kompletterat med 2 mM EDTA pH 8,0).
Obs: Med samma pipett och efter långsamt pipettering lösningen upp och ner, fördela 25 mL av den utspädda buffy coat i 6 koniskt centrifugrör 50 mL förfylld med 15 mL av polysackarid-baserade täthetlutning. - Centrifugera vid 800 x g 20 min med måttlig acceleration (inställd på 4 av 9) och utan broms som möjliggör separation av celler baserat på deras densiteter.
Obs: Efter centrifugering, kommer att tre lager vara synliga. en pellets som innehåller röda blodkroppar och granulocyter, ett övre lager av plasma, och mellan en vit ring som innehåller perifera mononukleära blodceller (PBMC). - Skörda PBMC ringen med en 10 mL pipett och överföring till nya 50 mL rör.
Obs: Två till tre 50 mL rör krävs normalt per buffy coat. I detta skede förorenar några plasma sannolikt de insamlade PBMC, som bör ha någon inverkan på de efterföljande anrikning steg. - Top upp till 50 mL varje tube använder PBS/EDTA och gå vidare till tre successiva tvättar med minskande centrifugeringstid och hastighet (15 min på 520 x g, 10 min vid 330 x g, 8 min på 150 x g).
Obs: Vid varje steg, supernatanten hälls upp i en flytande avfallsbehållare och cellpelleten är resuspended i 50 mL PBS/EDTA (pellets kan poolas efter första tvätten). - Efter den sista tvättningen, återsuspendera pelleten i 25 mL av en iskall lyseringsbuffert (se Tabell för material) för att lysera röda blodkroppar av osmotiskt tryck.
- Inkubera tills lösningen blir klar (≤5 min i rumstemperatur).
- Stoppa reaktionen genom att lägga till 25 mL separation buffert (PBS 1 x pH 7,4 som innehåller inga CaCl2 och inga MgCl2, kompletterat med 2% Värmeinaktiverade fetalt bovint serum (FBS) och 1 mM EDTA pH 8,0).
- Tvätta en gång vid 150 x g i 8 min.
Obs: I detta skede PBMC kan användas som en bulk population (se steg 3: PBMC och monocyter behandlingar och stimulerande villkor) eller bearbetas för monocyt berikning (se steg 2: beredning av monocyter från PBMC), eller fryst ner för senare användning (se steg 5: Monocyter och PBMC frysning/upptining förfaranden).
2. beredning av monocyter från PBMC
- Omsuspendera de PBMC erhålls vid steg 1.10 i separation buffert och räkna dem för att nå 5 x 107celler/mL.
- Överföra cellsuspensionen i en 14 mL koniskt centrifugrör med cap.
- Tillsätt 50 µL av monocyt anrikning antikroppar cocktail per mL cellsuspension, vortex, och inkubera i 10 minuter vid 4 ° C.
- Tillsätt 50 µL av monocyt anrikning pärlor per mL av celler.
Obs: Pärlorna måste vara grundligt vortexed att säkerställa homogenitet av suspensionen. - Efter att lägga pärlor, kort vortex cellsuspensionen och inkubera i 5 minuter vid 4 ° C.
- Skölj den övre delen av röret med separation buffert tills röret fylls upp till 10 mL.
- Långsamt blanda lösningen genom pipettering upp och ner.
- Placera röret utan mössa i en separation magnet.
- Inkubera i 2,5 minuter i rumstemperatur.
- Häll långsamt i en 15 mL koniskt centrifugrör.
- I detta skede använda monocyter direkt (se steg 3: PBMC och monocyter behandlingar och stimulerande villkor) eller skilja dem till jagmmature Monocyte-derived Dendritic Cells (iMoDCs) (se steg 4), eller frysa ner dem för senare användning (se steg 5).
3. PBMC och monocyter behandlingar och stimulerande villkor
- Räkna celler och späda ut dem i odlingsmedium (Roswell Park Memorial Institute medium (RPMI) 10% FBS + 1 mM natrium pyruvat + 100 U/mL Penicillin Streptomycin (penna/Strep) + 5 µM β-merkaptoetanol), ner till 1,25 x 104 celler per brunn.
- Fördela 30 µL cellsuspension per brunn av en plattan med 384 brunnar.
- Tillsätt 15 µL av 4 x koncentrerade sammansatta lösningar och Preinkubera för 1 h vid 37 ° C, 5% CO2.
- Lägga till lipopolysackarid (LPS) till en slutlig koncentration på 10 ng/mL, eller utarmat zymosan (DZ) till en slutlig koncentration på 100 µg/mL, eller hålla i vanligt medium.
- Inkubera över natten vid 37 ° C, 5% CO2.
- Ta 10 µL av supernatanten att mäta utsöndrade TNF-a (se steg 7: cytokiner och livskraft mätningar).
4. monocyter differentiering in iMoDCs och stimulerande villkor
- Räkna monocyter (berikad på steg 2) och centrifugera cellsuspension vid 520 x g i 5 min.
- Pipettera bort supernatanten och lägga till odlingsmedium (RPMI + 10% FBS att erhålla en slutliga cellsuspension av 0,4 x 106 celler/mL.
- Tillsätt 80 ng/mL rekombinant humant IL-4 + 100 ng/mL GM-CSF.
- Dosera 5 mL cellsuspension per brunn i en 6-bra platta.
- Inkubera i 7 dagar vid 37 ° C, 5% CO2.
- Dag 7, skörda celler genom pipettering försiktigt för att undvika deras aktivering.
- Centrifugera vid 520 x g under 5 minuter.
- Dammsug aspirera och resuspendera i 50 mL odlingsmedium utan tillväxtfaktorer.
- Centrifugera vid 520 x g i 5 min och resuspendera på 1 x 106 celler/mL i odlingsmedium.
- Dispensera 100 µL cellsuspension (105 celler) per brunn 96 brunnar platt botten platta.
- Pre incubate för 1 h vid 37 ° C efter att lägga till 50 µL av 4 x koncentrerad sammansatta lösningar som förberetts enligt beskrivningen i steg 8: föreningar förberedelse.
- Tillsätt 50 µL av stimuli (4 x koncentrerad), bereds enligt anvisningarna i steg 9.
- Inkubera 24 h vid 37 ° C.
- Blanda varje brunn och överföring celler och supernatanten (SN) till en platta med 96 brunnar i V-botten.
- Snurra ner vid 475 x g i 5 min.
- Överför supernatanten till en ny 96 brunnar flat bottenplatta, försegla och frysa vid-20 ° C tills vidare användning.
5. monocyter och PBMC frysning/upptining förfaranden
-
Frysning
- Snurra ner PBMC eller monocyt cell preparat på 520 x g i 5 min.
- Vakuum Aspirera supernatanten och återsuspendera cellerna i frysning medium på 1 x 107 celler/mL.
- Dosera 1 mL cellsuspension i frysrör, överföra rören till en viss kyla enhet (se material tabell) och placera den vid-80 ° C.
-
Upptining
- Tina cryotube och snabbt överföra dess innehåll i en 15 mL koniskt centrifugrör som innehåller 9 mL odlingsmedium.
- Centrifugera vid 520 x g under 5 minuter.
- Dammsug Aspirera supernatanten och återsuspendera cellpelleten i 5 mL odlingsmedium. Cellerna är nu klara för experimentell vidarebearbetning.
6. mus mjälte celler beredning och behandling
Obs: Vi har utfört djura offer enligt de riktlinjer och normer för Novartis djur välfärd organisationen. Studier godkändes av den etiska kommittén av den regionala statliga myndigheten (Kantonales Veterinäramt der Stadt Basel). Vi offrade djur av isofluran överexponering, med alla ansträngningar göras för att minimera lidande.
- Skörda mjälte och separera vävnad med hjälp av en slang utrustad med en mekanisk vävnad grinder enhet och fylld med 5 mL kall RPMI medium.
- Använda programmet mjälte dissociation maskinen för att slipa organ.
- Filtrera cellerna genom en 100 mm nylon cell SIL.
- Över till 50 mL rör och centrifugera vid 4 ° C under 10 minuter vid 320 x g.
- Vakuum Aspirera supernatanten, Återsuspendera cellpelleten i 3 mL iskallt lyseringsbuffert och inkubera i ≤2 min på is.
- Stoppa lysis genom att lägga till 7 mL RPMI medium.
- Filtrera igen genom en 100 µm nylon cell SIL.
- Snurra ner cellsuspension på 330 x g under 10 minuter vid 4 ° C.
- Dammsug Aspirera supernatanten och återsuspendera cellerna på 11 x 106 celler/mL i komplett medium (RPMI kompletteras med 10% FBS, 100 U/mL penna/steg och 5 µM β-merkaptoetanol).
- Tallrik 1 x 106 celler per brunn (90 µL) i en plattan med 96 brunnar (platt botten).
- Tillsätt 5 µL 20 x koncentrerad sammansatta lösning tidigare utspädd i RPMI medium som beskrivs i steg 8,3: Serial utspädning för murina mjältceller.
- Inkubera i 30 minuter vid 37 ° C, 5% CO2.
- Tillsätt 5 µL 20 x koncentrerad DZ (slutlig koncentration 30 µg/mL) eller 20 x koncentrerad LPS + IFN-g (TLR-4) (slutlig koncentration 1 µM LPS och 10 ng/mL IFN-g).
- Inkubera över natten vid 37 ° C, 5% CO2.
- Centrifugera vid 330 x g under 10 minuter.
- Överföra supernatanterna i nya plattor, försegla och frysa vid-20 ° C tills vidare användning.
7. cytokiner och livskraft mätningar
-
Humant TNF-en mätning av HTRF (homogen tid löst fluorescens)
Obs: Protokollet följt leverantörens rekommendationer, kort sammanfattas nedan.- Blanda 1 volymdel beredda reagens (anti TNF-a-cryptate och anti-TNF-a-XL665) med 19 volymdelar beredning buffert (50 mM fosfatbuffert pH 7.0, 0,8 M kalium fluor (KF), 0,2% bovint serumalbumin (BSA)).
- Blanda de två färdiga att använda antikropp lösningarna 1:1 bara före dispensering av reagenserna.
- Dosera 10 µL supernatanterna från steg 3.6 i vit 384 brunnar.
- Dispensera 10 µL av antikropp mixen.
- Täck plåten med en sealer och inkubera vid 4 ° C över natten.
- Läs plattan på en microplate reader (50 – 200 flash).
- Humant IL-23 mätning av HTRF (homogen tid löst fluorescens)
Obs: Protokollet följt leverantörens rekommendationer, kort sammanfattas nedan.- Blanda 1 volymdel beredda reagens (anti IL-23-cryptate-antikropp och anti-IL-23 D2-antikropp) med 19 volymdelar upptäckt buffert #3.
- Blanda de två färdiga att använda antikropp lösningarna 1:1 bara före dispensering av reagenserna.
- Dosera 10 µL supernatanterna från steg 3.6 i vit 384 brunnar.
- Dispensera 10 µL av antikropp mixen.
- Täck plåten med en sealer och inkubera vid 4 ° C över natten.
- Läs plattan på en microplate reader (50 – 200 nm flash).
-
Mänskliga IL-6, IL-8, IL-1β och TNF-α mätningar av elektrokemiluminescens
Obs: Alla prover späddes på 1/150 i spädningsvätska 2 (första spädning: 10 µL i 150 µL, sedan 20 µL i 180 µL). Protokollet följt leverantörens rekommendationer:- Späd prover och standard i spädningsvätska 2.
- Gå vidare till utspädning av standarden i spädningsvätska 2 använda en 1/4 seriell vik spädning.
- Tvätta plattorna tre gånger med tvättbuffert.
- Dispensera 50 µL prov eller standard per brunn.
- Inkubera i 2 h i rumstemperatur under agitation.
- Tvätta plattan fyra gånger med PBS + 0,05% polysorbat 20.
- Tillsätt 25 µL av detektionsantikropp (60 µL av varje antikropp för 3 mL slutlig) i spädningsvätska 3.
- Inkubera i 2 h i rumstemperatur under agitation.
- Tvätta plattan fyra gånger med PBS + 0,05% polysorbat 20.
- Att undvika bubblor, tillsätt 150 µL per brunn av Läsbuffertens (Tris-baserad buffert innehållande tripropylamine, utspädd 2 x i ddH20) som en samtidig reaktant för ljus generation i elektrokemiluminescens immunoanalyser.
- Läs plattan (utan fördröjning) på en Plattläsare med multiplex.
-
Mus TNF-en mätning av ELISA efter leverantörens protokoll
- Späd supernatanten 1:1 i assay spädningsvätska (klar att använda proteinhaltiga buffert).
- Förbereda reagenser, prover och standard utspädningar som beskrivs i kit. Tillsätt 50 μL av assay spädningsvätska till varje brunn.
- Tillsätt 50 μL standard, kontroll eller prov per brunn.
- Blanda genom att knacka på den tallrik ram för 1 min.
- Täck med den medföljande självhäftande remsan och inkubera i 2 h i rumstemperatur.
- Aspirera varje brunn och tvätta med 400 μL/brunn (Upprepa detta steg fem gånger totalt).
- Efter den sista tvättningen, avlägsna eventuella kvarvarande tvättbuffert genom att aspirera.
- Vänd på plattan och blot mot ren pappershanddukar.
- Tillsätt 100 μL av mus TNF-α-konjugat till varje brunn. Täck med en ny självhäftande remsa.
- Inkubera i 2 h i rumstemperatur.
- Upprepa den aspiration/tvätten som i steg 7.4.4.
- Tillsätt 100 μL arbetssubstratlösning i varje brunn och inkubera i 30 min i rumstemperatur skyddas från ljus.
- Tillsätt 100 μL av Utspädd saltsyralösning (stopplösning) till varje brunn. Knacka försiktigt på plattan för att säkerställa omsorgsfull blandning.
- Mäta optisk densitet vid 450 nm (med korrigering våglängden på 560 nm) med en microplate reader (för att göras inom 30 min).
- Späd supernatanten 1:1 i assay spädningsvätska (klar att använda proteinhaltiga buffert).
-
Cellernas viabilitet
- När supernatanterna ur PBMC eller monocyt preparat bör bedöma cellernas viabilitet med en klar för att använda resazurin lösning (oxidation-reduktion indikator) läggas till direkt på cellsuspensionen till slutliga koncentration av 10%.
- Inkubera i 1 till 2 timmar vid 37 ° C, 5% CO2.
- Läs fluorescens vid 590 nm (Excitation 540 nm) med en microplate reader.
8. sammansatta beredning
-
Seriell utspädning för iMoDCs
- Späd stamlösningen MLT-827 (10 mM i dimetyl sulfoxid (DMSO) till medium att nå 8 µM på en gång (4 x koncentrerad).
- Utföra en sex steg 1:5 följetong utspädning, använder medium + 0,08% DMSO. Använda samma medium + 0,08% DMSO lösning för fordon (ingen förening) villkoret.
-
Enstaka dos testning för iMoDCs
- Späd ut MLT-827, AFN700 och Cpd11 lager lösningarna till medium att nå 4 µM på en gång (4 x koncentrerad).
-
Seriell utspädning för murina mjältceller
- Späd en 10 µM MLT-827 lösning (erhålls från 10 mM stamlösning efter en en gå spädning i medium) till 0,01 µM, med DMSO slutet koncentration av 0,1%.
- Anvisningar om spädning, ta 2 µL av varje utspädning, lägga till 38 µL RPMI och Pipettera 5 µL i brunnen.
Obs: Alla behandlingar utförs i tre exemplar.
9. stimuli förberedelse
-
Utarmat zymosan (DZ)
- Tillsätt 2 mL av sterila endotoxinfria vatten 10 mg DZ.
- Vortex att homogenisera stamlösning, vortex också före varje användning.
- Alikvotens lösning och store alikvoter vid-20 ° C.
-
Trehalos-6,6-glyceroldibehenat (TDB)
- Tillsätt 100 µL av DMSO 1 mg TDB, värme vid 60 ° C i ett vattenbad för 15 – 30 s.
- Vortex och tillsätt omedelbart 900 µL sterilt PBS, vortex igen.
- Värme för 10 – 15 min vid 60 ° C och homogenisera genom Omskakas före varje användning.
- Förvara lösningen vid 4 ° C.
- Utföra seriespädningar och engångsdos förberedelser när det gäller MLT-827 föreningen.
Obs: Eftersom TDB behöver förberedas i DMSO, är en slutlig koncentration av 1% DMSO närvarande under cell stimulering.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
I myeloida celler reläer MALT1 aktiveringen signaler nedströms flera typ C lektin-liknande receptorer, såsom Dectin-1, Dectin-2 och MINCLE6. Dessa vägar är beroende av (nertill) ITAM motiv-innehållande receptorer (t.ex., Dectin-1) eller ITAM motiv-innehållande Co receptorer (t.ex., FcRγ, för Dectin-2 och MINCLE) som rekryterar och aktiverar den SYK kinase (figur 1). Detta leder till aktivering av ett protein kinase C isoform, nämligen PKCδ, som phosphorylates CARD9, därmed utlöser CARD9/BCL10/MALT1 komplexa bildande och rekrytering av TRAF6 för nedströms NF-κB aktiveringen12. Däremot rekryterar den TLR-4 vägen TRAF6 i en MALT1-oberoende men MYD88/IRAK-beroende sätt för NF-κB aktivering (figur 1). Beviset för detta differentiella inblandning av MALT1 erhölls med genetiska modeller av MALT1-brist samt farmakologisk behandling med peptidic active-site-hämmare z-VRPR-fmk11,13,,14.
Vi använde den nyligen rapporterade potent och selektiv MALT1 hämmaren MLT-82715 och frågade om denna förening skulle reglera TNF-produktionen nedströms av C typ lektin-liknande och Toll-liknande receptorer, respektive. Mänskliga PBMC och mus mjältceller stimuleras med utarmat zymosan (DZ, en känd agonist av Dectin-1) eller lipopolysackarid (LPS, en känd agonist av TLR-4) och vi mätt TNF-release i kulturen supernatanten efter 20 h. Både människan och mus analyserna spärrade MLT-827 selektivt TNF-produktionen drivs av Dectin-1 vägen, men inte av den TLR-4 vägen (figur 2). Vi fick liknande data vid inkubation med z-VRPR-fmk föreningen (kompletterande figur 1).
För att få väg insikter har vi genomfört ytterligare experiment i humana monocyter och omogna monocyter-derived dendritiska celler (iMoDCs), jämföra effekten av MLT-827 av SYK hämmare Cpd1116 och som av IKK-hämmaren AFN70015 . I monocyter stimuleras med LPS, produktion av TNF-α upphävdes nästan helt av AFN700 men var inte känslig för Cpd11 (figur 3A), vilket är förenligt med den beroende/oberoende av TLR-4 väg på NF-κB/SYK aktivitet, respektive () (se figur 1). Däremot produktion av TNF-α som drivs av Dectin-1 i iMoDCs visas känslighet för Cpd11 förutom känslighet för MLT-827 och AFN700 (figur 3B, kompletterande figur 2), som ger ytterligare bevis för inblandning av en SYK/CBM signalering kaskad i Dectin-1 väg (figur 1). Anmärkningsvärt, produktion av IL-1, IL-6 och IL-23 vid Dectin-1 stimulering var också känslig för de tre-hämmare, som därmed visar regleringsmekanismer liknar TNF-. Dock föreslog en begränsad effekt av de tre föreningarna på produktionen av IL-8 en distinkt reglerande mekanism för denna cytokin (figur 3B, kompletterande figur 2).
Förutom Dectin-1, andra CLLRs, såsom Dectin-2 och MINCLE, funktionen via stimulering av en CARD9 signalosome7. Därför testade vi MLT-827 i iMoDCs utmanas med den MINCLE-agonist trehalos-6,6-glyceroldibehenat (TBD). Att höja TBD halter över 50 µg/mL ledde till produktionen av TNF-, IL-6 och IL-1, som relied på MALT1 paracaspase verksamhet sett från blockerande effekten av MLT-827 (figur 4A). Konsekventa resultat erhölls när utmanande iMoDCs med ökande koncentrationer av DZ att stimulera Dectin-1 (figur 4B).
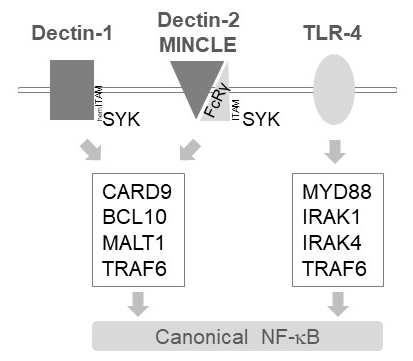
Figur 1: NF-κB signalering nedströms Dectin-1, MINCLE och TLR-4. Den tecknade serien skildrar de viktigaste funktionerna i kanoniska NF-κB aktiveringen vägar nedströms Dectin-1, Dectin-2, MINCLE eller TLR-4 i myeloida celler. HemITAM-innehållande Dectin-1 receptorn17 kan direkt engagera SYK att stimulera komplexa bildandet av CBM (CARD9/BCL10/MALT1), vilket leder till TRAF6 beroende av NF-κB aktivering. Andra C-typen lektin-liknande receptorer såsom Dectin-2 eller MINCLE behöver rekrytera en ITAM-innehållande FcRγ kedja för att engagera en CBM och aktivera NF-κB. TLR-4 receptorer använda en annan mekanism för NF-κB aktiveringen, förlitar sig på MYD88 och IRAK1/IRAK4 kinaser uppströms av TRAF6.

Figur 2: Dectin-1 signaler via MALT1 för produktion av TNF-α i mänskliga och mus celler. (A) mänskliga PBMC data som i Unterreiner et al., 2017 (figur 2A)11. Mänskliga PBMC stimuleras med 1 ng/mL av LPS (TLR-4 agonist) eller 100 µg/mL DZ (Dectin-1 receptoragonist) för 20 h i närvaro av graderade koncentrationer av MLT-827. TNF-släppt i supernatanten kvantifierades av HTRF. (B) mus mjältceller behandlades med en koncentration utbud av MLT-827 30 min och därefter stimuleras med 30 mikrog/mL DZ eller 1 µg/mL LPS + 10 ng/mL IFN - för 18 h. TNF-α i cellkultur supernatant mättes med ELISA. En av två experiment med liknande resultat visas som betyder ± SEM av tre mätningar.

Figur 3: IKK- eller SYK-beroendet av cytokin produktion nedströms TLR-4 och Dectin-1. (A) humana monocyter var förbehandlade för 1 h med MLT-827 (1 µM), Cpd11 (1 µM), eller AFN700 (3 µM) eller fordon (DMSO). Cellerna stimuleras med 10 ng/mL LPS för 20 h och TNF-i supernatanten kvantifierades av HTRF. (B) TNF-α, IL-1β, IL-6, IL-23 och IL-8 produktion av mänskliga monocyter-derived dendritiska celler (iMoDCs) stimuleras för 24 h med DZ (100 µg/mL) efter 1 h före inkubering med MLT-827, Cpd11, AFN700 (alla på 1 µM) eller DMSO. Cytokin nivåer i DMSO-behandlade prover fastställdes till 100%. Data är medel ± SD av tre mätningar, och företrädare för tre oberoende experiment. * P < 0,05; ** P < 0,01; P < 0,001, oparade tvåsidiga Students t-test.

Figur 4: C typ lektin-liknande-beroende cytokin produktion av iMoDCs. TNF-α, IL-1β och IL-6 produktion av iMoDCs stimuleras för 24 h med den MINCLE-agonist trehalos-6,6-glyceroldibehenat (TDB, 100 µg/mL) (A) eller med den Dectin-1-receptoragonist DZ (100 µg/mL) (B) efter 1 h före inkubering med MLT-827 (1 µM) eller DMSO. Data är medel ± SD av tre mätningar och företrädare för tre oberoende experiment.
Kompletterande fil 1. Vänligen klicka här för att hämta den här filen.
Kompletterande fil 2. Vänligen klicka här för att hämta den här filen.
Kompletterande fil 3. Vänligen klicka här för att hämta den här filen.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
I detta arbete använde vi enkla experimentella inställningar att studera signalvägar i mänskliga och mus medfödda celler och förhöra sitt beroende MALT1 proteolytiska funktion. Expanderande på föregående arbete11, visade vår studie att MALT1 paracaspase aktivitet styr typ C lektin-like receptor inducerad cytokin produktion, inklusive TNF-α. Däremot var TLR-4-inducerad TNF-α oberoende av MALT1 hos båda arterna. Sammantaget bekräftas dessa uppgifter den MALT1/CBM signalosome nedströms av typ C lektin-liknande receptorer, som presenterades av tidigare studier6,12,18nyckel och selektiva bidrag.
Om det klart oberoende av TLR-4 signalering på MALT1 i myeloida celler gäller för andra typer cell återstår att utforskas. Exempelvis i B-lymfocyter, var TLR signalering tidigare visat att bidra till B-cellsaktivering nedströms av B-cells antigen receptorn19. Vi i själva verket har opublicerade bevis att TLR-4 stimuleras mänskliga och mus B celler visar känslighet till MLT-827. Ytterligare mekanistiska insikter nedströms av B-cells receptor kommer därför värdefull. I detta sammanhang en senaste studie i B-cellslymfom som bevis för klustring av signalvägar nedströms av B-cells receptorn och TLR9 receptor20. TRAF6, som agerar som medlare för NF-κB aktivering både B-cells receptorn och den TLR vägar, kanske en punkt av överhörning, vilket skulle kunna förklara både vägar känslighet MALT1 proteashämmare hämning. Omvänt TRAF6 är också en gemensam nedströms CLLRs och TLRs för induktion av NF-κB men dessa två vägar verkar inte överhörning på ett MALT1 paracaspase-beroende sätt i myeloida celler.
Detta arbete inriktat på cytokin produktion, vilket ger en lätt avläsning för signalvägar och kan genomföras lätt för sammansatta profilering. Det markerade värdet av selektiv och potent hämmare av MALT1 för reda MALT1 biologi. Att erhålla ytterligare mekanistiska insikter kommer att kräva ytterligare arbete och utveckling av mer proximala analyser, t.ex., för att karakterisera de substrat för MALT1 involverade i medfödda signalering förordning.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
Författarna har något att avslöja.
Acknowledgments
Vi tackar Elsevier om deras tillstånd (licens antal 4334770630127) att återge här figur 2A från Unterreiner et al. (2017).
Materials
| Name | Company | Catalog Number | Comments |
| 100 µm nylon cell strainer | Sigma | CLS431752 | |
| 14 mL Falcon tube | BD Falcon | 352057 | |
| 15 mL Falcon tube | Falcon | 352090 | |
| 50 mL Falcon tube | Falcon | 352070 | |
| 6 well plates | Costar | 3516 | |
| 96 well flat-bottom plate, with low evaporation lid | Costar | 3595 | |
| 96 well V-bottom plate | Costar | 734-1798 | |
| Ammonium Chloride - NH4Cl | Sigma | A9434 | |
| Assay diluent RD1-W ELISA | R&D | 895038 | Assay diluent |
| Cell culture microplate, 384 well, black | Greiner | 781986 | |
| Depleted Zymosan | Invivogen | tlrl-dzn | now: tlrl-zyd |
| Dimethyl sulfoxide | Sigma | D2650 | DMSO |
| EDTA-Na2 | Sigma | E5134 | Ethylenediaminetetraacetic acid disodium salt dihydrate |
| ELISA muTNF-α | R&D | SMTA00 | |
| Ficoll-Paque Plus | GE Healthcare | 17-1440-03 | |
| gentleMACS C tubes | MACS Miltenyi Biotec | 130-096-334 | |
| gentleMACS dissociator | MACS Miltenyi Biotec | 130-093-235 | |
| GM-CSF | Novartis | - | |
| Heat-inactivated Fetal bovine serum | Gibco | 10082 | FBS |
| HTRF hu IL-23 | CisBio | 62HIL23PEG | |
| HTRF hu TNF-α | CisBio | 62TNFPEC | |
| HTRF reconstitution buffer | CisBio | 62RB3RDE | 50mM Phosphate buffer, pH 7.0, 0.8M KF, 0.2% BSA |
| IFN-γ | R&D | L4516 | |
| IL-4 | Novartis | - | |
| Isoflurane | Abbott | Forene | |
| Lipopolysaccharides (LPS) | Sigma | L4391 | LPS used in human samples |
| Lipopolysaccharides | Sigma | L4516 | LPS used in murine samples |
| Lysis buffer | Self-made | - | 155 mM NH4Cl, 10 mM KHCO3, 1 mM EDTA, pH 7.4 |
| Magnet | Stemcell | 18001 | |
| Microplate, 384 well white | Greiner | 784075 | |
| Monocytes enrichment kit | Stemcell | 19059 | |
| Nalgene Mr. Frosty Cryo 1°C Freezing Container | Nalgene | 5100-0001 | cooling device (containing Propanol-2) |
| PBS 1x pH 7.4 [-] CaCl2 [-] MgCl2 | Gibco | 10010 | Phosphate-buffered saline |
| Penicillin/Streptomycin | Gibco | 15140 | Pen/Strep |
| Potassium bicarbonate - KHCO3 | Sigma | P9144 | |
| PrestoBlue | Invitrogen | A13262 | Resazurin solution for viability assessment |
| Propanol-2 | Merck | 1.09634 | |
| Read buffer | MesoScale Discovery | R92TC-3 | Tris-based buffer containing tripropylamine |
| Recovery cell culture freezing medium | Gibco | 12648-010 | freezing medium |
| Roswell Park Memorial Institute Medium (RPMI) with Glutamax | Gibco | 61870 | + 10% FBS for iMoDCs + 10% FBS + 1 mM Sodium Pyruvate + 100 U/mL Pen/Strep + 5 µM β-mercaptoethanol for human PBMCs and monocytes + 10% FBS + Pen/Strep + 5 µM β-mercaptoethanol for murine splenocytes |
| Separation buffer | Self-made | - | PBS pH 7.4 + 2% FBS + 1 mM EDTA pH 8.0 |
| Sodium Pyruvate | Gibco | 11360 | |
| Trehalose-6,6-dibehenate | Invivogen | tlrl-tdb | TDB |
| Tween 20 | Sigma | P7949 | Polysorbate 20 |
| UltraPure 0.5 M EDTA pH 8.0 | Invitrogen | 15675 | Ethylenediaminetetraacetic acid |
| Viewseal sealer | Greiner BioOne | 676070 | |
| V-PLEX Proinflammatory Panel 1 Human Kit | MesoScale Discovery | K15049D | electrochemiluminescent multiplex assay (IL-1β, TNF-α, IL-6, IL-8) |
| β-Mercaptoethanol | Gibco | 31350 |
References
- Coornaert, B., et al. T cell antigen receptor stimulation induces MALT1 paracaspase-mediated cleavage of the NF-kappaB inhibitor A20. Nature immunology. 9 (3), 263-271 (2008).
- Rebeaud, F., et al. The proteolytic activity of the paracaspase MALT1 is key in T cell activation. Nature immunology. 9 (3), 272-281 (2008).
- Jaworski, M., Thome, M. The paracaspase MALT1: Biological function and potential for therapeutic inhibition. Cellular and Molecular Life Sciences. 73 (3), 459-473 (2016).
- Meininger, I., Krappmann, D. Lymphocyte signaling and activation by the CARMA1-BCL10-MALT1 signalosome. Biological Chemistry. 397 (12), 1315-1333 (2016).
- Qiao, Q., et al. Structural architecture of the CARMA1/Bcl10/MALT1 signalosome: nucleation-induced filamentous assembly. Molecular cell. 51 (6), 766-779 (2013).
- Gross, O., et al. Card9 controls a non-TLR signalling pathway for innate anti-fungal immunity. Nature. 442 (7103), 651-656 (2006).
- Chiffoleau, E. C-type lectin-like receptors as emerging orchestrators of sterile inflammation represent potential therapeutic targets. Frontiers in Immunology. 9 (FEB), 1-9 (2018).
- Taylor, P. R., et al. Dectin-1 is required for beta-glucan recognition and control of fungal infection. Nature Immunology. 8 (1), 31-38 (2007).
- Lanternier, F., et al. Primary immunodeficiencies underlying fungal infections. Current opinion in pediatrics. 25 (6), 736-747 (2013).
- Thome, M. Multifunctional roles for MALT1 in T-cell activation. Nature reviews. Immunology. 8 (7), 495-500 (2008).
- Unterreiner, A., Stoehr, N., Huppertz, C., Calzascia, T., Farady, C. J., Bornancin, F. Selective MALT1 paracaspase inhibition does not block TNF-α production downstream of TLR-4 in myeloid cells. Immunology Letters. , 48-51 (2017).
- Strasser, D., et al. Syk Kinase-Coupled C-type Lectin Receptors Engage Protein Kinase C-δ to Elicit Card9 Adaptor-Mediated Innate Immunity. Immunity. 36 (1), 32-42 (2012).
- Jaworski, M., et al. Malt1 protease inactivation efficiently dampens immune responses but causes spontaneous autoimmunity. The EMBO journal. 33 (23), 2765-2781 (2014).
- Yu, J. W., et al. MALT1 protease activity is required for innate and adaptive immune responses. PLoS ONE. 10 (5), 1-20 (2015).
- Bardet, M., et al. The T-cell fingerprint of MALT1 paracaspase revealed by selective inhibition. Immunology and Cell Biology. 96 (1), 81-99 (2018).
- Thoma, G., et al. Discovery and profiling of a selective and efficacious syk inhibitor. Journal of Medicinal Chemistry. 58 (4), 1950-1963 (2015).
- Bauer, B., Steinle, A. HemITAM: A single tyrosine motif that packs a punch. Science Signaling. 10 (508), 1-10 (2017).
- Gringhuis, S. I., et al. Selective c-Rel activation via Malt1 controls anti-fungal TH-17 immunity by dectin-1 and dectin-2. PLoS Pathogens. 7 (1), (2011).
- Dufner, A., Schamel, W. W. B cell antigen receptor-induced activation of an IRAK4-dependent signaling pathway revealed by a MALT1-IRAK4 double knockout mouse model. Cell Communication and Signaling. 9 (1), 6 (2011).
- Phelan, J. D., et al. A multiprotein supercomplex controlling oncogenic signalling in lymphoma. Nature. , In press (2018).



