Summary
ここでモルモット モデルにおける心筋細胞ヒト iPS 細胞由来心筋パッチの注入後、左心室 cryoinjury の誘導のためのプロトコルを提案する.
Abstract
大人の哺乳類中心の限られた再生能力、心筋梗塞は心筋細胞の不可逆的な損失の結果します。この損失心臓の筋肉の量の質量は心不全につながることができます。心臓移植以外にも末期心不全の治療オプションはありません。臓器提供者不足の時代に、器官の独立した治療法が必要です。左心室の補助装置は、ストローク、感染症、出血などの副作用によって制限先療法として特にしかし、有望な治療オプションです。近年では、幹細胞の注入、心臓前駆細胞や心筋のティッシュ エンジニア リングを含むいくつかの心臓の修復戦略を行った。細胞生物学の最近の改善は、大量 (iPSC) ひと誘導多能性幹細胞由来心筋細胞の分化。評価の下で現在心臓の修復戦略の一つ人工心臓組織を移植することです。設計された心臓ティッシュ (EHT) は、ネイティブの中心のティッシュの機能特性との立体生体外で作成された心筋細胞ネットワークです。派生による心筋細胞から EHT パッチを作成しました。ここでモルモット、注入による左心室心筋 cryoinjury の誘導は、左心室壁の EHT を派生プロトコルを提案します。
Introduction
高齢では心不全の患者が増えてきています。末期心不全のため同所性同種心移植、治療のみオプションです。しかし、ヨーロッパ諸国で特に増加の臓器ドナー不足があります。したがって、代替治療法の選択肢が必要です。機械的循環補助の最近の成果は有望であるが、特に長期的に実行、ポンプ血栓症、出血と感染性合併症1のようなその副作用によって制限します。
大人の人間の心の内因性の再生能力は非常に制限されています。したがって、心筋再生療法末期心不全患者2,3のための代替治療オプションになるかもしれない。幹細胞を用いた細胞の注入や組織工学的アプローチがされているを含むさまざまなテクニックは、3,4,5をについて説明します。
ヒト胚性幹細胞 (hESC) と同様に、ひと誘導多能性幹細胞 (こと) を心臓再生の分野で大きな成果となっているひと心筋細胞6が自発的に暴行に効果的に区別できます。療法。
心筋梗塞後心筋を交換して障害のある心臓の機能を向上させるには、心筋細胞および機械的および電気的ネイティブの心と結合の適切な数の生存が不可欠です。ヒト iPS 細胞由来心筋細胞の心筋再生療法の可能性を調べるためには、適切な研究モデルが必要です。理想的なモデルは費用対効果で、人間のような生理学、電気生理学があります。豚のような大動物モデルはその観点から理想的になる、しかし、これらの実験は非常に高価、心筋細胞の大量左心室に及ぼす影響を確認するために関連する心筋細胞数を交換する必要があります。豚梗塞モデルで機能します。
人間の細胞を用いた心筋再生に向けた小学校生物学的質問に答えるなど細胞の生存、血管新生、および電気的結合の小さい動物モデルより適しています。利用可能な小動物モデルからモルモット、ラットとマウスと比較して、最も有用な種人間7の状況によく似ていますその電気生理学。このモルモット モデル左心室の貫壁性 cryoinjury を誘導されます。立体化、心筋梗塞着床誘導後一週間腰細胞由来の心筋細胞を自発的に破ってパッチを行った。心筋細胞の生存は、病理検査で 28 日後を評価しました。
Subscription Required. Please recommend JoVE to your librarian.
Protocol
動物実験動物の原則のためのガイドに準拠した人道的なケアを受けて、実験動物資源の研究所でを準備、健康の国民の協会によって公開されました。動物のすべてのプロトコルがローカル責任がある権限によって承認された (「Amt こだわり健康を祝して und Verbraucherschutz、ハンザ」/動物プロトコル # 109/16).
1. 動物を入手します。
- 市販 500-600 g の重量を量る女性のモルモットを取得します。
- 動物ケージの中で従来の条件の下でそれらを収容します。標準的なラットの食事とオートクレーブ水広告 libidum を養います。
2. 経胸壁心エコー法
- 誘導室でモルモットを置き、イソフルラン (2-3%) を持つ動物を麻酔します。つま先ピンチへの応答の欠乏によって麻酔の深さを確認します。
- 仰臥位で地球温暖化のプラットフォーム (40-42 ° C) で麻酔下モルモットを配置します。鼻の円錐形 (イソフルラン 1.5-2%) 経由で麻酔を続ける
- 剃るし、動物の毛を電気シェーバーを使用してギニア pig´s 胸郭を depilate します。
- Prewarmed (~ 25 ° C) 超音波トランスデューサー ゲルを適用します。15 MHz 以上探触子周波数とが装備されているエコー システムを使用します。
- LV アペックスの同時可視化による大動脈弁の面で B モード画像の左脚とレコードの長い軸に向かって右の首から直面している guinea´s 豚胸部に探触子を置くことによって二次元傍胸骨長軸ビューを取得します。術前の左室機能を調査します。
- 半ば乳頭レベルで短い軸 B モードのビューを取得する 90 ° の位置で探触子電源を入れます。
注:動物、またはテーブルにすぐに転送されます。3% イソフルランと継続的に動物に麻酔がかかります。アトロピン 0.05 mg/kg (イオ ミン) は機械換気の間に気管支分泌物増加を避けるために注入されます。
3. 手術
-
心筋梗塞の誘導
- 21 G 針と 10 mL の注射器で皮下 4-5 mg/kg カルプロフェン、0.05 mg/kg ブプレノルフィン鎮痛のために挿入します。アトロピン 0.5 mg/kg は、21 G 針と 10 mL の注射器で皮下に注射されます。
- その裏にモルモットを置き、口と鼻を覆うマスクで麻酔を維持します。後部のフィート (ペダルの反射の欠如) をつまんで麻酔の深さを確認します。
- モルモットの足を広げ、テープを使用して位置を修正します。
- 胸や麻酔下の動物の気管領域を電気シェーバーで剃る。広く後 80% エタノールにヨウ素系のスクラブを使用して領域を消毒します。この消毒の手順を 2 回繰り返します。
- 気管領域で 1.5 cm の縦切開を行いますそして、にべもなく気管が表示されるまで、気管を覆う筋肉を解剖します。18 G 静脈カニューレと気管を穿刺、気管チューブとカニューレの柔軟な部分を挿入します。
- プロシージャの間にモルモットを継続的に換気する動物人工呼吸器を気管チューブに接続します。
注:麻酔は気管チューブを介してイソフルラン 3% で維持されます今 (インスピレーション補助換気と呼吸速度最高のインスピレーシヨン圧力: 100-120/分、ピークのインスピレーシヨン圧力: 18-22 cm 胸が開いている間にのぞき見換気を使用して Hg). - 最初の肋間スペースから始まるリブ スペースをカウントする、5番目の肋間スペースを識別します。モルモットのはさみとピンセットを使用しての左側にある、第五肋で 2 cm の横切開を実行します。小さな動物のリトラクターを挿入します。筋肉解剖、電気焼灼で、肋間筋に達するまでに達した皮下組織を除去後見ることができます。
- 軽くピンセットで肋間筋を解剖、胸膜腔に達するし、1 つ前の左の肺を見ることができます。肋骨の間リトラクターを挿入し、心臓の良い表示が得られるまで慎重に開きます。
- ハサミで前方の左心室壁の領域で心膜約 1 cm を開きます。左心室の cryoinjury を誘導するときの損傷からそれを保護するために左の肺に湿布を配置します。
- 3 分間液体窒素に断面直径 0.5 cm で侵食された金属スタンプ (アルミ製) の先端を配置します。
- プレス、窒素冷却 30 心の左前方壁にプローブ s。電気のはんだごて (250 ° C) それをウォーム アップするスタンプ内に配置を使用して心の底からそれを分離します。貫壁性の心筋障害を取得する 3 回のこの手順を繰り返します。心筋のブランチングを観察します。
- 最大圧力で肺を膨らませる (2 の人工呼吸器の流出管をクランプで s)、肺の無気肺を避けるために。肋間スペースから、リトラクターを削除します。
- 2 つの 3-0 縫合糸で肋骨を閉じます。すぐ、4-0 を実行するいると肋骨の筋肉を縫合します。皮膚の閉鎖 5-0 縫合単一ステッチを使用します。
- 1% に、イソフルランを減らします。動物が自発的に呼吸、気管チューブを削除してフェイス マスク (イソフルラン 2-3%) と麻酔を継続します。
- 十分な麻酔深度を監視する後肢を摘心によって反射の不在を保証します。単一の 8-0 を使用して縫合、気管で穿刺部位を閉じます。3 単一スティッチ 4-0 縫合糸で傷口を閉じます。
- 次の 5 日間、鎮痛薬のブプレノルフィン (0.05 mg/kg 12 時間ごと) とカルプロフェン (24 時間あたり 5 mg/kg) を使用します。
-
EHT (cryoinjury 後 7 日間) の注入
- 誘導室でモルモットを置き、つま先ピンチへの応答の欠乏によってイソフルラン麻酔の深さチェックと動物を麻酔します。
- 4-5 mg/kg カルプロフェンと注入ブプレノルフィン 0.05 mg/kg 皮下 21 G 針と 10 mL の注射器で麻酔導入後。その裏にモルモットを置き、口と鼻を覆うマスクで麻酔を維持します。
注:麻酔の自給は、後肢の足をつまんでチェック必要があります。 - モルモットの足を広げ、テープを使用して位置を修正します。
- ステップ 3.1.4–3.1.6 で説明したように、術前準備を実行します。はさみとピンセットを使用して左の側面の傷領域で 2 cm の横切開を行います。
- 優しく、電気焼灼器を使用して胸膜癒着を解剖します。慎重にハサミで胸膜腔を開きます。中心部を公開する肋骨の拡散機を挿入します。
- 視覚的に健全な周囲の心筋と比較しての淡い色で、梗塞の領域を識別します。梗塞領域に設計された心臓ティッシュのパッチを配置します。
- 2 つの 8-0 で固定します。両側に縫合します。心 (図 1) の非梗塞領域にパッチをセキュリティで保護することを確認します。肺の無気肺を避けるために、圧力で肺を膨らませます。肋間スペースから、リトラクターを削除します。
- 2 つの 3-0 縫合糸で肋骨を閉じます。すぐ、4-0 を実行するいると肋骨の筋肉を縫合します。皮膚の閉鎖 5-0 縫合単一ステッチを使用します。
- 1% に、イソフルランを減らします。動物が自発的に呼吸、気管チューブを削除してフェイス マスク (イソフルラン 2-3%) と麻酔を継続します。
- 十分な麻酔深度を監視する後肢を摘心によって反射の不在を保証します。単一の 8-0 を使用して縫合、気管で穿刺部位を閉じます。すぐ 3 つの単一の傷は、4-0 縫合糸をステッチします。
- 次の 5 日間、鎮痛薬のブプレノルフィン (0.05 mg/kg 12 時間ごと) とカルプロフェン (24 時間あたり 5 mg/kg) を使用します。
- EHT 注入後 4 週間は時間の経過とともに左室機能を監視する経胸壁心エコー検査 (前述の手順 2 で) を実行します。
注:EHT 注入と EHT 注入による心機能の改善を監視するため注入後 4 週間前に左心室機能を監視します。 - IACUC 承認プロトコル、動物を安楽死させるし、外科的さらなる分析のための心の変化します。
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
モルモット EHT パッチによる移植後心筋再生を調査するための適切なモデルです。それは再現性をもって大きい貫壁性心筋傷害をもたらします。瘢痕サイズは 4 週間後 cryoinjury 組織学によって評価されます。メイソン ヒアリン染色貫傷跡 (図 2) を明らかにします。瘢痕サイズ再現性8の高度を反映して負傷した動物の多数に類似していた。平均左室心筋の 25% は、瘢痕組織に置き換えられました。ジストロフィンは部分的に傷 (図 3 a) を remuscularized 実証の大きな心筋移植を染色します。人間 Ku80 の染色 (図 3 b) この新たに形成された心筋の人類の起源を証明しました。高倍率では、これらの移植は密集細胞から成っていることを明らかにしました。経胸壁心エコー法を用いた左室機能が監視されました。EHT インプラントの成功は、LVEF、ショートニング、小数のエリア、左心室末期径 (図 4) の減少の改善によって特徴付けられます。
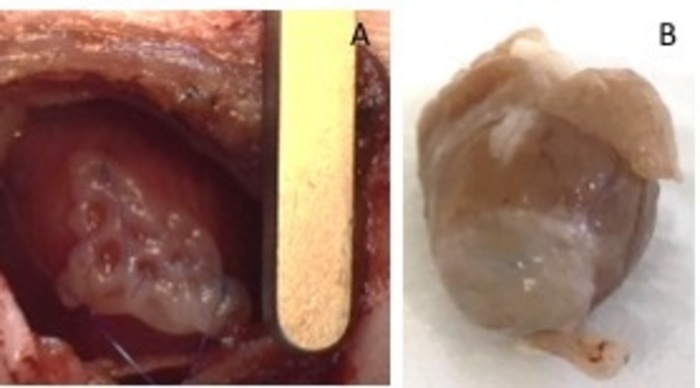
図 1: 注入後 hEHT パッチ。注入後すぐに (A) のパッチ。(B) パッチ移植後 4 週間。この図の拡大版を表示するのにはここをクリックしてください。
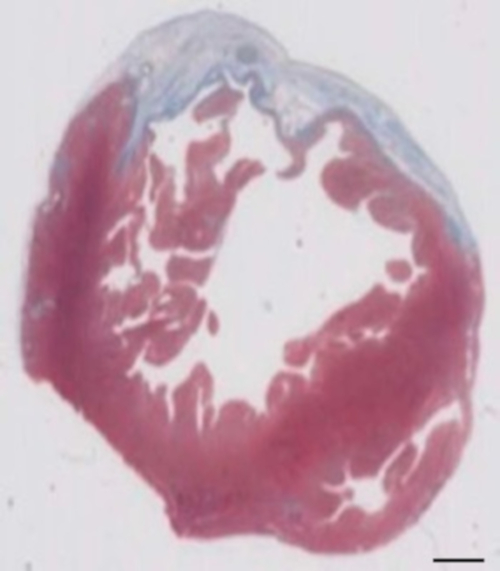
図 2: 28 日 cryoinjury 後パラフィン切片を染色、マッソンの梗塞の定量のヒアリン。梗塞は、線維組織を表すマッソンのヒアリン染色で青の色によって決定されます。スケール バー = 2 mm.この図の拡大版を表示するのにはここをクリックしてください。
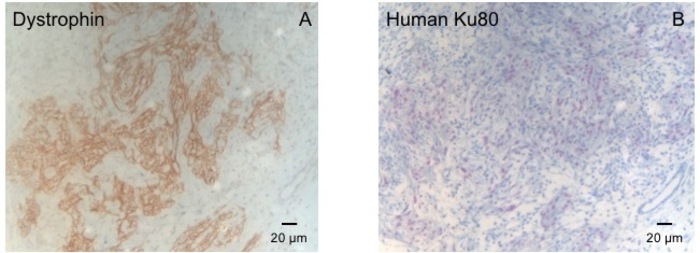
図 3: ジストロフィンと人間 Ku80 染色します。(A) ジストロフィン瘢痕領域 (B) (ブラウン) のショーの大きな筋肉の諸島で染色が心臓を断面パラフィンの区染色します。区 80 はひと特異抗体です。したがって、積極的に陽性細胞 (茶色)、人間の起源から。この図の拡大版を表示するのにはここをクリックしてください。
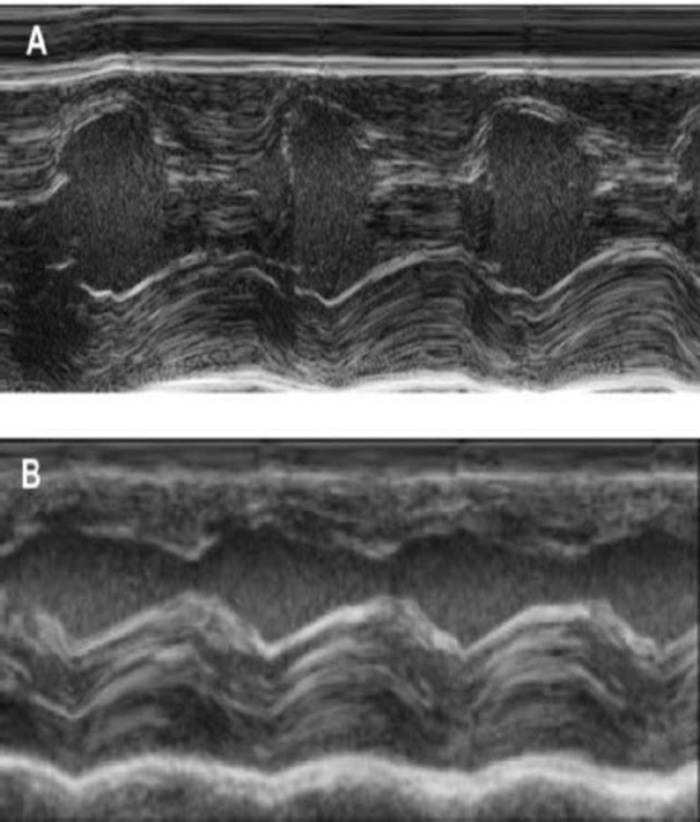
図 4: 経胸壁心エコーを用いた左心室の M-モードの測定。(A) 基準で (B) cryoinjury 後 1 週間。(IV: 心室中隔、LV: 左心室、PW: 後壁)。測定は 3 回が実行されます。ベースライン、1 週間後 cryoinfarction と EHT 注入後 4 週間でこの図の拡大版を表示するのにはここをクリックしてください。
Subscription Required. Please recommend JoVE to your librarian.
Discussion
細胞移植に及ぼす傷害心9,10,11の影響を研究するさまざまな小動物モデルがあります。我々 はすべての小動物のためのモルモット モデル モデル、その (電気) を選んだ生理最も密接に人間のそれに似ています。小動物モデルの利点は、単純な住宅、管理コスト、およびいくつかの労働力です。マウス、ラットと比較してギニア pigs´ 心臓 (電気) 生理は人間により似ています。特に中心頻度は低い (~250/min)、プラトー相を示していますを潜在的な心室のアクションとカリウム電流私kr再分極7にとって重要です。さらに動物の大きいサイズが容易、手術日時開胸は傷害の誘導後必要なの 1 週間は特に重要であります。しかし、モルモットは、いくつかの経験を必要とする麻酔に敏感です。
芝らは、50 mg/kg 2 mg/kg とケタミン キシラジン (i. p.) モルモット心臓 cryoinjury4を麻酔するの使い方を説明します。この麻酔連隊も評価しました。不利な点の 1 つはキシラジンと強力な解毒剤がないためケタミンの麻酔の効果を一時停止することが可能だという事実です。モルモットは手術中に低血糖の危険性が高いことを考えると、我々 は効果がコントロールし、したがって非常に短い麻酔回復局面に至る簡単な麻酔ガスを使用することを決めた。気管切開術は、プロシージャ全体で安全な換気を確保するために使用されます。オロ気管挿管は技術的に非常に厳しいモルモットの気管の開口部の可視化はしばしば困難であり安全な気管挿管を保証することはできませんにします。
冠動脈疾患それ正確に反映しない低温傷害を引き起こす重篤な心筋傷害が/ヒトの心筋梗塞。この点で、若者または虚血再灌流傷害モデルも複数の結紮は密接に人間の病態生理を繰り返します。ただし、モルモットの冠動脈解剖学は、広範な担保が特徴です。ため、左前方降順冠状動脈の結紮術では、モルモット12,13に大きな心筋傷害の再現性をもって発生しません。マウスおよびラットの若者結紮により、大規模な改造や最終的に前方の壁、この程度の人間には見られない特徴が薄くなります。ギニア豚の低温傷害モデル改造プロセスを誘発して心室壁ですがある程度薄くなる、もっと密接のような心筋損傷の人間に見られます。そのためより信頼性の高い心筋傷害の結果 cryoinjury モデルは、13を選ばれました。周の死亡率は、このモデルの主な問題です。最初に、動物の約 30% は、最初の操作中、または心臓外傷後 7 日以内に死亡しました。60% の全体的な死亡率の EHT 注入会計中に別の 30% が死亡しました。いくつかの変更は、死亡率の大幅な減少に します。イソフルランは重い流涎と気管支の分泌を誘導します。アトロピンは、気管支分泌物が減り、死亡率が低下する大きな要因だった。死亡率が大きく低下する第 2 の要因は、心の底から冷たい金属のスタンプを解放するはんだごての使用です。暖かい水最初心筋からのスタンプのデタッチに使用。ただし、胸腔内から水を除去することは困難だった。残りの水の影響の呼吸と animal´s 予後を悪化する密着性の開発につながる。プロシージャに肯定的に影響を与えたもう一つの変更は、圧縮と冷たい金属スタンプから左の肺の保護だった。これらの変更が実装された死亡率 ~ 20% (最初の術後 1 週間含む) 心臓傷害操作と EHT 移植のための別の 25% に落ちた。低温傷害の誘導は技術的に容易に操作を表し、後 5-10 動物が監督の下で運営されている一貫性のある結果を達成することができます。EHT 移植はより厳しいと再現性のある結果が得られるまで、監督の下で約 20 の手術が推奨されます。
初めに、中心部を洗浄し、したがって、左心室壁から冷凍プローブをデタッチ温かい生理食塩水を使用しました。この手順が扱いやすい、生理食塩水の数ミリリットルが呼吸不全のリスクが増大して胸郭に残ります。
結論として、描かれているモルモット モデルは、再現可能な安価な一貫性のある結果につながります。経胸壁心エコー検査は再手術前に心臓の疾患の存在を評価可能と非侵襲的なツールを提供して、グラフト注入が実行されます。
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
作者が競合する金銭的な利益やその他の利害の関係を宣言します。
Acknowledgments
この研究のための資金だった受信ないです。
Materials
| Name | Company | Catalog Number | Comments |
| Ventilator (VetFlo Dual Mode) | Kent Scientific | ||
| Forene | abbvie | 1000009819 | |
| Carprofen | Zoetis | 256692 | |
| Atropin | Braun | PZN 00648037 | |
| Buprenorphin | Sigma | ||
| Metal stamp | |||
| Electric soldering iron | Claytools | ||
| 3-0 prolene suture | Ethicon | ||
| 4-0 prolene suture | Ethicon | 662SLH | |
| 5-0 prolene suture | Ethicon | 8710H | |
| 8-0 prolene suture | Ethicon | 8841H | |
| Tungsten Carbide Scissor | FST | No. 14568-12 | |
| Stainless sterilization Container | FST | No. 20890-51 | |
| Graefe Forceps | FST | No.11652-10 | |
| Extra fine Graefe Forceps | FST | No.11150-10 | |
| Forceps | FST | No. 11022-15 | |
| Halsted- Mosquito | FST | No. 13009-12 | |
| Forceps | FST | No.13003-10 | |
| Baby Mixter | FST | No. 13013-14 | |
| Needle holder (Castroviejo with Tungsten Casbide Jaws) | FST | No. 12565-14 | |
| Needle Holder (Halsey) | FST | No. 12501-13 | |
| Alm Retractor with Blumt Teeth | FST | No. 17008-07 | |
| Spring Scissor | FST | No. 15000-00 | |
| Compress 5x5 | Fink + Walter | PZN 08821417 | |
| Venflon Pro Safety | Becton Dickinson | PZN11123964 | |
| Cautery High Temp 2" | Bovie Medical Corporation | 0100607151011055 |
References
- Kirklin, J. K., et al. Seventh INTERMACS annual report: 15,000 patients and counting. The Journal of heart and lung transplantation: the official publication of the International Society for Heart Transplantation. 34, 1495-1504 (2015).
- Soonpaa, M. H., Field, L. J. Survey of studies examining mammalian cardiomyocyte DNA synthesis. Circulation research. 83, 15-26 (1998).
- Shiba, Y., Hauch, K. D., Laflamme, M. A. Cardiac applications for human pluripotent stem cells. Current pharmaceutical design. 15, 2791-2806 (2009).
- Shiba, Y., et al. Human ES-cell-derived cardiomyocytes electrically couple and suppress arrhythmias in injured hearts. Nature. 489, 322-325 (2012).
- Chong, J. J., et al. Human embryonic-stem-cell-derived cardiomyocytes regenerate non-human primate hearts. Nature. 510, 273-277 (2014).
- Kattman, S. J., et al. Stage-specific optimization of activin/nodal and BMP signaling promotes cardiac differentiation of mouse and human pluripotent stem cell lines. Cell stem cell. 8, 228-240 (2011).
- Watanabe, T., Rautaharju, P. M., McDonald, T. F. Ventricular action potentials, ventricular extracellular potentials, and the ECG of guinea pig. Circulation research. 57, 362-373 (1985).
- Weinberger, F., et al. Cardiac repair in guinea pigs with human engineered heart tissue from induced pluripotent stem cells. Science translational medicine. 8, 363ra148 (2016).
- Shiba, Y., et al. Electrical Integration of Human Embryonic Stem Cell-Derived Cardiomyocytes in a Guinea Pig Chronic Infarct Model. Journal of Cardiovascular Pharmacology and Therapy. 19, 368-381 (2014).
- van Laake, L. W., et al. Human embryonic stem cell-derived cardiomyocytes survive and mature in the mouse heart and transiently improve function after myocardial infarction. Stem cell research. 1, 9-24 (2007).
- Zimmermann, W. H., et al. Engineered heart tissue grafts improve systolic and diastolic function in infarcted rat hearts. Nature medicine. 12, 452-458 (2006).
- Johns, T. N., Olson, B. J. Experimental myocardial infarction. I. A method of coronary occlusion in small animals. Annals of surgery. 140, 675-682 (1954).
- van den Bos, E. J., Mees, B. M., de Waard, M. C., de Crom, R., Duncker, D. J. A novel model of cryoinjury-induced myocardial infarction in the mouse: a comparison with coronary artery ligation. Heart and circulatory physiology. , H1291-H1300 (2005).



