Summary
सीरियल ब्लॉक-फेस स्कैनिंग इलेक्ट्रॉन माइक्रोस्कोपी (SBEM) को मूर्ति पर लागू किया जाता है और मुरीन हिप्पोकैम्पस में डेंड्रिटिक कताई का विश्लेषण किया जाता है।
Abstract
त्रि-आयामी इलेक्ट्रॉन माइक्रोस्कोपी (3 डी ईएम) नैनोस्केल रिज़ॉल्यूशन के साथ डेंड्रिटिक कताई के रूपात्मक मापदंडों का विश्लेषण करने की संभावना देता है। इसके अलावा, डेंड्रिटिक कताई की कुछ विशेषताएं, जैसे कि रीढ़ की मात्रा और पोस्ट-सिनैप्टिक घनत्व (PSD) (सिनैप्स के पोस्ट-सिनेप्टिक भाग का प्रतिनिधित्व करना), प्रेसिनैप्टिक टर्मिनल की उपस्थिति, और पीएसडी (जैसे, बहु-इनरवेटेड कताई) का चिकनी एंडोप्लाज्मिक रेटिकुलम या असामान्य रूप, केवल 3 डी ईएम के साथ देखा जा सकता है। धारावाहिक ब्लॉक-फेस स्कैनिंग इलेक्ट्रॉन माइक्रोस्कोपी (एसबीईएम) को नियोजित करके पारंपरिक धारावाहिक अनुभागिंग करने की तुलना में 3डी ईएम डेटा आसान और अधिक प्रजनन तरीके से प्राप्त करना संभव है। यहां हम दिखाते हैं कि SBEM विश्लेषण के लिए माउस हिप्पोकैम्पल नमूने कैसे तैयार करें और इस प्रोटोकॉल को डेंड्रिटिक कताई के इम्यूनोफ्लोरेसेंस अध्ययन के साथ कैसे जोड़ा जा सकता है। हल्के निर्धारण परफ्यूजन हमें मस्तिष्क के एक आधे हिस्से पर हल्के माइक्रोस्कोपी के साथ इम्यूनोफ्लोरेसेंस अध्ययन करने की अनुमति देता है, जबकि दूसरा आधा SBEM के लिए तैयार किया गया था। इस दृष्टिकोण से अध्ययन के लिए इस्तेमाल किए जाने वाले जानवरों की संख्या कम हो गई है ।
Introduction
केंद्रीय तंत्रिका तंत्र में अधिकांश उत्तेजक सिनेप्स डेंड्रिटिक कताई पर स्थित होते हैं - एक न्यूरोनल झिल्ली के छोटे फलाव। ये फलाव जैव रासायनिक डिब्बों को सीमित करते हैं जो इंट्रासेलुलर सिग्नल ट्रांसडक्शन को नियंत्रित करते हैं। डेंड्रिटिक कताई और सिनैप्स की संरचनात्मक प्लास्टिसिटी का सिनैप्टिक प्रभावकारिता में कार्यात्मक परिवर्तनों से गहरा संबंध है जो सीखने और स्मृति1,2के रूप में ऐसी महत्वपूर्ण प्रक्रियाओं को रेखांकित करता है। यह ध्यान रखना महत्वपूर्ण है कि इलेक्ट्रॉन माइक्रोस्कोपी (ईएम) एकमात्र तकनीक है जो यह निर्धारित करने की अनुमति देती है कि क्या एक डेंड्रिटिक रीढ़ में प्रेसिनैप्टिक इनपुट है। ईएम संकल्प को अल्ट्रास्ट्रक्चरल विवरणों जैसे कि एक पोस्टसिनैप्टिक घनत्व (पीएसडी) के आकार का अध्ययन करने की भी आवश्यकता है, जो एक सिनेप्स के एक पोस्टसिनैप्टिक भाग का प्रतिनिधित्व करता है, या एक डेंड्रिटिक रीढ़ के आयामों के साथ-साथ एक अक्षीय मुक्केबाज़ी के आकार और आकार का प्रतिनिधित्व करता है। इसके अतिरिक्त, ईएम के साथ सिनेप्स और उनके परिवेश की कल्पना करना संभव है।
इमेजिंग और कंप्यूटिंग प्रौद्योगिकियों में प्रगति के लिए धन्यवाद, पूरे तंत्रिका सर्किट का पुनर्निर्माण करना संभव है। वॉल्यूम इलेक्ट्रॉन माइक्रोस्कोपी तकनीक, जैसे सीरियल सेक्शन ट्रांसमिशन इलेक्ट्रॉन माइक्रोस्कोपी (एसएसईएम), सीरियल ब्लॉक-फेस स्कैनिंग इलेक्ट्रॉन माइक्रोस्कोपी (एसबीईएम), और केंद्रित आयन बीम स्कैनिंग इलेक्ट्रॉन माइक्रोस्कोपी (एफआईबी-एसईएम) आमतौर पर न्यूरोनल सर्किट पुनर्निर्माण 3 के लिए उपयोग कियाजाताहै।
हमारे अध्ययनों में, एसबीईएम विधि को माउस हिप्पोकैम्पस और ऑर्गेनोइटिक ब्रेन स्लाइस 4, 5के नमूनों में डेंड्रिटिक कताई और पीएसडी की संरचनात्मक प्लास्टिसिटी की जांच करने के लिए सफलतापूर्वकनियोजितकिया गया है। एसबीईएम स्कैनिंग इलेक्ट्रॉन माइक्रोस्कोप चैंबर 6 ,7,8,9केअंदर एक लघु अल्ट्रामाइक्रोटोम की स्थापना पर आधारित है । नमूना ब्लॉक के शीर्ष को चित्रित किया जाता है, और फिर नमूना अल्ट्रामाइक्रोटोपोम द्वारा एक निर्दिष्ट गहराई पर काटा जाता है, जो एक नए ब्लॉक-फेस का खुलासा करता है, जिसे फिर से इमेज किया जाता है और फिर प्रक्रिया8दोहराई जाती है। नतीजतन, केवल ब्लॉक-फेस की छवि बची है जबकि जो टुकड़ा काटा गया है वह मलबे के रूप में खो गया है। यही कारण है कि SBEM एक विनाशकारी तकनीक कहा जाता है, जिसका अर्थ है कि एक ही जगह को फिर से छवि करना संभव नहीं है। हालांकि, विनाशकारी ऑन-ब्लॉक विधियों का लाभ यह है कि वे विकृत समस्याओं और अनुभाग हानि से पीड़ित नहीं हैं जो डेटा गुणवत्ता और डेटा विश्लेषण3को काफी प्रभावित कर सकते हैं। इसके अलावा, SBEM उच्च संकल्प3पर अपेक्षाकृत बड़े क्षेत्र (> 0.5 मिमी × 0.5 मिमी) को छवि देने की संभावना देता है।
SBEM को नियोजित करने के लिए, नमूनों को छवियों को प्राप्त करने के लिए उपयोग किए जाने वाले बैकस्कैटर इलेक्ट्रॉन डिटेक्टर के कारण एक समर्पित, अत्यधिक विषम प्रोटोकॉल के अनुसार तैयार किया जाना चाहिए । हम यहां दिखाते हैं कि1 9 80 केदशकमें विकसित कम ऑस्मियम-थिओकार्बोहाइड्रेजाइड-ऑस्मिम (रोओटो) दाग का उपयोग करके डियरिंक 10 (नेशनल सेंटर फॉर माइक्रोस्कोपी एंड इमेजिंग रिसर्च (एनसीएमआईआर) विधि द्वारा विकसित प्रक्रिया के आधार पर प्रोटोकॉल के अनुसार नमूना तैयारी कैसेकरें। इसके अलावा, हम हल्के निर्धारण परफ्यूजन के साथ एक दो-चरण निर्धारण दृष्टिकोण पेश करते हैं जो हल्के माइक्रोस्कोपी और एसबीईएम के साथ इम्यूनोफ्लोरेसेंस अध्ययन के लिए एक ही मस्तिष्क का उपयोग करने की अनुमति देता है।
प्रोटोकॉल में एक माउस मस्तिष्क मुख्य रूप से एक हल्के फिक्सेटिव के साथ तय किया जाता है, और फिर हिस्सों में काट दिया जाता है, और एक गोलार्द्ध को इम्यूनोफ्लोरेसेंस (आईएफ) के लिए पोस्टफिक्स और तैयार किया जाता है, जबकि दूसरा ईएम अध्ययन(चित्रा 1)के लिए।

चित्रा 1। SBEM के साथ विश्लेषण के लिए डेंड्रिटिक कताई की तैयारी के लिए वर्कफ्लो का योजनाबद्ध प्रतिनिधित्व। चूहों का बलिदान किया गया था और एक हल्के प्राथमिक स्थिर के साथ छिद्रित किया गया था। मस्तिष्क को हिस्सों में काट दिया गया था, और एक गोलार्द्ध को इम्यूनोफ्लोरेसेंस (आईएफ) के साथ पोस्टफिक्स किया गया था- समर्पित फिक्सेटिव, क्रायोप्रोटेक्टेड, क्रायोस्टेट का उपयोग करके कटा हुआ और यदि अध्ययन के लिए संसाधित किया गया था, जबकि दूसरे गोलार्द्ध को ईएम फिक्सेटिव के साथ पोस्टफिक्स किया गया था, वाइब्रेटोम के साथ कटा हुआ था और ईएम अध्ययन के लिए तैयार किया गया था। SBEM अध्ययन के लिए मस्तिष्क स्लाइस विपरीत थे, राल में एम्बेडेड फ्लैट, तो हिप्पोकैम्पस के एक CA1 क्षेत्र पिन करने के लिए मुहिम शुरू की थी, और SBEM(चित्रा 1)के साथ छवि ) । एक पीले बॉक्स में प्रकाश डाला प्रोटोकॉल का हिस्सा वीडियो में चित्रित किया गया था । कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें ।
Subscription Required. Please recommend JoVE to your librarian.
Protocol
यह शोध Nencki संस्थान के दिशा-निर्देशों और स्थानीय नैतिक समिति की अनुमति के अनुपालन में किया गया था । यह अध्ययन 24 नवंबर १९८६ (86/609/EEC), पोलैंड के पशु संरक्षण अधिनियम के यूरोपीय समुदाय परिषद के निर्देश के अनुसार किया गया था और वारसॉ में पहली स्थानीय आचार समिति द्वारा अनुमोदित किया गया था । इस्तेमाल किए गए जानवरों की संख्या और उनकी तकलीफों को कम करने के लिए तमाम प्रयास किए गए।
सावधानी: नीचे वर्णित सभी प्रक्रियाओं को प्रयोगशाला धूम हुड में किया जाना चाहिए। इस्तेमाल किए गए रिएजेंट्स की खतरनाक प्रकृति के कारण। दस्ताने, लैब कोट, सुरक्षा चश्मा और एक चेहरा मुखौटा जैसे व्यक्तिगत सुरक्षा उपायों की आवश्यकता है।
1. परफ्यूजन के लिए फिक्सेटिव की तैयारी (2% wt/vol पैराफॉर्मलडिहाइड (पीएफए) और 0.5% vol/vol ग्लूटारल्डिहाइड (GA) में 0.1 एम फॉस्फेट बफर (पीबी), पीएच 7.4)
नोट: उसी दिन फिक्सेटिव समाधान तैयार करें क्योंकि इसका उपयोग किया जाएगा और इसे 3 घंटे तक स्टोर न करें। समय की कमी के मामले में, एक दिन पहले 0.1 एम पीबी में 2% पीएफए तैयार करें, इसे 4 डिग्री सेल्सियस पर स्टोर करें और परफ्यूजन से कुछ देर पहले ताजा जीए जोड़ें।
- बाँझ डबल आसुत पानी (डीडीएच2ओ) का 400 एमएल लें और एक सरगर्मी गर्म प्लेट का उपयोग करके इसे 60 डिग्री सेल्सियस तक गर्म करें। इसके बाद इसमें 20 ग्राम पीएफए डालें। 1 एम NaOH की बूंदें जोड़ें जब तक पीएफए पूरी तरह से भंग हो जाता है और मिश्रण को ठंडा करने की अनुमति देता है।
- 0.2 एम पीबी (पीएच 7.4) के 500 एमएल जोड़ें।
- किसी भी जमा को हटाने के लिए समाधान को फ़िल्टर करें और इसे 4 डिग्री सेल्सियस तक ठंडा करें।
- पर्फ्यूजन से ठीक पहले, समाधान में 25% GA के 20 एमएल जोड़ें और फिर डीडीएच 2 ओ से1एल के साथ वॉल्यूम को ऊपर करें।
2. SBEM के लिए पोस्टपरफ्यूजन फिक्सेटिव की तैयारी (2% wt/vol पीएफए और 2.5% vol/vol GA में 0.1 M PB, पीएच 7.4)
- परफ्यूजन के लिए फिक्सेटिव के 50 एमएल (0.1 एम पीबी में 2% पीएफए और 0.5% GA) लें।
- 25% GA के 5 एमएल जोड़ें।
3. यदि धुंधला (फॉस्फेट बफर खारा (पीबीएस) में 4% पीएफए के लिए पोस्टपरफ्यूजन फिक्सेटिव की तैयारी
- निर्माता निर्देशों के अनुसार एक शुद्ध और deionized पानी (एच 2 ओ) में 1x पीबीएस (पीएच7.4)की एक गोली भंग करें।
- समाधान को 60 डिग्री सेल्सियस तक गर्म करने के लिए एक सरगर्मी गर्म प्लेट का उपयोग करें और पीएफए के 40 ग्राम जोड़ें।
- पीएफए पूरी तरह से भंग होने तक 1 एम नाओएच की बूंदें जोड़ें और मिश्रण को ठंडा होने दें।
- 1 एम एचसीएल के साथ समाधान के पीएच को 7.5 तक समायोजित करें फिर एच 2 ओ से1एल के साथ वॉल्यूम को टॉप करें।
- किसी भी जमा को हटाने के लिए समाधान फ़िल्टर करें।
4. जानवरों का ट्रांसकार्डियल परफ्यूजन
नोट: सभी पीएफए और GA कचरे को एकत्र किया जाना चाहिए और स्थानीय नियमों के अनुसार निपटान के लिए संग्रहीत किया जाना चाहिए । संज्ञाहरण और पर्फ्यूजन स्थानीय नियमों का पालन करना चाहिए । वर्णित प्रोटोकॉल वयस्क में 3 महीने पुराने और 20±1 महीने पुरानी महिला Thy1-GFP (एम) चूहों (Thy1-GFP +/-)12 ग्लूटामेटर्जिक न्यूरॉन्स की एक विरल वितरित आबादी में हरी फ्लोरेसेंस प्रोटीन (GFP) व्यक्त किया गया था, लेकिन किसी भी अंय के रूप में अच्छी तरह से इस्तेमाल किया जा सकता है । जानवरों को Nencki प्रायोगिक जीव विज्ञान संस्थान के पशु घर में C57BL/6J पृष्ठभूमि के साथ heterozygotes के रूप में पैदा किया गया ।
- पर्फ्यूजन से पहले इंट्रापेरिटोनियल इंजेक्शन (27 गेज सुई) के माध्यम से एक केटामाइन/जाइलाज़ीन मिश्रण (९० मिलीग्राम/किलोग्राम शरीर वजन केटामाइन और 10 मिलीग्राम/किलोग्राम शरीर के वजन जाइलाज़ीन) के प्रशासन द्वारा एक माउस को एनेस्थेटाइज करें ।
- आकलन करें कि दर्द उत्तेजनाओं (चुटकी) और कॉर्नियल रिफ्लेक्स (भेंगापन) के लिए पलटा की जांच करके संज्ञाहरण की गहराई पर्याप्त है या नहीं।
- 20 मिनट के बाद सोडियम पेंटोबार्बिटल (50 मिलीग्राम/किलोग्राम शरीर के वजन) का इंट्रापेरिटोनियल इंजेक्शन (27 गेज सुई) करें।
- पण एट अल द्वारा वर्णित एक पर्फ्यूजन सर्जरी प्रोटोकॉल के अनुसार एक माउस को पर्फ्यूजकरें (बिंदु 4 देखें; चित्रा 5-6) । 3 मिनट के लिए 0.1 एम फॉस्फेट बफर, पीएच 7.4 (30 एमएल) के साथ एक पर्फ्यूजन पंप का उपयोग करना शुरू करना और 0.1 एम पीबी में 2% पीएफए और 0.5% GA के साथ जारी रखें, पीएच 7.4 6 मिनट (80 मिलीएल) के लिए।
- धीरे खोपड़ी से मस्तिष्क विच्छेदन और यह आधे में विभाजित (पण एट अल में चित्रा 9-10 देखें., २०१२13)। एक शीशी में एक टुकड़ा रखें जिसमें SBEM के लिए फिक्सेटिव होता है और दूसरा 4% पीएफए/पीएफबी के साथ शीशी में यदि धुंधला होने के लिए।
- गोलार्ध को रात भर 4 डिग्री सेल्सियस पर फिक्सेटिव में रखें।
5. इलेक्ट्रॉन माइक्रोस्कोपी के लिए मस्तिष्क स्लाइस तैयारी
- वाइब्रेटम सेटिंग्स चुनें (ब्लेड यात्रा की गति: 0.075 मिमी/
- स्लाइस चैंबर को धारक में रखें, इसे वाइब्रेटम से अटैच करें और इसे बर्फ से घेर लें। फिर एक रेजर ब्लेड को वाइब्रेटम ब्लेड धारक में रखें।
- एक चम्मच, या इसी तरह की वस्तु का उपयोग करें और ठंडा मस्तिष्क (पृष्ठीय सतह ऊपर) एक कठिन काटने की सतह पर जगह (उदाहरण के लिए, एक गिलास पेट्री डिश ढक्कन) । हिप्पोकैम्पस का एक कोरोनल टुकड़ा तैयार करने के लिए सेरेब्रल गोलार्द्ध और सेरिबैलम के बीच एक रेजर ब्लेड या स्केलपेल के साथ एक लंबवत कटौती करें, इस प्रकार सेरिबैलम को हटा दें। घ्राण बल्ब को भी हटाया जा सकता है।
- वाइब्रेटम के ड्राई प्लेटफॉर्म पर सायनोएक्रिलेट गोंद लगाएं।
- संदंश के साथ मस्तिष्क उठाओ और ध्यान से फिल्टर कागज पर सूखी।
- ऊपर की ओर रोस्ट्रल टिप के साथ काटने वाले ब्लेड के करीब मंच पर गोलार्द्ध को गोंद करें। धारक को मंच संलग्न करें और तुरंत इसे बर्फ-ठंड 0.1 मीटर पीबी, पीएच 7.4 से भरें। यदि लंबवत कटौती ठीक से की जाती है, तो गोलार्द्ध सीधे हिप्पोकैम्पस युक्त सममित कोरोनल कट बनाने के लिए आवश्यक 90 डिग्री कोण प्रदान करेगा। विश्वास दिलाता हूं कि मस्तिष्क पीबी से ढका हुआ है।
- गोलार्द्ध के सामने वाइब्रेटम ब्लेड की स्थिति और गोलार्द्ध के कोरोनल पक्ष को कम करें। ब्लेड को कौडल दिशा में 400 माइक्रोन तक कम करें और स्लाइसिंग शुरू करें। पहले दो स्लाइस पूरी तरह से ऊतक ब्लॉक से अलग हो रहे हैं जब तक टुकड़ा करने की क्रिया जारी रखें।
- ब्लेड को वापस लें और एक और 100 माइक्रोन कम करें, फिर फिर से स्लाइस करें।
- जब हिप्पोकैम्पस दिखाई देता है (माउस ब्रेन एटलस पैक्सिनोस और फ्रैंकलिन, 200414का उपयोग करें) छोटे तूलिका या चौड़ा प्लास्टिक पाश्चर पिपेट के साथ स्लाइस इकट्ठा करें।
- स्लाइस को ठंड 0.1 एम पीबी, पीएच 7.4 से भरी 12-अच्छी प्लेट में स्थानांतरित करें।
- एक रेजर ब्लेड या स्केलपेल का उपयोग करके 0.1 एम पीबी, पीएच 7.4 से भरे ग्लास पेट्री डिश में हिप्पोकैम्पस को विच्छेदन करें, और इसे उसी फॉस्फेट बफर के साथ ग्लास शीशियों में डाल दें।
नोट: स्लाइस के दीर्घकालिक भंडारण के लिए 0.05% सोडियम एजाइड (एनएएन3)के साथ 0.1 एम पीबी पूरक।
6. इम्यूनोदाता के लिए मस्तिष्क नमूना तैयारी
- एक धुएं के हुड में 4% पीएफए/पीबीएस समाधान में रात भर निर्धारण के बाद, मस्तिष्क के ऊतकों को क्रायोप्रिजर्वेशन समाधान में डाल दें (0.05% एनएएन 3 के साथ पीबीएस में30%सुक्रोज) और इसे 2 दिनों के लिए 4 डिग्री सेल्सियस पर रखें (डूबने तक)।
- एक एंटीफ्रीज समाधान (15% सुक्रोज/30% एथिलीन ग्लाइकोल/0.05% एनएएन3/पीबीएस) तैयार करें।
- क्रायोस्टेट के कैबिनेट तापमान को -19 डिग्री सेल्सियस पर सेट करें और सुनिश्चित करें कि आगे बढ़ने से पहले तापमान पहुंच गया है। सेक्शनिंग के दौरान, सुनिश्चित करें कि कैबिनेट का तापमान -18 डिग्री सेल्सियस और -20 डिग्री सेल्सियस के बीच रहता है।
- एक चम्मच, या इसी तरह की वस्तु का उपयोग करें और ठंडा मस्तिष्क (पृष्ठीय सतह ऊपर) एक कठिन काटने की सतह पर जगह (उदाहरण के लिए, एक गिलास पेट्री डिश ढक्कन) । हिप्पोकैम्पस का एक कोरोनल टुकड़ा तैयार करने के लिए सेरेब्रल गोलार्द्ध और सेरिबैलम के बीच एक रेजर ब्लेड या स्केलपेल के साथ एक लंबवत कटौती करें, इस प्रकार सेरिबैलम को हटा दें।
- एक पूर्व ठंडा नमूना डिस्क का चयन करें, यह एक मुक्त शेल्फ पर ठंड के लिए एक माध्यम के साथ कवर और संदंश का उपयोग कर एक रोस्ट्रल टिप के साथ डिस्क के लिए गोलार्द्ध को ठीक ऊपर की ओर और जब तक नमूना पूरी तरह से जमे हुए है रुको । नमूना डिस्क को एक नमूना सिर में डालें।
- क्रायो-चैंबर के अंदर एक ब्लेड धारक में एक ब्लेड स्थापित करें और 40 माइक्रोन मोटी स्लाइस काटें।
- ठंडे एंटी-फ्रीज समाधान से भरी 96-अच्छी प्लेट में एक छोटी तूलिका के साथ स्लाइस स्थानांतरित करें और धीरे-धीरे वर्गों को खोलें (स्लाइस कक्ष में खो जाने से रोकने के लिए टुकड़ा करने की क्रिया के प्रत्येक दौर के बाद एक टुकड़ा इकट्ठा करें)।
नोट: दिमाग या वर्गों को लंबे समय तक -20 डिग्री सेल्सियस पर एंटीफ्रीज समाधान में संग्रहीत किया जा सकता है।
7. मस्तिष्क स्लाइस की इम्यूनोदाता
नोट: सभी धुंधला कदम एक मंच शेखर पर एक 24 अच्छी तरह से थाली में प्रदर्शन किया गया ।
- स्लाइस को तीन बार पीबीएस के साथ धोएं, हर बार 6 मिनट के लिए।
- अवरुद्ध समाधान के 300 माइक्रोन में इनक्यूबेट स्लाइस (5% सामान्य गधा सीरम (एनडीएस) /0.3% ट्राइटन एक्स-100) 1 घंटे के लिए एक रोटेटर पर कोमल मिलाते हुए के साथ।
- पीएसडी-95 के खिलाफ प्राथमिक एंटीबॉडी के साथ स्लाइस को 5% एनडीएस/0.3% ट्राइटन एक्स-100/पीबीएस (300 माइक्रोल प्रति कुएं) में रात भर 4 डिग्री सेल्सियस पर पतला कर दिया गया। प्राथमिक एंटीबॉडी की अंतिम एकाग्रता 2 μg/mL है ।
- कमरे के तापमान (आरटी) पर 0.3% ट्राइटन एक्स-100/पीबीएस के साथ स्लाइस धोएं, हर बार 6 मिनट के लिए।
- माध्यमिक एंटीबॉडी के साथ इनक्यूबेट स्लाइस 0.3% ट्राइटन एक्स-100/ पीबीएस के 300 माइक्रोल में 1:500 पतला 90 मिनट के लिए। माध्यमिक एंटीबॉडी की अंतिम एकाग्रता 4 μg/mL है ।
- स्लाइस को तीन बार पीबीएस के साथ धोएं, हर बार 6 मिनट के लिए।
- एक बढ़ते माध्यम का उपयोग कर स्लाइड पर स्लाइस माउंट और फिर उन्हें एक कवर स्लाइड के साथ बंद करो।
- एक कॉन्फोकल माइक्रोस्कोप (63 × तेल उद्देश्य, एनए 1.4, पिक्सेल आकार 0.13 माइक्रोन × 0.13 माइक्रोन) का उपयोग करके नमूनों की जांच करें।
नोट: दीर्घकालिक भंडारण के लिए: नमूनों को 4 डिग्री सेल्सियस पर रखें, उन्हें प्रकाश से बचाएं।
8. SBEM नमूना तैयारी
सावधानी: अभिकर्मकों की खतरनाक प्रकृति के कारण नीचे वर्णित सभी प्रक्रियाओं का उपयोग प्रयोगशाला धूम हुड में किया जाना चाहिए। इन रसायनों का उपयोग करने से पहले ध्यान से सामग्री सुरक्षा डेटा निर्माताओं द्वारा प्रदान की चादरें पढ़ें और सुरक्षित हैंडलिंग और अपशिष्ट निपटान सुनिश्चित करने के लिए स्थानीय नियमों के बारे में सुरक्षा अधिकारी से पूछो ।
- नमूना विषम
नोट: स्लाइस धोने और कमरे के तापमान इनक्यूबेशन हल्के मिलाते हुए (उदाहरण के लिए, एक मंच शेखर पर) के साथ किया जाना चाहिए । ऑटोक्लेव डिगासेस्ड पानी का उपयोग किया गया था।- स्लाइस को ठंडे 0.1 एम पीबी, पीएच 7.4 पांच बार, हर बार 3 मिनट के लिए धोएं।
- 4% जलीय ऑस्मियम टेट्रोएक्साइड और 3% पोटेशियम फेरोसाइनाइड (vol द्वारा 1:1) का 1:1 मिश्रण तैयार करें। अंतिम उत्पाद भूरा हो जाएगा। इस मिश्रण में नमूनों को विसर्जित करें, उन्हें बर्फ पर रखें, और इस चरण के बाद से उन्हें प्रकाश से बचाना महत्वपूर्ण है। उन्हें 1 घंटे के लिए कोमल मिलाते हुए के साथ इनक्यूबेट।
- इस बीच एक थिओकार्बोहाइड्रेजाइड (TCH) समाधान तैयार करें। डबल-डिस्टिल्ड एच 2 ओ (डीडीएच2ओ) और0.1ग्राम TCH के 10 एमएल को मिलाएं और इसे 1 घंटे के लिए 60 डिग्री सेल्सियस पर सेट ओवन में रखें। समय-समय पर समाधान को चक्कर लगाना महत्वपूर्ण है (उदाहरण के लिए, हर 10 मिनट में)। तैयार होने पर, इसे कमरे के तापमान में ठंडा करें।
- स्लाइस को डीएच2O पांच बार, हर बार 3 मिनट के लिए धोएं।
- 0.22 माइक्रोन सिरिंज फ़िल्टर का उपयोग करके टीसीएच समाधान को फ़िल्टर करें और फ़िल्टर किए गए समाधान में नमूने को विसर्जित करें। स्लाइस काले हो जाएंगे। उन्हें कमरे के तापमान पर 20 मिनट के लिए इनक्यूबेट।
- नमूनों को डीएच2O पांच बार, हर बार 3 मिनट के लिए धोएं।
- कमरे के तापमान पर 30 मिनट के लिए ओसो4 के 2% जलीय समाधान के साथ नमूनों को इनक्यूबेट करें।
- नमूनों को डीएच2O पांच बार, हर बार 3 मिनट के लिए धोएं।
- नमूनों को फ़िल्टर किए गए 1% जलीय यूरेसिल एसीटेट में रखें और उन्हें रात भर 4 डिग्री सेल्सियस पर इनक्यूबेट करें। छानने के लिए 0.22 माइक्रोन सिरिंज फिल्टर का उपयोग करें।
- एल-एस्पार्टिक एसिड समाधान को 0.4 ग्राम एल-एस्पार्टिक एसिड और डीडीएच2ओ के 80 एमएल मिलाकर तैयार करें, आसान घुलने के लिए पीएच को 3.8 तक समायोजित करें, और फिर पानी के साथ 100 मिलीएल तक टॉप करें।
- अगले दिन, वाल्टन के नेतृत्व aspartate15 तैयारी के साथ शुरू करते हैं । एल-एस्पार्टिक एसिड सॉल्यूशन (पॉइंट 8.1.10) के 10 एमएल के साथ लीड नाइट्रेट के 0.066 ग्राम को 60 डिग्री सेल्सियस तक प्री-गर्म और पीएच को 1 एम नाओएच के साथ 5.5 (60 डिग्री सेल्सियस पर मापा जाता है) में समायोजित करें। शीशी को लेड एस्पार्टेट के साथ बंद करें और इसे वॉटर बाथ में 30 मिनट के लिए 60 डिग्री सेल्सियस पर छोड़ दें। समाधान स्पष्ट होना चाहिए। यदि यह बादल बदल जाता है, यह त्याग दिया जाना चाहिए और एक नया एक तैयार होने की जरूरत है ।
- इस दौरान हर बार 3 मिनट के लिए डीएच2ओ को पांच बार डिगासेड डीडीएच से धोएं। फिर इन्हें 30 मिनट के लिए 60 डिग्री सेल्सियस पर ओवन सेट में रखें।
- नमूनों को ताजा तैयार लेड एस्पार्टेट समाधान में विसर्जित करें और उन्हें 20 मिनट के लिए 60 डिग्री सेल्सियस पर ओवन सेट में इनक्यूबेट करें।
- नमूनों को डीएच2O पांच बार, हर बार 3 मिनट के लिए धोएं।
- निर्जलीकरण और राल एम्बेडिंग
- एपॉक्सी राल तैयार करें। सामग्री (घटक ए/एम के 33.3 ग्राम, घटक बी के 33.3 ग्राम, और घटक डी के 1 ग्राम) का वजन करें और राल को अच्छी तरह से मिलाएं (उदाहरण के लिए, इसे 15 एमएल ट्यूब में रोटरी शेकर पर हिलाएं) एक्सीलेटर डीएमपी 30 की 16 बूंदों को जोड़ने से पहले कम से कम 30 मिनट के लिए। एक और 10 मिनट के लिए फिर से हिलाओ ।
नोट: धुएं हुड के नीचे सामग्री का वजन करें। घटकों की यह राशि राल के लगभग 60 एमएल देता है जो नमूनों के साथ 15 शीशियों के लिए पर्याप्त है। आप कम तैयारी कर सकते हैं या 4 डिग्री सेल्सियस पर एक सिरिंज में राल के बाकी स्टोर और अगले दिन इसका उपयोग कर सकते हैं। सिरिंज की नोक को सील करना याद रखें। - इथेनॉल (30%, 50%, 70%, 90%, 100%, पानी में 100% इथेनॉल और 100% एक आणविक छलनी पर सूख) के ग्रेडेड कमजोर पड़ने के साथ शीशियों को तैयार करें।
- 50% राल प्राप्त करने के लिए 1:1 अनुपात में 100% इथेनॉल के साथ राल मिलाएं। इसे अच्छी तरह मिला लें।
- 30% से शुरू इथेनॉल के प्रत्येक कमजोर पड़ने में 5 मिनट के लिए नमूनों को निर्जलित करें और आणविक छलनी पर सूख गए 100% निर्जल इथेनॉल के साथ समाप्त होते हैं। याद रखें, नमूनों को पूरी तरह से सूखना नहीं चाहिए।
- 30 मिनट के लिए 50% राल में पहले नमूनों घुसपैठ, एक घंटे के लिए 100% राल में अगले, और फिर रात भर 100% राल में। लगातार धीमी गति से मिलाते हुए सभी घुसपैठ कदम प्रदर्शन करते हैं।
- अगले दिन, नमूनों को एक घंटे के लिए ताजा 100% राल में रखें और फिर उन्हें फ्लोरोपॉलिमर एम्बेडिंग शीट्स के बीच एम्बेड करें। इथेनॉल के साथ एम्बेडिंग शीट के डेग्रीज टुकड़े, और फ्लैट समर्थन के रूप में दो ग्लास स्लाइड का उपयोग करके, इसके दो परतों के बीच नमूनों को एम्बेड करते हैं। नमूने पर या उसके करीब राल में हवा के बुलबुले से बचने की कोशिश करें।
- कम से कम 48 घंटे के लिए 70 डिग्री सेल्सियस पर ओवन में नमूनों का इलाज करें।
- एपॉक्सी राल तैयार करें। सामग्री (घटक ए/एम के 33.3 ग्राम, घटक बी के 33.3 ग्राम, और घटक डी के 1 ग्राम) का वजन करें और राल को अच्छी तरह से मिलाएं (उदाहरण के लिए, इसे 15 एमएल ट्यूब में रोटरी शेकर पर हिलाएं) एक्सीलेटर डीएमपी 30 की 16 बूंदों को जोड़ने से पहले कम से कम 30 मिनट के लिए। एक और 10 मिनट के लिए फिर से हिलाओ ।
- ट्रिमिंग और बढ़ते
- एम्बेडिंग शीट को अलग करें और एम्बेडेड नमूने का एक टुकड़ा (लगभग 1 मिमी x 1 मिमी) एक रेजर ब्लेड के साथ काटें। इसे पैराफिल्म में ट्रांसफर करें। इससे इलेक्ट्रोस्टैटिक्स के कारण सैंपल खोने का खतरा कम हो जाएगा।
- एक एल्यूमीनियम पिन लें जिसे इथेनॉल से डीग्रीड किया गया है। एक प्रवाहकीय एपॉक्सी को अच्छी तरह से मिलाएं और नमूने को पिन पर माउंट करने के लिए थोड़ी मात्रा का उपयोग करें। 10 मिनट के लिए 70 डिग्री सेल्सियस पर प्रवाहकीय एपॉक्सी का इलाज करें।
- हीरे के चाकू के साथ नमूना ब्लॉक के प्रत्येक पक्ष ट्रिम और फिर ऊतक उजागर होने तक ब्लॉक के चेहरे पॉलिश।
नोट: इस कदम पर, कुछ वर्गों को इकट्ठा करके और टोलुइडीन ब्लू स्टेनिंग16 प्रदर्शन या इलेक्ट्रॉन माइक्रोस्कोप के तहत जांच करके ब्याज के क्षेत्र की उपस्थिति की पुष्टि करें। - जितना हो सके नमूने के आकार को कम करें। फिर नमूने को प्रवाहकीय पेंट के साथ पिन पर ग्राउंड करें और इसे ठीक करें (कमरे के तापमान पर 24 घंटे के लिए या ओवन में 40 मिनट के लिए 65 डिग्री सेल्सियस पर)।
- चार्जिंग कलाकृतियों को कम करने के लिए, सोने या सोने/पैलेडियम की पतली परत के साथ नमूनों को स्पटर कोट करें ।
9. SBEM इमेजिंग
- सीरियल ब्लॉक-फेस स्कैनिंग इलेक्ट्रॉन माइक्रोस्कोप के चैंबर में एक नमूने के साथ पिन रखें। नमूने को चाकू में संरेखित करें। चैंबर बंद करें और पैरामीटर सेट करें।
- वांछित आवर्धन, पिक्सेल आकार, स्लाइस मोटाई, त्वरित वोल्टेज (ईएचटी), अपर्चर, दबाव आदि पर छवियों का ढेर एकत्र करें।
नोट: पैरामीटर नमूने और प्रयोग के लक्ष्य पर निर्भर करते हैं। अनुकरणीय प्रारंभिक इमेजिंग सेटिंग्स सामग्री की तालिका में शामिल हैं।
10.3D पुनर्निर्माण
नोट: नीचे उल्लिखित चरणों के लिए हम ओपन-एक्सेस सॉफ्टवेयर जैसे फिजिज17 (इमेजजे संस्करण 1.49 b), माइक्रोस्कोपी इमेज ब्राउजर (एमआईबी)18 और पुनर्निर्माण19 का उपयोग करते हैं लेकिन विभिन्न अन्य सॉफ्टवेयर को नियोजित किया जा सकता है।
- डिजिटल माइक्रोग्राफ (डीएम) फाइलों को टिफ फॉर्मेट में परिवर्तित करें। पहले इमेज सीक्वेंस (फिजीजे में) फाइल > 8 बिट फॉर्मेट चुनने > > इमेज सीक्वेंस का आयातकरें और फिर झगड़ा के रूप में सहेजें (फिजीजे में: फाइल > सेव > इमेज सीक्वेंस > चुनिए टिफ)।
- छवियों के ढेर की चमक और इसके विपरीत समायोजित करें (फिजज में: इमेज > > ब्राइटनेस/कंट्रास्ट को समायोजित करें)और, यदि आवश्यक हो, तो इसे संक्षेप में करें (फिजे20 के लिए डेनोइसईएम प्लगइन का उपयोग करें: प्लगिंस > DenoiseEM > Denoise)।
- स्टैक को संरेखित करें (फिजिज में: प्लगइन्स > स्टैगरेग या एमआईबी: डेटासेट > अलाइनमेंट टूल)।
- सेगमेंट डेंड्रिटिक कताई और सिनेप्स (एमआईबी या पुनर्निर्माण सॉफ्टवेयर में, व्यापक ट्यूटोरियल उपलब्ध हैं (विवरण के लिए सामग्री की तालिका देखें)।
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
उच्च विपरीत ऊपर वर्णित विधि का उपयोग करना, माउस मस्तिष्क ऊतक की अच्छी संकल्प छवियों को प्राप्त किया जा सकता है। SBEM तकनीक द्वारा प्रदान किए गए दृश्य का एक बड़ा क्षेत्र ब्याज के क्षेत्र के सटीक चयन की सुविधा प्रदान करता है। हिप्पोकैम्पस के CA1 क्षेत्र की बड़ी छवि स्ट्रैटम रेडिएटम (एसआर)(चित्रा 2 ए)की लंबाई को मापने और इमेजिंग को केंद्र(चित्रा 2B)में ठीक सेट करने के लिए लिया गया था। इसके बाद, छवियों के ढेर का अधिग्रहण किया गया था और ब्याज की वस्तुओं, जैसे कि डेंड्राइट्स, डेंड्रिटिक कताई, सिनेप्स के पोस्टसिनैप्टिक घनत्व(चित्रा 2C,D)को खंडित किया गया था।
एसबीईएम तकनीक का उपयोग ऊतक की अपेक्षाकृत बड़ी मात्रा का विश्लेषण करने और दुर्लभ घटनाओं जैसे बहु-इनरवेट डेंड्रिटिकस्पाइन (चित्रा 2E)को पहचानने की संभावना देता है - एक विशेष प्रकार का सिनैप्स जो एक ही पोस्टसिनैप्टिकस्पाइन 21से संपर्क करने वाले कई प्रेसिनैप्टिक टर्मिनलों की विशेषता है।

चित्रा 2। माउस हिप्पोकैम्पस CA1 क्षेत्र में डेंड्रिटिक कताई। माउस हिप्पोकैम्पल CA1 क्षेत्र की प्रतिनिधि छवि। स्ट्रैटम रेडिएटम (एसआर) को सफेद तीर(ए)के साथ दिखाया गया है। एसआर के बीच में क्षेत्र इमेजिंग(बी)के लिए चुना गया था । डेंड्रिटिक कताई(सी)के साथ डेंड्राइट के एक टुकड़े का पुनर्निर्माण। ऊतक(डी)की मात्रा में डेंड्रिटिक कताई का पुनर्निर्माण। एक बहु-इनरवेट डेंड्रिटिक स्पाइन(ई)का पुनर्निर्माण। एक ही पोस्टसिनैप्टिक स्पाइन से संपर्क करने वाले दो प्रेसिनैप्टिक टर्मिनल (मैजेंटा और हरे रंग में) दिखाए जाते हैं। कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें ।
SBEM नमूना तैयारी के लिए प्रस्तुत प्रोटोकॉल ने हमें मस्तिष्क के ऊतकों की उच्च गुणवत्ता वाली छवियों को भारी विषम झिल्ली के साथ प्राप्त करने की अनुमति दी, जो झिल्ली से घिरे संरचनाओं के आसान विभाजन और पुनर्निर्माण में सक्षम बनाता है। पीएफए(चित्रा 3बी)की उच्च एकाग्रता और दो-चरण निर्धारण दृष्टिकोण के साथ मानक निर्धारण के परिणामस्वरूप समान ऊतक आकृति विज्ञान(चित्रा 3 ए)हुआ।

चित्रा 3। रूपात्मक विवरण। यहां प्रस्तुत प्रोटोकॉल के उपयोग के साथ अच्छी गुणवत्ता वाली छवियां सिनैप्टिक वेसिकल्स की आकृति विज्ञान दिखाती हैं, पीएसडी और माइटोकॉन्ड्रिया प्राप्त किए गए थे। मस्तिष्क के ऊतकों को दो-चरण दृष्टिकोण(ए)या मानक फिक्सेटिव(बी)के साथ ठीक किया गया। स्केल बार 2 माइक्रोन करें इस आंकड़े का एक बड़ा संस्करण देखने के लिए कृपया यहां क्लिक करें।
परिणाम प्रजनन योग्य हैं, जिसका अर्थ है कि इस प्रोटोकॉल का उपयोग करके तैयार किया गया हर नमूना, न केवल मस्तिष्क ऊतक बल्कि सुसंस्कृत कोशिकाओं का मोनोलेयर भी अच्छी तरह से विपरीत था।
हल्के प्राथमिक निर्धारण का उपयोग एक हल्के माइक्रोस्कोप से जुड़े इम्यूनोफ्लोरेसेंस अध्ययन के लिए भी ऊतक का उपयोग करने का अवसर प्रदान करता है। PSD-95 एंटीबॉडी के मामले में, हम दो कदम निर्धारण (हल्के प्राथमिक और फिर एक पारंपरिक निर्धारक के साथ माध्यमिक) के साथ तय नमूनों के बीच परिणामों इम्यूनोस्टेटिंग में अंतर का पालन नहीं किया और एक 4% पीएफए के साथ पारंपरिक निर्धारण का उपयोग कर प्राप्त केवल(चित्रा 4A और 4B, क्रमशः) ।

चित्रा 4। विभिन्न प्रोटोकॉल के साथ तय नमूनों में पीएसडी-95 इम्यूनोफ्लोरेसेंस की तुलना। पृष्ठीय हिप्पोकैम्पस में सीए1 क्षेत्र के स्ट्रैटम रेडिएटम लेयर में पीएसडी-95 इम्यूनोस्टेटिंग के प्रतिनिधि माइक्रोफोटोग्राफ। (A)हल्के प्राथमिक निर्धारण के बाद कॉन्फोकल इमेज जिसके बाद मानक फिक्सेटिव के साथ पोस्टफिक्सेशन होता है । (ख)मानक के बाद कॉन्फोकल छवि, मजबूत निर्धारण। स्केल बार: 5 माइक्रोन करें. कृपया इस आंकड़े का एक बड़ा संस्करण देखने के लिए यहां क्लिक करें।
Subscription Required. Please recommend JoVE to your librarian.
Discussion
201010में डियरिंक द्वारा वर्णित प्राथमिक एनसीआईआर विधि के कई रूप हैं। बुनियादी सिद्धांत एक ही रहते हैं, लेकिन, अध्ययन सामग्री के प्रकार के आधार पर, मामूली परिवर्तन लागू कर रहे हैं । यह पहले वर्णित किया गया था कि विभिन्न रालों का उपयोग एसबीईएम के लिए नमूनों को एम्बेड करने के लिए किया जा सकता है और उदाहरण के लिए पौधों के मामले में, स्पर अपनी कम चिपचिपाहट के कारण पसंद का राल है जो सेल की दीवारों22, 23के माध्यम से बेहतर घुसपैठ की अनुमति देता है। इसके अलावा, विभिन्न बफ़र्स को निर्धारण (जैसे, कैकोडिलेट बफर, एचईपीईएस, या फॉस्फेट बफर के साथ-साथ ग्लूटारल्डिहाइड (2-3%) और पैराफॉर्मलडिहाइड (2-4%)23,24, 25,26,27,28)की एक अलग सांद्रता के लिए लागू किया जा सकता है। पौधों की सामग्री23,30 के धुंधला में सुधार करने के लिए एक्सट्रासेलुलर मैट्रिक्स29 या रूथेनियम लाल में समृद्ध नमूनों के धुंधला बढ़ाने के लिए टैनिक एसिड का उपयोग एक और संशोधन है जिसका उपयोग किया जा सकता है। जहां तक निर्जलीकरण का संबंध है , आमतौर पर एप्लोकी राल24,28के लिए इथेनॉल और / या एसीटोन की सिफारिश की जाती है ।
एक ही प्रोटोकॉल के रूप में यहां वर्णित है, या बहुत समान है, सफलतापूर्वक हमारी टीम और अंय समूहों द्वारा पहले इस्तेमाल किया गया है4,5,24। इस विधि के अनुसार संसाधित नमूने टेम इमेजिंग31के अनुकूल होते हैं . 201010 में प्रकाशित मूल एनसीओआर प्रोटोकॉल की तुलना में हम कुछ मामूली बदलाव पेश करते हैं जैसे कि फिक्सेशन के दौरान विषाक्त कैकोडिलेट बफर के प्रतिस्थापन और फॉस्फेट बफर के साथ ऑस्मियम पोस्ट-फिक्सेशन चरण। जैसा कि ऊपर बताया गया है, ईएम तैयारी के दौरान विविध बफ़र्स का उपयोग किया जा सकता है, और हमारे अनुभव के अनुसार, गैर-विषाक्त पीबी संतोषजनक परिणाम देता है।
एक और परिवर्तन निर्जलीकरण के अंतिम चरण के दौरान कम उपयोगकर्ता-हानिकारक इथेनॉल के साथ एसीटोन का प्रतिस्थापन है। एंबेडिंग प्रक्रिया के दौरान इथेनॉल का उपयोग राल सॉल्वेंट के रूप में भी किया जाता था। इसके अलावा, 32, 33 से पहले प्रकाशित एपॉक्सी राल घटक सी के बजाय डीएमपी-30 का उपयोग किया गया था।
इम्यूनोफ्लोरेसेंस अध्ययन के लिए एक ही दिमाग का उपयोग करने की आवश्यकता के कारण दो-चरण निर्धारण दृष्टिकोण पेश किया गया था। सबसे पहले, जानवरों को एक बफर के साथ प्रेरित किया गया था जिसमें ग्लूटाराल्डिहाइड की कम एकाग्रता (2% पीएफए और 0.5% GA युक्त बफर के साथ परफ्यूजन द्वारा हल्के प्राथमिक निर्धारण) और उसके बाद मस्तिष्क का केवल आधा हिस्सा समर्पित था। ईएम को ग्लूटारल्डिहाइड (2% पीएफए और 2.5% GA) की उच्च एकाग्रता के साथ पोस्टफिक्स किया गया था, जबकि मस्तिष्क के अन्य आधे को इम्यूनोस्टेटिंग (4% पीएफए) के लिए एक मानक स्थिर के साथ पोस्टफिक्स किया गया था। पीएफए की कम सांद्रता वाले निम फिक्सेटिव का उपयोग दूसरों और हमारे समूह 4 , 5 ,31,34द्वारा प्रकाशित किया गया था । यहां प्रस्तुत दो कदम निर्धारण एक पारंपरिक एक कदम दृष्टिकोण(चित्रा 3 और चित्रा 4)के रूप में पर्याप्त है । हालांकि, चूंकि हम प्रस्ताव करते हैं कि मस्तिष्क के प्रत्येक आधे को अलग से संसाधित किया जा सकता है, इसलिए हमारा प्रोटोकॉल उपयोग किए जाने वाले जानवरों की संख्या को कम करने की अनुमति देता है। हल्के प्राथमिक निर्धारण सफलतापूर्वक ऊतक एंटीजेनिकिटी को बनाए रखता है, जिससे आगे इम्यूनोफ्लोरेसेंस को सक्षम किया जाता है जैसा कि पीएसडी-95 प्रोटीन के खिलाफ एंटीबॉडी के लिए प्रदर्शित किया गया है। हालांकि इस बात पर जोर देना होगा कि हमारे दृष्टिकोण की उपयोगिता को अन्य एंटीबॉडी के लिए मान्य किया जाना चाहिए ।
प्रस्तुत विधि स्पष्ट रूप से दिखाई झिल्ली के साथ मस्तिष्क के ऊतकों की उच्च विपरीत छवियों में परिणाम है। हालांकि, यह उल्लेखनीय है कि वहां एक ही कदम विफलता के लिए प्रवण हैं, के रूप में SBEM नमूना तैयारी के किसी भी अंय विधि के मामले में, और विशेष रूप से ध्यान देने की जरूरत है उंहें भुगतान की जरूरत है । ऊतक आकृति विज्ञान की गुणवत्ता ही ज्यादातर परफ्यूजन पर निर्भर करती है। यह एक महत्वपूर्ण कदम है, क्योंकि केवल सफलतापूर्वक तय नमूने संतोषजनक परिणाम देते हैं। दुर्भाग्य से, निर्धारण परफ्यूजन जानवरों के बीच व्यक्तिगत परिवर्तनशीलता से प्रभावित होता है, इस प्रकार छवियों की गुणवत्ता एक जानवर से दूसरे जानवर में भिन्न हो सकती है। इसके अलावा, किसी को निर्जलीकरण के दौरान नमूना सूखने के लिए सावधान नहीं रहना होगा; अन्यथा, नमूने राल के साथ ठीक से घुसपैठ नहीं की जाएगी। एक अन्य महत्वपूर्ण पहलू पिन के लिए बढ़ते नमूना है। एपॉक्सी रेजिन गैर-प्रेरक होते हैं, और इसलिए वे इमेजिंग के दौरान इलेक्ट्रॉनों को जमा करते हैं जो कलाकृतियों को चार्ज करने का कारण बनता है। SBEM में चार्जिंग प्रभाव को कम करने के लिए, नमूने के हर तरफ राल की अधिकता को ध्यान से हटाना आवश्यक है और चांदी के पेंट और स्पटर कोटिंग के साथ नमूने को सही ढंग से जमीन पर रखना आवश्यक है।
वर्तमान प्रोटोकॉल मस्तिष्क के ऊतकों पर केंद्रित है; हालांकि, इसे सेल मोनोलेयर, ऑर्गेनोइटिक स्लाइस या अन्य ऊतकों के लिए अनुकूलित किया जा सकता है। मूल एनसीएमआईआर प्रोटोकॉल की तरह, यहां प्रस्तुत किए गए एक अत्यधिक विपरीत नमूनों का परिणाम है जो न केवल एसबीईएम के लिए उपयुक्त हैं, बल्कि एफआईबी-एसईएम और एटम-एसईएम प्रयोगों के लिए भी उपयुक्त हैं।
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
लेखकों के पास खुलासा करने के लिए कुछ नहीं है ।
Acknowledgments
SBEM इमेजिंग, लाइट माइक्रोस्कोपी इमेजिंग और इलेक्ट्रॉन माइक्रोस्कोपी नमूना तैयारिंग इमेजिंग ऊतक और समारोह की प्रयोगशाला के उपकरणों के उपयोग के साथ किया गया जो प्रयोगात्मक जीव विज्ञान के Nencki संस्थान में एक इमेजिंग कोर सुविधा के रूप में कार्य करता है ।
चित्रा 1 की तैयारी के लिए, माउस (Souris_02) की छवि और https://smart.servier.com/ से एक शीशी का उपयोग किया गया था।
इस काम को केआर को दिए गए नेशनल साइंस सेंटर (पोलैंड) ग्रांट ओपस (यूएएम-2018/31/बी/NZ4/01603) ने सपोर्ट किया ।
Materials
| Name | Company | Catalog Number | Comments |
| Anesthetic: | |||
| Ketamine/xylazine mixture (Ketamina/Sedazin) | Biowet Pulawy, Pulawy, Poland | ||
| Sodium pentobarbital (Morbital) | Biowet Pulawy, Pulawy, Poland | ||
| Fixatives: | |||
| Glutaraldehyde (GA) | Sigma-Aldrich,St. Louis, MI, USA | G5882 | Grade I, 25% in H2O, specially purified for use as an electron microscopy fixative |
| Hydrochloric acid (HCl) | POCH, Gliwice, Poland | 575283115 | pure p.a. |
| Paraformaldehyde (PFA) | Sigma-Aldrich,St. Louis, MI, USA | 441244 | prilled, 95% |
| Phosphate buffered saline (PBS), pH 7.4 | Sigma-Aldrich,St. Louis, MI, USA | P4417-50TAB | tablets |
| Sodium hydroxide (NaOH) | Sigma-Aldrich,St. Louis, MI, USA | S5881 | reagent grade, 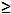 98%, pellets (anhydrous) 98%, pellets (anhydrous) |
| Sodium phosphate dibasic (Na2HPO4) | Sigma-Aldrich,St. Louis, MI, USA | S3264 | |
| Sodium phosphate monobasic (NaH2PO4) | Sigma-Aldrich,St. Louis, MI, USA | S3139 | |
| Perfusion: | |||
| Large blunt/blunt curved scissors (~14.5 cm) | Fine Science Tools, Foster City, CA, USA | 14519-14 | |
| Micro-spatula (double 2" flat ends, one rounded, one tapered to 1/8") | Fine Science Tools, Foster City, CA, USA | 10091-12 | |
| Needle tip, 15 GA, blunt (perfusion needle) | KD Medical GmbH Hospital Products, Berlin, Germany | KD-FINE 900413 | 1.80 x 40 mm |
| Pair of fine (Graefe) tweezers | Fine Science Tools, Foster City, CA, USA | 11050-10 | |
| Perfusion pump | Lead Fluid | BQ80S | |
| Plastic vials | Profilab, Warsaw, Poland | 534.02 | plastic vials with blue cap for tissue storage, 20 ml, 31 x 48 mm |
| Straight iris scissors (~9 cm) | Fine Science Tools, Foster City, CA, USA | 14058-11 | |
| Brain slices preparation for EM: | |||
| 12-well plate | NEST, Rahway, NJ, USA | 712001 | |
| Cyanoacrylic glue | Fenedur, Montevideo, Uruguay | ||
| Glass vials | Electron Microscopy Sciences, Hatfield, PA, USA | 72632 | 20 ml Scintillation Vial, a pack of 100 |
| Pasteur pipette | VWR, Radnor, PA, USA | 612-4545 | LDPE, disposable, 7.5 ml |
| Razor blade | Wilkinson Sword, London, UK | Classic double edge safety razor blades | |
| Scalpel blade | Swann-Morton, Sheffield, UK | No. 20 | |
| Vibratome | Leica Microsystems, Vienna, Austria | Leica VT1000 S | |
| Brain slices preparation for IF: | |||
| 96-well plate | NEST, Rahway, NJ, USA | 701101 | |
| Criostat | Leica Microsystems, Vienna, Austria | Leica CM 1950 | |
| Ethylene glycol | Bioshop, Burlington, Canada | ETH001 | |
| Low-profile disposable blade 819 | Leica Biosystems Inc., USA | 14035838925 | |
| Scalpel blade | Swann-Morton, Sheffield, UK | No. 20 | |
| Sodium azide (NaN3) | POCH, Gliwice, Poland | 792770426 | |
| Sucrose | POCH, Gliwice, Poland | 772090110 | |
| Tissue freezing medium for cryosectioning, OCT-Compound | Leica Biosystems, Switzerland | 14020108926 | |
| Immunostaining: | |||
| 24-well plate | NEST, Rahway, NJ, USA | 702001 | |
| Anti-Post Synaptic Density Protein 95 Antibody | Merck-Millipore, Burlington, MA, USA | MAB1598 | |
| Confocal microscope | Zeiss, Göttingen, Germany | Zeiss Spinning Disc microscope (63 × oil objective, NA 1.4, pixel size 0.13 µm × 0.13 µm) | |
| Cover slide | Menzel Glaser, Braunschweig, Germany | B-1231 | 24 x 60 mm |
| Donkey anti-Mouse IgG (H+L) Highly Cross-Adsorbed Secondary Antibody, Alexa Fluor 555 | Invitrogen, Carlsbad, CA, USA | A31570 | |
| Fluoromount-G Mounting Medium, with DAPI | Invitrogen, Carlsbad, CA, USA | 00-4959-52 | |
| Microscope slide | Thermo Scientific, Waltham, MA, USA | AGAA00008 | SuperFrost |
| Normal donkey serum (NDS) | Jackson ImmunoResearch Laboratories, West Grove, PA, USA | 017-000-121 | |
| Shaker | JWElectronic, Warsaw, Poland | KL-942 | |
| TritonT X-100 Reagent Grade | Bioshop, Burlington, Canada | TRX506 | |
| Electron microsocpy sample preparation | |||
| Potassium hexacyanoferrate(II) trihydrate | POCH, Gliwice, Poland | 746980113 | |
| Aclar 33C Film | Electron Microscopy Sciences, Hatfield, PA, USA | 50425 | Fluoropolymer Film embedding sheet |
| DMP-30, 2,4,6-Tris(dimethylaminomethyl)phenol | Sigma-Aldrich,St. Louis, MI, USA | T58203 | Epoxy embedding medium accelerator |
| Durcupan ACM single component A, M | Sigma-Aldrich,St. Louis, MI, USA | 44611 | Durcupan ACM single component A, M epoxy resin |
| Durcupan ACM single component B | Sigma-Aldrich,St. Louis, MI, USA | 44612 | Durcupan ACM single component B, hardener 964 |
| Durcupan ACM single component D | Sigma-Aldrich,St. Louis, MI, USA | 44614 | Durcupan ACM single component D , plasticizer |
| Ethyl alcohol absolute | POCH, Gliwice, Poland | 64-17-5 | Ethyl alcohol absolute 99.8 % pure P.A.-BASIC |
| Genlab laboratory oven | Wolflabs, York, UK | Mino/18/SS | Oven Genlab MINO/18/SS 18l volume, no fan circulation, no digital display, standard temperature gradient, standard recovery rate, no timer, 250°C maximum temperature, 240V electrical supply |
| L-Aspartic acid | Sigma-Aldrich,St. Louis, MI, USA | A-9256 | reagent grade, 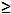 98% (HPLC) 98% (HPLC) |
| Lead (II) nitrate | Sigma-Aldrich,St. Louis, MI, USA | 467790 | 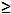 99.95% trace metals basis 99.95% trace metals basis |
| Osmium tetroxide | Sigma-Aldrich,St. Louis, MI, USA | 75632 | for electron microscopy, 4% in H2O |
| pH meter | Elmetron, Zabrze, Poland | CP-5-5 | |
| Rotator | BioSan, Józefów, Poland | Multi Bio RS-24 | rotator Multi Bio RS-24 |
| Sodium hydroxide (NaOH) | Sigma-Aldrich,St. Louis, MI, USA | S5881 | reagent grade, 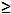 98%, pellets (anhydrous) 98%, pellets (anhydrous) |
| Sunflower mini shaker | Grant bio, Shepreth,UK | PD-3D | |
| Syringe filter | Millipore, Burlington, MA, USA | SLGP033NB | 0,22 µm pore size |
| Thiocarbohydrazide | Sigma-Aldrich,St. Louis, MI, USA | 88535 | purum p.a., for electron microscopy, 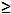 99.0% (N) 99.0% (N) |
| Uranyl acetate | Serva, Heidelberg, Germany | 77870 | Uranyl acetate·2H2O, research grade |
| Water bath | WSL, Swietochlowice, Poland | LWT | |
| Specimen mounting for SBEM | |||
| 96-well culture plate | VWR, Radnor, PA, USA | 734-2782 | 96-well plates, round bottom, non treated |
| AM Gatan 3View stub handling tweezers | Micro to Nano, Haarlem, Netherlands Netherlands |
50-001521 | |
| Binocular | OPTA-TECH, Warsaw, Poland | X2000 | |
| Conductive glue | Chemtronics, Georgia, USA | CW2400 | conductive eopxy |
| Gatan 3View sample pin stubs | Micro to Nano, Haarlem, Netherlands Netherlands |
10-006003 | |
| Parafilm | Sigma-Aldrich,St. Louis, MI, USA | P7793 | roll size 20 in. × 50 ft |
| Pelco conductive silver paint | Ted Pella, Redding, CA, USA | 16062-15 | PELCO® Conductive Silver Paint, 15g |
| Razor blades double edge | Electron Microscopy Sciences, Hatfield, PA, USA | 72000 | Stainless Steel "PTFE" coated. PERSONNA brand .004" thick, wrapped individually, 250 blades in a box. |
| Scanning Electron Microscope | Zeiss, Oberkochen, Germany | Sigma VP with Gatan 3View2 chamber, acceleration voltage 2.5 kV, variable pressure 5 Pa, aperture 20 µm, dwell time 6 µs, slice thickness 60 nm, magnification 15 000 x, image resolution 2048 x 2048 pixels, pixel size 7.3 nm | |
| trim 90° diamond knife | Diatome Ltd., Nidau, Switzerland | DTB90 | |
| Ultramicrotome | Leica Microsystems, Vienna, Austria | Leica ultracutR | |
| Software | webpage | tutorials | |
| FijiJ | https://fiji.sc/ | ||
| Microscopy Image Browser | http://mib.helsinki.fi/ | http://mib.helsinki.fi/tutorials.html | |
| Reconstruct | https://synapseweb.clm.utexas.edu/software-0 | https://synapseweb.clm.utexas.edu/software-0) | |
| Animals | |||
| Mice | Adult 3-month old and 20±1 month old female Thy1-GFP(M) mice (Thy1-GFP +/-) (Feng et al.,2000) which express GFP in a sparsely distributed population of glutamatergic neurons. Animals were bred as heterozygotes with the C57BL/6J background in the Animal House of the Nencki Institute of Experimental Biology. |
References
- Bosch, M., Hayashi, Y. Structural plasticity dendritic spines. Current Opinion in Neurobiology. 22 (3), 383-388 (2012).
- Borczyk, M., Radwanska, K., Giese, K. P. The importance of ultrastructural analysis of memory. Brain Research Bulletin. 173, 28-36 (2021).
- Wanner, A. A., Kirschmann, M. A., Genoud, C. Challenges of microtome-based serial block-face scanning electron microscopy in neuroscience: challenges of SBEM in neuroscience. Journal of Microscopy. 259 (2), 137-142 (2015).
- Śliwińska, M. A., et al. Long-term Memory Upscales Volume of Postsynaptic Densities in the Process that Requires Autophosphorylation of αCaMKII. Cerebral Cortex. 30 (4), 2573-2585 (2020).
- Borczyk, M., Śliwińska, M. A., Caly, A., Bernas, T., Radwanska, K. Neuronal plasticity affects correlation between the size of dendritic spine and its postsynaptic density. Scientific Reports. 9 (1), 1693 (2019).
- Leighton, S. B. SEM images of block faces, cut by a miniature microtome within the SEM - a technical note. Scanning Electron Microscopy. , Pt 2 73-76 (1981).
- Denk, W., Horstmann, H. Serial Block-Face Scanning Electron Microscopy to Reconstruct Three-Dimensional Tissue Nanostructure. PLoS Biology. 2 (11), 329 (2004).
- Smith, D., Starborg, T. Serial block face scanning electron microscopy in cell biology: Applications and technology. Tissue and Cell. 57, 111-122 (2019).
- Titze, B., Genoud, C. Volume scanning electron microscopy for imaging biological ultrastructure: Volume scanning electron microscopy. Biology of the Cell. 108 (11), 307-323 (2016).
- Deerinck, T. J., Bushong, E. A., Thor, A., Ellisman, M. H. NCMIR methods for 3D EM: A new protocol for preparation of biological specimens for serial block face scanning electron microscopy. , 6-8 (2010).
- Willingham, M. C., Rutherford, A. V. The use of osmium-thiocarbohydrazide-osmium (OTO) and ferrocyanide-reduced osmium methods to enhance membrane contrast and preservation in cultured cells. Journal of Histochemistry & Cytochemistry. 32 (4), 455-460 (1984).
- Feng, G., et al. Imaging Neuronal Subsets in Transgenic Mice Expressing Multiple Spectral Variants of GFP. Neuron. 28 (1), 41-51 (2000).
- Gage, G. J., Kipke, D. R., Shain, W. Whole Animal Perfusion Fixation for Rodents. Journal of Visualized Experiments. (65), e3564 (2012).
- Paxinos, G., Franklin, K. B. J. The mouse brain in stereotaxic coordinates. , Acad. Press. San Diego, Calif. (2004).
- Walton, J. Lead aspartate, an en bloc contrast stain particularly useful for ultrastructural enzymology. Journal of Histochemistry & Cytochemistry. 27 (10), 1337-1342 (1979).
- Mercer, E. H. a scheme for section staining in electron microscopy. Journal of the Royal Microscopical Society. 81 (3-4), 179-186 (1963).
- Schindelin, J., et al. Fiji: an open-source platform for biological-image analysis. Nature Methods. 9 (7), 676-682 (2012).
- Belevich, I., Joensuu, M., Kumar, D., Vihinen, H., Jokitalo, E. Microscopy Image Browser: A Platform for Segmentation and Analysis of Multidimensional Datasets. PLOS Biology. 14 (1), 1002340 (2016).
- Fiala, J. C. Reconstruct: a free editor for serial section microscopy. Journal of Microscopy. 218 (1), 52-61 (2005).
- Roels, J., et al. An interactive ImageJ plugin for semi-automated image denoising in electron microscopy. Nature Communications. 11 (1), 771 (2020).
- Radwanska, K., et al. Mechanism for long-term memory formation when synaptic strengthening is impaired. Proceedings of the National Academy of Sciences. 108 (45), 18471-18475 (2011).
- Kittelmann, M., Hawes, C., Hughes, L. Serial block face scanning electron microscopy and the reconstruction of plant cell membrane systems: SBFSEM Methods for Plant Cells. Journal of Microscopy. 263 (2), 200-211 (2016).
- Fendrych, M., et al. Programmed Cell Death Controlled by ANAC033/SOMBRERO Determines Root Cap Organ Size in Arabidopsis. Current Biology. 24 (9), 931-940 (2014).
- Russell, M. R. G., et al. 3D correlative light and electron microscopy of cultured cells using serial blockface scanning electron microscopy. Journal of Cell Science. 130 (1), 278-291 (2017).
- Płachno, B. J., Świątek, P., Jobson, R. W., Małota, K., Brutkowski, W. Serial block face SEM visualization of unusual plant nuclear tubular extensions in a carnivorous plant (Utricularia, Lentibulariaceae). Annals of Botany. 120 (5), 673-680 (2017).
- Genoud, C., Titze, B., Graff-Meyer, A., Friedrich, R. W. Fast Homogeneous En Bloc Staining of Large Tissue Samples for Volume Electron Microscopy. Frontiers in Neuroanatomy. 12, (2018).
- Puhka, M., Joensuu, M., Vihinen, H., Belevich, I., Jokitalo, E. Progressive sheet-to-tubule transformation is a general mechanism for endoplasmic reticulum partitioning in dividing mammalian cells. Molecular Biology of the Cell. 23 (13), 2424-2432 (2012).
- Gluenz, E., Wheeler, R. J., Hughes, L., Vaughan, S. Scanning and three-dimensional electron microscopy methods for the study of Trypanosoma brucei and Leishmania mexicana flagella. Methods in Cell Biology. 127, 509-542 (2015).
- Starborg, T., et al. Using transmission electron microscopy and 3View to determine collagen fibril size and three-dimensional organization. Nature Protocols. 8 (7), 1433-1448 (2013).
- Hughes, L., Borrett, S., Towers, K., Starborg, T., Vaughan, S. Patterns of organelle ontogeny through a cell cycle revealed by whole-cell reconstructions using 3D electron microscopy. Journal of Cell Science. 130 (3), 637-647 (2017).
- Bojko, A., et al. Improved Autophagic Flux in Escapers from Doxorubicin-Induced Senescence/Polyploidy of Breast Cancer Cells. International Journal of Molecular Sciences. 21 (17), 6084 (2020).
- Knott, G. W., Holtmaat, A., Trachtenberg, J. T., Svoboda, K., Welker, E. A protocol for preparing GFP-labeled neurons previously imaged in vivo and in slice preparations for light and electron microscopic analysis. Nature Protocols. 4 (8), 1145-1156 (2009).
- Glauert, A. M., Lewis, P. R. Biological specimen preparation for transmission electron microscopy. , Princeton University Press. Princeton. (2014).
- Genoud, C. Altered Synapse Formation in the Adult Somatosensory Cortex of Brain-Derived Neurotrophic Factor Heterozygote Mice. Journal of Neuroscience. 24 (10), 2394-2400 (2004).



