Overview
Fonte: Laboratorio di Jeff Salacup - Università del Massachusetts Amherst
Il prodotto di un'estrazione con solvente organico, un estratto lipidico totale (TLE), è spesso una miscela complessa di centinaia, se non migliaia, di composti diversi. Il ricercatore è spesso interessato solo a una manciata di composti o, se interessato a molti, potrebbe aver bisogno di rimuovere i costituenti indesiderati che sono "in mezzo" o co-eluizione. Ad esempio, le concentrazioni di singoli composti in un campione sono spesso determinate su un gascromatografo accoppiato a un rivelatore ionizzante di fiamma (GC-FID), perché la relazione tra la risposta FID (in pA) e la quantità di composto in un campione(ad esempio,ng / μL) è sia lineare che sensibile. La porzione GC dello strumento separa diversi composti in un campione in base al loro punto di ebollizione, alla struttura chimica e all'affinità con una fase solida che può cambiare in base all'applicazione. Il risultato è un cromatogramma (Figure 1), che mostra la separazione dei diversi costituenti chimici nel tempo, nonché la loro concentrazione relativa (calcolata come l'area sotto la curva). Tuttavia, a volte più di un composto eluisce il GC alla volta (Figure 1). In questo caso, è necessaria la purificazione del campione prima che i composti possano essere quantificati con sicurezza.
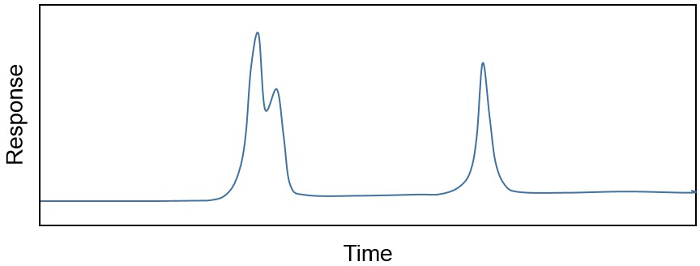
Figura 1. Un cromatogramma che mostra la separazione di diversi costituenti chimici nel tempo e la loro concentrazione relativa (area sotto la curva). Vengono mostrati picchi co-eluinti e separati.
Principles
I FAME (esteri metilici degli acidi grassi) sono importanti costituenti dei microbi terrestri e marini e sono spesso utilizzati, in combinazione con tecniche genetiche, per descrivere la diversità microbica degli ecosistemi nei sistemi moderni e antichi. Tuttavia, la presenza di FATE in un campione non è sempre utile. A causa delle loro dimensioni e chimica simili, i FAFEM chiamati alchenoni co-eluiscono comunemente con chetoni alchilici a catena lunga, chiamati alchenoni (Figura 2). La distribuzione degli alchenoni in un campione mette in relazione le informazioni sulla temperatura superficiale del mare al momento e/o al luogo in cui il campione è stato prelevato, e quindi la loro caratterizzazione accurata e precisa è importante.
La saponificazione è una tecnica di purificazione comune utilizzata per convertire i FAME in acidi grassi, modificando così le loro caratteristiche chimiche abbastanza da rimuoverli dalla coeluizione con gli alchenoni (Figura 3). La saponificazione è una forma di idrolisi. Nell'idrolisi, l'acqua viene utilizzata per dividere le molecole. La saponificazione è un'idrolisi che viene accelerata in presenza di una base, come l'idrossido di potassio (KOH). KOH si dissolve in K+ e OH- in acqua. L'anione idrossido (OH-, ione caricato negativamente) si aggiunge all'atomo di carbonio terziario leggermente caricato positivamente nel cuore del FAME(Figura 3,in alto). Tuttavia, questa configurazione chimica è instabile ,il carbonio si è legato a troppi altri atomi) e l'alcossido (ROH-) viene espulso. Ma l'H della base coniugata che questa espulsione forma si sposta rapidamente verso l'alcossido per formare il metanolo alcolico e il sale di potassio degli acidi grassi (Figura 3, al centro). A questo punto, il FAME incriminato (alchenoato) è stato convertito in una sostanza chimica che non co-eluisce più con esso. Tuttavia, se si desidera analizzare anche la chimica FAME, possono essere recuperati mediante l'aggiunta di acido (HCl) alla soluzione, fino a quando il pH raggiunge ~ 2. A questo pH, il sale di potassio dell'acido grasso viene diviso per formare un acido carbossilico e sale ionico (KCl; Figura 3, in basso).

Figura 2. Le strutture chimiche di un alchenone con 37 atomi di carbonio e 2 doppi legami (in alto) e il suo alchenoato associato FAME (in basso).

Figura 3. Schema della saponificazione dell'acido palmitico utilizzando idrossido di potassio (KOH) per aumentare il tasso di idrolisi (http://www.mpbio.com/).
La saponificazione è una tecnica comunemente usata per rimuovere gli esteri metilici degli acidi grassi da una miscela organica complessa.
I campioni organici complessi vengono spesso analizzati mediante gascromatografia, che viene utilizzata per determinare le concentrazioni relative dei singoli componenti.
Tuttavia, i composti che sono simili per dimensioni e struttura non possono essere distinti dallo strumento, distorcendo i risultati. Pertanto, i composti indesiderati che producono segnali sovrapposti devono essere rimossi per ottenere risultati accurati.
Questo video copre l'uso della saponificazione per purificare gli alchenoni per la paleoclimatologia. È il primo di una serie che descrive in dettaglio la purificazione di campioni di biomarcatori complessi. Coprirà la procedura, così come alcuni altri usi della tecnica.
Gli alchetoni alchilici polinsaturi a catena lunga, chiamati alchenoni, hanno dimostrato di fornire informazioni utili sulla temperatura superficiale del mare passata.
Tuttavia, gli organismi che producono alchenoni spesso creano esteri metilici degli acidi grassi che sono simili per dimensioni e struttura chimica, chiamati alchenoati. A causa di queste somiglianze, gli alchenoati devono essere rimossi prima di poter ottenere un'analisi accurata.
La saponificazione è una tecnica comune utilizzata per prevenire la co-eluizione di queste molecole. La saponificazione utilizza l'acqua per dividere il legame molecolare di un estere. Una base si attacca al carbonio nel cuore dell'alchenoato. Questa reazione di aggiunta crea un intermedio instabile e l'alcossido viene espulso.
L'idrogeno dall'acido appena formato si sposta verso l'alcossido espulso e l'anione carbossilato risultante forma un legame ionico con il catione dalla base. Il risultato è un sale alcolico e un sale di acidi grassi. L'aggiunta di un acido forte rigenererà l'acido carbossilico. A questo punto, l'alchero incriminato è stato convertito in una forma che non co-eluisce più con l'alchenone di interesse.
Ora che hai capito come la saponificazione può essere utilizzata per purificare una miscela organica, sei pronto per iniziare la procedura.
In primo luogo, acquisire un estratto lipidico totale essiccato - o TLE - che è stato ottenuto utilizzando un metodo di estrazione con solvente. Quindi, preparare le soluzioni di saponificazione come delineato nel protocollo di testo. Assicurarsi che tutti i componenti siano puri e privi di idrocarburi. Una volta preparate le soluzioni, aggiungere il TLE essiccato in un flaconcino di vetro borosilicato da 60 ml. Aggiungere 2 mL di 2 idrossido di potassio normale e sigillare il flaconcino. Quindi, riscaldare il flaconcino a 60 °C per 2,5 ore per scindere il legame estere. Al termine, lasciare raffreddare il campione a temperatura ambiente. Una volta che il campione si è raffreddato, aggiungere 2 ml di soluzione di cloruro di sodio al 5% al flaconcino. Tappare il flaconcino e agitare brevemente. Aggiungere 6 N di acido cloridrico a goccia fino a raggiungere un pH di 2 - usando carta pH per testare. L'aggiunta di questo acido protonerà l'anione carbossilato per formare il prodotto finale - l'acido carbossilico stabile.
Ora che la soluzione acidificata è priva di esteri, aggiungere 5 ml di esano. Tappare e agitare vigorosamente per 5 secondi per estrarre i composti organici dall'acqua. Lasciare riposare la soluzione fino a quando le fasi organica e acquosa si separano completamente. Sali, ioni e acido cloridrico non reazioni rimarranno nella fase acquosa, mentre i composti organici si separeranno nell'esano. Una volta che le fasi sono completamente separate, rimuovere circa il 75% dell'esano usando una pipetta ed erogare in un altro flaconcino da 40 ml. Ripetere questo processo di estrazione altre due volte, aggiungendo 5 ml di esano ogni volta. Una volta completato, scartare la soluzione acquosa rimanente in un contenitore per rifiuti adeguato. Etichettare il flaconcino contenente la fase organica appena saponificata. Gli acidi carbossilici prodotti non possono essere iniettati negli strumenti comunemente utilizzati per l'analisi degli alchenoni senza un'ulteriore purificazione. Gli acidi carbossilici iniettati in un gascromatografo si accumulano rapidamente e rovinano le insenature, le fodere di ingresso e l'estremità anteriore delle colonne. Per rimuovere questi acidi, il campione deve prima sottoporsi a un'altra tecnica di purificazione: la separazione tramite cromatografia su colonna.
La saponificazione ha diverse applicazioni nell'estrazione e purificazione di molecole organiche.
La saponificazione può essere utilizzata non solo per separare i biomarcatori, ma anche per estrarre singoli componenti da utilizzare in prodotti commerciali. In questo esempio, i composti dell'albero del tabacco - Nicotiana glauca - sono stati isolati e analizzati per studiare il loro potenziale come materia prima per un'ampia varietà di prodotti a base biologica, come carburante, calore e una serie di composti chimici.
Le foglie sono state prima omogeneizzate, poi centrifugate, per concentrare le molecole di interesse. Il materiale vegetale concentrato è stato poi saponificato. Il materiale estratto è stato analizzato con cromatografia liquida-spettrometria di massa, per determinare la concentrazione di tocoferolo - una famiglia di composti vitaminici della vitamina E tipicamente presenti nelle piante.
Il materiale estratto può anche essere ricostituito in vitro alla sua composizione originale. In questo esempio, la saponificazione è stata utilizzata per estrarre i carotenoidi dalle piante di spinaci, per essere successivamente ricostituiti in vitro. Gli spinaci sono stati prima omogeneizzati, poi centrifugati, per raccogliere le molecole di pigmento. Queste molecole sono state poi sospese in una soluzione di idrossido di potassio in un imbuto separatore, iniziando la saponificazione. I carotenoidi saponificati separati in uno strato di etere, che è stato raccolto e asciugato. Utilizzando una serie di tamponi di soluzione, i carotenoidi - e altre molecole di pigmentazione - sono stati successivamente ricostituiti in vitro. Questa purificazione ha permesso l'analisi di questi pigmenti senza l'interferenza di composti organici strutturati in modo simile.
A causa della sua capacità di idrolizzare gli esteri, la saponificazione può essere utilizzata per "liberare" composti che sono altrimenti legati alle macromolecole. In questo esempio, una fase di saponificazione anidra viene utilizzata per convertire il 4-fluorobenzoato di etile nel sale dell'acido carbossilico del potassio4-fluorobenzoato. Questa deprotezione attraverso la saponificazione consente la produzione di SFB grezzo - una reazione che non sarebbe possibile se la molecola fosse rimasta "bloccata".
Hai appena visto l'introduzione di JoVE alla purificazione di Uk'37 campioni attraverso la saponificazione. Ora dovresti capire come funziona la saponificazione e come usarla per purificare gli alchenoni in un estratto lipidico totale. Ulteriori processi di purificazione saranno dimostrati nei video successivi.
Grazie per l'attenzione!
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. Impostazione e preparazione dei materiali
- Ottenere un estratto lipidico totale (TLE) utilizzando un metodo di estrazione con solvente (sonicazione, Soxhlet o estrazione con solvente accelerato (ASE)).
- Preparare una soluzione di 2 N KOH in 5% H2O in metanolo.
- KOH e metanolo possono essere acquistati presso i rivenditori di prodotti chimici. Queste sostanze chimiche dovrebbero essere pure e prive di idrocarburi.
- La massa molare di KOH è ~ 56 amu che produce 1 mol di OH- per ogni mol di KOH. Pertanto, per ottenere una concentrazione di 2 N, sciogliere 112 g di KOH in 0,95 L di acqua pura e 0,05 L di metanolo.
- Si noti che la dissoluzione di KOH in acqua è esotermica e crea una grande quantità di calore. Fare attenzione ad aggiungere lentamente i pellet KOH all'acqua per evitare una reazione violenta.
- Sciogliere 112 g di pellet KOH in 0,95 L di acqua pura su una piastra di agitazione automatica.
- Aggiungere 0,05 L di metanolo una volta che tutto il KOH è disciolto per aiutare nella dissoluzione dei biomarcatori organici nella soluzione acquosa.
- KOH e metanolo possono essere acquistati presso i rivenditori di prodotti chimici. Queste sostanze chimiche dovrebbero essere pure e prive di idrocarburi.
- Preparare una soluzione di acido cloridrico 6 N (HCl) in H2O.
- HCl può essere acquistato presso i rivenditori di prodotti chimici. Questa sostanza chimica dovrebbe essere pura e priva di idrocarburi.
- HCl viene generalmente concentrato come 13 N. Pertanto, una miscela 1: 1 di HCl e acqua pura produce una miscela di 6,5 N di HCl, che è abbastanza vicina a 6 N ai fini di questo esperimento.
- Assicurati di aggiungere l'HCl all'acqua e non il contrario, poiché l'aggiunta di acqua all'HCl concentrato è esotermica e genera calore. Ciò potrebbe causare lo schizzo di HCl.
- Versare delicatamente e lentamente 100 mL HCl in un becher contenente 100 ml di acqua pura, facendo roteare la miscela tra le aggiunte di HCl.
- Preparare una soluzione di NaCl al 5% (sale da cucina) in H2O.
- NaCl può essere acquistato presso i rivenditori di prodotti chimici. Questa sostanza chimica dovrebbe essere pura e priva di idrocarburi.
- Calcolare e pesare la massa di sale necessaria per produrre ~1 L di soluzione al 5% (p/p). 1 L di acqua pesa ~ 1 kg o 1.000 g. Pertanto, 50 g di NaCl disciolti in 950 ml danno una soluzione al 5% (50 g + 950 g = 1.000 g; 50 g / 1.000 g = 0,05 o 5%).
- Aggiungere delicatamente 50 g di NaCl all'acqua pura su una piastra automatica e attendere che si sciolga.
- Ottenere i seguenti materiali: 2 flaconcini di vetro borosilicato puliti e bruciati (550 °C per 6 ore) da 40 mL con tappo rivestito in PTFE; un forno riscaldante o blocchi riscaldanti; pipette e lampadine in vetro borosilicato bruciato (550 °C per 6 ore); nastro pH (intervallo acido); Esano (l'esano può essere acquistato dai rivenditori di prodotti chimici. Questa sostanza chimica dovrebbe essere Optima Grade o equivalente).
2. Metodi
- Iniziare con il TLE essiccato (contenente esteri) in uno dei flaconcini di vetro borosilicato da 40 ml.
- Aggiungere circa 10 ml di 2 N KOH al TLE e al tappo.
- Riscaldare in forno o su un blocco riscaldante a 60 °C per 2,5 ore per scindere il legame estere (Figura 3).
- Togliere il campione dal fuoco e lasciarlo raffreddare a temperatura ambiente.
- Aggiungere circa 10 ml della soluzione naCl al 5% al TLE (Figura 3). Questo aiuta a mantenere l'interfaccia tra la fase acquosa e organica (da aggiungere) dalla formazione di schiuma. Tappare e agitare brevemente.
- Aggiungere 6 N HCl al TLE salato a goccia fino a raggiungere il pH 2 per protonare l'O- e formare il prodotto finale, un acido carbossilico stabile (Figura 3; utilizzare carta a pH per testare). Se il TLE è stato colorato, potrebbe esserci un cambiamento di colore in coincidenza con pH 2.
- Aggiungere circa 20 ml di esano alla soluzione acidificata, che ora è priva di esteri. Tappare e agitare vigorosamente per 5 s per estrarre i composti organici dall'acqua.
- Lasciare impostare fino a quando le fasi acquose e organiche completamente separate. Sali, ioni, acqua e HCl non reazioni rimangono nella fase acquosa. I composti organici sono ora nell'esano.
- Rimuovere circa il 75% dell'esano surnatante usando una pipetta ed erogare nell'altro flaconcino di vetro borosilicato da 40 mL.
- Ripetere 2,7 - 2,9 due volte, aggiungendo circa 10 ml di esano ogni volta.
- Scartare la miscela acquosa avanzata in un contenitore per rifiuti adeguato.
- Etichettare il flaconcino contenente esano e sostanze organiche prive di esteri "TLE - saponificato.
La saponificazione è una tecnica comunemente usata per rimuovere gli esteri metilici degli acidi grassi da una miscela organica complessa.
I campioni organici complessi vengono spesso analizzati mediante gascromatografia, che viene utilizzata per determinare le concentrazioni relative dei singoli componenti.
Tuttavia, i composti che sono simili per dimensioni e struttura non possono essere distinti dallo strumento, distorcendo i risultati. Pertanto, i composti indesiderati che producono segnali sovrapposti devono essere rimossi per ottenere risultati accurati.
Questo video copre l'uso della saponificazione per purificare gli alchenoni per la paleoclimatologia. È il primo di una serie che descrive in dettaglio la purificazione di campioni di biomarcatori complessi. Coprirà la procedura, così come alcuni altri usi della tecnica.
Gli alchetoni alchilici polinsaturi a catena lunga, chiamati alchenoni, hanno dimostrato di fornire informazioni utili sulla temperatura superficiale del mare passata.
Tuttavia, gli organismi che producono alchenoni spesso creano esteri metilici degli acidi grassi che sono simili per dimensioni e struttura chimica, chiamati alchenoati. A causa di queste somiglianze, gli alchenoati devono essere rimossi prima di poter ottenere un'analisi accurata.
La saponificazione è una tecnica comune utilizzata per prevenire la co-eluizione di queste molecole. La saponificazione utilizza l'acqua per dividere il legame molecolare di un estere. Una base si attacca al carbonio nel cuore dell'alchenoato. Questa reazione di aggiunta crea un intermedio instabile e l'alcossido viene espulso.
L'idrogeno dall'acido appena formato si sposta verso l'alcossido espulso e l'anione carbossilato risultante forma un legame ionico con il catione dalla base. Il risultato è un sale alcolico e un sale di acidi grassi. L'aggiunta di un acido forte rigenererà l'acido carbossilico. A questo punto, l'alchero incriminato è stato convertito in una forma che non co-eluisce più con l'alchenone di interesse.
Ora che hai capito come la saponificazione può essere utilizzata per purificare una miscela organica, sei pronto per iniziare la procedura.
In primo luogo, acquisire un estratto lipidico totale essiccato - o TLE - che è stato ottenuto utilizzando un metodo di estrazione con solvente. Quindi, preparare le soluzioni di saponificazione come delineato nel protocollo di testo. Assicurarsi che tutti i componenti siano puri e privi di idrocarburi. Una volta preparate le soluzioni, aggiungere il TLE essiccato in un flaconcino di vetro borosilicato da 60 ml. Aggiungere 2 mL di 2 idrossido di potassio normale e sigillare il flaconcino. Quindi, riscaldare il flaconcino a 60 °C per 2,5 ore per scindere il legame estere. Al termine, lasciare raffreddare il campione a temperatura ambiente. Una volta che il campione si è raffreddato, aggiungere 2 ml di soluzione di cloruro di sodio al 5% al flaconcino. Tappare il flaconcino e agitare brevemente. Aggiungere 6 N di acido cloridrico a goccia fino a raggiungere un pH di 2 - usando carta pH per testare. L'aggiunta di questo acido protonerà l'anione carbossilato per formare il prodotto finale - l'acido carbossilico stabile.
Ora che la soluzione acidificata è priva di esteri, aggiungere 5 ml di esano. Tappare e agitare vigorosamente per 5 secondi per estrarre i composti organici dall'acqua. Lasciare riposare la soluzione fino a quando le fasi organica e acquosa si separano completamente. Sali, ioni e acido cloridrico non reazioni rimarranno nella fase acquosa, mentre i composti organici si separeranno nell'esano. Una volta che le fasi sono completamente separate, rimuovere circa il 75% dell'esano usando una pipetta ed erogare in un altro flaconcino da 40 ml. Ripetere questo processo di estrazione altre due volte, aggiungendo 5 ml di esano ogni volta. Una volta completato, scartare la soluzione acquosa rimanente in un contenitore per rifiuti adeguato. Etichettare il flaconcino contenente la fase organica appena saponificata. Gli acidi carbossilici prodotti non possono essere iniettati negli strumenti comunemente utilizzati per l'analisi degli alchenoni senza un'ulteriore purificazione. Gli acidi carbossilici iniettati in un gascromatografo si accumulano rapidamente e rovinano le insenature, le fodere di ingresso e l'estremità anteriore delle colonne. Per rimuovere questi acidi, il campione deve prima sottoporsi a un'altra tecnica di purificazione: la separazione tramite cromatografia su colonna.
La saponificazione ha diverse applicazioni nell'estrazione e purificazione di molecole organiche.
La saponificazione può essere utilizzata non solo per separare i biomarcatori, ma anche per estrarre singoli componenti da utilizzare in prodotti commerciali. In questo esempio, i composti dell'albero del tabacco - Nicotiana glauca - sono stati isolati e analizzati per studiare il loro potenziale come materia prima per un'ampia varietà di prodotti a base biologica, come carburante, calore e una serie di composti chimici.
Le foglie sono state prima omogeneizzate, poi centrifugate, per concentrare le molecole di interesse. Il materiale vegetale concentrato è stato poi saponificato. Il materiale estratto è stato analizzato con cromatografia liquida-spettrometria di massa, per determinare la concentrazione di tocoferolo - una famiglia di composti vitaminici della vitamina E tipicamente presenti nelle piante.
Il materiale estratto può anche essere ricostituito in vitro alla sua composizione originale. In questo esempio, la saponificazione è stata utilizzata per estrarre i carotenoidi dalle piante di spinaci, per essere successivamente ricostituiti in vitro. Gli spinaci sono stati prima omogeneizzati, poi centrifugati, per raccogliere le molecole di pigmento. Queste molecole sono state poi sospese in una soluzione di idrossido di potassio in un imbuto separatore, iniziando la saponificazione. I carotenoidi saponificati separati in uno strato di etere, che è stato raccolto e asciugato. Utilizzando una serie di tamponi di soluzione, i carotenoidi - e altre molecole di pigmentazione - sono stati successivamente ricostituiti in vitro. Questa purificazione ha permesso l'analisi di questi pigmenti senza l'interferenza di composti organici strutturati in modo simile.
A causa della sua capacità di idrolizzare gli esteri, la saponificazione può essere utilizzata per "liberare" composti che sono altrimenti legati alle macromolecole. In questo esempio, una fase di saponificazione anidra viene utilizzata per convertire il 4-fluorobenzoato di etile nel sale dell'acido carbossilico del potassio4-fluorobenzoato. Questa deprotezione attraverso la saponificazione consente la produzione di SFB grezzo - una reazione che non sarebbe possibile se la molecola fosse rimasta "bloccata".
Hai appena visto l'introduzione di JoVE alla purificazione di Uk'37 campioni attraverso la saponificazione. Ora dovresti capire come funziona la saponificazione e come usarla per purificare gli alchenoni in un estratto lipidico totale. Ulteriori processi di purificazione saranno dimostrati nei video successivi.
Grazie per l'attenzione!
Subscription Required. Please recommend JoVE to your librarian.
Results
Questa purificazione produce un TLE privo di esteri che possono essere co-eluinti con gli alchenoni. Tuttavia, la purificazione ha prodotto acidi carbossilici, che non possono essere iniettati su strumenti comunemente usati per analizzare campioni per concentrazioni di alcheni a causa della loro bassa volatilità. Ad esempio, il punto di ebollizione dell'esano, un idrocarburo a 6 atomi di carbonio, è di 68 °C, ma il punto di ebollizione del suo acido (acido esanoico) è di 205 °C. La maggior parte dei biomarcatori suscettibili di GC hanno da 20 a 35 atomi di carbonio (il punto di ebollizione generalmente aumenta con un numero crescente di atomi) e la maggior parte dei programmi di temperatura GC si fermano a circa 300 ° C. Gli acidi carbossilici iniettati in un GC si accumulano rapidamente e rovinano le insenature, le fodere di ingresso e l'estremità anteriore delle colonne. Per rimuovere questi acidi, il campione deve prima sottoporsi a un'altra tecnica di purificazione di separazione tramite cromatografia su colonna.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Come accennato in precedenza, la saponificazione è comunemente usata nei laboratori di geochimica organica per rimuovere gli esteri metilici degli acidi grassi (FAME) degli alchenoni, chiamati alchenoati, che co-eluiscono con gli alchenoni sui gascromatografi (Figure 1). La saponificazione viene anche utilizzata per "liberare" gli acidi grassi "legati" a sedimenti o macromolecole. La degradazione e la conservazione della materia organica e dei biomarcatori nei sedimenti comporta la rimozione di gruppi funzionali (N, O e S) e l'eventuale polimerizzazione di singoli biomarcatori in macromolecole e/o l'adsorbimento di biomarcatori e macromolecole su superfici minerali. Non tutti i biomarcatori in un ambiente diventano legati e il rapporto tra biomarcatori legati e liberi può cambiare in base all'impostazione e all'età dei sedimenti per ragioni ancora non completamente spiegate. La saponificazione, a volte a temperature superiori a quelle qui discusse (>200 °C), viene utilizzata per liberare questi biomarcatori legati nello sforzo di descriverli, la loro fonte e i meccanismi responsabili della loro natura legata.
Subscription Required. Please recommend JoVE to your librarian.




