Overview
출처: 지미 프랑코 박사 연구소 - 메리맥 칼리지
재결정화는 고체 화합물을 정화하는 데 사용되는 기술입니다. 1 고형체는 차가운 액체보다 뜨거운 액체에서 더 용해되는 경향이 있습니다. 재결정화 하는 동안, 불순한 고체 화합물은 용액이 포화 될 때까지 뜨거운 액체에 용해되고 액체가 냉각 될 수 있습니다. 2 화합물은 상대적으로 순수한 결정을 형성해야합니다. 이상적으로, 존재하는 모든 불순물이 용액에 남아 있으며 성장하는 결정(도 1)에통합되지 않습니다. 그런 다음 수정을 여과하여 용액에서 제거할 수 있습니다. 모든 화합물을 복구할 수 있는 것은 아닙니다 - 일부는 용액에 남아 분실됩니다.
재결정화는 일반적으로 분리 기술로 생각되지 않습니다. 오히려 소량의 불순물이 화합물로부터 제거되는 정화 기술이다. 그러나, 두 화합물의 용해도 특성이 충분히 다른 경우, 재결정화는 거의 동일한 양으로 존재하는 경우에도 이를 분리하는 데 사용될 수 있다. 대부분의 불순물이 이미 추출 또는 기둥 크로마토그래피와 같은 다른 방법에 의해 제거되었을 때 재결정화가 가장 효과적입니다.
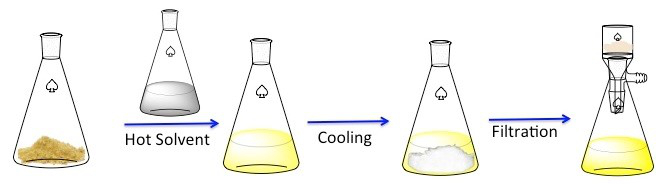
그림 1. 재결정에 대한 일반적인 계획입니다.
Principles
성공적인 재결정화는 용매의 적절한 선택에 따라 달라집니다. 화합물은 뜨거운 용매에 용해되어야하며 추울 때 동일한 용매에서 용해되지 않아야합니다. 재결정화를 목적으로, 수용성과 불용성 사이의 구분선을 3% w/v로 고려하십시오: 3g의 화합물이 용매의 100mL에서 용해되면 용해성으로 간주됩니다. 용매를 선택할 때, 뜨거운 용해도와 차가운 용해도의 차이가 클수록 재결정화에서 더 많은 제품을 회수할 수 있습니다.
냉각 속도는 결정의 크기와 품질을 결정합니다: 빠른 냉각은 작은 결정을 선호하며, 느린 냉각은 크고 일반적으로 순수한 결정의 성장을 선호합니다. 재결정화의 비율은 일반적으로 물질의 융점 아래 약 50 °C에서 가장 크다; 결정의 최대 형성은 융점 아래 약 100 °C에서 발생합니다.
"결정화"와 "재결정화"라는 용어는 때때로 상호 교환적으로 사용되지만 기술적으로 다른 프로세스를 참조합니다. 결정화는 화학 반응에 의한 새로운 용해성 제품의 형성을 말합니다. 이 제품은 많은 갇힌 불순물을 포함하는 무정형 고체로서 반응 용액에서 침전됩니다. 재결정화는 화학 반응을 포함하지 않습니다; 원유 제품은 단순히 용액에 용해되고 결정이 다시 형성될 수 있도록 조건이 변경됩니다. 재결정화는 보다 순수한 최종 제품을 생산합니다. 이러한 이유로, 결정화에 의해 고체 제품을 생산하는 실험 절차는 일반적으로 순수한 화합물을 제공하기 위해 최종 재결정화 단계를 포함한다.
Procedure
용매 연기에 노출되지 않도록 연기 후드의 모든 단계를 수행합니다.
1. 용매 선택
- 에를렌마이어 플라스크에 50 mg의 샘플(N-bromosuccinimide)을 놓습니다.
- 끓는 용매 (물)의 0.5 mL을 추가합니다. 시료가 완전히 용해되면, 차가운 용매의 용해도가 너무 높아서 좋은 재결정화 용매가 된다.
- 시료가 차가운 용매에 용해되지 않으면 용매가 끓을 때까지 테스트 튜브를 가열합니다.
- 이 시점에서 샘플이 완전히 용해되지 않은 경우 모든 고체가 용해될 때까지 끓는 용매 드롭 와이즈를 더 추가합니다. 뜨거운 용매에 시료를 용해시키기 위해 3mL 이상이 걸리는 경우, 이 용매의 용해도가 너무 낮아서 좋은 재결정화 용매가 될 수 있습니다.
- 용매의 첫 번째 선택이 좋은 재결정화 용매가 아닌 경우 다른 사람을 시도하십시오. 작동하는 단일 용매를 찾을 수 없는 경우 두 개의 용매 시스템을 시도하십시오.
- 적합한 단일 용매 시스템을 찾을 수 없는 경우 용매 쌍이 필요할 수 있습니다. 용매 쌍을 식별할 때 몇 가지 주요 고려 사항이 있습니다 1) 첫 번째 용매는 고체를 쉽게 용해시켜야 합니다. 2) 두 번째 용매는 1st 용매와 오해해야하지만, 솔테에 대한 훨씬 낮은 용해도가 있다.
- 일반적으로 "좋아 용해 좋아"극성 화합물은 극성 용매및 비 극성 화합물이 종종 더 용해성 비 극성 화합물에 용해되는 경향이 있음을 의미합니다.
- 일반적인 용매 쌍(표 1)
- 용매가 적어도 40 °C의 비등점을 가지고 있는지 확인, 그래서 끓는 용매와 실온 용매 사이에 합리적인 온도 차이가있다.
- 용매가 약 120°C 이하의 비등점을 가지고 있는지 확인하여 결정에서 용매의 마지막 흔적을 쉽게 제거할 수 있습니다.
- 또한 용매의 비등점이 화합물의 융점보다 낮은지 확인하므로 화합물은 불용성 오일이 아닌 고체 결정으로 형성됩니다.
- 불순물이 뜨거운 용매에서 불용성(화합물이 용해되면 열색 여과될 수 있음) 또는 차가운 용매에 용해되도록 합니다(전체 공정 중에 용해상태를 유지).
2. 뜨거운 용매에서 시료를 용해
- 에를렌마이어 플라스크에서 재결정될 화합물을 놓습니다. 경사진 면이 용매 증기를 트랩하고 증발 속도를 늦추는 데 도움이되기 때문에 이것은 비커보다 더 나은 선택입니다.
- 용매(물)를 별도의 Erlenmeyer 플라스크에 넣고 끓는 칩이나 스터디 바를 추가하여 끓여줍니다. 뜨거운 접시에 끓이도록 가열합니다.
- 화합물을 소량으로 함유하는 실온에서 플라스크에 뜨거운 용매를 넣고, 화합물이 완전히 용해될 때까지, 첨가후 소용돌이를 가한다.
- 용해 과정에서 핫플레이트에 놓아 항상 용액을 뜨겁게 유지하십시오. 시료를 용해시키기에 충분하기 때문에 필요한 것보다 더 많은 핫 용매를 추가하지 마십시오.
- 고체의 일부가 용해되지 않는 경우, 더 뜨거운 용매가 첨가 된 후에도, 매우 불용성 불순물의 존재로 인해 가능성이 높습니다. 이 경우 용매 추가를 중지하고 진행하기 전에 뜨거운 여과를 하십시오.
- 뜨거운 여과를 수행하려면 필터 용지 한 조각을 플루티드 콘 모양으로 접고 유리 줄기없는 깔때기에 넣습니다.
- 10-20% 초과 된 핫 용매를 핫 솔루션에 추가하여 절차에서 증발할 수 있습니다.
- 용지를 통해 용액을 붓습니다. 공정 중에 언제든지 결정이 형성되기 시작하면 따뜻한 용매의 작은 부분을 추가하여 이를 용해시합니다.
3. 솔루션 냉각
- 벤치탑에 놓인 종이 타월과 같이 열을 너무 빨리 수행하지 않는 표면에 용존 화합물이 들어 있는 플라스크를 설정합니다.
- 플라스크를 가볍게 덮어 증발을 방지하고 먼지가 용액에 떨어지는 것을 방지합니다.
- 플라스크가 실온으로 냉각될 때까지 방해받지 않고 둡니다.
- 결정이 형성되면 최대 양의 결정이 얻어지도록 용액을 얼음 욕조에 놓습니다. 용액은 얼음 욕조에서 30 분에서 1 시간까지 방해받지 않고 방치해야하며 화합물이 용액에서 완전히 결정화 된 것처럼 보입니다.
- 결정 형성이 분명하지 않으면, 플라스크의 내부 벽을 유리 막대로 긁거나 동일한 화합물의 작은 종자 결정을 추가하여 유도될 수 있다.
- 그래도 작동하지 않으면 용매가 너무 많이 사용되었을 수 있습니다. 용액을 다시 가열하고 용매의 일부가 끓인 다음 식힙니다.
4. 크리스탈을 분리하고 건조
- 새로 형성된 크리스탈을 벤치탑에 담은 차가운 플라스크를 놓습니다.
- 플라스크를 가볍게 덮어 증발을 방지하고 먼지가 용액에 떨어지는 것을 방지합니다.
- Büchner 또는 Hirsch 깔때기를 사용하여 진공 여과로 결정을 분리합니다 (플라스크를 링 스탠드에 먼저 고정하십시오).
- Büchner 깔때기에 소량의 신선하고 차가운 용매 (재결정에 사용되는 동일한 용매)로 결정을 헹구어 결정에 달라붙을 수있는 불순물을 제거합니다.
- 결정을 건조하려면 필터 깔때기에 두고 몇 분 동안 공기를 그립니다. 크리스탈은 또한 몇 시간 또는 며칠 동안 발견 될 수 있도록하여 공기 건조 될 수있다. 보다 효율적인 방법은 진공 건조 또는 건조기에 배치를 포함한다.
| 폴라 용매 | 덜 극성 용매 |
| 에틸 아세테이트 | 헥산 |
| 메탄올 | 메틸렌 염화물 |
| 물 | 에탄올 |
| 톨루엔 | 헥산 |
표 1. 일반적인 용매 쌍.
재결정화는 고체 화합물을 위한 정화 기술입니다.
재결정화를 수행하기 위해 불순한 고체 화합물을 열용매와 혼합하여 포화 용액을 형성합니다. 이 솔루션이 냉각되면 화합물의 용해도가 감소하고 순수한 결정이 용액에서 증가합니다.
재결정화는 종종 추출, 또는 컬럼 크로마토그래피와 같은 다른 분리 방법 후 최종 단계로 사용된다. 재결정화는 또한 매우 다른 용해도 특성을 가진 두 개의 화합물을 분리하는 데 사용될 수 있다. 이 비디오는 재결정용매 선택, 용액으로부터의 유기 화합물 정제를 설명하고 화학 분야에서 몇 가지 응용 프로그램을 소개합니다.
결정화는 핵형성으로 시작됩니다. 솔루트 분자는 안정적인 작은 결정을 형성하기 위해 함께 모여, 이는 결정 성장 다음에. 핵형성은 종자 결정, 스크래치 또는 고체 불순물과 같은 핵 형성 부위에서 자발적으로 용액보다 더 빠르게 발생합니다. 동요는 또한 급속한 핵형성을 격려할 수 있습니다. 그러나, 급속한 성장은 최적의 조건에서 성장하지 않을 경우 불순물의 통합으로 이어질 수 있습니다.
화합물의 용해도는 온도에 따라 증가하는 경향이 있으며 용매의 선택에 크게 의존합니다. 고온과 저온에서 용해도의 차이가 클수록 용액이 냉각되고 결정을 형성할 가능성이 높아집니다.
선택한 용매는 적어도 40 °C의 비등점이 있어야하므로 끓는 것과 실온 사이에 상당한 온도 차이가 있습니다. 용매의 비등점은 결정화를 가능하게 하기 위해 솔트의 융점 아래에 있어야 합니다. 용액의 신속한 냉각은 많은 핵 형성 부위의 형성을 유도하므로 많은 작은 결정의 성장을 선호합니다. 그러나, 느린 냉각은 더 적은 핵 형성 사이트의 형성을 유도하고, 더 크고 순수한 결정을 선호합니다. 따라서, 느린 냉각이 바람직하다.
또한 불순물을 최소화하기 위해 용매를 선택할 수 있습니다. 용액 불순물이 솔루트 자체보다 용해성인 경우, 차가운 용매로 완전히 형성된 결정에서 씻어낼 수 있습니다. 그러나 불순물이 용해가 적으면 먼저 결정화되고, 솔루트의 재결정 전에 가열된 용액에서 여과될 수 있다.
단일 용매가 필요한 특성을 가지고 있지 않으면 용매의 혼합물을 사용할 수 있습니다. 용매 쌍의 경우 첫 번째 용매는 고체를 쉽게 용해해야합니다. 두 번째 용매는 솔테에 대한 용해도가 낮고 첫 번째 용매로 오해되어야합니다. 일반적인 용매 쌍은 에틸 아세테이트와 헥산, 톨루엔과 헥산, 메탄올 및 디클로로메탄, 물 및 에탄올을 포함한다.
이제 재결정의 원리를 이해하게 되었으므로, 재결정에 의한 유기 화합물의 정화 절차를 살펴보겠습니다.
이 절차를 시작하려면 유리 테스트 튜브에 50 mg의 샘플을 배치하십시오.
실온 용매0.5mL를 추가합니다. 화합물이 완전히 용해되면, 차가운 용매의 용해도가 너무 높아서 재결정에 사용됩니다. 그렇지 않으면, 끓는 테스트 튜브에 혼합물을 가열.
화합물이 끓는 용매에 완전히 용해되지 않으면 용매의 다른 부분을 끓이도록 가열합니다. 고체가 완전히 녹을 때까지 또는 테스트 튜브가 3mL의 용매를 포함 할 때까지 끓는 용매를 테스트 튜브에 드롭 방향으로 추가합니다. 고체가 여전히 용해되지 않으면 이 용매의 용해도가 너무 낮습니다.
불순물이 뜨거운 용매에서 용해되거나 차가운 용매에서 용해 된 후 여과될 수 있으므로 재결정화가 완료된 후에도 용액에 남아 있는지 확인합니다. 용매가 모든 기준을 충족하는 경우 재결정에 적합합니다.
재결정을 시작하려면 용매를 가열하여 에를렌마이어 플라스크의 핫 플레이트에 스티어 바로 끓입니다. 화합물을 실온에서 다른 에렌마이어 플라스크에 재결정할 수 있도록 배치합니다.
다음으로, 화합물에 핫 솔벤트의 작은 부분을 추가합니다. 플라스크에 혼합물을 소용돌이다음 핫 플레이트에 놓습니다. 샘플이 완전히 용해될 때까지 또는 용매를 추가할 때까지 이 프로세스를 반복하면 더 이상 용해되지 않습니다.
증발을 고려하여 용액에 10% 초과된 핫 솔벤트를 추가합니다. 필터 용지를 뷔흐너 깔때기 설정에 배치합니다. 용액을 필터링하여 불용성 불순물을 제거합니다. 여과 중에 결정이 형성되면 뜨거운 용매 방울로 녹입니다.
벤치탑에서 솔루션을 식힙니다. 플라스크를 덮어 용매가 증발하는 것을 방지하고 미립자를 용액에서 분리하십시오.
플라스크가 실온으로 냉각될 때까지 방해받지 않고 둡니다. 냉각 중 동요는 빠른 결정화를 일으킬 수 있으며 순수한 결정을 줄입니다. 냉각 시 결정 형성이 명확하지 않은 경우, 플라스크의 내부 벽을 유리 막대로 부드럽게 긁거나 재결정되는 화합물의 작은 종자 결정을 추가하여 결정화를 유도하십시오.
결정 형성을 유도할 수 없는 경우 용액을 다시 가열하여 용매의 일부를 끓인 다음 용매를 다시 실온으로 냉각시킵니다.
결정이 형성되면 얼음 목욕을 준비하십시오. 용액을 덮고 결정화가 완료될 때까지 얼음 욕조에서 용액을 식힙니다.
여과 플라스크를 링 스탠드에 고정하고 플라스크를 진공 선에 연결합니다. 플라스크 의 입에 뷔흐너 깔때기와 어댑터를 설정합니다.
용액과 결정의 혼합물을 깔때기에 붓고 진공 여과를 시작합니다. 플라스크에 남아 있는 모든 결정을 차가운 용매로 깔때기에 헹구세요. 냉용 불순물을 제거하기 위해 차가운 용매로 깔때기의 결정을 씻으시면 됩니다.
깔때기를 통해 공기를 계속 끌어들여 결정을 말린 다음 진공 펌프를 끕니다. 필요한 경우, 결정은 결정화 된 고체를 저장하기 전에 건조하거나 건조기에 실온에서 서 있을 수 있습니다.
원유 화합물에 존재하는 황색 불순물이 제거되어 흰색이 아닌 고체가 생성됩니다. 화합물과 불순물의 정체성에 기초하여, 결정의 순도는 NMR 분광법, 융점 측정 또는 육안 검사에 의해 검증될 수 있다.
재결정에 의한 정제는 화학 합성 및 분석을 위한 중요한 도구입니다.
X선 결정예학은 분자의 3차원 원자 구조를 식별하는 강력한 특성화 기술입니다. 이를 위해서는 순수한 단일 결정이 필요하며, 이는 재결정에 의해 얻어진다. 단백질과 같은 분자의 몇몇 종류는 결정화하기 어렵습니다, 그러나 그들의 구조물은 그들의 화학 기능을 이해하기 위하여 극단적으로 중요합니다. 재결정 조건의 주의 깊은 선택으로, 분자의 이 종류조차 엑스레이 결정학에 의해 분석될 수 있습니다. 이 과정에 대해 자세히 알아보려면 결정학을 위한 크리스탈을 성장시키는 이 컬렉션의 비디오를 참조하십시오.
불순한 반응제는 원치 않는 측면 반응을 일으킬 수 있습니다. 재결정화로 정화 된 반응은 제품의 순도와 수율을 향상시킵니다. 고체 제품이 분리되고 세척되면, 응고물에서 휘발성을 제거하고 생성된 고체로부터 제품을 재결정함으로써 반응 수율을 높일 수 있습니다. 부동액 단백질, 또는 AFP는, 얼음 환경에 사는 많은 유기체에서 표현됩니다. AFP는 얼음 비행기에 결합하여 내부 얼음 성장을 방해하여 더 큰 얼음 결정으로 재결정화를 억제합니다. 다른 AFP는 얼음 결정 평면의 다른 유형에 바인딩합니다. AFP 결합 메커니즘을 조사하는 것은 단일 얼음 결정에 흡착하는 것을 포함합니다. 단일 얼음 결정의 적절한 성장은 명확하고 유익한 결과를 위해 필수적입니다. 이 단백질은 냉동 수술에 방온 성 작물의 엔지니어링에서 응용 프로그램이 있습니다.
당신은 단지 재결정에 의해 화합물을 정화하는 JoVE의 소개를 보았다. 이제 기술의 원리, 정화 절차 및 화학의 재결정화에 대한 일부 응용 분야에 대해 잘 알고 있어야 합니다.
시청해 주셔서 감사합니다!
Results
재결정 결과의 예는 도 2에도시된다. 원유 화합물에 존재하는 황색 불순물이 제거되고 순수한 제품은 오프 화이트 고체로 남아 있습니다. 재결정된 화합물의 순도는 이제 핵 자기 공명(NMR) 분광법 또는, 공표된 융점이 있는 화합물인 경우, 그 융점이 문헌 융점에 얼마나 유사한지에 의해 검증될 수 있다. 필요한 경우 순도가 허용될 때까지 여러 번의 재결정화를 수행할 수 있습니다.

그림 2. 2a) 원유 화합물(왼쪽), 2b) 변과(가운데) 및 2c 전에 재결정된 생성물은 재결정후(오른쪽)이다.
Applications and Summary
재결정화는 혼합될 수 있는 불순물을 제거하여 화합물을 정화하는 방법입니다. 화합물이 뜨거운 용매에서 매우 용해될 때 가장 잘 작동하지만 동일한 용매의 차가운 버전에서 매우 불용성입니다. 화합물은 실온에서 고체여야 합니다. 재결정화는 종종 더 많은 양의 불순물을 제거하는 데 효과적이지만 최종 화합물의 순도를 충분히 높은 수준으로 올리지 않는 다른 방법(추출 또는 컬럼 크로마토그래피과 같은)이 끝난 후 최종 정화 단계로 사용됩니다.
재결정화는 화합물의 절대적으로 순수하고 완벽한 단일 결정을 생성 할 수있는 유일한 기술입니다. 이러한 결정은 분자의 구조와 3차원 형상을 결정하는 궁극적인 권위자인 X선 분석에 사용될 수 있다. 이러한 경우, 재결정화는 몇 주에서 몇 달 동안 매우 느리게 진행되어 어떤 불순물을 포함하지 않고 결정 격자가 형성될 수 있도록 허용된다. 특수 유리 웨어는 용매가이 시간 동안 가능한 한 천천히 증발 할 수 있도록 필요, 또는 용매가 매우 천천히 화합물이 불용성되는 다른 용매와 혼합 할 수 있도록 (항 솔벤트 추가라고).
제약 산업은 또한 재결정화를 많이 사용합니다, 그것은 열 크로마토그래피보다 더 쉽게 확장 정화의 수단이기 때문에. 3 산업 응용 분야에서 재결정화의 중요성은 교육자가 실험실 교육 과정의 재결정화를 강조하도록 촉발시켰습니다. 4 예를 들어, HIV의 효과를 감소시키는 데 사용되는 Stavudine 약물은 일반적으로 결정화에 의해 격리됩니다. 5 종종 분자는 여러 가지 결정 구조를 사용할 수 있으므로 냉각 속도, 용매 조성 등과 같은 조건에서 어떤 결정 형태가 격리되어 있는지 평가하고 이해해야 합니다. 이러한 다른 결정 형태는 다른 생물학적 특성을 가질 수 있습니다 또는 다른 속도로 신체에 흡수 될 수 있습니다.
재결정화의 일반적인 사용은 바위 사탕을 만드는 것입니다. 바위 사탕은 포화 지점까지 뜨거운 물에 설탕을 용해하여 만들어집니다. 나무 막대기는 용액에 배치되고 용액이 천천히 냉각되고 증발 할 수 있습니다. 며칠 후, 큰 설탕 결정은 나무 막대기 전체에 걸쳐 성장했습니다.
Disclosures
- 마요, 디 W.; 파이크, R.M.; 포브스, D.C., 마이크로 스케일 유기 실험실 : 멀티 스텝 및 다중 규모의 신디사이저. 5 번째 에드.; J. 와일리와 아들: 호보켄, 뉴저지, p xxi, 681 p (2011).
- 아르마레고, 더블유 엘 에프; 차이, C. L. L., 실험실 화학 물질의 정화. 5 번째 에드.; 버터워스 하이네만: 암스테르담; 보스턴; p xv, 609 p (2003).
- 레이, P.C.; 텀마나팔리, J.M.C.; 골란라, S. R., 스타부딘의 대규모 생산을위한 프로세스. 구글 특허: (2011).
- 하이 타워, T. R.; Heeren, J. D., 벤조산의 재결정을 위한 향상된 용매 시스템의 개발을 위한 시뮬레이션 된 산업 설정을 사용 하 여: 학생 중심 프로젝트. 화학 교육 저널 83 (11), 1663 (2006).
- 로하니, S.; 호른, S.; Murthy, K., 제약 및 미세 화학 물질의 배치 결정화에서 제품 품질의 제어. Part 1: 결정화 공정의 설계 및 용매의 효과. 유기 공정 연구 및 개발 9 (6), 858-872 (2005).
References
- Mayo, D. W.; Pike, R. M.; Forbes, D. C., Microscale organic laboratory : with multistep and multiscale syntheses. 5th ed.; J. Wiley & Sons: Hoboken, NJ, p xxi, 681 p (2011).
- Armarego, W. L. F.; Chai, C. L. L., Purification of laboratory chemicals. 5th ed.; Butterworth-Heinemann: Amsterdam ; Boston; p xv, 609 p (2003).
- Ray, P. C.; Tummanapalli, J. M. C.; Gorantla, S. R., Process for the large scale production of Stavudine. Google Patents: (2011).
- Hightower, T. R.; Heeren, J. D., Using a Simulated Industrial Setting for the Development of an Improved Solvent System for the Recrystallization of Benzoic Acid: A Student-Centered Project. Journal of Chemical Education 83 (11), 1663 (2006).
- Rohani, S.; Horne, S.; Murthy, K., Control of Product Quality in Batch Crystallization of Pharmaceuticals and Fine Chemicals. Part 1: Design of the Crystallization Process and the Effect of Solvent. Organic Process Research & Development 9 (6), 858-872 (2005).




