Overview
Quelle: Labor von Dr. Jimmy Franco - Merrimack College
Rekristallisation ist eine Technik verwendet, um feste Verbindungen zu reinigen. 1 Feststoffe tendenziell besser löslich in heißer Flüssigkeiten als in kalten Flüssigkeiten. Während Rekristallisation ist eine unreine solide Verbindung in eine heiße Flüssigkeit aufgelöst, bis die Lösung gesättigt ist, und dann die Flüssigkeit darf abkühlen lassen. 2 die Verbindung sollte dann relativ reines Kristalle bilden. Im Idealfall Verunreinigungen, die vorhanden sind in der Lösung bleiben und fließen nicht in die wachsenden Kristalle (Abbildung 1). Die Kristalle können dann die Lösung durch Filtration entfernt werden. Nicht alle der Verbindung ist wiederherstellbar – einige bleiben in der Lösung und werden verloren gehen.
Rekristallisation wird im Allgemeinen als eine Trennung Technik nicht gedacht; Vielmehr ist es eine Reinigung-Technik, bei der eine kleine Menge einer Verunreinigung von einer Verbindung entfernt wird. Jedoch wenn die Löslichkeit Eigenschaften der beiden Verbindungen ausreichend unterscheiden, Rekristallisation lässt sich trennen, auch wenn sie in fast gleicher Höhe vorhanden sind. Rekristallisation funktioniert am besten, wenn die meisten Verunreinigungen bereits durch eine andere Methode, wie z. B. Extraktion oder Spalte Chromatographie entfernt wurden.
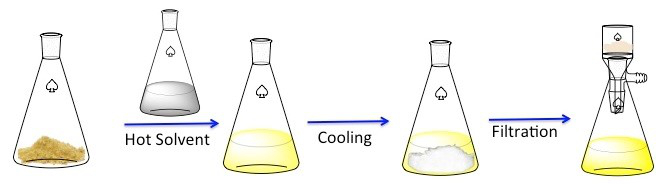
Abbildung 1. Der allgemeinen Regelung für Rekristallisation.
Principles
Eine erfolgreiche Rekristallisation hängt die richtige Wahl des Lösungsmittels. Die Verbindung muss in die heiße Lösungsmittel und unlöslich in dem gleichen Lösungsmittel löslich sein, wenn es kalt ist. Für die Zwecke der Rekristallisation, 3 % w/V betrachten die Trennlinie zwischen löslichen und unlöslichen: Wenn 3 g eines Stoffes in 100 mL Lösungsmittel auflöst, wird es als löslich. Bei der Wahl eines Lösungsmittels, je größer der Unterschied zwischen heißen Löslichkeit und kalten Löslichkeit, das mehr Produkt erzielbare von Rekristallisation.
Die Rate des Abkühlens bestimmt die Größe und Qualität der Kristalle: schnelle Abkühlung begünstigt kleine Kristalle und langsame Abkühlung begünstigt das Wachstum der großen und in der Regel reiner Kristalle. Rekristallisation beträgt in der Regel größte bei ca. 50 ° C unterhalb des Schmelzpunktes des Stoffes; die maximale Bildung von Kristallen tritt bei etwa 100 ° C unterhalb des Schmelzpunktes.
Obwohl die Begriffe "Kristallisation" und "Rekristallisation" manchmal synonym verwendet werden, beziehen sie sich technisch auf unterschiedliche Prozesse. Kristallisation bezieht sich auf die Bildung eines neuen, unlöslichen Produktes durch eine chemische Reaktion; Dieses Produkt fällt dann aus der Reaktionslösung aus als eine amorphe Festkörper mit vielen eingeschlossenen Verunreinigungen. Rekristallisation ist nicht erforderlich, eine chemische Reaktion. Das Rohprodukt wird einfach in der Lösung aufgelöst, und dann die Bedingungen geändert werden, um Kristalle zu re-form zu ermöglichen. Rekristallisation produziert ein reineres Endprodukt. Aus diesem Grund gehören experimentelle Verfahren, die ein solides Produkt durch Kristallisation normalerweise produzieren einen endgültige Rekristallisation Schritt um die reine Verbindung zu geben.
Procedure
Führen Sie alle Schritte in einer Dampfhaube, Belastung durch Lösemitteldämpfe zu verhindern.
1. Auswahl eines Lösungsmittels
- Legen Sie 50 mg der Probe (N-Bromsuccinimid) in einen Erlenmeyerkolben.
- Hinzugeben Sie 0,5 mL kochendes Lösungsmittel (Wasser). Wenn die Probe vollständig auflöst, ist die Löslichkeit in den kalten Lösungsmittel zu hoch, um eine gute Rekristallisation Lösungsmittel.
- Wenn die Probe nicht im kalten Lösungsmittel löst, erhitzen Sie das Reagenzglas, bis das Lösungsmittel kocht.
- Wenn die Probe nicht zu diesem Zeitpunkt vollständig aufgelöst hat, fügen Sie mehr kochendes Lösungsmittel tropfenweise, bis alle festen auflöst. Wenn es mehr als 3 mL die Probe in die heiße Lösungsmittel auflösen dauert, ist die Löslichkeit in diesem Lösungsmittel vermutlich zu gering zu machen, eine gute Rekristallisation Lösungsmittel.
- Ist die erste Wahl des Lösungsmittels nicht gut Rekristallisation Lösungsmittel, versuchen Sie andere. Wenn ein einziges Lösungsmittel, das funktioniert nicht gefunden werden kann, versuchen Sie zwei Lösungsmittelsystem.
- Wenn Sie ein geeignetes Lösungsmittels System nicht finden können, kann ein Lösungsmittel paar erforderlich sein. Wenn ein Lösungsmittel paar identifizieren, gibt es mehrere wichtige Überlegungen 1) das erste Lösungsmittel sollten leicht festen auflösen. (2) das zweite Lösungsmittel muss mit 1St Lösungsmittel mischbar, aber haben eine viel geringere Löslichkeit für die gelösten.
- Als allgemeine Regel "likes" gerne auflösen was bedeutet, dass die polare Verbindungen sind in der Regel löslich in polaren Lösungsmitteln und unpolaren Verbindungen sind oft mehr lösliche unpolaren Verbindungen.
- Allgemeine Lösungsmittel Paare (Tabelle 1)
- Stellen Sie sicher, dass das Lösungsmittel hat einen Siedepunkt von mindestens 40 ° C, so gibt es ein angemessene Temperatur-Unterschied zwischen kochendes Lösungsmittel und Raumtemperatur Lösungsmittel.
- Stellen Sie sicher, dass das Lösungsmittel einen Siedepunkt unter ca. 120 ° C, hat so ist es einfacher, die letzten Spuren des Lösungsmittels aus der Kristalle zu entfernen.
- Stellen Sie außerdem sicher, dass der Siedepunkt des Lösungsmittels ist niedriger als der Schmelzpunkt der Verbindung, so dass die Verbindung als feste Kristalle nicht als unlösliche Öl bildet.
- Bestätigen, dass die Verunreinigungen entweder sind in die heiße Lösungsmittel (so heiß-herausgefiltert, können sie die Verbindung aufgelöst ist) unlöslich oder löslich in kalten Lösungsmittel (so dass sie während des gesamten Prozesses gelösten bleiben).
(2) auflösen die Probe in heiße Lösungsmittel
- Legen Sie die Masse in einen Erlenmeyerkolben umkristallisiert werden. Dies ist eine bessere Wahl als ein Becherglas, da die abfallenden Seiten Falle Lösungsmitteldämpfe helfen und die Rate von Verdampfung verlangsamen.
- Das Lösungsmittel (Wasser) in einem separaten Erlenmeyer-Kolben, geben Sie und kochendes Chips oder Stir Bar kochendem glatt zu halten. Bis zum Sieden auf einer Kochplatte erhitzen.
- Fügen Sie heiße Lösungsmittel in einem Kolben bei Raumtemperatur, enthält die Substanz in kleinen Portionen, nach jeder Zugabe, wirbeln, bis die Verbindung vollständig gelöst ist.
- Halten Sie bei der Auflösung die Lösung heiß aller Zeiten durch ruht es auf der Herdplatte zu. Fügen Sie mehr heiße Lösungsmittel als nötig - nicht gerade genug, um die Probe auflöst.
- Wenn ein Teil des Festkörpers nicht aufzulösen scheint, auch nach mehr heiße Lösungsmittel hinzugefügt wurde, dürfte aufgrund der Anwesenheit von sehr unlösliche Verunreinigungen. In diesem Fall stoppen Sie, Hinzufügen von Lösungsmittel und machen Sie eine heiße Filtration, bevor Sie fortfahren.
- Eine heiße Filtration, Falten ein Stück Filterpapier in eine geriffelte Kegelform und legen Sie sie in ein Glas stammlose Trichter.
- Die heiße Lösung, um Verdampfung im Verfahren ermöglichen fügen Sie eine 10-20 % Überschuss an heiße Lösungsmittel hinzu.
- Gießen Sie die Lösung durch das Papier. Wenn Kristalle jederzeit während des Prozesses zu bilden beginnen, fügen Sie einen kleinen Teil des warmen Lösungsmittel um sie aufzulösen.
3. Kühllösung die
- Legen Sie die Flasche mit der gelösten Verbindung auf eine Oberfläche, die nicht die Wärme Weg zu schnell, wie ein Papiertuch legen auf eine Tischplatte zu leiten.
- Decken Sie leicht die Küvette abkühlen um Verdunstung zu verhindern und zu verhindern, dass Staub in die Lösung fallen.
- Lassen Sie den Kolben ungestört, bis es auf Raumtemperatur abkühlt.
- Sobald die Kristalle gebildet haben, legen Sie die Lösung in ein Eisbad um sicherzustellen, dass der Höchstbetrag der Kristalle gewonnen wird. Die Lösungen sollten Links ungestört im Eisbad für 30 min bis 1 h, oder bis die Verbindung scheint völlig aus der Lösung kristallisieren haben.
- Wenn keine Kristallbildung ersichtlich ist, kann es durch Kratzen innen induziert werden Wände des Kolbens mit einem Glasstab oder durch das Hinzufügen einer kleinen Impfkristall der gleichen Verbindung.
- Wenn dies noch nicht funktioniert, dann wahrscheinlich zu viel Lösungsmittel verwendet wurde. Erwärmen der Lösung, erlauben einige des Lösungsmittels aus Kochen, dann abkühlen.
(4) zu isolieren und die Kristalle trocknen
- Legen Sie die kalte Flasche enthält die neu gebildeten Kristalle auf einem Benchtop.
- Decken Sie leicht die Flasche um Verdunstung zu verhindern und zu verhindern, dass Staub in die Lösung fallen.
- Isolieren Sie die Kristalle durch Vakuumfiltration mit Büchner oder Hirsch Trichter (Klemme der Kolben zu einem Ring stehen zuerst).
- Spülen Sie die Kristalle auf den Büchner-Trichter mit einer kleinen Menge von frischen, kalten Lösungsmittel (die gleichen Lösungsmittels für Rekristallisation) um eventuelle Verunreinigungen zu entfernen, die auf die Kristalle stecken kann.
- Um die Kristalle zu trocknen, lassen Sie sie in den Trichtereinsatz und ziehen Sie Luft durch sie für einige Minuten. Kristalle können auch luftgetrocknet werden, indem sie sich für mehrere Stunden oder Tage unbedeckt stehen. Eine effizientere Methoden gehören Vakuumtrocknung oder Platzierung in den Exsikkator gestellt.
| Polares Lösungsmittel | Weniger polares Lösungsmittel |
| Ethylacetat | Hexan |
| Methanol | Methylenchlorid |
| Wasser | Ethanol |
| Toluol | Hexan |
Tabelle 1. Allgemeine Lösungsmittel Paare.
Rekristallisation ist eine Reinigung Technik für feste Verbindungen.
Rekristallisation ausführen, wird eine unreine solide Verbindung mit heiße Lösungsmittel zu einer gesättigten Lösung vermischt. Da diese Lösung abkühlt, die Löslichkeit des zusammengesetzten abnimmt und reine Kristalle wachsen von Lösung.
Rekristallisation wird oft als letzter Schritt nach dem anderen Trennverfahren wie Extraktion oder Säulenchromatographie verwendet. Rekristallisation kann auch verwendet werden, um zwei Verbindungen mit sehr unterschiedlichen Löslichkeit Eigenschaften zu trennen. Dieses Video wird Lösungsmittel Auswahl für Rekristallisation, Reinigung einer organischen Verbindung aus Lösung, illustrieren und präsentieren einige Anwendungen in der Chemie.
Kristallisation beginnt mit Keimbildung. Gelöste Moleküle kommen zusammen, um eine stabile kleine Kristall bilden, von Kristallwachstum gefolgt. Keimbildung tritt schneller auf Keimbildung Seiten wie Saat Kristalle, Kratzer oder festen Verunreinigungen als spontan in Lösung. Agitation ermutigt vielleicht auch schnelle Keimbildung. Schnelles Wachstum kann jedoch zur Aufnahme von Verunreinigungen nicht gewachsen in optimalen Bedingungen führen.
Die Löslichkeit eines Stoffes tendenziell mit der Temperatur zu erhöhen, und ist stark abhängig von der Wahl des Lösungsmittels. Je größer der Unterschied in der Löslichkeit bei hohen und niedrigen Temperaturen, desto wahrscheinlicher ist es für die gelösten, aus der Lösung zu kommen, wenn es abkühlt, und Kristalle bilden.
Das gewählte Lösungsmittel sollten einen Siedepunkt von mindestens 40 ° C haben, so gibt es einen erheblichen Temperaturunterschied zwischen Kochen und Raumtemperatur. Auch muss das Lösemittel Siedepunkt unterhalb des Schmelzpunktes des gelösten Stoffes Kristallisation zu ermöglichen. Schnelle Abkühlung der Lösung induziert die Bildung von Keimbildung Sehenswürdigkeiten, so begünstigt das Wachstum von vielen kleinen Kristallen. Aber langsame Abkühlung induziert die Bildung von weniger Keimbildung Websites, und größer und reiner Kristalle begünstigt. Somit ist die langsame Abkühlung bevorzugt.
Darüber hinaus kann ein Lösungsmittel ausgewählt werden, um Verunreinigungen zu minimieren. Wenn eine Lösung Verunreinigung besser löslich als der gelöste Stoff selbst ist, kann es aus den voll ausgebildeten Kristallen mit kalten Lösungsmittel gewaschen werden. Jedoch wenn eine Verunreinigung weniger löslich ist, wird zuerst kristallisieren, und dann aus der beheizten Lösung vor der Rekristallisation des gelösten Stoffes gefiltert werden kann.
Wenn kein einziges Lösungsmittel die nötigen Eigenschaften hat, kann ein Gemisch von Lösungsmitteln verwendet werden. Für einen solventen paar sollte das erste Lösungsmittel leicht festen auflösen. Das zweite Lösungsmittel muss eine geringere Löslichkeit für die gelösten und mit dem ersten Lösungsmittel mischbar. Allgemeine Lösungsmittel Paare enthalten Ethylacetat und Hexan, Toluol und Hexan, Methanol und Dichlormethan, und Wasser und Ethanol.
Nun, Sie die Prinzipien der Rekristallisation verstehen, durchlaufen Sie Lasst uns ein Verfahren für die Reinigung einer organischen Verbindung durch Rekristallisation.
Um diesen Vorgang zu starten, legen Sie 50 mg der Probe in ein Reagenzglas.
0,5 mL Lösungsmittel Raumtemperatur hinzugeben. Wenn die Verbindung vollständig auflöst, ist die Löslichkeit in den kalten Lösungsmittel zu hoch für Rekristallisation verwendet werden. Ansonsten, erhitzen Sie die Mischung in das Reagenzglas bis zum Sieden.
Wenn die Verbindung nicht vollständig in den kochenden Lösungsmittel löst, erhitzen Sie ein weiterer Teil des Lösungsmittels zum Sieden. Hinzufügen der kochenden Lösungsmittels tropfenweise das Reagenzglas bis festen vollständig auflöst oder das Reagenzglas 3 mL Lösungsmittel enthält. Wenn das fest noch nicht löst, ist seine Löslichkeit in diesem Lösungsmittel zu niedrig.
Bestätigen Sie, dass Verunreinigungen sind entweder in die heiße Lösungsmittel unlöslich, so dass sie nach Auflösung herausgefiltert werden können, oder in der kalten Lösungsmittel löslich, so dass sie in Lösung bleiben, nachdem die Rekristallisation abgeschlossen ist. Wenn ein Lösungsmittel alle Kriterien erfüllt, ist es geeignet für Rekristallisation.
Pour commencer Rekristallisation, erhitzen Sie das Lösungsmittel zum Kochen auf einer heißen Platte in einen Erlenmeyerkolben mit Stir Bar. Legen Sie die Masse in eine andere Erlenmeyer-Kolben bei Raumtemperatur umkristallisiert werden.
Fügen Sie dann eine kleine Portion heiße Lösungsmittel auf die Verbindung. Schwenken Sie die Mischung in die Flasche und dann legen Sie es auf der Heizplatte sowie. Wiederholen Sie diesen Vorgang, bis die Probe vollständig gelöst hat oder Zugabe von Lösungsmittel keine weitere Auflösung führt.
Fügen Sie eine Selbstbeteiligung von 10 % der heiße Lösungsmittel zur Lösung, um Verdunstung zu berücksichtigen. Filterpapier in einem Büchner-Trichter-Setup zu platzieren. Filtern Sie die Lösung um unlösliche Verunreinigungen zu entfernen. Kristalle bilden sich während der Filtration, mit Tropfen heiße Lösungsmittel auflösen.
Kühlen Sie die Lösung auf die Tischplatte. Decken Sie den Kolben, solvent Verlust um Verdunstung zu verhindern und Partikel aus der Lösung zu halten.
Lassen Sie den Kolben ungestört, bis es auf Raumtemperatur abgekühlt ist. Unruhe im Kühlfall verursachen schnelle Kristallisation, wodurch weniger reine Kristalle. Wenn keine Kristallbildung beim Abkühlen hervorgeht, induzieren Kristallisation durch Kratzen leicht innen Wände des Kolbens mit einem Glasstab oder das Hinzufügen einer kleinen Impfkristall der Verbindung wird umkristallisiert.
Wenn Kristallbildung induziert werden kann nicht, erwärmen Sie die Lösung für einige des Lösungsmittels zu kochen und kühlen Sie des Lösungsmittels auf Raumtemperatur noch einmal ab.
Sobald Kristalle gebildet haben, bereiten Sie ein Eisbad. Halten Sie die Lösung bedeckt, die Lösung in das Eisbad kühlen Sie bis Kristallisation scheint abgeschlossen zu sein ab.
Klemmen Sie ein Fläschchen Filtration zu einem Ring Stand und verbinden Sie den Kolben mit einer Vakuumleitung. Legen Sie einen Büchner-Trichter und Adapter in den Mund des Kolbens.
Gießen Sie die Mischung der Lösung und Kristalle in den Trichter und beginnen Sie Vakuumfiltration. Spülen Sie alle Kristalle, die noch in der Küvette in den Trichter mit kalten Lösungsmittel. Waschen Sie die Kristalle auf den Trichter mit kalten Lösungsmittel lösliche Verunreinigungen zu entfernen.
Zeichnen Sie Luft durch den Trichter um die Kristalle zu trocknen und dann schalten Sie die Vakuumpumpe weiter. Wenn nötig, die Kristalle dürfen bei Raumtemperatur an der Luft trocken oder in einem Exsikkator stehen vor dem Speichern der kristalliner Feststoff.
Die gelbe Verunreinigungen in die krude Mischung vorhanden wurden entfernt, eine wollweiße Solid nachgeben. Auf Basis der Identität von der Verbindung und die Verunreinigungen, kann die Reinheit der Kristalle durch NMR-Spektroskopie, Schmelzpunkt Messungen oder Sichtkontrolle überprüft werden.
Reinigung durch Rekristallisation ist ein wichtiges Instrument für chemische Synthese und Analyse.
Röntgen-Kristallographie ist eine leistungsstarke Charakterisierung-Technik, die die dreidimensionale atomare Struktur eines Moleküls identifiziert. Dies erfordert einen reine Einkristall, das durch Umkristallisation gewonnen wird. Einige Klassen von Molekülen wie Proteinen sind schwierig zu kristallisieren, aber ihre Strukturen sind extrem wichtig für das Verständnis ihrer chemischen Funktionen. Mit der sorgfältigen Auswahl der Rekristallisation Bedingungen können auch diese Klassen von Molekülen durch Röntgen-Kristallographie analysiert werden. Erfahren Sie mehr über diesen Prozess sehen Sie diese Sammlung Video auf wachsende Kristalle für Kristallographie.
Unreinen Reaktionspartner können unerwünschte Nebenreaktionen verursachen. Reinigen der Reaktanden durch Rekristallisation verbessert die Produktreinheit und Ertrag. Sobald ein solides Produkt isoliert und gewaschen hat, kann auch Reaktion Ertrag erhöht werden, durch flüchtige Bestandteile aus dem Filtrat entfernen und das Produkt aus dem daraus resultierenden vollen recrystallizing. Frostschutzmittel Proteine oder PST, werden in vielen Organismen ausgedrückt, die in eisigen Umgebungen leben. PST behindern das interne Eis Wachstum durch Bindung an Flugzeugen, Hemmung der Rekristallisation in größeren Eiskristalle Eis. Verschiedene PST binden an verschiedene Arten von Eis-Kristall-Flugzeuge. AFP verbindliche Mechanismen beinhaltet adsorbierenden sie auf einzelne Eiskristalle. Richtiges Wachstum von einem einzigen Eiskristall ist Voraussetzung für klare und informative Ergebnisse. Diese Proteine haben Anwendungen vom Engineering kältebeständig Kulturen, Kryochirurgie.
Sie sah nur Jupiters Einführung in Verbindungen durch Umkristallisation reinigen. Sie sollten jetzt mit den Prinzipien der Technik, eine Reinigungsprozedur und einige Anwendungen der Rekristallisation in der Chemie vertraut sein.
Danke fürs Zuschauen!
Results
Ein Beispiel für die Ergebnisse der Rekristallisation ist in Abbildung 2dargestellt. Die gelbe Verunreinigungen in die krude Mischung vorhanden wurde entfernt, und das reine Produkt bleibt als eine wollweiße Feststoff. Die Reinheit der umkristallisiert Verbindung nun von Kernresonanzspektroskopie (NMR) überprüft werden kann, oder wenn es eine Verbindung mit einem veröffentlichten Schmelzpunkt ist, wie ähnlich seinem Schmelzpunkt wird auf den Literatur-Schmelzpunkt. Bei Bedarf können mehrere Recrystallizations durchgeführt werden, bis die Reinheit akzeptabel hoch ist.

Abbildung 2. 2a) eine grobe Verbindung (links), 2 b) umkristallisiert Produkt vor der Filtration (Mitte) und 2 c) die gleiche Verbindung nach Rekristallisation (rechts).
Applications and Summary
Rekristallisation ist eine Methode der Reinigung einer Verbindung durch die Beseitigung von Verunreinigungen, die mit ihm gemischt werden könnte. Es funktioniert am besten, wenn die Verbindung sehr gut in eine heiße Lösungsmittel löslich, aber in der kalten Version des gleichen Lösungsmittels sehr unlöslich ist. Die Verbindung muss eine solide bei Raumtemperatur. Rekristallisation dient oft als letzter Schritt bereinigen, nach anderen Methoden (z. B. Extraktion oder Spalte Chromatographie), die effektiv bei der Beseitigung größerer Mengen von Verunreinigungen, aber, dass nicht die Reinheit der letzten Verbindung auf ein ausreichend hohes Niveau erhöhen.
Rekristallisation ist die einzige Technik, die absolut rein, perfekte Einkristalle einer Substanz produzieren kann. Diese Kristalle einsetzbar für Röntgenstrahlanalyse, die die höchste Autorität in der Bestimmung der Struktur und dreidimensionale Form eines Moleküls ist. In diesen Fällen darf die Rekristallisation sehr langsam im Laufe von Wochen bis Monaten, erlauben das Kristallgitter zu bilden, ohne die Aufnahme von Verunreinigungen umgesetzt. Spezielle Glaswaren wird benötigt, um das Lösungsmittel so langsam wie möglich während dieser Zeit verdunsten, oder das Lösungsmittel mit einem anderen Lösungsmittel sehr langsam mischen in dem die Verbindung unlöslich ist (so genannte antisolvent Zusatz) zu ermöglichen.
Die Pharmaindustrie macht intensiven Gebrauch von Rekristallisation, auch, da es ein Mittel der Reinigung mehr als Säulenchromatographie leicht skaliert ist. 3 die Bedeutung der Rekristallisation in industriellen Anwendungen hat ausgelöst, Erzieher um Rekristallisation im Labor Curriculum zu betonen. 4 zum Beispiel ist das Medikament Stavudin, die verwendet wird, zur Verringerung der Auswirkungen von HIV in der Regel durch Kristallisation isoliert. 5 oft Moleküle haben mehrere verschiedene Kristallstrukturen vorhanden, so ist es notwendig für die Forschung zu beurteilen und zu verstehen, unter welchen Bedingungen, wie Kühlung, Preis, solvent Zusammensetzung und So weiter die Kristallform isoliert ist. Diese verschiedenen Kristallformen möglicherweise unterschiedliche biologische Eigenschaften oder in den Körper unterschiedlich schnell aufgenommen werden.
Ein häufiger Einsatz von Rekristallisation ist bei der Herstellung von Kandiszucker. Kandiszucker erfolgt durch Auflösen von Zucker in heißem Wasser bis hin zur Sättigung. Holzstäbchen befinden sich in der Lösung und die Lösung darf abkühlen lassen und langsam verdunsten. Nach einigen Tagen sind große Kristalle des Zuckers überall auf die Holzstäbchen gewachsen.
References
- Mayo, D. W.; Pike, R. M.; Forbes, D. C., Microscale organic laboratory : with multistep and multiscale syntheses. 5th ed.; J. Wiley & Sons: Hoboken, NJ, p xxi, 681 p (2011).
- Armarego, W. L. F.; Chai, C. L. L., Purification of laboratory chemicals. 5th ed.; Butterworth-Heinemann: Amsterdam ; Boston; p xv, 609 p (2003).
- Ray, P. C.; Tummanapalli, J. M. C.; Gorantla, S. R., Process for the large scale production of Stavudine. Google Patents: (2011).
- Hightower, T. R.; Heeren, J. D., Using a Simulated Industrial Setting for the Development of an Improved Solvent System for the Recrystallization of Benzoic Acid: A Student-Centered Project. Journal of Chemical Education 83 (11), 1663 (2006).
- Rohani, S.; Horne, S.; Murthy, K., Control of Product Quality in Batch Crystallization of Pharmaceuticals and Fine Chemicals. Part 1: Design of the Crystallization Process and the Effect of Solvent. Organic Process Research & Development 9 (6), 858-872 (2005).




