Overview
Fonte: Kerry M. Dooley e Michael G. Benton, Dipartimento di Ingegneria Chimica, Louisiana State University, Baton Rouge, LA
L'elaborazione di sostanze biochimiche comporta operazioni unitarie come la cristallizzazione, l'ultracentrifugazione, la filtrazione a membrana e la cromatografia preparativa, che hanno tutte in comune la necessità di separare le molecole grandi da piccole o solide da liquide. Di questi, la cristallizzazione è la più importante dal punto di vista del tonnellaggio. Per questo motivo, è comunemente impiegato nelle industrie farmaceutiche, chimiche e di trasformazione alimentare. Importanti esempi biochimici includono separazioni chirali,1 purificazione di antibiotici,2 separazione di amminoacidi dai precursori,3 e molti altri prodotti farmaceutici,4-5 additivi alimentari,6-7 e purificazioni agrochimiche. 8 Il controllo della morfologia dei cristalli e della distribuzione dimensionale è fondamentale per l'economia di processo, in quanto questi fattori influenzano i costi delle operazioni di lavorazione a valle come l'essiccazione, la filtrazione e il trasporto dei solidi. Per ulteriori informazioni sulla cristallizzazione, consultare un libro di testo specializzato o un libro di testo Unit Operations. 9 anni
L'unità cristallizzante (Figura 1) consente di studiare: (a) gli effetti di parametri chiave, quali la sovrasaturazione e le velocità di raffreddamento/riscaldamento, sul contenuto di solidi, sulla morfologia e sulla distribuzione dimensionale dei cristalli; b) e il controllo in linea dei processi di cristallizzazione. La sovrasaturazione può essere controllata alterando condizioni come la velocità di agitazione e la temperatura. Le diverse classificazioni della cristallizzazione includono raffreddamento, evaporazione, oscillazione del pH e modifica chimica. In questo esperimento, un microscopio offline misurerà da cristalli di dimensioni variabili da 10-1000 μm, una gamma di dimensioni tipiche per i biologici.
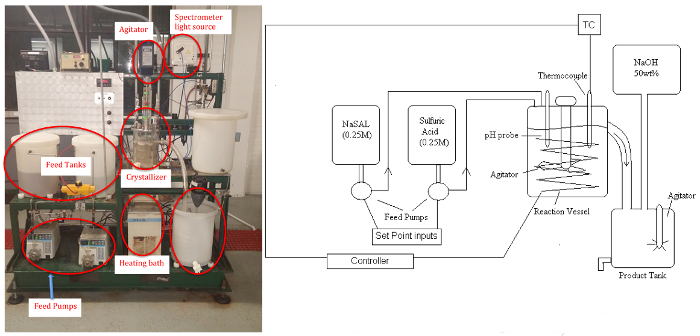
Figura 1: Schema P&ID (a sinistra) e immagine (a destra) di Crystallizer. Fare clic qui per visualizzare una versione più grande di questa figura.
Questo esperimento dimostrerà una "modificazione chimica", o cristallizzazione "pH-swing", per generare cristalli di acido salicilico (SAL) (precursore dell'aspirina) dalla reazione rapida di soluzioni acquose di salicilato di sodio basico (NaSAL), che sono basici, e acido solforico (H2SO4) ovunque da 40 - 80 ° C.11
Na+SAL + 0,5 H2SO4 SAL (ppt) + Na+ + 0,5 SO42-
Il sottoprodotto solfato di sodio rimane solubile. L'apparecchio è costituito da due serbatoi di alimentazione, tre pompe a velocità variabile (peristaltiche), il cristallizzatore (serbatoio agitato per approssimare temperatura e concentrazione uniformi, ~ 5 L), un bagno circolante per il controllo della temperatura, un regolatore di potenza, un serbatoio del prodotto e un serbatoio di trucco per la rigenerazione dell'alimentazione con soluzione NaOH (se lo si desidera). I campioni saranno analizzati da uno spettrometro UV-Vis per lo ione salicilato solubile residuo e il prodotto cristallino di acido salicilico sarà essiccato e pesato. Una sonda di pH può essere utilizzata per determinare lo stato stazionario quando le condizioni di reazione sono alterate.
Principles
Un cristallizzatore MSMPR (Mixed-Suspension, Mixed-Product-Removal) è analogo a un reattore a serbatoio agitato continuo - si presume una perfetta miscelazione di entrambe le fasi solida e liquida. I cristallizzatori industriali raramente (se non mai) si avvicinano al comportamento MSMPR, ma il concetto è utile nelle unità da banco e su scala pilota. Questo perché fornisce un modo semplice per stimare parametri chiave come il tasso di crescita, G e il tasso di nucleazione, B0. Sia i cristalli esistenti che altre superfici solide, come l'agitatore, catalizzano la nucleazione. La densità numerica, n, dei cristalli è una densità di probabilità rispetto a L, la dimensione primaria del cristallo. Pertanto, n dL/(Σn dL) rappresenta la frazione di cristalli dilunghezza da L a L+dL. Nei testi standard è dimostrato che per un cristallizzatore MSMPR, la soluzione del modello di bilancio generale della popolazione per n è:
 (1)
(1)
dove B0 è la funzione di cristallizzazione in mols/vol/time, e G è il tasso di crescita dei cristalli, dL/dt. L'equazione (1) prevede una distribuzione esponenziale per la densità numerica prodotta in un MSMPR. Usando lo zero (relativo alla concentrazione del cristallo) e il primo (relativo alla dimensione media del cristallo) momenti della distribuzione, B0 e G sono:
 (2)
(2) (3)
(3)
dove Cs è la concentrazione di cristalli solidi nel liquame, τ è il tempo di permanenza, che è approssimativamente il volume liquido diviso per la portata volumetrica di alimentazione, ed  è la lunghezza media su base numerica, che è determinata microscopicamente.
è la lunghezza media su base numerica, che è determinata microscopicamente.
Pertanto, per un cristallizzatore MSMPR, le velocità di crescita e nucleazione sono determinate dai normali parametri di controllo (velocità di agitazione, temperatura, portate, ecc.). Tuttavia, la distribuzione dovrebbe sempre essere esponenziale e qualsiasi deviazione da una distribuzione esponenziale rappresenta una miscelazione imperfetta dei solidi o del liquido. Il cristallizzatore MSMPR (stirred tank) è poco adatto alle cristallizzazioni industriali perché fornisce una distribuzione esponenziale delle dimensioni dei cristalli, mentre nella maggior parte delle applicazioni si desidera una distribuzione relativamente stretta, gaussiana, per uniformità del prodotto. Il suo studio è rilevante perché: (a) è quasi sempre un elemento di un disegno di cristallizzatore più grande; b) è ideale per lavori su scala di banco e di impianti pilota, in quanto il grado di sovrasaturazione e i tassi di crescita e di nucleazione possono essere facilmente estratti dai dati grezzi; e (c) è l'esempio più semplice per cui la geometria può essere collegata alla distribuzione delle dimensioni dei cristalli.
Per la temperatura costante e la velocità dell'agitatore, sia B0 che G sono direttamente correlati alla sovrasaturazione ΔC, che è la forza motrice di trasferimento di massa per la cristallizzazione:12
 (4)
(4)
Le potenze b e g sono specifiche del sistema e possono variare in un ampio intervallo (ad esempio, 1-7,2 per g). 12 anni
Subscription Required. Please recommend JoVE to your librarian.
Procedure
Le soluzioni organiche (salicilato di sodio, NaSAL) e acide (acido solforico, 0,25 M = 0,50 N) saranno alimentate al cristallizzatore. Assicurarsi di indossare guanti in lattice quando si maneggia NaSAL, acido salicilico o le loro soluzioni e acido solforico 0,25 M.
L'intero sistema è controllato da un PC utilizzando un controller distribuito commerciale con un'interfaccia simile a quella della Figura 1. Tutte le elettrovalvole on-off o a 3 vie e i set point del controller possono essere azionati e modificati utilizzando questa interfaccia. Uno schema mostra le tendenze dei valori analogici (portate, temperatura) associati all'unità.
1. Avvio del Crystallizer
All'inizio di una corsa, tutti i controller continui devono essere in modalità manuale e tutte le elettrovalvole devono essere chiuse (on-off) o in modalità di riciclo (a 3 vie).
- Assicurarsi che il cristallizzatore sia pieno fino al livello di troppo pieno, (~ 4,15 L) indicato sul serbatoio agitato, con acqua e liquame di acido salicilico (in cristallizzazione, il liquame è spesso chiamato "magma"). Se non sono pieni, aggiungili tramite la porta di aggiunta.
- Accendere l'agitatore per il cristallizzatore e iltermostato per il bagno e le pompe.
- Impostare il regolatore di temperatura per la temperatura del bagno su AUTO e il setpoint alla temperatura desiderata. La temperatura consigliata è di ~ 53 ° C per un cristallizzatore di 50 ° C.
- Impostare le velocità della pompa utilizzando l'interfaccia (ad esempio, 30% aperto). Conoscendo le concentrazioni delle alimentazioni, impostare le portate per l'equivalenza stechiometrica in base all'equazione (1).
- Verificare che il serbatoio del prodotto non sia pieno e che la valvola di scarico sia chiusa.
- Accendere l'apparecchiatura dello spettrometro e stabilire una comunicazione con un collegamento fornito nella console di controllo. Le procedure dello spettrometro sono dettagliate nel manuale operativo (SpectraSuite). Viene fornita la calibrazione dello spettrometro.
2. Funzionamento del Crystallizer
- Aumentare l'uscita della pompa secondo necessità per ottenere le portate desiderate. Per la soluzione acida, questo è ~ 25-35 ml / min. Per il NaSAL, è determinato dall'equivalenza stechiometrica.
- Passare alla modalità di alimentazione su entrambe le valvole a 3 vie. Questo è il tempo zero per un esperimento.
- Controllare periodicamente la linea di overflow. In determinate condizioni potrebbe bloccarsi. In tal caso, utilizzare un pezzo di tubo d'acciaio per risamare la linea che entra nel serbatoio del prodotto.
- Raccogliere cinque campioni direttamente dal cristallizzatore attraverso la porta del campione utilizzando una pipetta a bocca larga e trasferirli in provette da 15 mL o centrifughe. Prendi due serie di campioni a circa 10-15 minuti di distanza.
- Ripeti in altri due tempi di residenza ampiamente distanziati, controllando
 (tempo di residenza) variando le portate volumetriche, ma mantenendo l'equivalenza stechiometrica.
(tempo di residenza) variando le portate volumetriche, ma mantenendo l'equivalenza stechiometrica.
3. Spegnimento del cristallizzatore
- Per arrestare il sistema, impostare le valvole a 3 vie per il riciclo e le uscite della pompa allo 0 %.
- Riportare il regolatore di temperatura a MANUALE allo 0% di uscita e spegnere le pompe, gli agitatori e il bagno termostatato.
- Se si utilizza lo spettrofotometro, ricordarsi di spegnere le lampade.
4. Analisi
Le concentrazioni di NaSAL disciolto e acido salicilico possono essere misurate simultaneamente mediante spettroscopia UV/Vis. Le assorbanze del salicilato disciolto e dell'acido salicilico possono essere assunte additive perché si osserva lo stesso cromoforo. Ulteriori istruzioni sono incluse nell'Appendice A. La concentrazione di acido salicilico può anche essere determinata gravimetricamente in unità di kg/m3 di liquame.
- Centrifugare i tubi da 15 ml per 5 minuti e registrare il volume del campione liquido recuperato mediante decantazione. Il liquido travasato può essere utilizzato per l'analisi spettrofotometrica NaSAL.
- Asciugare le provette contenenti i solidi in posizione verticale nel forno a convezione a 70ºC, per due giorni.
- Pesare, pulire i tubi, quindi asciugare brevemente prima di ripapesare per ottenere il peso dei cristalli.
La cristallizzazione industriale viene applicata per la separazione e la purificazione di composti e miscele. Per progettare sistemi economici, è necessario studiare vari parametri. La cristallizzazione viene utilizzata per la separazione di composti chirali e amminoacidi o per la purificazione di antibiotici, additivi alimentari e composti agrochimici. Diversi mezzi di cristallizzazione includono raffreddamento, modifica chimica, evaporazione o oscillazione del pH. Un cristallizzatore può essere utilizzato per studiare i parametri chiave che influenzano lo sviluppo del cristallo, come il raffreddamento e le velocità o la sovrasaturazione. Con il microscopio, la dimensione e la morfologia del cristallo possono essere monitorate e le dipendenze di vari fattori osservati. In questo esperimento, il salicilato di sodio viene fatto reagire con l'acido solforico, portando alla precipitazione dell'acido salicilico, che è un precursore dell'aspirina. I campioni vengono analizzati mediante UV vis, un'analisi gravimetrica e microscopia. Questo video illustrerà il concetto, l'analisi e l'applicazione di un'unità cristallizzante.
Per uno scale-up di un cristallizzatore, è importante stimare i parametri chiave. Questi possono essere studiati utilizzando un'unità MSMPR. Sebbene i cristallizzatori industriali si comportino davvero come MSMPR, il concetto è ancora rilevante per le unità da banco e su scala pilota. Il cristallizzatore MSMPR è analogo a un reattore continuo con serbatoi agitati. Presuppone una perfetta miscelazione delle fasi solida e liquida. Gli MSMPR vengono utilizzati per valutare i parametri chiave di cristallizzazione, come il tasso di nucleazione del cristallo, noto anche come funzione di nascita e tasso di crescita del cristallo. La nucleazione è catalizzato da cristalli esistenti e superfici solide come le pareti del reattore. Il modello di bilancio generale della popolazione per un cristallizzatore MSMPR produce la densità numerica N dei cristalli, che è una densità di probabilità rispetto a L, la dimensione primaria del cristallo. In un MSMPR, si prevede che la distribuzione numerica sia una distribuzione esponenziale. La funzione di nascita e il tasso di crescita possono essere determinati utilizzando lo zero e i primi momenti di questa distribuzione. Ancora più importante, possono anche essere correlati alla sovrasaturazione, che è la forza motrice del trasferimento di massa nella cristallizzazione e che, a sua volta, dipende dalla velocità di agitazione e dalla temperatura. Per una temperatura costante e la velocità dell'agitatore, sia la funzione di nascita che il tasso di crescita sono direttamente correlati alla sovrasaturazione e le potenze B e G possono essere determinate dalla regressione lineare. Secondo il modello MSMPR, la densità numerica dei cristalli diminuisce esponenzialmente con la lunghezza. Una deviazione dalla distribuzione esponenziale implicherebbe una miscelazione imperfetta di solidi o liquidi. Nelle applicazioni industriali, sono necessarie distribuzioni gaussiane relativamente strette di dimensioni cristalline, piuttosto che esponenziali. Tuttavia, il modello MSMPR è ancora utile, in particolare negli impianti pilota, in quanto consente di determinare i tassi di crescita e natalità, nonché il grado di sovrasaturazione dai dati grezzi. Ora che hai familiarità con il modello MSMPR, applichiamo il concetto all'esperimento.
Indossare DPI adeguati quando si maneggiano soluzioni di salicilato di sodio e acido solforico. Annotare le proprietà fisiche di base dell'acido salicilico per un uso successivo. Prima di iniziare, familiarizzare con il sistema di cristallizzazione. L'apparecchio è costituito da due serbatoi di alimentazione, pompe a velocità variabile, un serbatoio agitato a cristallizzatore da cinque litri, un bagno circolante per il controllo della temperatura, un regolatore di potenza, un serbatoio del prodotto e un serbatoio di trucco per la rigenerazione dell'alimentazione, utilizzando una soluzione di idrossido di sodio. Il sistema viene azionato utilizzando un sistema di controllo distribuito e un'interfaccia grafica, da cui è possibile azionare valvole per controllare la temperatura e il flusso. È inoltre disponibile un output schematico che fornisce le tendenze della portata e della temperatura.
Verificare che tutti i controllori continui siano impostati sulla modalità manuale e che tutte le elettrovalvole siano chiuse, bidirezionali o in modalità di riciclo a tre vie. Assicurarsi che il cristallizzatore sia pieno d'acqua e un po 'di liquame di acido salicilico al livello di trabocco di circa 4,15 litri, come indicato sul serbatoio agitato. Aggiungere acqua e acido salicilico usando la porta di aggiunta se il serbatoio non è pieno. Accendere l'agitatore per il cristallizzatore e il bagno termostatato e le pompe. Impostare il regolatore di temperatura per la temperatura del bagno su auto e il set point alla temperatura desiderata, di solito circa 53 gradi Celsius per un cristallizzatore di 50 gradi Celsius. Impostare le velocità della pompa in modo da fornire circa 25-35 millilitri al minuto per la soluzione acida. Per il salicilato di sodio, la portata è determinata da equivalenti stechiometrici. Utilizzando le concentrazioni di alimentazione note, impostare le portate per gli equivalenti stechiometrici. Assicurarsi che il serbatoio del prodotto non sia pieno e che la valvola di scarico sia chiusa. Quindi, accendere lo spettrometro e utilizzare un collegamento fornito nella console di controllo per verificare che sia stabilita la comunicazione tra l'apparecchio.
Passare alla modalità di alimentazione su entrambe le valvole a tre vie. Questo imposta il tempo zero per un esperimento. Controllare periodicamente la linea di troppo pieno per eventuali blocchi. Utilizzare un pezzo di tubo d'acciaio per remoto la linea che entra nel serbatoio del prodotto utilizzando il foro fornito se viene rilevato un blocco. Dopo un'ora, utilizzare una pipetta a bocca larga e inserirla nella porta campione del cristallizzatore. Raccogliere un campione sufficiente per riempire un numero sufficiente di cinque centrifughe da 15 millilittere prepesate o provette. Prendere due serie di campioni da 10 a 15 minuti di distanza. Variare le portate volumetriche per controllare il TOW e regolare per altri due tempi di permanenza ampiamente distanziati. Mantenere gli equivalenti stechiometrici e raccogliere campioni come prima. Al termine, impostare l'uscita della pompa a zero per cento, le valvole a tre vie da riciclare. Riportare il regolatore di temperatura a manuale a zero per cento di uscita e spegnere le pompe, gli agitatori e il bagno termostatato.
La concentrazione di ioni salicilato può essere determinata utilizzando UV vis e la concentrazione di acido salicilico solido può essere determinata gravimetricamente come chilogrammi per metro di liquame cubettato. Prima dell'analisi, centrifugare prima i campioni per cinque minuti e decantare il liquido. Registrare il volume totale del campione recuperato. Combinare i campioni liquidi da un determinato set e diluire da 50 a 100 volte. Per il liquido, misurare l'assorbanza del salicilato di sodio e dell'acido salicilico utilizzando lo spettrometro UV vis. Si presume che l'assorbanza sia additiva, poiché lo stesso cromoforo viene rilevato per entrambi i campioni. Per la determinazione gravimetrica, utilizzare i solidi rimasti nella centrifuga o nelle provette. Asciugare i tubi in posizione verticale nel forno a convezione a 70 gradi Celsius per due giorni. Quindi ripesare le provette raffreddate per determinare il peso dei cristalli e la concentrazione in chilogrammi per litro. Infine, utilizzando un microscopio, determinare la distribuzione della lunghezza dei cristalli di acido salicilico a forma di ago.
Calcola la concentrazione di cristalli solidi per tutte le corse tramite il metodo gravimetrico. Generare un bilancio di massa su salicilato. Quindi, calcola la sovrasaturazione e il tempo di residenza. Quindi, determinare i rendimenti dei cristalli su una base di mangime e prodotto, utilizzando le moli del prodotto, del mangime e del prodotto salicilato disciolto. Usa la concentrazione del cristallo, la dimensione del cristallo e il tempo di residenza per risolvere la funzione di nascita e il tasso di crescita. Quindi stimare le potenze G e B attraverso regressioni lineari delle funzioni logaritiche. Ecco un esempio di cristallizzazione a 50 gradi Celsius. La potenza di B è due volte più grande di G, indicando che la sovrasaturazione sta influenzando il tasso di natalità più del tasso di crescita. Questi poteri verrebbero utilizzati per lo scale-up se la supersaturazione è invariata. I confronti con altri esperimenti possono identificare fattori che influenzano le funzioni di crescita e nascita, come la miscelazione inadeguata, il pH e le impurità ioniche nell'acqua di preparazione.
La cristallizzazione industriale è ampiamente applicata nelle industrie farmaceutiche, chimiche e alimentari per la separazione e la purificazione di vari composti. Danazolo è uno steroide sintetico che viene utilizzato per il trattamento dell'endometriosi. Come con molti altri composti farmaceutici, Danazol è idrofobo e scarsamente solubile in acqua. Pertanto, il prodotto danazolo grezzo viene inizialmente disciolto in etanolo e quindi ricristallizzato mescolandolo con un po 'd'acqua, che produce cristalli di prodotto puri e di piccole dimensioni particellari. I cristallizzatori industrializzati possono essere utilizzati nella produzione di lisosomi. L'apparecchio può essere progettato per produrre una distribuzione di dimensioni cristalline molto stretta attraverso l'applicazione di una pompa attorno allo scambiatore di calore, che aumenta leggermente la temperatura per dissolvere i cristalli più piccoli. La distribuzione dimensionale può essere regolata separando le particelle cristalline sulla base delle loro velocità terminali. Questo concetto trova applicazione anche nella cristallizzazione dei sali inorganici.
Hai appena visto l'introduzione di Jove alla cristallizzazione industriale. Ora dovresti capire il modello di cristallizzatore MSMPR, come utilizzare l'unità di cristallizzazione e come analizzare i risultati. Grazie per l'attenzione.
Subscription Required. Please recommend JoVE to your librarian.
Results
La Figura 2 presenta dati rappresentativi che suggeriscono deviazioni modeste dalla distribuzione dimensionale cristallina dell'ideale MSMPR anche a velocità relativamente elevate e basse concentrazioni di alimentazione.

Figura 2. Distribuzione cristallina per alimentazione NaSAL 0,16 M, 540 giri/min, 60 °C
I cristalli che si formano da questo esperimento sono tipicamente a forma di ago e la distribuzione della lunghezza può essere determinata al microscopio. Le lunghezze dei campioni con dimensioni (in micron) dei cristalli tipici sono mostrate nella Figura 3. La gamma normale e preferita di cristalli è 100-1000 micron.

Figura 3. Cristalli di acido salicilico ingranditi. Le dimensioni sono in micron. Fare clic qui per visualizzare una versione più grande di questa figura.
Assumendo le equazioni del cristallizzatore MSMPR (1-4), e usando un bilancio di massa su salicilato, viene eseguita la concentrazione di cristalli solidi nel magma (CSAL),i tempi di permanenza (τ), le funzioni del tasso di crescita G, le quantità di sovrasaturazione nella fase acquosa ΔC su base molare, la funzione di nucleazione B0e le rese dei cristalli sia su un prodotto che su una base di alimentazione sono state determinate. La funzione G è stata calcolata dall'equazione (3) usando la distribuzione dimensionale. E le equazioni di sovrasaturazione e bilancio di massa sono:
 (5)
(5)
 (6)
(6)
dove Q1 è la portata volumetrica della soluzione naSAL, Qt è la portata volumetrica totale, (CNaSAL)0 è la concentrazione di alimentazione di NaSAL in Q1e CNaSAL e CSAL sono le concentrazioni di prodotto di salicilato solubile e cristalli, rispettivamente. Ceq è la concentrazione di equilibrio (interfacciale) di salicilato, che era ~ 2,2 g / L nell'intervallo di temperatura utilizzato in questa dimostrazione.
La resa è stata definita su base feed come:
 (7)
(7)
E su base di solo prodotto come:
 (8)
(8)
Se l'errore % nel bilancio di massa sul salicilato è grande, è probabile che CSAL o CNaSAL siano in errore, poiché entrambi sono difficili da misurare con precisione. Osservando i valori di Y1 e Y2 (a cui si ottiene una tendenza più ragionevole), è possibile determinare la fonte primaria dell'errore.
Dai valori per G e B0, le potenze "g" e "b" nell'equazione (4) sono state stimate usando la regressione lineare. Franck et al. riportano una potenza "g" di ~ 3 e "b" di ~ 6 per questo sistema11 utilizzando condizioni altamente sterili e alte velocità dell'agitatore. Determinare le differenze tra le potenze sperimentali "g" e "b" e quelle di Franck et al. è utile per identificare i fattori che potrebbero influenzare le funzioni di crescita e nucleazione. I dati rappresentativi per una cristallizzazione a 50°C con concentrazioni di alimentazione di 0,35 M (NaSAL) e 0,25 M (H2SO4) sono riportati nella Tabella 1.
Tabella 1. Dati di cristallizzazione
| Portata, mL/min | τ |  |
CNaSAL | CSAL | Y1 | Y2 | |
| Nasale | H2SO4 | Min | millimetro | mol/L | g/mL | % | % |
| 119 | 59.5 | 23.3 | 700 | 0.063 | 0.022 | 69 | 72 |
| 85 | 42.5 | 32.6 | 876 | 0.059 | 0.026 | 81 | 76 |
| 51 | 25.5 | 54.3 | 1190 | 0.055 | 0.026 | 81 | 77 |
Questi dati sono stati utilizzati anche per risolvere per G e B0 e la regressione lineare è stata eseguita per determinare le potenze "g" e "b" usando l'equazione linearizzata (4). La regressione lineare delle funzioni di log (un esempio è mostrato in Figura 4) ha dato g = 1.1 e b = 2.4. Mentre la tendenza delle potenze (b circa due volte più grande di g) era la stessa osservata in Franck et al., le potenze stesse differivano significativamente e le dipendenze dalla sovrasaturazione ΔC erano molto più piccole. Ciò suggerisce che fattori diversi dal ΔC potrebbero influenzare i tassi di crescita e di nucleazione, come la miscelazione inadeguata, il pH relativamente elevato (per i mangimi equimolari i pH sono compresi tra 2,2-2,4) e le impurità ioniche introdotte nell'acqua (la fornitura municipale). Queste potenze sperimentali sarebbero utilizzate in qualsiasi calcolo di scale-up, perché oltre a ΔC, questi fattori sarebbero presumibilmente presenti sia nella scala pilota che nei progetti industriali.

Figura 4. Regressione lineare del tasso di crescita G in funzione della sovrasaturazione ΔC
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Questo esperimento ha dimostrato come effettuare misurazioni grezze di concentrazione, flusso e temperatura e utilizzare la teoria MSMPR per stimare i parametri chiave necessari per progettare un sistema di cristallizzatori grande e complesso. È stato esplorato il ruolo critico che il tempo di permanenza gioca nell'ottenere alte rese di cristallo e nel controllare la dimensione media dei cristalli. Spesso c'è un tempo di residenza ottimale perché raramente sono desiderabili cristalli molto grandi. Lo stesso vale per la miscelazione: la miscelazione deve essere sufficiente per impedire ai cristalli solidi di depositarsi sul fondo, ma allo stesso tempo la velocità dell'agitatore è spesso un costo operativo significativo.
Alcuni dei problemi spesso riscontrati con questa unità - blocchi parziali dovuti all'agglomerazione delle particelle, difficoltà nell'ottenere una sovrasaturazione uniforme a causa di una miscelazione imperfetta e tempi lunghi per raggiungere lo stato stazionario - sono comuni anche ai cristallizzatori industriali ben progettati. Questo è il motivo per cui i progetti di cristallizzatori visti nella letteratura dei produttori sono spesso incredibilmente complessi.
Questo processo è simile alle cristallizzazioni di altri biologici, come L-ornitina-L-aspartato, che viene usato per trattare l'insufficienza epatica cronica. 5 Il precursore L-ornitina cloridrato costa > $ 300 / kg ed è difficile da riciclare, quindi la progettazione per alte rese di cristalli è fondamentale. Un esempio di cristallizzazione biologica antisolvente, al contrario dell'oscillazione del pH, è il raffinamento del danazolo, uno steroide sintetico usato per trattare l'endometriosi. 13 Molti farmaci sono idrofobici con scarsa solubilità in acqua. Sciogliendo il prodotto grezzo di danazolo in etanolo e quindi cristallizzandolo mescolando con acqua, si può ottenere un prodotto cristallino di granulometria più puro e più piccolo. La cristallizzazione delle proteine è un'altra importante applicazione, un esempio è la produzione di lisozima. 14
I cristallizzatori industriali possono essere progettati per produrre distribuzioni dimensionali dei cristalli molto strette attraverso l'applicazione di rimozione fine (ad esempio, uno scambiatore di calore a pompa che aumenta leggermente la temperatura per dissolvere i cristalli più piccoli) e classificazione dimensionale (ad esempio, una "gamba di elutriazione" che separa le particelle sulla base delle loro velocità terminali, raccogliendo solo le più grandi della popolazione). Questi concetti di progettazione sono stati sviluppati per la cristallizzazione del sale inorganico, ma ora si stanno spostando nel regno biologico.
Elenco dei materiali
| Nome | Società | Numero di catalogo | Commenti |
| Agitatore, 150 W | Caframo · | BDC 3030 | sul reattore |
| Riscaldatore circolante | Neslab · | RTE 110 | 0-100°C, per reattore |
| Pompe peristaltiche (2) | Cole-Parmer · | Masterflex L/S 7550-60, 1.6-100 giri/min, 0.1 CV | Per entrambi i mangimi NaSAL e H2SO4 |
| Pompa centrifuga | Cole-Parmer · | 7553-00, 6-600 giri/min | Per il riciclo dei prodotti |
| Spettrofotometro UV-Vis | Ottica oceanica | USB 2000 | Per l'analisi solubile di NaSAL |
| Alimentatore UV-Vis | Ottica oceanica | DT1000 CE | Per l'utilizzo con USB 2000 |
APPENDICE A – UTILIZZO DELLO SPETTROMETRO
- Aprire il software SpectraSuite. Accendere entrambe le lampade UV e VIS sulla sorgente. Assicurarsi di spegnere le lampade dopo l'uso. Impostare la modalità di acquisizione su Ambito (pulsante S blu sulla barra degli strumenti).
- Sulla barra degli strumenti modificare il tempo di integrazione a 250 ms, le scansioni a media a 25e la larghezza Boxcar a 2. Seleziona le caselle per Attivazione strobo/lampada, Correzione oscura elettricae Correzione luce vagante.
- Preparare i file Dark Spectrum e Reference Spectrum. Lo spettrometro richiede la generazione di un file Dark Spectrum e di un file Reference Spectrum.
- Immergere la sonda in una provetta riempita con acqua DI.
- Per creare un file Dark Spectrum, scollegare la sonda dalla sorgente luminosa (scatola bianca). Il grafico dovrebbe quasi tracciare l'asse x. Per salvare il tuo Dark Spectrumappena creato, fai clic sulla lampadina grigia, quindi su File -> Store -> Store Dark Spectrum.
- Per creare un file dello spettro di riferimento, ricollegare la connessione della sonda alla sorgente luminosa. Alcuni picchi dovrebbero apparire sul grafico in SpectraSuite. Per salvare questo spettro di riferimento,fare clic sulla lampadina gialla, quindi su File -> Store -> Store Reference Spectrum.
- Se VENGONO modificate TUTTE le impostazioni (ad esempio, tempo di integrazione, ecc.), Sia lo spettro oscuro che lo spettro di riferimento devono essere generati di nuovo.
- Passare dalla modalità Scope alla modalità Absorbance (A). Per le soluzioni NaSAL, l'assorbanza deve essere osservata a ~ 300 - 330 nm.
La quantificazione è possibile solo se le soluzioni di Acido NaSAL/salicilico seguono la legge di Beer-Lambert (A è nella "regione lineare"). Per lo ione salicilato, questa regione è A < ~ 0,9 - 1. Dati i risultati passati, questo criterio suggerisce che le soluzioni di NaSAL DEVONO essere diluite (con acqua DI) a 0,05 g/ L o meno per la quantificazione. Quindi, le soluzioni sconosciute possono essere quantificate confrontando l'assorbanza di una soluzione standard opportunamente diluita:

dove C è concentrazione, A assorbanza, "u" un'incognita e "s" una soluzione standard di NaSAL. Si noti che SIA "u" che "s" devono mostrare assorbanza all'interno dell'intervallo lineare.
In spettroscopia, l'assorbanza dipende da due fattori, il tipo di sostanza chimica e la sua concentrazione, e la lunghezza del percorso nel fluido. Modificare la concentrazione per diluizione.
Subscription Required. Please recommend JoVE to your librarian.
References
- C. Wibowo, L. O’Young and K.M. Ng, Chem. Eng. Prog., Jan. 2004, pp. 30-39.
- W.J. Genck, Chem. Eng. Prog., Oct. 2004, pp. 26-32.
- S. Takamatsu and D.D.Y. Ryu, Biotechnol. Bioeng., 32, 184-191 (1988).
- F. Wang and K.A. Berglund, Ind. Eng. Chem. Res., 39, 2101-2104 (2000).
- Y. Kim, S. Haam, Y.G. Shul, W.-S. Kim, J.K. Jung, H.-C. Eun and K.-K. Koo, Ind. Eng. Chem. Res., 42, 883-889 (2003).
- K. Hussain, G. Thorsen and D. Malthe-Sorenssen, Chem. Eng. Sci., 56, 2295-2304 (2001).
- H. Gron, A. Borissova and K.J. Roberts, Ind. Eng. Chem. Res., 42, 198-206 (2003).
- F. Lewiner, G. Fevotte, J.P. Klein and F. Puel, Ind. Eng. Chem. Res., 41, 1321-1328 (2002).
- For example: W.L. McCabe, J.C. Smith, and P. Harriott, “Unit Operations of Chemical Engineering”, 7th Ed., McGraw-Hill, New York, 2005, Ch. 27, or C.J. Geankoplis, “Transport Processes and Unit Operations”, 3rd Ed., 1993, Ch. 12.
- P. Barrett, Chem. Eng. Prog., Aug. 2003, pp. 26-32.
- R. Franck, R. David, J. Villermaux and J.P. Klein, Chem. Eng. Sci., 43, 69-77 (1988).
- J. Garside, Chem. Eng. Sci., 40, 3-26 (1985).
- H. Zhao, J.-X. Wang, Qi-An Wang, J.-F. Chen and J. Yun, Ind. Eng. Chem. Res. 46, 8229-8235 (2007).
- J.S. Kwon, M. Nayhouse, G. Orkoulas and P.D. Christofides, Ind. Eng. Chem. Res., 53, 15538-15548 (2014).





 (tempo di residenza) variando le portate volumetriche, ma mantenendo l'equivalenza stechiometrica.
(tempo di residenza) variando le portate volumetriche, ma mantenendo l'equivalenza stechiometrica.