Overview
מקור: פרצ'טתיבו 1,2,3, מונירסילבן 1,2,3, סופי נובאלט4, רחל גולוב1,2,3
יחידה אחת ללימפופוליס, המחלקה לאימונולוגיה, מכון פסטר, פריז, צרפת
2 INSERM U1223, פריז, צרפת
3 100é Paris Diderot, סורבון פריז סיטה, צ'רול פסטר, פריז, צרפת
4 פלטפרום ציטומטריה זרימה, ציטומטריה וסמנים ביולוגיים UtechS, המרכז למדע תרגום, מכון פסטר, פריז, צרפת
הפונקציה הכללית של המערכת החיסונית היא להגן על הגוף מפני אורגניזמים זיהומיים ופולשים אחרים. תאי דם לבנים, או לויקוציטים, הם שחקני המפתח של מערכת החיסון. לאחר זיהום, הם מופעלים וליזום תגובה חיסונית. ניתן לחלק לויקוציטים לתת-אוכלוסיות שונות (למשל, תאים מיאלואידיים, לימפוציטים, תאים דנדריטיים) בהתבסס על פרמטרים שונים שיכולים להיות ביולוגיים, פיזיים ו/או פונקציונליים (למשל, גודל, פירוט והפרשה). דרך אחת לאפיין לויקוציטים היא באמצעות חלבוני השטח שלהם, שהם בעיקר קולטנים. כל אוכלוסיית לויקוציטים מבטאת שילוב מסוים של קולטנים (למשל, ציטוטוקסיים, הפעלה, קולטני הגירה) שיכולים להגדיר תת-קבוצות בקרב אוכלוסיות. מכיוון שמערכת החיסון מקיפה מגוון רחב של אוכלוסיות תאים, חיוני לאפיין אותן כדי לפענח את השתתפותן בתגובה החיסונית.
ציטומטריית זרימה (FC או FCM) היא שיטה נפוצה לניתוח הביטוי של פני השטח של התא ומולקולות תאיות, אפיון והגדרת סוגי תאים שונים בתערובת תאים הטרוגניים. ציטומטרי זרימה מורכבים משלוש תתי-מערכות עיקריות: נוזלים, אופטיקה ואלקטרוניקה. מערכת הנוזלים מעבירה את התאים בזרם כך שהם עוברים מול לייזר בזה אחר זה. מערכת האופטיקה מורכבת ממקורות אור (לייזרים) להארת החלקיקים, מסננים אופטיים לכוון את האור המתקבל, ואותות פלואורסצנטיים לגלאים מתאימים. לבסוף, מערכת האלקטרוניקה ממירה את אותות האור שזוהו לאותות אלקטרוניים שניתן לעבד על ידי המחשב. כאשר תא בודד עובר מול קרן הלייזר, הוא מפזר אור. גלאי מול הקרן מודד פיזור קדימה (FS) ומספר גלאים לצד למדוד פיזור צד (SC). ה- FS מתואם עם גודל התא ו- SC הוא פרופורציונלי לפרטיון התאים. באופן זה, אוכלוסיות תאים לעתים קרובות ניתן להבחין בהתבסס על הבדלים בגודלם ובגרגריותם בלבד.
בנוסף לניתוח גודלו, צורתו ומורכבותו של התא, ציטומטריית הזרימה נמצאת בשימוש נרחב לזיהוי הביטוי של קולטני פני התא (1). זה מושג באמצעות נוגדנים חד שבטיים בעלי תווית פלואורוכרום אשר נקשרים לקולטנים ידועים ספציפיים לתא. עם עירור, פלואורוכרום קשור זה פולט אור של אורך גל מסוים, הנקרא אורך גל פליטה, אשר ניתן לזהות ולהבקיע. מדידות פלואורסצנטיות מספקות נתונים כמותיים ואיכותיים על קולטני פני תא המסומנים בפלואורוכרום. המטולוגים היו הראשונים להשתמש FC למעקב טיפולי של אוכלוסיות תאי החיסון (2). עכשיו, הוא משמש עבור מגוון רחב של יישומים כגון אימונופנוטיפינג, כדאיות תאים, ביטוי גנים, ספירת תאים, וניתוח GFP.
FACS (פלואורסצנטי מופעל Cell Sorter) הוא סוג מיוחד של ציטומטריית זרימה, אשר ממיין אוכלוסייה של תאים לתוך תת-אוכלוסייה באמצעות תיוג פלואורסצנטי. בדיוק כמו ציטומטריית זרימה קונבנציונלית, נתונים ראשונים FS, SC, פלואורסצנטי נאספים. לאחר מכן, המכונה מחילה מטען (שלילי או חיובי) ומערכת הסטה אלקטרוסטטית (אלקטרומגנטים) מקלה על איסוף טיפות טעונות המכילות תאים לצינורות מתאימים.
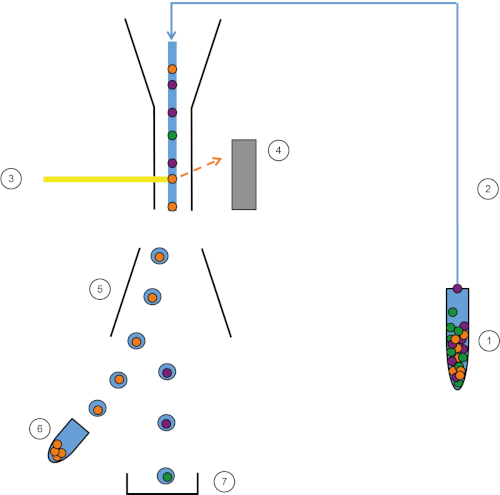
איור 1: ייצוג סכמטי של FACS. מדגם (1) שאפתן ב- FACS (2) ומועבר מול הלייזר (3). פלואורסצנטיות של תאים חשה בגלאי פלואורסצנטיות (4). לבסוף, התאים משולבים בטיפות ותאי העניין נוטים על ידי לוחות הסטה (5) ונאספים בצינור איסוף (6). התאים הנותרים נכנסים לפח (7). אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
היבט המיון של ה- FACS מציג יתרונות רבים. בדיקות רבות יכולות לעזור להבין את תפקידם של תאים ספציפיים במערכת החיסון, כגון ניתוחים של ביטוי גנים כמו RT-qPCR, מחזור תאים או הפרשת ציטוקינים. עם זאת, יש לטהר תאים במעלה הזרם כדי לקבל תוצאות ברורות וספציפיות. כאן, FACS מגיע שימושי ואת התאים הרצויים ניתן למיין עם טוהר גדול, מניב תוצאות אמינות מאוד לשחזור. FACS יכול לשמש גם כדי למיין תאים המבוססים על כתמים תאיים גרעיניים או אחרים ועל פי נוכחות, היעדר, וצפיפות של קולטני פני השטח. FACS היא כעת טכניקה סטנדרטית לטיהור של תת-אוכלוסיות של תאים ויש לה את היכולת למיין עד ארבע אוכלוסיות בו זמנית.
תרגיל מעבדה זה מדגים כיצד לבודד לויקוציטים בטחול ולאחר מכן כיצד למיין באופן ספציפי תאי לימפה B מתערובת תאי לויקוציטים בטחול באמצעות FACS.
Procedure
1. הכנה
- לפני שתתחילו, לבשו כפפות מעבדה וביגוד מגן מתאים.
- לחטא את כל כלי הניתוח, תחילה עם חומר ניקוי ולאחר מכן עם 70% אתנול ולאחר מכן יבש ביסודיות.
- הכן 50 מ"ל מתמיסת המלח המאוזנת של האנק (HBSS) המכילה סרום עגל עוברי 2% (FCS).
2. ניתוח
- באמצעות מערכת אספקת פחמן דו חמצני, להרדים את העכבר על ידי היפוקסיה. אבטחו את העכבר המתת חסד על צלחת ניתוח בתנוחת העפרוניזציה ובצעו לפרוסטומיה אורך באמצעות מספריים ומלקחיים.
- באמצעות מלקחיים, להזיז את המעיים ואת הבטן בצד ימין של הבטן כדי לחשוף את הבטן ואת הטחול. הטחול מחובר לקיבה.
- באמצעות מלקחיים, לנתק בזהירות את הטחול מהבטן ומניחים אותו בצלחת פטרי המכילה 5 מ"ל של HBSS 2% FCS.
3. בידוד תאי מערכת החיסון
- מניחים את הטחול במסננת תא 40μm מעל אותה צלחת פטרי. למחוץ את הטחול עם בוכנה כדי לנתק אותו באותה מנה.
- מעבירים את הטחול המנותק ואת הנוזל לצינור צנטריפוגה 15 מ"ל.
- צנטריפוגות הצינור ב 370 x g במשך 7 דקות ב 10 מעלות צלזיוס ולהשליך את supernatant, הימנעות הכדור.
- resuspend הכדור ב 2mL של אשלגן אצטט ליזה אריתרוציטים. המתן 2 דקות ולאחר מכן האיפור את עוצמת הקול עד 15 מ"ל באמצעות HBSS 2% FCS.
- צנטריפוגות הצינור שוב ב 370 x גרם במשך 7 דקות ב 10 מעלות צלזיוס. להשליך את supernatant ו resuspend הכדור ב 5mL של HBSS 2% FCS.
- ספירת התאים באמצעות בדיקות כתמים כחולות טריפן ולהתאים את ריכוז התא הסופי ל 107 תאים / מ"ל באמצעות נפח מתאים של HBSS 2% FCS.
4. כתמי תאים
- העבר 200μL של השעיית התא לתוך שישה צינורות FACS, שכותרתו 1 עד 6.
- צנטריפוגות הצינורות ב 370 x גרם במשך 7 דקות ב 10 מעלות צלזיוס ולהשליך את supernatant הימנעות הכדור.
- לאחר מכן, להכין שישה תערובות נוגדנים חדשניים על ידי הוספת כמות מתאימה של נוגדן 200μL HBSS 2% FCS על פי טבלה 1.
- לאחר מכן, העבר תערובות נוגדנים אלה לצינורות FACS ממוספרים המתאימים.
- לדגור על התליות התא מעורבב עם הנוגדנים במשך 20 דקות על קרח בחושך.
- הוסף 1mL של HBSS 2% FCS לכל צינור ולאחר מכן צנטריפוגה שוב ב 370 x g במשך 3 דקות ב 10 °C.
- להשליך את supernatant ו resuspend הכדור ב 200μL של HBSS 2% FCS.
- העבר את הכדורים המחודשים לצינורות FACS חדשים.

טבלה 1: קומפוזיציה לערבב נוגדנים. שישה תערובות של 200μL של נוגדן HBSS + הוכנו לניסוי. Mix 1 מיועד להגדרת PMT, ערבובים 2 עד 5 מיועדים להגדרות פיצוי, ומיקס 6 מיועד למיון תאים.
5. כיול FACS
- ראשית, הפעל את הממיין ובצע את"הפעלה Fluidics."
- הפעל את הנחל ולאחר מכן לחכות 15 דקות עבור הזרם להתייצב.
- התאם את המשרעת של הזרם כדי לקבל היווצרות טיפה מנותקת. לאחר מכן לחץ על "הנקודה המתוקה" כדי להשלים את התאמת המשרעת.
- שים את מסנן הצפיפות הניטרלית (N.D. ) - 1.0 ופתח את ממשק "CST" אשר מייצג התקנה ומעקב cytometer.
- כדי לבצע בקרת איכות יומית, תחילה לדלל את חרוזי CST עם בינוני FACS בעקבות הוראות היצרן ולאחר מכן, בצע את פקד CST.
- לאחר השלמת בקרת CST, החלף את מסנן N.D. 1.0 במסנן N.D. 2.0 בציטומטר.
- לאחר מכן, לדלל חרוזי השהיית טיפה במדיום FACS בהתאם להוראות היצרן ולאחר מכן לטעון לתוך FACS.
- כדי להבטיח ביצוע מיון נכון -
- תחילה לחץ על "מתח" ולאחר מכן על "מסנן אופטי". הרביע הימני צריך להיות שווה ל-100%. במידת הצורך, להתאים את בורג הלייזר האדום על cytometer שמאל או ימין כדי להשיג 100% ברביע הימני.
- לאחר מכן, בצע מיון בדיקה כדי להבטיח שהזרם נופל לתוך צינור האיסוף. כדי לעשות זאת, לחץ על "מגירת פסולת" ולהתחיל "מיון מבחן". תבדוק שזרמים צדדיים נופלים לצינורות איסוף. אם הם לא, להתאים מתח עד שהם עושים.
- נווט אל תבנית הניסוי. לאחר מכן, פתח את הניסוי "עיכוב שחרור אקרופרופ" ולחץ על "פריסת מיון".
- שנה את קצב הזרימה כדי להשיג 1000 עד 3000 אירועים לשניה.
- לחץ על "מתח" ולאחר מכן על "מסנן אופטי". הרביע השמאלי צריך להיות שווה ל-0 ורביע ימין ל-100.
- בחלון "פריסת מיון" לחץ על "מיון" ולאחר מכן לחץ על "ביטול". הרביע השמאלי צריך להיות שווה ל-100 ורביע ימין ל-0. אם הרביע השמאלי קטן מ- 95 לחץ על "השהיה אוטומטית" כדי להתאים אותו באופן אוטומטי.
6. ציטומטריה של זרימה ובקרת טוהר
- התחל ציטומטריית זרימה על ידי התחלה עם הצינור 1 (תאים לא מזוהמים) כדי להגדיר את מורפולוגיה התא ואת הפסגות השליליות של פלואורכרום. הגדר את הפיזור קדימה ואת הצד ולהגדיר את המתחים של כל פרמטר פלואורסצנטי. מקם את האוכלוסייה השלילית בעשור הראשון באמצעות הרשתות בכל חלקת נקודות.
- לאחר מכן, עומס צינור 2 (בקרת צבע יחיד) בציטומטר. התאם את החפיפה הספקטרלית עד חציוני האוכלוסייה השליליים והחיוביים מיושרים או משתמשים בתוכנת החישוב האוטומטית. חשוב לשמור על האות בקנה מידה. בקרות פיצוי חייבות להתאים להגדרות הפלורוכרום והגלאים הניסיוניים. להקליט 10,000 אירועים.
- חזור על שלבים אלה באמצעות צינור 3, 4 ו- 5 (פקדי צבע בודדים אחרים).
- לאחר מכן, עומס צינור 6 (תאים מוכתמים) ולהגדיר אוכלוסיות תאים של עניין באמצעות אסטרטגיית gating ספציפית.
- בחלון פריסת מיון, בחר את אוכלוסיית התאים בעלי עניין. בחר את סף התא ב "אירועי יעד" ואת רמת הדיוק ב "דיוק". כאן רק אוכלוסייה אחת ממוינת, עם זאת, ניתן למיין ארבע אוכלוסיות שונות בו זמנית.
- לאחר שתוכן לחץ על "מיין" ועל "אישור", ולאחר מכן המתן למיון תאים.
- לאחר השלמת מיון התאים, בצע בקרת טוהר על ידי צנרת ראשונה של 10μL של תאים ממוינים לתוך צינור FACS חדש עם 90 microliters של HBSS 2% FCS.
- לאחר מכן, לטעון את הצינור cytometer. להקליט ולנתח את הפנוטיפים של התאים כדי לוודא כי אסטרטגיית gating עבד כמתוכנן.
7. ניתוח נתונים
- פתח את תוכנת 'FlowJo' וגרור את הקבצים עבור כל צינור בחלון "כל הדוגמה".
- לחץ פעמיים על קובץ כדי לפתוח אותו בחלון חדש.
- לחץ על "מצולע" ושחזור אסטרטגיית הגטינג ששימשה בעבר.
- חזור על השלבים עם כל הקבצים האחרים.
- כדי להמחיש את התוויות הנקודות, לחץ על "עורך הפריסה" וגרור את האוכלוסיות העניין מצינור 6 ובקרת טוהר בכרטיסיה עורך הפריסה. התאים אמורים להופיע רק באוכלוסיית העניין בבקרת טוהר (ראו איור 2).
- כדי לבדוק את הטוהר של לימפוציטים B בתאים ממוינים, לחץ על "עורך השולחן". גרור אוכלוסיית לימפוציטים B מצינור 6 ובקרת טוהר בטבלה.
- בתפריט "סטטיסטיקה" בחר את התדירות של CD45+ תאים כדי לבדוק את הטוהר של אוכלוסיית תאים זו ולאחר מכן לחץ על "צור טבלה".
- ערכי פרמטר מופיעים בטבלה חדשה. בחלון בקרת טוהר, בדוק את התדירות של לימפוציטים B בתוך CD45+ תאים, אשר צריך להיות גבוה מ 98% (ראה איור 2, הלוח התחתון).
המערכת החיסונית מגנה על הגוף מפני פלישת פתוגנים על ידי יצירת לויקוציטים, הנקראים גם תאי דם לבנים. כאשר פתוגן מדביק בהצלחה אורגניזם, מגוון רחב של לויקוציטים מופעלים ותגובה מתואמת זו נקראת תגובה חיסונית.
לעתים קרובות, זה שימושי עבור חוקרים כדי להיות מסוגל לזהות את הסוג הספציפי ואת מספר תאי החיסון שהופעלו בתגובה פתוגן. ציטומטריית זרימה היא טכניקה המאפשרת לחוקרים להפריד תאים בהתבסס על אפיטופים ספציפיים המובעים על פני השטח שלהם. זה מושג באמצעות נוגדנים חד שבטיים מתויגים פלואורוכרום אשר נקשרים לאפיטופים ספציפיים לתאי החיסון הידועים, ועם עירור, פלואורכרום קשור אלה פולטים אורך גל של אור אשר ניתן לזהות ולהבקיע על ידי ציטומטר זרימה.
ציטומטרי זרימה מורכבים משלוש מערכות. המערכת הנוזלית מעבירה תאים בזרם כך שהם עוברים מול לייזר אחד אחד. המערכת האופטית מורכבת מלחיצים וגלאים המזהים את נוכחותם או היעדרם של הפלורופורים. לבסוף, המערכת האלקטרונית ממירה את הנתונים האופטיים שנאספו לקבצים אלקטרוניים לניתוח.
הרחבה של ציטומטריית הזרימה היא מסדר התאים המופעל על-ידי פלואורסצנטיות, או FACS, המאפשר העשרה של אוכלוסיות תאים ספציפיות כדי שניתן יהיה ללמוד בהן באופן עצמאי. מיון תאים מתבצע באמצעות זרבובית רוטטת בתוך זרם הנוזלים היוצר טיפות מיקרו, שכל אחת מהן מכילה תא בודד. לאחר מכן, גלאי קובע אם אור פלואורסצנטי נפלט מכל טיפה, ובהתבסס על מידע זה, אלקטרומגנט מעניק לכל תא מטען שלילי או חיובי. לאחר מכן, שדה חשמלי חזק ממיין את הטיפות הטעונות באופן שונה למכולות נפרדות. בסופו של דבר, אחד המכולות יכיל אוכלוסייה הומוגנית של תאים המבוססת על ביטוי של מולקולת פני תא ספציפית.
בסרטון זה, תלמד כיצד להשתמש בציטומטריית זרימה כדי לבודד לויקוציטים מרקמת טחול העכבר ו- FACS כדי לבחור עבור לימפוציטים B.
ראשית, לבשו כפפות מעבדה וביגוד מגן מתאים. לאחר מכן, לשטוף זוג מספריים לנתח מלקחיים תחילה עם חומר ניקוי ולאחר מכן עם 70% אתנול ולאחר מכן לייבש אותם עם מגבת נייר נקי.
לאחר מכן, להוסיף 49 מיליליטר של תמיסת מלח מאוזנת של האנק, או HBSS, לצינור 50 מיליליטר. הוסף מיליליטר אחד של סרום עגל עוברי, או FCS, כדי ליצור פתרון HBSS 2% FCS ולערבב על ידי צנרת בעדינות למעלה ולמטה בערך 10 פעמים.
לאחר מכן, הנח עכבר מורדם בתנוחת העגמום על צלחת ניתוח. עם המספריים והמלקחיים, בצע לפרוסטומיה אורך כדי לגשת לחלל הבטן. השתמש במלקחיים כדי להזיז את המעיים בצד ימין של הבטן לצד אחד כדי לחשוף את הבטן ואת הטחול. הטחול מחובר לקיבה. לאחר מכן, עם פיפטה, מניחים חמישה מיליליטר של HBSS 2% FCS לתוך צלחת פטרי. בעזרת מלקחיים, מנתקים בזהירות את הטחול מהבטן ומניחים את הטחול לתוך צלחת הפטרי.
כדי לבודד את תאי החיסון, מניחים תחילה את הטחול על מסננת תאים של 40 מיקרון בצלחת פטרי. מרסקים את הטחול עם בוכנה כדי לנתק אותו לצלחת. לאחר מכן, pipette הטחול מנותק ונוזל מצלחת פטרי לתוך צינור צנטריפוגה 15 מיליליטר. צנטריפוגות הצינור ב 370 פעמים g במשך שבע דקות ב 10 מעלות צלזיוס ולאחר מכן לאחזר את הצינור בזהירות כדי לא להפריע לכדור.
עכשיו, להסיר את supernatant, הימנעות הכדור, ולהשליך את הנוזל במיכל פסולת מתאים. לאחר מכן, להוסיף שני מיליליטר של ACK ליסינג חוצץ לתוך צינור הצנטריפוגה כדי resuspend ולתיר את האריתרוציטים. המתן שתי דקות ולאחר מכן הוסף HBSS 2% FCS כדי להשיג נפח כולל של 15 מיליליטר. חזור על צנטריפוגה. לאחזר את הצינור בזהירות ולהשליך את supernatant. resuspend הכדור שוב בחמישה מיליליטר של HBSS 2% FCS.
כדי לספור את התאים המותפנים מחדש, לדלל חמישה microliters של השעיית התא עם חמישה microliters של טריפאן כחול. לאחר מכן, הפקד בעדינות טיפה של חמישה מיקרו-ליטר של השעיית התאים מדוללים בין שעון הכיסוי למגלשת Malassez. עכשיו, תחת מיקרוסקופ בהגדלה של פי 40, ספרו את מספר התאים הקיימים. לאחר מכן, התאם את ריכוז התאים ל- 10 עד התא השביעי למיליליטר על-ידי הוספת הנפח המתאים של HBSS 2% FCS.
כדי להכתים את תאי החיסון, התחל על ידי תיוג שישה צינורות FACS מאחד עד שישה. לאחר מכן, העבר 200 מיקרוליטרים של פתרון התא לכל אחד מששת הצינורות. צנטריפוגות צינורות אלה ב 370 פעמים גרם במשך שבע דקות ב 10 מעלות צלזיוס ולהסיר את supernatant.
לאחר מכן, סמן שישה צינורות FACS חדשים כאחד עד שישה ו pipette 200 מיקרוליטרים של HBSS 2% FCS לתוך כל אחד. הכן את שש תערובות הנוגדנים החדשות על ידי הוספת הכמות המתאימה של נוגדן לכל צינור על פי שולחן אחד. מיקס אחד הוא לתאים לא נגועים ללא תוספת של נוגדנים. ערבובים של שתיים עד חמש כל אחד מכילים נוגדן יחיד שונה להגדרות פיצוי. תערובת שש מכילה את כל ארבעת הנוגדנים עבור תאים מוכתמים שישמשו למיון.
לאחר מכן, העבר תערובות נוגדנים אלה לצינורות FACS ממוספרים המתאימים. לדגור פתרונות אלה במשך 20 דקות בארבע מעלות צלזיוס או על קרח בחושך. לאחר מכן, להוסיף מיליליטר אחד של HBSS 2% FCS לכל צינור ולאחר מכן צנטריפוגה שוב. להשליך את supernatant ולאחר מכן resuspend הכדורים ב 200 microliters של HBSS 2% FCS. לבסוף, להעביר את הכדורים resuspended לצינורות FACS חדשים שכותרתו.
כדי לבצע FACS, הפעל תחילה את הממיין. לאחר מכן, בחר בתפריט cytometer ולחץ על אתחול fluidics. בצע את ההוראות המופיעות על המסך.
בכרטיסיה זרם, לחץ על הצלב האדום כדי להפעיל את הזרם ולאחר מכן המתן 15 דקות עד שהזרם יתייצב. כוונן את המשרעת של הזרם עד שתראה ירידה מנותקת ברורה מופיעה בכרטיסיית הזרם. לאחר מכן, לחץ על נקודה מתוקה כדי להשלים את התאמת המשרעת. הכנס את המסנן 1.0 לפני הלייזר בצפיפות נייטרלית.
פתח את תפריט cytometer בחלק העליון של המסך ובחר CST, אשר מייצג את ההתקנה והמעקב של Cytometer. כדי לבצע בקרת איכות יומית, תחילה לדלל חרוזי CST עם FACS בינוני בצינור FACS בעקבות הוראות היצרן. לאחר מכן, לטעון את הצינור לתוך המחשב ולבצע את פקד CST על ידי לחיצה על הפעל בכרטיסיה CST.
לאחר השלמת פקד CST, החלף את מסנן ND 1.0 במסנן ND 2.0 בציטומטר. לאחר מכן, לדלל חרוזי עיכוב טיפה במדיום FACS בעקבות הוראות היצרן ולאחר מכן לטעון את הצינור לתוך FACS. כדי להבטיח מיון נכון, בצע השהיית ירידה על-ידי לחיצה תחילה על מתח ולאחר מכן על מסנן אופטי. הרביע הימני של המסנן האופטי צריך להיות שווה ל- 100%, המציין כי 100% מהנטיפות נרשמות על ידי המכונה. במידת הצורך, להתאים את בורג הלייזר האדום על cytometer שמאל או ימין כדי להשיג 100% ברביע הימני. חשוב לוודא כי הנחל נופל לתוך צינור האיסוף. כדי לעשות זאת, בצע מיון בדיקה על ידי לחיצה על מגירת פסולת ולאחר מכן לבדוק מיון. בדוק שהזרמים הצדדיים נופלים לתוך צינורות האיסוף. אם הם לא, להתאים את המתח תחת לשונית המיון עד שהם עושים.
נווט אל תבנית הניסוי על-ידי בחירת כרטיסיית הדפדפן ולחיצה על תצוגה משותפת. לאחר מכן, פתח את הניסוי Accudrop_DROP DELAY ולחץ על לחצן פריסת המיון. כעת, שנה את שיעור הסף בלוח המחוונים של הרכישה על-ידי מניפולציה בקצב הזרימה עד שיגיע ל-3,000 אירועים בשנייה. לחץ על מתח ולאחר מכן לחץ על מסנן אופטי. הרביע השמאלי צריך להיות שווה לאפס ורביע ימני השווה ל- 100.
לבסוף, בחלון פריסת המיון, לחץ על מיון ולאחר מכן לחץ על ביטול. הרביע השמאלי צריך להיות שווה ל-100 והרביע הימני שווה לאפס. אם הרביע השמאלי הוא פחות מ- 95, לחץ על השהיית אוטומטית כדי להורות לתוכנה להגדיל באופן אוטומטי את המתח כדי להשיג 100% מהנטיפות ברביע השמאלי.
כדי להתחיל ציטומטריית זרימה, נשתמש תחילה בתאים לא נגועים כדי להגדיר את מורפולוגיית התא ואת הפסגות השליליות של הפלואורכרום. כדי לעשות זאת, מקם צינור אחד המכיל תאים לא נגועים במכונה ותחת כרטיסיית לוח המחוונים של הרכישה לחץ על עומס. בכרטיסיה cytometer, התאם את מתחי הפיזור קדימה וצדד עד שתראה את אוכלוסיית התאים שלך כריכוז צפוף של נקודות על המסך. לימפוציטים הם תאים קטנים, כך שיהיה להם פיזור נמוך קדימה ופיזור צד נמוך.
לאחר מכן, הסר פלואורסצנטיות ברקע על-ידי התאמת המתח עבור הפלואורכרומים בכרטיסיה cytometer עד שאוכלוסיות התאים ברמה שלילית נמצאות בעשור הראשון בלשונית גליון העבודה העולמית. בתפריט cytometer, לחץ על תצורת התצוגה וודא כי כל פלואורכרום קיימים. לאחר מכן, למקם צינור שני ב cytometer ולחץ על עומס. התאם את החפיפה הספקטרלית בכרטיסיה cytometer עד חציוני האוכלוסייה השליליים והחיוביים מיושרים בכרטיסיית גליון העבודה הכללי. בכרטיסיה רכישה, הגדר את האירועים לפרמטר שיא ל- 10,000 ולחץ על רשומה. חזור על צעדים אלה עם צינורות שלוש, ארבע וחמש.
לאחר מכן, צינור עומס שש המכיל את התאים המוכתמים. כדי לבודד לימפוציטים B, תחילה להגדיר את הפרמטרים כדי למיין את התאים בהתבסס על המורפולוגיה שלהם. בחלון הראשון, התווה אזור פיזור קדימה של FSC-A בציר ה- y ובאזור הפיזור הצדדי של SSC-A בציר x. בתיוו ההחלקה, כל נקודה מייצגת תא. לחץ על שער המצולע בגליון העבודה הכללי ולאחר מכן בחר את האוכלוסייה עם פיזור נמוך קדימה ופיזור צד ביניים. בחלון התוויית נקודות חדש, לחץ באמצעות לחצן העכבר הימני על החלון ובחר הצג אוכלוסיות מהתפריט ולחץ על P1.
לאחר מכן, בחלון החדש, שער את התאים החיוביים CD45 קיימא על ידי התוויית הכדאיות על ציר y ו- CD45 על ציר x. השתמש בשער מצולע כדי להקיף את התאים עם יכולת עילאית נמוכה ואות CD45 גבוה ובחר P2 כדי להציג את התאים שנבחרו בחלון חדש. בחלון הבא, שער עבור CD45 לויקוציטים חיוביים, למעט לימפוציטים T. עם CD45 בציר ה- x ו- CD3 בציר ה- y, הקיפו את האוכלוסייה באות CD45 גבוה ובאות CD3 שלילי נמוך ובחרו P3. לבסוף, שער עבור תאים חיוביים CD19 המזהים את לימפוציטים B. עם CD19 בציר ה-y ו-CD3 בציר ה-x, הקיפו את האוכלוסייה באות CD19 גבוה ובאות CD3 שלילי נמוך ובחרו P4.
כל פרמטרי המיון מוגדרים כעת. לאחר מכן, בחלון פריסת המיון, בחר את אוכלוסיית התאים שלך של עניין - P4, שהיא האוכלוסייה הרביעית כי היה מגודר, ואומר למכונה רק למיין לימפוציטים B. הגדר אירועי יעד ל-10,000 תאים והגדר דיוק לטוהר. אנחנו ממיין רק אוכלוסייה אחת. עם זאת, ניתן למיין עד ארבע אוכלוסיות שונות בו זמנית. לאחר שתוכן, לחץ על מיון ועל אישור. לאחר מכן, המתן למיון תאים.
לאחר השלמת מיון התאים, בצע בקרת טוהר על ידי צנרת 10 מיקרוליטרים של התאים ממוינים לתוך צינור FACS חדש עם 90 מיקרוליטרים של HBSS 2% FCS. מקם את הצינור ב cytometer, לחץ על עומס ולאחר מכן לחץ על רשומה כדי לנתח את הפנוטיפים של התאים כדי לוודא כי אסטרטגיית gating עבד כמתוכנן.
עכשיו, ננתח את התאים ממוינים כדי לקבוע את אחוז הלימפוציטים B בין הלויקוציטים שהיו מבודדים מטחול העכבר. כדי להתחיל, לחץ פעמיים על סמל FlowJo וגרור את הקבצים עבור כל צינור לתוך כל החלון לדוגמה.
לחץ על מצולע ושחזור אסטרטגיות הגטינג ששימשו בסעיף הקודם. לאחר מכן, לחץ על עורך הפריסה וגרור את אוכלוסיות הלימפוציטים B שמעניינים מצינור 6 ואת בקרת הטוהר לכרטיסיה עורך הפריסה. חלקות נקודה המייצגות לימפוציטים B יופיעו. בדוגמה זו, העלילה בפינה הימנית העליונה מייצגת את לימפוציטים B ממוינים מההשעיה הכוללת של תאי הטחול והתוויה בפינה הימנית התחתונה היא בקרת הטוהר. תאים צריכים להופיע רק באוכלוסיית העניין בבקרת הטוהר.
כדי לבדוק את הטוהר של לימפוציטים B בתאים ממוינים, לחץ על עורך הטבלה. גרור את אוכלוסיית הלימפוציטים B מצינור שש ובקרת טוהר בטבלה. בתפריט הסטטיסטיקה, בחר תדירות של תאים חיוביים CD45 כדי לבדוק את הטוהר של אוכלוסיית תאים זו. לאחר מכן, לחץ על צור טבלה. ערכי פרמטר מופיעים בטבלה חדשה. בחלון בקרת הטוהר, בדוק את התדירות של לימפוציטים B בתוך התאים החיוביים CD45, אשר צריך להיות גבוה מ 98%.
Subscription Required. Please recommend JoVE to your librarian.
Results
בפרוטוקול זה, טיהרנו לימפוציטים מסוג B באמצעות טכנולוגיית FACS. תחילה בודדנו לויקוציטים מהטחול והכתמנו אותם. באמצעות שילוב של סמני משטח של תאי B, יצרנו אסטרטגיית גיטינג כדי למיין אותם (איור 2, החלונית העליונה). בסוף הניסוי אימתנו אם תאים בצינור האיסוף היו תאי B באמצעות "בדיקת טוהר". שמרנו על אותה אסטרטגיית גטינג והבחנו שיותר מ-98% מהתאים אכן היו תאי B (איור 2, לוח תחתון). לכן, FACS הוא פרוטוקול יעיל כדי לבודד אוכלוסיות תאי החיסון עם רמה גבוהה של טוהר. לאחר מכן ניתן להשתמש בתאים שנאספו לניסויים במורד הזרם כגון תרבית תאים, RT-qPCR ובוחות ציטוקסיה.

איור 2: אסטרטגיית גיטינג ובדיקת טוהר לאחר מיון. (A) תאים היו מגודרים תחילה בהתבסס על המורפולוגיה שלהם (משמאל: FSC-A, SSC-A), ואז רק חיים (שמאל אמצעי: כדאיות, CD45), CD45+ תאים (CD45, CD3) היו מותווים נגד CD19 ו- CD3. רק CD19+ תאים מוינו. (ב) תוצאות בדיקת טוהר של שבריר תאים שהושגו לאחר מיון תאים. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
ציטומטריית זרימה היא טכניקה ממקור ראשון לאפיון ומיון אוכלוסיות תאי החיסון עם רמה גבוהה של טוהר. זהו כלי קדמוני בתחום המחקר שכן הוא מאפשר העשרה של אוכלוסיות תאים ספציפיות ולפענח את התגובה החיסונית לפתוגנים. עם הגידול במספר פלואורוכרום זמין וציטומטרים, מספר הפרמטרים הניתנים לזיהוי גדל מאוד. כתוצאה מכך, ניתוח ביואינפורמטי של נתוני FACS החל לצוץ ופתח אופקים חדשים לציטומטריה זורמת (3). ציטומטריית זרימה מציעה יישומים אחרים בהמטולוגיה ואונקולוגיה (4) שם היא משמשת לפיתוח כלי אבחון.
Subscription Required. Please recommend JoVE to your librarian.
References
- Lanier, L. L. Just the FACS. The Journal of Immunology, 193 (5), 2043-2044 (2014).
- Walker, J. M. Epiblast Stem Cells IN Series Editor.
- Tung, J. W., Heydari, K., Tirouvanziam, R., Sahaf, B., Parks. D. R., Herzenberg, L. A., and Herzenberg. L. A. Modern Flow Cytometry: A Practical Approach. Clinics in Laboratory Medicine. 27 (3), 453-468 (2007).
- Walker, J. M. Tumor Angiogenesis Assays IN Series Editor.




