Overview
מקור: טוניה ג'יי ווב1
1 המחלקה למיקרוביולוגיה ואימונולוגיה, בית הספר לרפואה של אוניברסיטת מרילנד ומרכז הסרטן המקיף מרלן וסטיוארט גרינבאום, בולטימור, מרילנד 21201
ELISPOT הוא מדוקנן, ניתן לשחזור המשמש לזיהוי תגובות חיסוניות תאיות. הבחינה משתמשת בשיטה מבוססת בדיקה חיסונית הקשורה לאנזים (ELISA) כדי לזהות תגובות חיסוניות חד-תאיות שניתן לדמיין לפי כתמים, ומכאן השם ELISPOT. ELISPOT תוארה לראשונה בשנת 1983, על ידי צ'רקינסקי, כשיטה למנות את מספר ההיברידיות של תאי B המייצרות אימונוגלובולינים ספציפיים לאנטיגן (1). אותה קבוצה פיתחה עוד יותר את ההסתה כדי למדוד את התדירות של ציטוקינים המייצרים לימפוציטים T. עכשיו ELISPOT הפך תקן זהב למדידת חסינות תאי T ספציפיים אנטיגן בניסויים קליניים ומועמדים לחיסון. לדוגמה, לאחר חיסון או במהלך זיהום, תאי פלזמה ותאי זיכרון B מפרישים נוגדנים המספקים הגנה. בדרך כלל, תגובות תאי B אלה מוערכות על ידי מדידת טיטרים בסרום של נוגדנים ספציפיים לאנטיגן. עם זאת, סוג זה של ניתוח, נמדד בדרך כלל על ידי ELISA, לא יכול לכלול תאי זיכרון B, אשר יכול להיות נוכח גם בהיעדר רמות נוגדנים בסרום לגילוי. יתר על כן, זה כבר מבוסס היטב כי תאי זיכרון B במחזור חשובים לתגובה נוגדנים מהירה ומגנה שנצפו בעקבות חשיפה מחדש פתוגן, ולכן זה קריטי כדי להיות מסוגל לזהות תאים אלה. לכן, כדי להעריך בבירור תגובות תאי B זיכרון ספציפי אנטיגן, הן ELISA ו ELISPOT יש להשתמש (2).
ELISPOT assay משתמש בצלחת המכילה בארות מרופדות ממברנה מצופות בנוגדנים על מנת ללכוד חלבונים מופרשים של עניין. לאחר מכן, הצלחת עמוסה בתאים וגירויים כדי לגרום לייצור חלבון. החלבונים המופרשים נלכדים על ידי הנוגדנים המצופים על פני השטח. לאחר זמן הדגירה המתאים, תאים מוסרים והמולקולה המופרשת מזוהה באמצעות נוגדן ביוטינילציה ספציפי לאפיטופ אחר, בהשוואה לנוגדן הלכידה. לאחר מכן מתווסף סטרפטאבידין פרוקסידאז, ואחריו הוספת מצע המאפשר זיהוי של הכתמים (איור 1). הכוח של ההסתה הזו הוא שהוא מאפשר כמות מספר התאים המייצרים את החלבון המעניין. חשוב לציין, ניתן להעריך אם יש שינויים במספר הכולל של תאים המייצרים חלבון מסוים או אם תאים בודדים בתוך אוכלוסייה מייצרים יותר חלבון. יתר על כן, הוא יכול לספק מידע לגבי קינטיקה והוא יכול לשמש להערכת ההפעלה החיסונית הכוללת (גירוי מיטוגן) ביחס לתגובות ספציפיות אנטיגן (סימולציית אנטיגן). בדיקות ELISPOT יאפשרו את הזיהוי תא אחד מופעל בין 300,000 תאים לאחר הפעלה מיטוגנית או אנטיגן ספציפי.
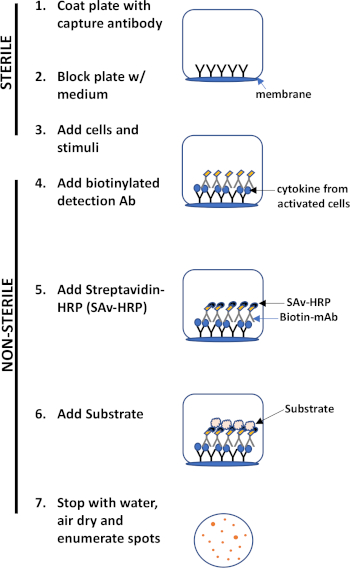
איור 1: מבט כולל על פרוטוקול ELISPOT.
היתרונות העיקריים של ההסתייגות הזו הם שלה. פשטות - הפרוטוקול הוא פשוט יחסית ופשוט. זה לא דורש מומחיות טכנית, ב. רגישות - היא מאפשרת זיהוי של תאי מערכת החיסון ברמת התא הבודד ודורשת מעט מאוד תאים בהשוואה לשיטות אחרות כגון ציטומטריית זרימה, c. פונקציונליות - הוא מספק נתונים כמותיים לגבי תפקוד מערכת החיסון.
תרגיל מעבדה זה מדגים את פרוטוקול ELISPOT לגילוי של IFN-γ הפרשת-טחול, אבל כאמור לעיל הבדיקה הזאת יכולה לשמש גם כדי להעריך הפרשת נוגדנים על ידי תאי B (3).
Procedure
1. הגדרת
מאגרים ריגנטים
- תמיסת מלח סטרילית עם אגירה בפוספט (PBS) ללא סידן או מגנזיום
- חוצץ ציפוי - PBS סטרילי או חוצץ קרבונט
- דילול אסאי - 10% סרום בקר עוברי (FBS) ב- PBS
- תרבית תאים בינונית - RPMI 1640 עם 10% FBS, פניצילין/סטרפטומיצין, ו- L-גלוטמין
- מאגר כביסה - PBS המכיל 0.05% Tween20
- מים מזוקקים כפולים (ddH2O)
- מצע זיהוי - 100 מ"ג AEC (3-אמינו-9-אתיל-קרבזול) ב-10 מ"ל DMF (N,N, דימתילפורמיד).
ציוד
- מכסה המנוע של זרימה למינאר
- אינקובטור לח (מוגדר ב 37°C, 5% CO2)
- קורא ELISPOT אוטומטי או מיקרוסקופ ניתוח
חומרים
- לוחות אליספוט
- מאגרים סטריליים ולא סטריליים
- פיפטורים וטיפים
- פיפטות סרולוגיות סטריליות
- צינורות פוליפרופילן סטריליים חרוטיים
- שני בקבוקי סחיטה לשטיפת צלחת
ריאגנטים ספציפיים לאסיי
- תאים- תאים ראשיים או קווי תאים (כאן, נעשה שימוש בטחול מ- C57BL/6 עכברים)
- ממריצים- מיטוגן או אנטיגן (כאן, פוטבול 12-myristate 13-אצטט (PMA, 50 ng/mL) ויונומיצין (1 מיקרומטר) שימשו)
- נוגדן ראשוני - אנטי ציטוקינים ביוטילציה גילוי נוגדן (מדולל ל 2 מיקרוגרם / מ"ל בדלל אסאי)
- נוגדן משני- פרוקסידאז סטרפטאבידין-חזרת (SAv-HRP)
2. הליך
ציפוי
- שמירה על התנאים סטריליים ובתוך מכסה המנוע זרימה למינאר, לדלל את נוגדן לכידת אנטי ציטוקינים מטוהר לריכוז סופי של 0.5-4.0 מיקרוגרם / מ"ל במאגר ציפוי סטרילי. (הערה: עבור IFN- γ ו- IL-6 להשתמש 5 מיקרוגרם / מ"ל).
- העבר את פתרון נוגדני לכידת, 100 μL / well, ללוח ELISPOT.
- מכסים את הצלחת בכיסוי צלחת ולאטום אותה כדי למנוע אידוי.
- לדגור על הצלחת לילה ב 4°C.
חסימת
- למחרת, לחשוף את צלחת ELISPOT במכסה המנוע זרימה למינאר. הפוך במהירות את הצלחת על מגבונים סטריליים כדי להסיר את פתרון נוגדני לכידת מכל באר.
- לאחר מכן, הוסף 200 μL של תרבית תאים מדיום לכל באר. שלב זה יחסום כריכה לא ספציפית במהלך ההסתה.
- החליפו את כיסוי הצלחת ודגרו את הצלחת במשך שעתיים ב-37 מעלות צלזיוס.
ציפוי והפעלת תאים
- בזמן הלוח הוא דגירה, להכין פתרון mitogen 2X המכיל 50 ng / mL PMA ו 1 μM ionomyצין במדיום תרבית התא.
- לאחר מכן, להכין השעיות הסלולר היעד לריכוז מלאי של 2 x 106 תאים / מ"ל.
- לאחר הדגירה הושלמה, להסיר את המדיום תרבית התא מכל באר על ידי היפוך מהיר את הצלחת על מגבונים סטריליים בתוך מכסה המנוע זרימה למינאר.
- לאחר מכן, צור דילול טורי פי 2 של פתרון ההשעיה של תא המלאי. כדי לעשות זאת, תחילה להוסיף 200 μL של פתרון מלאי מתלה סלולרי מוכן לתוך בארות בשורה העליונה של צלחת ELISPOT.
- לאחר מכן, הוסף 100 μL של תרבית תאים רגילים בינוני לחמש השורות הבאות של הלוח מתחת לשורות המכילות פתרון מלאי סלולרי.
- לאחר מכן, בצע דילול טורי פי 2 על ידי צנרת 100 μL של המתלה הסלולרי מהשורה העליונה לשורה ישירות מתחת. ודא ערבוב נכון על ידי צנרת בעדינות פתרון זה למעלה ולמטה כדי להבטיח אפילו להפיץ את התאים.
- חזור על תהליך זה עבור ארבע השורות הנותרות.
- השאר את השורה השישית עם מדיום התרבות בלבד. זה ישמש כשליטה ניסיונית.
- לאחר מכן, להוסיף 100 μL של פתרון מיטוגן מוכן הבארות הניסיוניות של חמש השורות הראשונות של הלוח. בבארות הבקרה והשורה השישית, הוסף 100 μL של מדיה תרבית התא ללא מיטוגן.
- החליפו את כיסוי הצלחת ואת צלחת הדגירה ב 37°C, 5% CO2 באינקובטור במשך 20-48 שעות. (הערה: 20-24 שעות בדרך כלל מספיק לאיתור IL-2 ו- TNF- α, בעוד 48 שעות הוא אופטימלי עבור IL-4 ו- IFN-γ).
זיהוי
נוגדן ראשי
- הכן את נוגדן אנטי ציטוקינים ביוטינילה לריכוז של 2 מיקרוגרם /מ"ל בדילול אסאי.
- הכן 20-25 מ"ל של חוצץ כביסה בשלב זה על ידי ערבוב 0.05% Tween-20 ב- PBS.
- לאחר הדגירה הושלמה, לפתוח את הצלחת במהירות הפוך אותו על כיור כדי להסיר את כל הנוזל מן הבארות. (הערה: לאחר נקודה זו הצלחת כבר לא צריך להישמר סטרילי).
- לאחר מכן, לשטוף את הצלחת על ידי הוספת ~ 200 μL לשטוף חוצץ לכל באר. לגרש את הנוזל הזה על ידי היפוך מהיר והטלת הצלחת מעל כיור. חזור על תהליך זה בסך הכל חמש כביסות.
- לאחר מכן, להוסיף 100 μL של ביוטיניל מדולל אנטי ציטוקינים גילוי פתרון נוגדנים לכל באר. יש לדגור בטמפרטורת החדר למשך שעתיים בטמפרטורת החדר או בלילה בטמפרטורה של 4 מעלות צלזיוס.
נוגדן משני
- לאחר השלמת הדגירה, לגרש את נוגדן הזיהוי על ידי היפוך והטלת הצלחת מעל הכיור.
- כמו קודם, לשטוף את הצלחת 5 פעמים עם ~ 200 μL לשטוף חוצץ, גירוש הנוזל בין כל לשטוף.
- לאחר מכן להוסיף 100 μL של פתרון peroxidase סטרפטאבידין-חזרת מדולל לכל באר (מדולל לריכוז האופטימלי שנקבע מראש בדילול אסאי).
- החליפו את כיסוי הצלחת ודגרו בטמפרטורת החדר למשך שעה וחצי-שעתיים ב-37°C.
המצע
- לאחר הדגירה, לא יותר מ 15 דקות לפני השימוש, הראשון להפעיל פתרון מצע AEC על פי הוראות היצרן.
- לאחר מכן, להשליך את התוכן של הבארות לשטוף את הצלחת חמש פעמים עם חוצץ לשטוף, כמו קודם.
- לאחר מכן, מיד להוסיף 100 μL של פתרון מצע AEC מוכן לתוך כל באר.
- לדגור על הצלחת בטמפרטורת החדר במשך ~ 10-20 דקות תוך ניטור התפתחות המקום.
- עצור את התגובה על ידי שטיפה של הצלחת במים והזזת הצלחת מעל הכיור.
- כתם את הצלחת על מגבות נייר ולאפשר את הצלחת לאוויר יבש לילה או עד שהוא יבש לחלוטין. הסרת מגש הפלסטיק מתחת לצלחת תקל על הייבוש.
3. רכישת נתונים וניתוח נתונים
- לאחר הייבוש, הכתמים מוכנים לספירה עם קורא לוחות אוטומטי. כאן, קורא חיסון CTL משמש, אבל פרוטוקול זה יכול להיות מותאם עבור כל קורא.
- קודם תדליק את המכשיר, אחר כך את המחשב. לאחר מכן, פתח את תוכנית ה- CTL ולחץ על "ספירת סריקות".
- לחץ על "נפלט" כדי שהמגש יימשך מהמכונה. לאחר מכן, להסיר את מתאם פלסטיק וליישר שורה "A" על צלחת ELISPOT ומתאם.
- בחר שם קובץ ומיקום לשמירת הקובץ וטען את הצלחת על המגש.
- לאחר מכן, לחץ על "לטעון" על התוכנה ולסגור את הדלת בצד של המכונה.
- לחץ על "התחל- לאחר הספירה". ודא שהקובץ נשמר ולאחר מכן פתח את תוכנת בקרת האיכות "QC" כדי לנתח את הנתונים ולספור את מספר המקומות.
הערות:
- המספר המינימלי של תאים צריך להיקבע בניסויים ראשוניים. המספר האופטימלי של כתמים הוא ~ 50 / טוב. אם תאים רבים מדי נטענים, יהיה קשה לזהות נקודות נפרדות. בנוסף, התאים יחפפו ולא יוכלו ליצור monolayer על הממברנה, ולכן רמת הזיהוי עשויה להיות מופחתת.
- בעת אופטימיזציה של הניסוי, שקול את רמת הביטוי הצפויה של חלבון היעד. עם הביטוי נמוך יותר, כך מספר התאים הנדרש לבאר גבוה יותר.
- שלא כמו אליסה, עדיף לשטוף את הצלחת ביד ולא להשתמש מכונת כביסה צלחת. לוחות ELISPOT הם עדינים יותר ויש להימנע ניקוב קרום PVDF.
- יש להגביל את תנועת הצלחת במהלך תקופת הדגירה כפי שהוא יכול לגרום כתמים כתם.
- לוחות צריך להיות מאוחסן בחושך, כמו חשיפה לאור ישיר גורם כתמים לדעוך.
אימונוסקופ הקשורים לאנזים, או ELISPOT, היא שיטה לנתח את התגובה החיסונית לפתוגן או נזק לתא. זה מאפשר לכמת את ההפעלה של תאים חיסוניים שונים על ידי זיהוי חלבונים ספציפיים שהם מפרישים. לדוגמה, ELISPOT משמש בדרך כלל למדידת תגובות תאי T עם חשיפה לאנטיגן זר על ידי זיהוי ציטוקינים מופרשים.
לבדיקת ELISPOT מבוססת ציטוקינים, התהליך מתחיל בציפוי של מיקרו-לוח ELISPOT עם נוגדן לכידה, הספציפי לציטוקינים היעד. לאחר ציפוי הנוגדנים, תאי T מתווספים לבארות ומוגרים על ידי חומר חיצוני, כמו נוגדן נגד CD3, למשל. לאחר מכן, התאים מפרישים את ציטוקין המטרה, אשר מיד משותק על ידי נוגדן לכידת. מאז החלבון נתפס מיד לאחר הפרשה מתאים חיים, ללא דילול או השפלה, זה בדיקת יש דיוק גבוה. לאחר שציטוקינים המטרה משותקת, מתווסף נוגדן זיהוי, שנקשר גם לציטוקינים שנתפסו.
טכניקת ELISPOT יכולה לשמש גם כדי לכמת תאי B זיכרון לאחר זיהום או חיסון על ידי ניתוח הייצור שלהם של נוגדנים ספציפיים. ב- ELISPOT מבוסס נוגדנים, אנטיגן ספציפי משמש במקום נוגדן עבור שלב הלכידה, שבו האנטיגן יהיה קשור לצלחת, או בשלב הזיהוי, שבו האנטיגן מזהה את נוגדן היעד לאחר הלכידה. בכל הווריאציות של התהליך, עבור תאי T או תאי B, נוגדן האיתור או האנטיגן הוא ביוטינילציה, המאפשרת לו להיקשר לאנזים זיהוי מצומד סטרפטווידין, כגון peroxidase חזרת. לאחר מכן, עם הוספת המצע של peroxidase, AEC, משקעים כהים, מסיסים מיוצרים. משקעים אלה מסמנים את מיקומו של החלבון שנתפס, וכל תא הפרשה גורם לנקודה גלויה, שניתן לכמת באמצעות קורא ELISPOT או מיקרוסקופ. גודל הכתמים הוא הערכה יחסית של כמות החלבון המופרשת מכל תא. בדיקות חיסון אלה יכולות לזהות תגובות חיסוניות מתאים בודדים, אפילו בתת-אוכלוסין קטן יחסית של תאים מפרישים, מה שהופך אותו לשימושי לחקר תגובות מערכת החיסון ברמה התאית.
בסרטון וידאו זה, תלמד כיצד לבצע ניסיון ELISPOT ולאחר מכן לכמת את הכתמים המייצגים את תאי ההפרשה.
לאורך כל הניסוי, להבטיח תנאים סטריליים על ידי עבודה במכסה המנוע זרימה למינאר ללבוש כפפות.
כל החישובים בפרוטוקול זה מבוססים על אמצעי האחסון הדרוש עבור לוח אחד של 96 בארות.
ראשית, לדלל את נוגדן לכידת אנטי ציטוקינים. כדי לעשות זאת, להעביר 10 מיליליטר של חוצץ לתוך צינור חרוט סטריליטר 15 מיליליטר. לאחר מכן, השתמש פיפטה כדי להוסיף 10 microliters של מיליגרם אחד למיליליטר של נוגדן חד שבטי למאגר כדי ליצור פתרון עם ריכוז סופי של מיקרוגרם אחד למיליליטר. לאחר מכן, יוצקים את תמיסת נוגדני הלכידה למאגר סטרילי, ובאמצעות פיפטה רב-ערוצית, מחלקים 100 מיקרוליטרים לכל באר של צלחת ELISPOT בעלת 96 בארות.
מכסים את הצלחת בכיסוי צלחת, אוטמים אותה למניעת אידוי, ודגרה למשך הלילה בארבע מעלות צלזיוס. למחרת, לחשוף את צלחת ELISPOT במכסה המנוע זרימה למינאר. הפוך במהירות את הצלחת על מגבונים סטריליים כדי להסיר את פתרון נוגדני לכידת מכל באר. לאחר מכן, השתמש בצינור רב-ערוצי כדי להוסיף 200 מיקרוליטרים של תרבית תאים בינונית לכל באר. שלב זה יחסום כריכה לא ספציפית במהלך ההסתה. החליפו את כיסוי הצלחת ודגרה באינקובטור של 37 מעלות צלזיוס במשך שעתיים.
בזמן הלוח הוא דגירה, להכין פתרון mitogen 2X על ידי הוספת microliter אחד של PMA ו 20 microliters של ionomycin כדי 10 מיליליטר של תרבית התא בינוני כדי להשיג ריכוז סופי של 15 ננוגרם למיליליטר PMA ואחד ionomycin מיקרומולר.
מתלים סלולריים של טחול עכבר צריך להיות מוכן גם בשלב זה במכסה המנוע סטרילי. באמצעות מיקרוסקופ והמוציטים, מודדים את ריכוז התאים ומתאימים את הנפח הכולל עד להגעה לריכוז מלאי של שני מיליון תאים למיליליטר.
לאחר הדגירה הושלמה, במהירות הפוך את הצלחת על מגבונים סטריליים כדי להסיר את המדיום תרבית התא מכל באר. לאחר מכן, הוסף 200 מיקרוליטרים של פתרון מלאי מתלה הסלולר מוכן לבארות בשורה העליונה של צלחת ELISPOT. הגדר את הניסוי במשולש, כך שכל סוג תא שנבדק יהיה מצופה בקבוצה של שלוש עמודות מקובצות. מתחת לזה, להוסיף 100 microliters של תרבית תאים רגילים בינוני לחמש השורות הבאות של הלוח, מתחת לשורות המכילות פתרון מלאי סלולרי.
לאחר מכן, בצע דילול סדרתי על ידי צנרת 100 microliters של ההשעיה התא מהשורה העליונה לשורה ישירות מתחת, בעדינות pipetting הפתרון למעלה ולמטה כדי להפיץ באופן שווה את התאים. חזור על תהליך זה עבור השורות הנותרות, העברת 100 מיקרו-לייטר מהשורה הקודמת לשורה שלהלן בכל שלב, וממשיך עד שהשורה החמישית תדולל באופן סדרתי. השאר את השורה השישית עם מדיום תרבית התא בלבד, כדי לשמש כפקד. כדי לעורר את התאים בבארות הניסוי של הצלחת, להוסיף 100 microliters של פתרון מיטוגן מוכן ההשעיות הסלולר בכל באר של שורות אחת עד חמש. הקפד לעזוב את השורה השישית, אשר ישמש את השליטה, ללא גינוי. החלף את המכסה ודגר את הצלחת ב 37 מעלות צלזיוס ו 5% CO2 במשך 24 עד 48 שעות.
הכן את נוגדן האנטי-ציטוקינים המורחב בביוטינילה. ראשית, להכין 50 מיליליטר של דילול אסאי על ידי הוספת 5 מיליליטר של 10% סרום בקר עוברי ל 45 מיליליטר של PBS. לאחר מכן, לדלל את הנוגדן המזהה לריכוז של 2 מיקרוגרם למיליליטר בדילול אסאי. כמו כן, להכין 20 עד 25 מיליליטר של חוצץ לשטוף בשלב זה, על ידי ערבוב .05% Tween-20 ו PBS.
לאחר הדגירה הושלמה, לפתוח את הצלחת במהירות הפוך אותו כדי להסיר את כל הנוזל מן הבארות. לשטוף את הצלחת על ידי הוספת כ 200 microliters של חוצץ לשטוף לכל באר. לגרש את הנוזל הזה על ידי היפוך מהיר והטלת הצלחת מעל כיור. חזור על תהליך זה ארבע פעמים נוספות בסך הכל חמש כביסות. לאחר מכן, הוסיפו 100 מיקרוליטרים של תמיסה נוגדנית זיהוי מדוללת לכל באר, החליפו את המכסה ודגרו בטמפרטורת החדר במשך שעתיים. לאחר הדגירה, לגרש את פתרון נוגדן הזיהוי מן הבארות של הצלחת על ידי היפוך והבהלה את הצלחת מעל הכיור.
כמו קודם, לשטוף את הצלחת חמש פעמים עם חוצץ לשטוף, גירוש הנוזל בין כל לשטוף. לאחר הכביסה הסופית, להכין את פתרון peroxidase סטרפטבידין- חזרת על ידי דילול זה על פי הוראות היצרן. לאחר מכן, עם בארות של הצלחת ריקה, להוסיף 100 microliters של סטרפטאבידין מדולל - פתרון peroxidase חזרת לכל באר. מניחים את המכסה בחזרה על הצלחת ודגור בטמפרטורת החדר במשך שעתיים.
לאחר הדגירה, לא יותר מ 15 דקות לפני השימוש, להפעיל פתרון מצע AEC מראש. להשליך את התוכן של הבארות לשטוף את הצלחת חמש פעמים עם חוצץ לשטוף, כמו קודם. לאחר מכן, מיד להוסיף 100 microliters של פתרון מצע AEC מוכן לתוך כל באר. השאירו את הצלחת בטמפרטורת החדר להתפתח במשך כ 10 עד 20 דקות, תוך ניטור פיתוח נקודתי. כתמים אלה יופיעו כעיגולים קטנים וכהים על פני השטח של הבארות. לאחר מכן, לעצור את התגובה על ידי שטיפה הצלחת עם מים והבהיק אותו על הכיור. כתם את הצלחת על מגבות נייר ולאפשר אוויר יבש לילה או עד יבש לחלוטין. הסרת מגש הפלסטיק מתחת לצלחת תקל על הייבוש. לאחר הייבוש, הכתמים מוכנים לספירה עם קורא לוחות אוטומטי.
כאן, קורא CTL ImmunoSpot משמש, אך פרוטוקול זה יכול להיות מותאם עבור כל קורא. לאחר מכן, פתח את תוכנית CTL ולחץ על ספירת סריקות. לחץ על הוצאת המגש כדי להאריך מהמכונה. לאחר מכן, הסר את מתאם הפלסטיק ויישר שורה A בצלחת ובמתאם ELISPOT. בחר שם קובץ ומיקום לשמירת הקובץ וטען את הלוח והמתאם על המגש. לחץ על טען על התוכנה וסגור את הדלת בצד של המכונה. לאחר מכן, לחץ על התחל לאחר הספירה. ודא שהקובץ נשמר ולאחר מכן פתח את תוכנת QC בקרת איכות כדי לנתח את הנתונים ולספור את מספר המקומות. יצא נתונים אלה כקובץ Excel. לאחר השלמת הניתוח, לחץ על נפלט כדי לאחזר את הלוח.
בניסוי זה, תאים מסוג בר ועכברים נושאי גידולים היו מצופים ונותחו עבור גמא IFN. שים לב כי מספר כתמים פוחת עם ירידה בריכוז התא. בדרך כלל, נתוני ELISPOT מוצגים כמספר ספירות הספוטים לפי מספר תאים מצופים. בדוגמה זו, מספר הכתמים הוצגו בגרף עמודות, כאשר כל ריכוז תאי בהתאמה מופיע בציר ה- x. שים לב שמספר הכתמים מציין את מספר התאים הפעילים למספר הכולל של תאים באוכלוסייה נתונה.
Subscription Required. Please recommend JoVE to your librarian.
Results
בבדיקת ELISPOT זו, לויקוציטים טחול מן wildtype ועכברים נושאי גידול נותחו עבור IFN-γ. איור 2 A מציג את התמונה החזותית של תוצאת ההסתה. המספרים בצבע הירוק מציינים את מספר הכתמים לבאר (TNTC מציין "רבים מכדי לספור"). שים לב כי מספר כתמים פוחת עם ירידה בריכוז התא.

איור 2A: ירידה בתגובות החיסוניות בעכברים הנושאים גידולים. אנא לחץ כאן כדי להציג גירסה גדולה יותר של איור זה.
בדרך כלל, נתוני ELISPOT מוצגים כמספר ספירות הספוטים לפי מספר תאים מצופים. באיור 2 B מספר הכתמים מוצג בגרף עמודות, כאשר כל ריכוז תאי בהתאמה מופיע בציר ה-X. למטרות גרף, 150 שימש לציון המספר המרבי של כתמים. מספר ה-IFN-γ המייצרים לויקוציטים מורינים בטחול בבעלי חיים הנושאים גידולים נמוך יותר מאלה של סוג הבר.

איור 2B: ירידה בתגובות החיסוניות בעכברים הנושאים גידולים. טחול נקצרו משליטה C57BL/6 (סוג בר) ועכברים נושאי גידולים ועוררו PMA /ionomycin במשך 48 שעות. בדיקות ELISPOT שימשו כדי כמות של IFN-γ לייצר לויקוציטים בטחול. (א) ייצוג חזותי ו-(B) גרפי של הנתונים. TNTC מציין רבים מדי לספור. למטרות גרף, 150 שימש לציון המספר המרבי של כתמים. המספרים הירוקים מציינים את מספר הכתמים שנספרו לבאר. המספרים האדומים מציינים את בארות הייחוס ששימשו לקביעת הכתמים שהיו תאים ואלו כתמים היו פסולת, ממצאים או אפקטי קצה ויש לא לכלולם בניתוח.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
בדיקות ELISPOT מאפשרות להעריך את הפעלת תאי החיסון על ידי קביעת מספר התאים המפרשים ניתוח ספציפי. הגודל והעוצמה של הכתמים מספק מידע לגבי כמות הניתוח המיוצר על ידי כל תא. הפרוטוקול המתואר לעיל פירט את איתורו של ציטוקין יחיד. עם זאת, ההתפתחויות האחרונות שיפרו את התועלת של מטען זה. נכון לעכשיו, ניתן להשתמש בצבעי זיהוי פלואורסצנטיים על מנת לזהות ניתוחים מרובים בתוך באר. הדבר מאפשר זיהוי של תת-אוכלוסין שונים של תאים המפרשים ניתוח אחד או שניהם.
Subscription Required. Please recommend JoVE to your librarian.
References
- Czerkinsky, C. C., Nilsson, L. A., Nygren, H., Ouchterlony, O., & Tarkowski, A. A solid-phase enzyme-linked immunospot (ELISPOT) assay for enumeration of specific antibody-secreting cells. Journal of Immunological Methods, 65 (1), 109-121(1983).
- Wahid, R., Simon, J. K., Picking, W. L., Kotloff, K. L., Levine, M. M., & Sztein, M. B. Shigella antigen-specific B memory cells are associated with decreased disease severity in subjects challenged with wild-type Shigella flexneri 2a. Clinical Immunology, 148 (1), 35-43 (2013).
- Roberts, T. J., Lin, Y., Spence, P. M., Van Kaer, L., & Brutkiewicz, R. R. CD1d1-dependent control of the magnitude of an acute antiviral immune response. The Journal of Immunology, 172, 3454-3461 (2004).




