Overview
출처: 안나 블렉버그1,롤프 루드1
1 임상 과학 룬드학과, 감염 의학 학과, 생물 의학 센터, 룬드 대학, 221 00 룬드 스웨덴
항생제와 박테리아 사이의 상호 작용에 대한 지식은 미생물이 항생제 저항을 어떻게 진화하는지 이해하는 데 중요합니다. 에서 1928, 알렉산더 플레밍 페니실린발견, 세포 벽 재생을 방해 하 여 항균 기능을 발휘 하는 항생제 (1). 행동의 다양 한 메커니즘을 가진 다른 항생제 는 이후 발견 되었습니다., DNA 복제 및 박테리아에 단백질 번역을 억제 하는 약물을 포함 하 여; 그러나, 새로운 항생제는 최근 몇 년 동안 개발되지 않았습니다. 현재 항생제에 대한 내성이 증가하여 효과적으로 치료할 수 없는 심각한 전염병(2)이 발생하고 있습니다. 여기에서, 우리는 세균성 인구에 있는 항생 저항을 평가하기 위하여 몇몇 방법을 기술합니다. 세균성 죽음이 측정된 결과이기 때문에 이러한 방법의 각각은 사용되는 항생제의 작용 메커니즘에 관계없이 작동합니다. 항생 저항은 병원 설정을 통해 특히 급속하게 전파될 뿐만 아니라 사회 전반에 걸쳐 전파됩니다. 이러한 저항 수단을 조사하기 위해 엡실로미터 시험(E-test) 및 국물 희석 시험(3)을 포함한 다양한 방법이 개발되었다.
E-test는 잘 확립된 방법이며 미생물의 눈에 보이는 성장을 억제하는 항균제의 가장 낮은 농도인 최소한의 억제 농도(MIC) 데이터를 정량화하는 비용 효율적인 도구입니다. 사용되는 세균균 및 항생제에 따라 MIC 값은 서브 μg/mL에서 >1000 μg/mL(4)에 따라 달라질 수 있습니다. E-Test는 미리 정의된 항생제 그라데이션을 포함하는 플라스틱 스트립을 사용하여 수행되며, 이는 Μg/mL의 MIC 판독 척도로 각인됩니다. 이 스트립은 접종된 한천 판에 적용될 때 한천 매트릭스에 직접 전달됩니다. 인큐베이션 후, 대칭 타원형 억제 영역은 세균 성장이 방지됨에 따라 스트립을 따라 볼 수 있습니다. MIC는 타원이 스트립과 교차하는 끝점인 억제 영역에 의해 정의됩니다. MIC를 결정하는 또 다른 일반적인 방법은 마이크로브로스 희석 방법입니다. 마이크로브로스 희석은 접종된 박테리아를 함유하는 국물 배지에 첨가된 항균제의 상이한 농도를 통합한다. 배양 후, MIC는 가시성장을 방지하는 항생제의 가장 낮은 농도로 정의된다(5). 또한 정량적 방법이며 여러 박테리아에 적용 될 수 있습니다. 이 방법의 단점은 시약의 농도를 준비할 때 오류의 가능성과 실험에 필요한 많은 수의 시약이 포함된다. 항생 저항을 측정하는 것은 임상 및 연구 관점 둘 다에서 필수적이며, 저항을 조사하는 이 체외 방법은 토론되고 아래에 전시됩니다.
특정 박테리아에 대한 저항의 프로파일은 환자가 단일 치료 대 조합 치료에서 혜택을 받을 지 여부를 결정하기 위해 항생제 치료를 최적화하기 위해 적용 될 수 있습니다. 한 번에 하나 이상의 항생제를 사용하려면 서로상호 작용하고 첨가제, 시너지 효과 또는 적대적 효과가 있는 경우 알아야 합니다. 항생제의 관절 효과가 동일한 용량으로 주어진 개별 항생제의 효능과 같을 때 첨가제 효과를 볼 수 있습니다. 항생제 간의 시너지 효과, 다른 한편으로는, 항생제의 관절 효과 혼자 주어진 것 보다 더 강력한 경우 존재 (6). 항균 치료의 조합을 적용하면 항균 성 내성의 발생을 피하기 위해 개별 항생제 치료 (7)의 효과를 향상시키기 위해 사용됩니다. 길항증에 대한 지식은 항균 조합의 불필요한 사용을 방지하는 것도 중요합니다. E-Test 방법론은 다른 항균제 간의 가능한 시너지 효과와 적대감을 결정하는 간단하고 여러 가지 방법을 제공합니다. 항생제 내성 병원균의 증식에 직면하기 위해 특정 항생제의 가능한 시너지 및 길항 메커니즘에 대한 지식은 임상 효능과 다제 내성을 퇴치하는 데 중요합니다.
E-테스트를 사용하여 시너지 효과를 결정하는 것은 교차 및 비교차 테스트의 두 가지 광범위한 접근 법으로 나눌 수 있습니다. 두 시너지 테스트 모두 개별 MIC 값에 대한 이전 지식에 의존하지만 두 가지 방법은 방법론과 개념적 접근 방식에서 약간 다릅니다. 비 교차 시너지 테스트에서, 시험할 쌍의 첫 번째 항생제는 박테리아로 접종된 한천 판에 놓입니다. 제1 스트립에서 항생제를 허용한 후 플레이트(예: 1시간 후)를 주입한 후, 스트립이 제거되고 두 번째 항생제를 함유하는 새로운 스트립이 제1과 동일한 지점에 배치되어 두 개의 개별 MIC 값을 서로 위에 배치하도록 합니다. 결과 억제 영역은 전술한 바와 같이 분석될 수 있으며, 수학식 1을 기반으로 계산된 시너지 효과이다.
방정식 1 - 분수 억제 농도 (FIC)
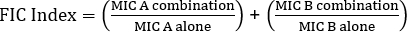
값 >0.5는 시너지 효과를 보여 줍니다.
분석하기 쉬운 플레이트로 심사관에게 보상하는 동안, 이 방법은 스트립의 변경뿐만 아니라 실험당 두 개의 플레이트를 사용해야 하기 때문에 다소 힘들고 시간이 많이 걸립니다. 대신, 교차 테스트는 종종 사용됩니다. 두 개의 서로 다른 E-테스트 스트립을 추가하는 대신(첫 번째 제거 후) 둘 다 동시에 동시에 배치되지만  교차(90° 각도)의 형태로 배치되며, 이전에 결정된 두 개의 MIC 값이 90° 각도를 형성합니다. 이 접근법에 의해 시너지 테스트당 하나의 플레이트만 필요하며, 적은 작업으로 분석하기가 약간 더 어려웠음에도 불구하고 선호하는 선택이 될 수 있습니다. 결합된 항생제 접근법에 있는 새로운 MIC 값은 수정된 억제 영역으로 시각화될 수 있고, 그 후에 시너지는 방정식 1에 의해 결정될 수 있다.
교차(90° 각도)의 형태로 배치되며, 이전에 결정된 두 개의 MIC 값이 90° 각도를 형성합니다. 이 접근법에 의해 시너지 테스트당 하나의 플레이트만 필요하며, 적은 작업으로 분석하기가 약간 더 어려웠음에도 불구하고 선호하는 선택이 될 수 있습니다. 결합된 항생제 접근법에 있는 새로운 MIC 값은 수정된 억제 영역으로 시각화될 수 있고, 그 후에 시너지는 방정식 1에 의해 결정될 수 있다.
한천 판 접근법을 사용하는 대신, 마이크로브로스 접근법은 종종 높은 유연성(예: E-test 스트립의 한계 밖에서 항생제의 특정 농도를 선택하는 능력)으로 인해 우선적일 수 있습니다. 또한, 마이크로브로스 검사는 고체 상(agar plate)내의 해리에 의존하지 않고 액체 용액에 항생제의 균등한 분포로 인해 더 민감하도록 제안된다. 96웰 마이크로플레이트의 우물은 정해진 수의 박테리아(106cfu/mL: 세균 농도는 OD600 nm 측정, 탁도 기준 또는 10x 세균 연쇄 희석제로부터 도금 시료를 확산시킴으로써 추정될 수 있음)으로 접종될 것이며, 다른 희석제의 항생제가 우물에 첨가될 것이다. 유사하게, E-test 스트립MIC는 박테리아의 눈에 보이는 성장을 억제하는 항생제의 가장 낮은 농도를 가진 교차(well/spot)로 결정된다.
실험 적 목표
- 아래 프로젝트는 페니실린 G의 MIC 값과 연쇄상 구균 그룹 G의 젠타미신을 두 가지 방법으로 결정하는 전략을 설명합니다. E-Test의 경우, 연쇄상 구균 그룹 G로 접종된 뮬러-힌튼 천 플레이트는 페니실린 G 및/또는 젠타미신의 그라데이션 스트립과 함께 사용되었습니다. MH-국물은 50% 용액 말 혈액과 20 mg/mL β-NAD를 마이크로브로스 접근법으로 연쇄상 구균 그룹 G와 함께 용해성 항생제로 사용하였다.
자료
- 혈액 한천 판에 세균성 식민지, 저장 <7 4°C
- 혈액 한천 접시
- 0.5 맥팔랜드 표준
- 1% 바클2
- 1% H2SO4
- 식염수 튜브 (2 mL)
- 면 팁 어플리케이터
- 뮬러-힌튼 한천 플레이트 (MHA 플레이트)
- 50% 용액 말 혈액과 20 mg /mL β-NAD (MH-F)와 MH 국물
- E-테스트 페니실린/젠타미신(또는 관심 있는 항생제) (BioMerieux, Marcy l'Etoile, 프랑스, 스웨덴)
- 항생제 페니실린/젠타미신(또는 관심 있는 항생제(분말/용액))
참고: 세균 성장에 사용되는 특정 미디어는 다른 종에 따라 다를 수 있습니다.
Procedure
1. 엡실로계 테스트 (전자 테스트)
-
설정
- 장갑과 랩 코트를 착용하십시오.
- 70% 에탄올을 사용하여 살균하여 작업 공간을 준비하십시오.
- 뮬러 힌튼 한천 접시 수집 (MHA 플레이트)
-
맥팔랜드 탁도 기준 0.5호기 준비
- 염화 바륨 1% 용액 준비 (BaCl2):
1그램 의 무수염 염화물(BaCl2)을100mL 증류수에 넣습니다. 소용돌이 잘. - 황산 1% 용액(H2SO4)을준비합니다.
증류수 99mL에 농축 H2SO4 1mL을 추가합니다. 소용돌이 잘. - 맥팔랜드 탁도 표준 No.5 준비:
50 μL BaCl2 용액5mL 1% H2SO4 용액. 용액을 잘 소용돌이쳐 탁탁 액수 서스펜션을 얻을 수 있습니다. - 호일 덮인 튜브에 맥팔랜드 탁도 표준 No.5를 유지하십시오. 최대 6개월 동안 25°C에 보관하십시오. 사용 전에 균질성 용액에 잘 소용돌이.
- 염화 바륨 1% 용액 준비 (BaCl2):
-
MHA 플레이트 준비
- 멸균 루프를 사용하여 혈액 천차 플레이트에서 연쇄상 구균 군 G 박테리아를 긁어. 식염수의 1mL에 혼합하고, 박테리아의 현탁액에 소용돌이.
- 서스펜션을 McFarland 표준 No.5와 비교하여 실험 중에 동일한 난접종 크기를 갖기 위해 동일한 탁도를 달성합니다. 추가 식염수 또는 박테리아를 사용하여 농도를 조정합니다.
- 멸균 면 팁 어플리케이터를 사용하여 MHA 플레이트를 접종하십시오. 표면을 덮기 위해 접시를 부드럽게 면봉합니다. 아래에 설명된 세 가지 방법 중 하나(1.4-1.6)를 진행한다.
-
단일 항생 저항 시험. 연쇄상 구균 그룹 G, 페니실린 G 또는 젠타미신에 대한 저항
- MHA 플레이트의 중앙에 E-테스트 스트립(페니실린 G 또는 젠타미신)을 놓습니다(그림1 A, B).
- 18-20 시간, 37 ° C에 대한 인큐베이션.
- 결과를 읽어보십시오. MIC는 등급이 매겨진 항생제 시험스트립(도 1 C,D)을교차하는 억제 영역으로 측정된다.

그림 1: 단일 전자 테스트. A) 페니실린 G와 B) 젠타미신의 E-test 스트립을 37°C 5%CO2에서그룹 G 연쇄상 구균(A 및 B)과 이후(C 및 D)야간 배양물의 세균 콜로니로 덮인 뮬러 힌턴 한고 플레이트에 배치한다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
-
시너지 테스트 교차 접근 방식. 연쇄상 구균 그룹 G, 페니실린 G와 젠타미신에 대한 저항.
- 교차 형성에 접종 된 MHA 플레이트에 다른 항생제 (예 : 페니실린 G 및 젠타미신)를 가진 두 개의 전자 테스트 스트립을 놓습니다.
- 가장 정확한 결과를 위해, 이전에 단일 항생제 내성시험(그림 2 A)에서결정된 그들의 MIC 값에 있는 저울 사이의 교차점에 대략 90° 각도로 십자가를 배치하는 것을 목표로 한다.
- 스트립이 한천 판에 놓이면 일부 항생제가 이미 접시에 흡수되었을 수 있기 때문에 이동해서는 안됩니다. 따라서 스트립을 약간 잘못된 각도(예: 85°)와 실제 MIC 값에서 최대 1-2mm로 유지하는 것이 더 적합합니다. 이 문제를 줄이기 위해 삼중에서 실험을 실행하는 것이 좋습니다.
- 18-20 시간, 37 ° C에 대한 인큐베이션.
- 결과를 읽어보십시오. MIC는 각각의 E-test스트립(도 2 B)에서등급이 매겨진 항생제 시험 스트립을 교차시키는 억제 영역으로 측정된다.
- 분수 억제 농도(FIC)(수학식 1)에대한 수식을 사용하여 시너지 효과를 결정합니다.
- 교차 형성에 접종 된 MHA 플레이트에 다른 항생제 (예 : 페니실린 G 및 젠타미신)를 가진 두 개의 전자 테스트 스트립을 놓습니다.

그림 2: 시너지 감지 - 교차 테스트. 37°C 5%CO2에서하룻밤 사이에 배양하기 전(A) 및 이후(B)배양에 대한 페니실린 G 및 젠타미신의 MIC의 항균 시너지 테스트 결과. 90° 각도는 두 개의 개별 MIC 값 사이에 형성됩니다 (페니실린 G: 0.094 μg/mL, 젠타미신: 8 μg/mL). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
-
교차가 아닌 접근 방식을 시너지 효과로 테스트합니다. 연쇄상 구균 그룹 G, 페니실린 G와 젠타미신에 대한 저항.
- MHA 플레이트의 중앙에 E-테스트 스트립을 놓습니다(그림3 A, D).
- 이전에 결정된 MIC 값이 각 스트립에 있는 위치를 표시합니다.
- 실온에서 1시간 동안 배양하십시오.
- 각 MHA 플레이트에 대한 E-테스트 스트립을 폐기합니다(그림3 B, E).
- 두 번째 E-테스트 스트립(다른 항생제 함유)을 각각 이전 제거된 스트립 영역에 배치하여 MIC 값이 마크에 대응하고 정렬되도록 합니다.
- 18-20 시간, 37 ° C에 대한 인큐베이션.
- 결과를 읽어보십시오. MIC는 각각의 E-테스트스트립(도 3 C,F)에서등급이 매겨진 항생제 시험 스트립을 교차시키는 억제 영역으로 측정된다.
- 시너지 효과를 결정하기 위해 분수 억제 농도(FIC)에 대한 포뮬러가사용된다(수학식 1).

그림 3: 시너지 감지 - 교차가 아닌 테스트. 연쇄상 구균 그룹 G에 페니실린 G와 젠타미신의 MIC의 항균 시너지 테스트의 결과. A) 연쇄상 구균 그룹 G 박테리아, B) 겐타미신 스트립의 제거, C) 결합 된 젠타미신 / 페니실린 G 스트립 (0.094 μg /mL 중심) 스트렙토 코커스 그룹 G 박테리아의 상단에, D) 페니실린 G 스트립 (0.094 μg/mL 중심), E) 페니실린 G 스트립의 제거, F) 결합 페니실린 G/젠타미신 스트립 (8 μg/mL 중심) 스트렙토 코커스 그룹 G 박테리아의 상단에. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
2. 국물 테스트
-
설정
- 장갑과 랩 코트를 착용하십시오.
- 70% 에탄올을 사용하여 살균하여 작업 공간을 준비하십시오.
- 15mL MH 국물을 50% 용액 말 혈액과 20 mg/mL β-NAD(MH-F)를 수집합니다.
-
(선택 사항) 고체 매체에서 MIC를 결정하기 위해 E-Test [프로토콜 1]을 수행합니다.
- 선택 사항이지만, 이러한 지식은 더 나은 실험 설계를 가능하게 할 것입니다 (예를 들어 추가 된 항생제의 농도는 플레이트에서 결정된 MIC 값을 둘러싸고 설계 될 수 있음), 성공적인 실험의 가능성을 향상시키게 합니다.
-
세균성 접종을 준비합니다. 위에서 언급한 바와 같이, 세균 농도는 OD nm 측정 또는 맥팔랜드 탁도 기준에 의해 추정될 수 있습니다.
-
OD600 nm 방법
- 확립된 세균 농도로 세균 현탁액 획득
- MH-F 국물에 있는 문화를 희석하여 0.003의 OD600을 달성합니다.
-
맥팔랜드 탁도 방법
- 멸균 튜브에 15mL MH-F 국물을 넣습니다.
- MH-F 국물을 박테리아(접시에서)로 맥팔랜드 수준으로 접종합니다. 적극적으로 용액을 소용돌이. 용액을 멸균 페트리 접시에 붓습니다.
-
OD600 nm 방법
-
항생제 준비
- 원하는 항생제의 농도 결정
- E-테스트에서 MIC 값을 식별합니다(예. 페니실린 G용 0.125 μg/mL, 젠타미신의 경우 8μg/mL)
- 식기 플레이트 MIC 값을 24-27로곱하여 4-7 2배 직렬 희석에 해당합니다. 이것은 항생제의 시작 농도가 될 것입니다. (예: 페니실린 G, 72x 직렬 희석: 0.125 μg/mL x 27 = 16 μg/mL; 젠타미신, 4개의 2x 직렬 희석 8 μg/mL/mL x24 = 128 μg/mL
- 항생제의 주식 농도를 생성하기 위해 원하는 시작 값 100x를 곱합니다(예: 주식 1.6 mg/mL 페니실린 G 및 12.8 mg/mL gentamicin)
- 그에 따라 100배 항생제 재고 농도 를 준비
- 항생제를 10mL 의 오토클레이브 워터에 녹여 서 주식 용액을 생성합니다(예: 16 mg 페니실린 G 및 128 mg 젠타미신)
- 원하는 항생제의 농도 결정
-
마이크로 플레이트 우물에 박테리아 추가
- Aliquot 200 μl MH-F 국물은 트리플리케이트 에서 실험을 위해 96웰 마이크로티터 플레이트의 처음 3행에서 우물에 박테리아 접종을 함유하고 있습니다.
-
마이크로 플레이트 우물에 항생제 추가
- 우물의 첫 번째 열(A1, B1, C1)에 박테리아가 있는 200 μL 추가 MH-F 국물을 추가하여 총 부피를 400 μL로 가져옵니다.
- 우물의 첫 번째 열에 항생제의 재고 농도의 4 μL을 추가합니다. 시료에 400 μL이 포함되어 있기 때문에 항생제의 100배 희석을 초래할 것이다.
- A1에서 A2로 200 μL 박테리아/항생제를 전송하여 2배 연속 희석을 생성합니다. 희석 사이에 적극적으로 파이프. 추가 행에 대한 단계를 반복합니다.
- 열 11에서 200 μL을 제거하여 모든 우물의 최종 부피가 200 μL이 되도록 합니다.
- 항생제없이 마지막 열 (A12, B12, C12)을 대조군으로 둡니다.
-
MIC 값 결정
- 흔들림 없이 37°C에서 24시간 동안 96웰 마이크로티터 플레이트를 배양합니다.
- MIC 값은 박테리아의 눈에 보이지 않는 성장을 나타내는 희석 계열의 마지막 우물로 정의된다(도4). 그러나 이 값은 원래 접종 크기가 올바른 경우에만 신뢰할 수 있습니다.

그림 4: 국물 희석에 의한 MIC 결정. MIC는 탁도를 변경하기 전에 명확성 (박테리아의 성장 없음)을 나타내는 마지막 우물로 정의됩니다. 행은 페니실린 G및 행의 MIC 값의 중복은 젠타미신의 MIC 값의 중복, 모두 연쇄상 구균 그룹 G. A의 분리 대, B) A로부터값의 회로도 해석 (회색 = 성장 없음; 흰색 = 성장). 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.

그림 5: 희석 계열의 회로도 절차는 원래 박테리아 농도를 계산합니다. 희석제는 설명된 바와 같이 수행되었다(180 μL에서 희석된 10배 희석 계열), 그리고 A-H행으로부터 10μL이 표시된 대로 두 개의 별도 혈액 천고 판에 도금된다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
-
원래 접종 크기 결정
참고: 마이크로브로스 어세이드는 사용되는 원래 의무문 크기에 매우 민감합니다. 과도 한 접종 크기는 거짓 긍정적인 결과 줄 것 이다, 항생제 추가 그 비율에 더 이상 성장을 억제 할 수 없습니다 이후. 따라서 마이크로웰에 얼마나 많은 박테리아가 추가되었는지 확인하는 것이 중요합니다. 실험 시점에서 데이터를 사용할 수 없지만(24시간 인큐베이션이 필요하기 때문에) 제어 역할을 합니다. 추가된 박테리아의 수가 명시된 농도 범위 내에 있는 경우 MIC 값을 신뢰할 수 있습니다. 접종이 너무 높거나 너무 낮은 경우 실험을 반복해야합니다.-
박테리아를 일련 적으로 희석
- 96웰 마이크로티터 플레이트를 준비하여 원래 세균 농도를 희석시켜 접종 크기를 결정합니다. 최적체는 105-6 박테리아를 가진 200 μL의 부피입니다. 희석을 수행하기 위해, 먼저 b-H (triplicate 1-3)에서 각 우물에 제1 aliquot 180 μL 멸균 PBS.
- 다음으로, 세균용 용액 100μl을 A에 추가합니다(트리플리케이트 1-3).
- 20 μl 박테리아를 A에서 B로 이송하여 10배 직렬 희석(삼중 희석)을 생성하여 적극적으로 파이펫을 생성합니다. C-H의 단계를 반복합니다.
-
접종 크기 측정을 위한 세균 희석제 플레이트
- 그림 5에따라 혈액 천 판을 표시합니다.
- 도 5에따라 직렬 희석에서 플레이트로 10 μL을 전송합니다.
- 플레이트를 37°C에서 20-24시간 동안 배양합니다.
-
세균성 접종 크기 결정
- 5-50 식민지 내의 반점에 세균 수를 계산합니다(그림 6).
- 삼중염 샘플의 평균을 계산하여 초기 접종 크기를 계산하고, 희석 계수(예: B 샘플의 경우 10배, C 샘플100배, D 샘플 1000x 등)에 곱한 다음 10μL의 스포팅 부피를 보정한 다음 100μL 크기의 ccuom/cl의 크기를 보정합니다. 접종이 105-6 cfu / mL 이내인 경우 MIC 데이터를 신뢰할 수 있습니다.
-
박테리아를 일련 적으로 희석

그림 6: 접종 크기 결정. 그림 5에 따라 접종된 박테리아는 37°C에서 20-24시간 동안 배양한 다음 계산하였다. 행 D에는 많은 수의 콜로니가 있습니다(예: 5-50). A의 샘플은 희석되지 않고, B는 10배 희석되고, C는 100배 희석되고, D는 1000배 희석되고, 각 지점에서 10μL만 도금된다. 이 그림의 더 큰 버전을 보려면 여기를 클릭하십시오.
항생제 감수성은 항생제에 대한 박테리아의 감도로 정의되며, E-test라고도 하는 국물 희석 검사 또는 엡실로미터 테스트를 사용하여 측정될 수 있다.
국물 희석 방법에서, 표준화된 수의 박테리아가 일련 항생제 희석제를 포함하는 성장 매체에 첨가된다. 민감하면 박테리아는 더 높은 항생제 농도에서 자랄 수 없지만 항생제 농도가 낮을 수록 항석이 됩니다. 박테리아가 더 이상 생존하거나 번식할 수 없는 가장 낮은 항생제 농도는 주어진 박테리아에 대한 항생제의 최소 억제 농도 또는 MIC로 지칭된다.
E-테스트에서, 항생제의 미리 정의 된 그라데이션함으로 함침 플라스틱 스트립은 뮬러 힌튼 한천에 박테리아의 갓 확산 잔디밭위에 적용, 또는 MH-A, 페트리 플레이트. 항생제는 박테리아에 의해 채택되는 천 매체로 확산. 취약한 경우 박테리아가 번식할 수 없으며 죽어가며 성장 억제 영역이라고 하는 E-스트립 주변의 명확한 영역을 형성합니다. 성장이 E-스트립과 교차하는 시점에서, 규모의 해당 값은 항생제의 MIC 값을 제공합니다.
종종 항생제는 박테리아의 항생제 내성 긴장의 출현을 방지하기 위해 조합에서 사용됩니다. 이것은 종종 시너지 효과를 초래, 오히려 첨가제보다, 효과. 시너지 효과는 두 항생제의 결합 효과가 개별 활동의 합보다 크다는 것을 의미합니다. 그러나, 항생제 조합의 MIC 값이 적어도 2배 감소하는 경우에만 효과가 유의하다고 여겨진다. 이러한 기준은 분수 억제 농도 또는 FIC 지수를 계산하여 평가된다. 각 항생제의 MIC의 비율을 개별적으로 합산함으로써, FIC 지수가 0.5 미만이 시너지 효과를 나타낸다.
항생제 시너지 효과는 두 가지 E-테스트 기반 방법을 사용하여 측정할 수 있습니다: 비교차 시험 또는 교차 테스트. 비 교차 테스트에서, 첫째, 소정의 MIC 값을 가진 두 개의 다른 항생제에 대한 E-스트립은 두 개의 별도의 플레이트에 적용됩니다. 항생제가 매체로 확산된 후, 원래 의 E-스트립이 제거되고 대체 항생제에 대한 E-스트립은 그들의 MIC 스케일이 이전 스트립의 MIC 저울 위에 정확하게 배치됩니다. 비교차 시험의 빠른 버전인 교차 테스트에서, 두 항생제의 E-스트립은 교차 형성에 함께 배치되어 MIC 마크의 비늘이 교차점에서 90도 각도를 형성합니다. 두 기술 모두에서 배양에 이어, 다른 항생제와 결합하여 각 항생제의 MIC 값은 성장 억제 영역이 E-스트립의 가장자리와 교차하는 지점에서 읽습니다. 그런 다음 FIC 인덱스가 계산됩니다.
이 비디오는 E-테스트 및 마이크로 국물 희석 테스트를 사용하여 주어진 박테리아에 대한 주어진 항생제의 MIC 값을 결정하는 방법을 보여줍니다. 또한 교차 검사와 비 교차 테스트를 사용하여 두 항생제 간의 시너지 효과를 결정하는 방법을 배우게 됩니다.
먼저 실험실 장갑과 실험실 코트를 포함한 적절한 개인 보호 장비를 착용하십시오. 다음으로, 70% 에탄올을 사용하여 작업 공간을 살균합니다. 다음으로, 멸균 된 뮬러 힌턴 국물 15 밀리리터를 50 % lysed 말 혈액과 밀리리터 베타 니코티나미드 당 20 밀리그램을 수집합니다. 그리고 5~8개의 뮬러-힌턴 한천 접시. 이제 맥팔랜드 탁도 표준 번호 0.5를 준비하기 위해 1 % 황산 용액의 9.95 밀리리터를 측정하십시오. 그런 다음 염산 용액에 염화염 1% 바륨 용액의 50 마이크로리터를 추가합니다. 용액을 잘 소용돌이하여 탁탁액을 얻을 수 있습니다. 튜브를 알루미늄 호일로 덮고 따로 둡니다. 다음으로 식염수 용액 1밀리리터를 15밀리리터 튜브에 분배합니다.
멸균 루프를 사용하여 세균 성 테스트 플레이트에서 세균 성장 샘플을 긁어, 여기, 연쇄상 구균 그룹 G. 그런 다음 박테리아가 함유된 루프를 식염수 용액에 넣고 부드럽게 저어준 다음 튜브를 잘 소용돌이시습니다. 지금, 세균 성 현탁액및 맥팔랜드 탁도 기준을 나란히 놓고 탁도 동등성에 대해 비교하십시오. 세균 현탁액의 탁도가 표준의 것과 일치할 때까지 추가 식염수 또는 세균성 식민지를 추가합니다. 원하는 탁도를 얻으면 멸균 면 팁 어플리케이터를 세균 현탁액에 담급드세요. MH-A 플레이트를 접종하려면 지그재그 동작으로 플레이트 전체 표면을 부드럽게 헤징합니다. 다음으로, 박테리아와 날짜의 이름으로 플레이트의 하단 측면을 레이블.
시작하려면 페니실린 G E-테스트 스트립을 꺼내서 집게로 가장자리를 잡습니다. 갓 헤비한 MH-A 플레이트의 중앙에 스트립을 부드럽게 놓고 뚜껑을 교체합니다. 이 예에서, 두 번째 항생제, 젠타미신은 또한 시험됩니다. 따라서, 스트립 배치 과정은 제2 플레이트 및 겐타미신 E-테스트 스트립으로 반복된다. E-테스트 결과를 확인하려면 페니실린 G E-테스트 스트립을 포함하는 첫 번째 플레이트를 수집합니다. 지금, 억제 영역이 항생제 스트립과 교차하는 지점을 결정합니다. 축척에서 해당 숫자 값을 읽습니다. 이 값은 페니실린 G.의 MIC 값을 나타내며 젠타미신에 대한 MIC 값을 동일한 방식으로 결정합니다.
시작하려면, 연쇄상 구균 그룹 G 변형 박테리아와 MH-A 플레이트를 접종. 박테리아의 이름으로 접시의 바닥을 레이블, 항생제사용, 그리고 날짜. 지금, 플레이트의 중심에 관심의 항생제에 대한 E-테스트 스트립을 배치. 그런 다음 두 번째 테스트 스트립을 90도 각도로 첫 번째 스트립에 고정하고 MIC 마크를 찾습니다. 두 MIC 값이 교차하는 지점에서 두 번째 E 스트립을 첫 번째 에 부드럽게 놓습니다. 스트립이 배치되면 스트립을 이동하지 마십시오. 다음으로, 18~20시간 동안 섭씨 37도에서 플레이트를 배양합니다.
연쇄상 구균 그룹 G 균균 박테리아와 함께 두 개의 MH-A 플레이트를 접종 한 후 한 판의 표면에 하나의 항생제에 대한 E 테스트 스트립을 배치합니다. 이어서, 입증된 바와 같이 다른 항생제에 대한 E-test 스트립을 두 번째 플레이트에 놓는다. 플라스틱 접종 루프를 사용하여 각 판의 표면에 각 항생제의 MIC 값을 표시합니다. 다음으로 접시를 덮고 실온에서 1 시간 동안 배양하십시오. 이 후, E 스트립을 제거하기 위해 집게를 사용합니다. 다음으로, 다른 항생제에 대한 플레이트 중 하나와 E-테스트 스트립을 수집합니다. 첫 번째 스트립이 남긴 각인 위에 E-test 스트립을 잡고 E 스트립의 MIC 값이 표시된 선과 정렬되는 지점을 찾습니다. 이 교차 점에 스트립을 부드럽게 놓습니다. 두 번째 플레이트에 대해 이 과정을 반복하고 두 플레이트를 섭씨 37도에서 18~20시간 동안 배양합니다.
먼저, 확립된 세균 농도를 가진 세균현탁액을 획득하고 MHF 국물에 배양을 희석하여 0.003의 OD600을 달성한다. 다음으로, 체중 16 페니실린 G의 밀리 그램과 128 겐타미신의 밀리그램. 215 밀리리터 원판 튜브로 각 무게 건조 항생제를 전송합니다. 각 원물 튜브에 증류수 10밀리리터를 넣고 소용돌이에 잘 섞습니다. 항생제 이름과 농도로 튜브에 라벨을 붙입니다.
triplicate에서 분석법을 수행, 96 웰 마이크로 티터 플레이트의 세 행의 첫 번째 우물에 작업 세균 용액의 400 마이크로 리터를 추가합니다. 다음으로, MHF 국물에 작동하는 세균 용액 200마이크로리터를 3열의 우물에 추가합니다. 지금, 2 배 연속 항생제 희석을 생성하기 위하여는, 첫번째 우물에 항생제 주식의 4개의 마이크로리터를 추가하여 100 배 희석을 생성합니다. 순차적으로, 세균-항생제 용액 200마이크로리터를 각 우물로 옮기고, 첫 번째 우물부터 두 번째 행까지 각 행에서 잘 지속되도록, 매 번 전달후 2~3회 피펫팅하여 적절한 혼합을 보장한다. 박테리아 항생제 용액의 마지막 200 마이크로 리터를 폐기하십시오.
페니실린 G에 대한 국물 마이크로 희석 테스트의 결과를 결정하기 위해, 먼저 탁도의 부족으로 표시된 눈에 보이는 세균 성장을 나타내는 우물을 찾습니다. 이 우물에서, 가장 낮은 항생제 농도와 우물을 식별. 이것은 시험된 박테리아를 위한 페니실린 G의 MIC 값을 나타냅니다. gentamicin의 MIC 값은 동일한 분석 및 기술을 사용하여 결정될 수 있습니다.
비 교차 테스트의 결과를 확인하려면 페니실린 G E 스트립을 포함하는 첫 번째 플레이트를 수집합니다. 이어서, 성장 억제 영역이 항생제 스트립과 교차하는 지점을 결정한다. 스케일의 해당 값은 젠타미신과 함께 페니실린 G에 대한 MIC 값을 나타냅니다. 이 예에서, 조합된 MIC 값은 밀리리터당 0.064 마이크로그램이다.
이제 젠타미신 E 스트립을 포함하는 두 번째 플레이트를 수집하고 이전에 설명한 대로 MIC 값을 조합하여 결정합니다. 조합의 효과를 평가하기 위해, 먼저 항생제의 MIC에 의해 조합하여 페니실린 G에 대한 분수 억제 농도 또는 FIC를 계산한다. 젠타미신에 대한이 과정을 반복합니다. 그런 다음 여기에 표시된 방정식을 사용하여 FIC 인덱스를 계산합니다. 조합에서 MIC 값이 2배 감소하면 FIC 지수 값이 0.5 미만이거나 동일하며 페니실린 G와 젠타미신 간의 시너지 효과를 보여줍니다. 이 경우 계산된 FIC 값은 0.5보다 큰 1.18입니다. 따라서, 결과는 연쇄상 구균 그룹 G 균주에 대한 페니실린 G와 젠타미신 사이의 시너지 효과를 보여주지 않는다.
교차 테스트의 결과를 결정하기 위해 먼저 성장 억제 영역이 각각의 E 스트립과 교차하는 지점을 결정합니다. 이 교차점에 해당하는 각 E-테스트 스트립의 숫자 값을 읽어보십시오. 이러한 값은 페니실린 G와 젠타미신을 조합하여 MIC 값을 나타냅니다. 다음으로 조합의 효과를 평가하려면 여기에 표시된 방정식을 사용하여 FIC 인덱스를 계산합니다. 이 예제에서는 계산된 FIC 값이 0.5보다 큰 1.18입니다. 즉, 페니실린 G와 젠타미신은 연쇄상 구균 그룹 G 변형에 대해 시너지 효과를 발휘하지 않는다는 것을 의미합니다.
Subscription Required. Please recommend JoVE to your librarian.
Results
E-테스트에서 MIC 값
개별 MIC 값은 페니실린 G 및 8 μg/mLfor 젠타미신에 대해 도 1에서 0.094 μg/mL로 확인되었다. 시너지 효과 테스트의 경우, 둘 다 0.064 μg/mL(그림2, 3)의페니실린 G에 대한 MIC 값을 입증했으며, 젠타미신은 교차 및 비교차 테스트를 위한 MIC 4 μg/mL을 가졌다. 두 설정에서 스트립의 다른 배양 시간으로 인해 교차 테스트와 비 교차 테스트 간의 약간의 불일치가 발생할 수 있습니다.
시너지 계산
FIC의 방정식은 다음과 입니다.
 = 1.18 >0.5 (시너지 없음)
= 1.18 >0.5 (시너지 없음)
국물에 MIC 결정
우물의 흐림은 세균 성장을 나타내었고, 따라서 억제가 발생하지 않았다. 페니실린 G(도 4)와함께 첫 번째 명확한 잘 포함 0.12 μg /mL 페니실린 G, 따라서이것은 MIC 값이었다. 젠타미신의 경우 첫 번째 맑은 우물은 8 μg/mL 젠타미신에 존재했다. 페니실린 G 값은 스트립의 높은 해상도로 인해 E-test를 사용할 때보다 약간 높았습니다(예: 2배 인자가 아닌 1.5x 계수 직렬 희석기준).
이노큐럼 크기
접종 크기를 확인하려면 그림 5 및 6에 설명된 접근 방식이 사용되었습니다. 콜로니는 D-행(1000x 희석)으로 계산되어 평균 값인 7.67 cfu를 가진 트리플리케이트 시리즈에서 최대 7, 8, 8을 추가했습니다. 희석 계수(예: 1000x)와 100개의 cfu/mL을 얻기 위해 100개의 콜로니수를 곱하여 약 8 x105의접종 크기를 제공하여 105-6 cfu/mL의 표적 접종 크기 내에서 도포하였다.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
항생 저항은 세계적인 건강 문제입니다. 미생물의 저항 기전을 결정하기 위하여는, 다른 항생제를 가진 시너지 및 길항증을 위한 방법 시험은 중요합니다. E-test 방법은 빠르고 복제하기 쉬우며 조합 요법의 시너지 잠재력을 조사하는 데 사용할 수 있습니다. 국물 희석 방법은 또한 bactericidal 활동을 예측하기 위하여 평가될 수 있습니다. 다른 미생물의 저항 메커니즘을 조사하기 위해, 시너지 효과와 길항성 항생제 상호 작용의 지식은 매우 중요합니다. 항생제를 결합하는 것은 치료 효능을 증가시키고 항생제 저항에 직면하는 전략일 수 있습니다. 여기에서 수행된 시험에서는, 우리는 그룹 G 연쇄상 구균에대한 페니실린 G와 젠타미신의 MIC 값을 결정할 수 있었습니다. 우리는 또한 2개의 항생제가 시너지 효과를 표시하지 않는다는 것을 보여주었습니다, 따라서 그 같은 감염을 위한 바람직한 처리 선택권이 되지 않을 것입니다.
Subscription Required. Please recommend JoVE to your librarian.
References
- Tan SY, Tatsumura Y. Alexander Fleming (1881-1955): Discoverer of penicillin. Singapore Medical Journal. 56 (7):366-7. (2015)
- Aminov RI. A brief history of the antibiotic era: lessons learned and challenges for the future. Frontiers in Microbiology. 1:134. (2010)
- Pankey GA, Ashcraft DS, Dornelles A. Comparison of 3 E-test (®) methods and time-kill assay for determination of antimicrobial synergy against carbapenemase-producing Klebsiella species. Diagnostic Microbiology and Infectious Disease. 77 (3):220-6. (2013)
- EUCAST: European Committee On Antimicrobial Susceptibility Testing (www.eucast.org).
- Wiegand I, Hilpert K, Hancock RE. Agar and broth dilution methods to determine the minimal inhibitory concentration (MIC) of antimicrobial substances. Nature Protocols. 3 (2):163-75. (2008)
- Doern CD, When does 2 plus 2 equal 5? A review of antimicrobial synergy testing. Journal of Clinical Microbiology. 52 (12):4124-28. (2014)
- Worthington RJ, Melander C. Combination approaches to combat multi-drug resistant bacteria. Trends in Biotechnology. 31 (3):177-84. (2013)




