Overview
资料来源: 实验室的博士 Andreas Züttel-瑞士联邦实验室材料科学与技术
理想气体定律描述最常见气体在附近环境条件下的行为和所有化学物质在稀释极限下的趋势。它在系统中,是三个可衡量宏观系统变量 (压力、 温度和体积) 与气体分子的数目之间的基本关系,因此是微观和宏观的宇宙之间必不可少的环节。
理想气体定律的历史可以追溯到17 世纪中叶时候的压力和体积的空气之间的关系被发现是成反比,证实了由罗伯特 · 波义耳和我们现在称之为 · 博伊尔的法律 (方程 1) 的表达式。
P 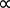 V-1 (方程 1)
V-1 (方程 1)
发表的作品,由雅克 · 查尔斯在 1780 年代,并被给予大量的气体和蒸气的约瑟夫 · 路易斯 · 吕报道于 1802 年,成立的绝对温度和气体体积的正比关系。这种关系称为查尔斯的法律 (方程 2)。
V 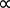 T (方程 2)
T (方程 2)
纪尧姆 · Amontons 通常归功于18 世纪初第一次发现固定体积内空气的压力与温度的关系。这项法律还向许多其他气体由约瑟夫 · 路易斯 · 吕19 世纪初,因此也被称为 Amontons 的法律或同性恋者 Lussac 法,指出方程 3中所示。
P 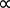 T (方程 3)
T (方程 3)
在一起,可以结合这三组关系给关系方程 4中。
V 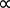 T (方程 4)
T (方程 4)
最后,在 1811 年,它提出了阿米阿佛加德罗任何两种气体,在相同的体积和在相同的温度和压力,举行包含相同数目的分子。这导致所有气体可以通过一个共同的常数,理想气体常数 R,即独立的气体的性质进行都描述的结论。这就是所谓的理想气体定律 (方程 5)。1,2
PV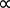 T (方程 5)
T (方程 5)
Principles
理想气体定律,因此其特性的不断研发,可也雄辩地从第一原理理论在许多方面,分子有没有固有的卷和不进行交互的重要的简化假设在哪里。这些假设有有效稀释物质限制,在什么地方空每个分子 (例如~ 10-23 L 在环境条件下) 所占用的空间量远大于分子本身 (~ 10-26 L),哪里的相互作用是不大可能。它因此可以很容易在通过各种方式使用普通实验室设备在室温,证明,可准确地测量各种气体在压力甚至 10 条 (图 1)。然而,理想气体定律不能准确地考虑和在附近环境条件下 (例如,丙烷) 密度气体的性质或冷凝,因分子间相互作用而产生的现象。为此,许多更详细的状态方程的年以来它的发现,通常降低到理想气体定律在稀事极限成功理想气体定律。1,2

图 1。理想气体法密度对各种其他常见气体在 25 ° C 和 0-100 之间的比较栏。
在本教程中,我们仔细地将测量氢气在增加的压力和温度固定体积内的密度由称重的已知体积的悬浮固体样品: 精确加工的铝块。在样品重量的变化是直接关系到改变流体的密度,在其中它浮动的由阿基米德定律。我们还将演示在高压下使用较少的理想气体 (如二氧化碳) 的缺点。最后,我们将直观地演示,并定性地通过执行一个简单的台式实验,由于氢释放的贮氢材料,系统体积的变化测量确认理想气体定律。使用任意一种的这些实验,我们可以确定描述压力、 温度和气体 — — 理想气体常数,R.给定数量的卷之间的关系的通用的常数
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1.测量体积的样品
- 仔细清洁样品和干燥它。
- 一个高分辨率的量筒装满足够蒸馏水覆盖样品。请注意初始音量
- 掉进了水的样本,并注意体积的变化。这是样本体积,V。
- 删除示例然后擦干。注意: 或者,测量样品的侧 length(s),并计算其体积使用几何。
2.负载平衡中的示例
- 挂在磁悬浮平衡样品。
- 安装压力/温度室围绕样品。
- 撤离的示例环境和加氢气,到 1 栏。
- 测量样品重量在 1 酒吧和室温下,w00。
3.测量样品重量为常温压力的函数
- 增加或减少在 Pi0样品环境压力。
- 允许样品环境平衡。
- 测量样本,wi0的重量。
- 3.1-3.3 重复无数次。
4.测量样品重量作为压力在不同温度下的函数
- 设定的温度为 Tj并允许它保持平衡。
- 设置的氢气压力为 1 个酒吧。
- 测量样品重量在 1 酒吧和 Tj,w0j。
- 增加或减少的压力 Pij ,允许它平衡。
- 测量的样本,wij重量。
- 4.4-4.5 重复无数次。
- 重复 4.1-4.6 作为所需。
5.计算理想气体常数
- 统计测量的值 {Tj、 Pij和 wij} P0j总是 1 栏,T0是实测的室温。
- 计算并制成表格的差异 Δwij和 δ Pij在每个温度 Tj使用6 方程和方程 7。
Δwij = wij - w0j (方程 6)
Δwij = Pij - P0j = Pij -1 酒吧 (方程 7) - 计算 Rij为每个度量值和平均以上所有的值来确定理想气体常数,R.或者,情节 δ Pij与 V 的乘积作为 Δwij (除以分子量 MW) 产品的功能和 Tj,和氢为执行线性回归分析,以确定边坡,R.(方程 8和9)MW = 2.016 g/mol。
ΔP V = Δn RT (方程 8)
 (方程 9)
(方程 9)
理想气体定律是科学中的一种基本的有用的关系,因为它描述了最常见的气体,在附近环境条件下的行为。
理想气体定律,PV = nRT,定义在一个封闭的系统中的气体分子的数量和可量测系统的三个变量之间的关系: 压力、 温度和体积。
从第一原理推导理想气体定律,依赖于两个假设。第一,气体分子本身有没有卷。第二,分子从来没有交互,或者交换能量。气体偏离这个理想的行为,在高压下,在气体密度的增加,和真实气体分子的体积变得重要。同样,气体偏离在极低温度下,哪里有吸引力的分子间相互作用变得重要。较重的气体可能偏离甚至在环境温度和压力,因为他们更高的密度和较强的分子间相互作用。
这个视频将实验,确认理想气体定律测量气体温度和压力的函数作为密度改变。
理想气体定律推导出四个重要关系。首先,波义耳法描述气体体积与压力成反比关系。接下来,同性恋者 Lussac 定律,温度和压力是比例。同样,查尔斯的法律是温度和体积之间相称性语句。这三组关系形成联合的气体定律,使单一气体比较跨许多不同的条件。
最后,阿佛加德罗确定任何两种气体,在相同的体积、 温度和压力,举行包含相同数目的分子。因为在相同条件下的气体通常具有相同的行为,可以发现常数的相称性,称为通用气体常数 (R),涉及这些参数,使各种不同的气体比较。R 有能量的单位每温度每个分子;例如,焦耳每开尔文每摩尔。
理想气体定律是一个宝贵的工具,在了解国家之间的关系在气体系统。例如,在恒定的温度和压力的系统中,更多的气体分子的加法结果量增大。
同样,在恒定的温度,在一个封闭的系统,在那里没有分子添加或减去,气体的压力增加时体积下降。
磁悬浮平衡可以用于确认理想气体定律实验通过测量系统的物理特性。恒定的质量和体积的固体样品的重量可以作为探针在它附近的气体的性质。
随着压力的增加在系统中,在定常系统体积和温度,系统中的气体分子的数量增加,从而增加气体密度。刚性的固体样品,淹没在这种气体是受浮力,和它明显的重量减少,虽然它的质量是不变。阿基米德原理,物体重量的变化是等于流离失所的气体重量变化可以就确定气体密度的变化。
在不同压力和温度条件下气体密度的精确行为将对应于理想气体定律如果先前描述的近似为真,能够直接计算出普遍的气体常数,。
在以下一系列实验,电子天平将用于确认理想气体定律和确定通用的气体常数 R,通过测量密度的氢作为温度和压力的函数。首先,仔细清洁样本,在这种情况下的精细加工的铝块,用丙酮,和干燥.通过填充一个毕业测量体积的样品缸有足够蒸馏水覆盖样品。请注意初始音量。沉浸在水中,样品,并注意体积的变化。
删除仔细清洁和干燥的样品。下一步,加载到磁悬浮平衡,在这种情况下位于手套箱内。安装压力-温度室围绕样品。示例现在磁悬浮在一个封闭的系统,不触碰到任何墙。
撤离的示例环境和加氢气压力 1 栏。
测量样品重量,并贴上标签的初始重量在室温。接下来,增加到 2 栏示例环境中的压力,并允许它保持平衡。测量重量为新的压力。重复这些步骤多次在各种压力,以获得一系列的样本权重在相应的压力下,所有在室温。
下一步,测量重量作为压力在较高温度的函数。首先撤离样品环境,然后将温度增加到 150 ° C 并允许它平衡。然后,增加到 1 栏的压力。测量样品的重量,并贴上标签作为初始重量为 150 ° C 和 1 间酒吧。增加的压力,让它保持平衡,和量度的重量。为了测量一系列的样本权重的压力范围内重复这些步骤。若要获取更多的数据,请重复在其他恒定的温度和压力的重量测量系列。
若要计算理想气体常数,制成表格在每个温度和压力的样品重量的测量的值。
下一步,计算所有成对的样本权重内获得所有可能组合的重量变化作为变化的压力或 Δw 的功能,设置单一温度之间的差异。这种变化是相当于氢气,流离失所的样品重量的变化。
同样,计算所有相应的区别,在获得压力或 δ P 变化的压力。列出所有成对的重量和压力为每个温度的变化。转换温度单位为开尔文和帕斯卡压力单位。
由于体积与温度保持不变,每个系列的测量,理想气体定律可以写为 ΔPV = ΔnRT。由于 δ n 等于 Δw 除以氢分子重量,计算每个值 δ n Δw 的每个值。
绘制压力变化的产物和抽样量,作为产品的 δ n 和温度的函数。执行线性回归分析,以确定边坡,将平等普遍的气体常数,如果做得正确。
理想气体状态方程用于许多现实世界场景中,通常是那些执行与在环境温度和压力的气体。所有气体都偏离理想的行为,在高压力;然而,一些气体,如二氧化碳,偏离比别人更多。在这个实验中,理想的行为偏离测量气体中的二氧化碳。程序是与氢以前实验相同。
情节与痣次温度压力倍体积策划,和理想气体常数计算从情节的边坡。二氧化碳显著偏离理想的行为,即使在环境条件下。这种行为被造成的有吸引力的分子间相互作用,没有观察到的与氢。
理想气体定律用于识别和量化的爆炸性气体的空气样本。这一研究领域是极端重要的军事和安全。
在这里,炸药成分的气体样品进行量化温度解吸气体色谱法。然后用数据,以及理想气体定律来量化这些危险物质。
你刚看了理想气体定律的朱庇特的简介。看过这个视频,你应该了解的概念的法律和方程适用的情况。
谢谢观赏 !
Subscription Required. Please recommend JoVE to your librarian.
Results
理想气体定律是有效的描述实际气体性质的许多常见气体在附近环境 (图 1插图) 条件的因此在很多应用程序的上下文中很有用。理想气体定律描述高压力或温度低的条件下系统的局限性可以解释由分子间的相互作用的日益重要性和/或有限大小的气体分子系统的性能作出贡献。因此,与强、 有吸引力的分子间相互作用 (如偶极-偶极相互作用,包括氢键、 离子-偶极相互作用或范德瓦尔斯相互作用所引起) 的气体会表现出更高的密度比理想气体。所有气体都亦会令人厌恶的组件在密度高,多个分子不能占用相同的位置,放款超过理想气体的密度减少。气体,如氢和氦所示的更大的贡献,从排斥力有限的分子尺寸,由于,因此在高压力下稍低密度。甲烷和二氧化碳给更多贡献他们的属性从相互的吸引作用,贷款他们更高的密度比理想气体直到非常高的压力,在那里令人厌恶的词占主导地位 (在很多高于 100 栏在 25 ° C)。

图 2。平衡吸附吸收等温线的 CO2对高比表面积,椰壳碳 MSC-30,在 25 ° c。
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
理想气体定律是化学的科学,它具有大量的使用在日常实验室活动以及计算和建模的甚至高度复杂的系统,至少第一近似的基本方程。其适用性有限只能由逼近固有的法律本身;在附近环境的压力和温度,在理想气体定律哪里好有效的许多共同的气体,它广泛采用气体为基础的系统和过程的解释。两个例子的经营原则,这可以通过调和的设备使用的理想气体定律,气体温度计和斯特林发动机。
一个特定的应用程序是在测量气体吸附 (吸附) 的数量在固体材料的表面上。吸附是固体与气体之间的吸引力分子间相互作用 (色散力) 的物理现象,藉以气体分子离开气相和进入致密表面附近的固体 (或也许是一种液体) 阶段。吸附作用对于许多散装材料 (如玻璃和不锈钢) 钢在环境条件下,可以忽略,但变得非常重要,为多孔材料与访问表面积大,尤其是在低温。3容积弗法和重量法量化物理吸附的依靠知道系统的气体状态方程。在低压力和环境温度,理想气体定律对许多气体,有效和可以用来准确地确定的气体的吸附的量以类似的方式确定 R 上述协议中所述。例如,在重力测量的高比表面积,理想气体法事实上有效,Δw实际之间的差异的测量的条件下脱硫剂和 Δw理想浮力的计算使用理想的状态方程可以归因于重量的吸附相的变化。(方程 10)平衡气体吸附等温线因而可测定制表此偏差、 Δw广告,作为在一个固定的温度压力的函数 (见图 2),在多孔材料表征的标准程序。
Δw广告= Δw实际-Δw理想(方程 10)
Subscription Required. Please recommend JoVE to your librarian.
References
- Zumdahl, S.S., Chemical Principles. Houghton Mifflin, New York, NY. (2002).
- Kotz, J., Treichel, P., Townsend, J. Chemistry and Chemical Reactivity. 8th ed. Brooks/Cole, Belmont, CA (2012).
- Rouquerol, F., Rouquerol, J., Sing, K.S.W., Llewellyn, P., Maurin, G. Adsorption by Powders and Porous Solids: Principles, Methodology and Applications.Academic Press, San Diego, CA. (2014).





 (方程 9)
(方程 9)