Overview
Source : Laboratoire de Dr. Yuriy Román, Massachusetts Institute of Technology
Un potentiostat/galvanostat (souvent dénommée simplement un potentiostat) est un instrument qui mesure actuelle à un potentiel appliqué (opération potentiostatique) ou des mesures potentielles à un courant appliqué (opération galvanostatique) (Figure 1). C’est l’instrument le plus couramment utilisé dans la caractérisation électrochimique des matériaux de l’anode et la cathode pour piles à combustible, électrolyseurs, batteries et supercapacités.
Classiquement, ces matériaux d’anode et la cathode est interfacé avec un potentiostat via une cellule électrochimique de trois électrodes. Les fils des électrodes de la potentiostat sont connectés à l’électrode de référence, la contre-électrode (souvent appelé l’électrode auxiliaire) et l’électrode de travail (qui contient le matériel de test d’intérêt). La cellule électrochimique est ensuite remplie avec une solution d’électrolyte de force ionique élevée, telle qu’une solution acide, alcaline ou sel. Les médias pour cette solution de force ionique élevée sont généralement aqueuse ; Toutefois, pour les applications nécessitant plus d’exploitation windows potentiels cellulaires, tels que des batteries et supercapacités, non aqueux, est souvent utilisé. Les médias de la cellule sont dégazé avec un gaz inerte (pour éviter les réactions secondaires indésirables) ou avec un gaz d’essai (si l’essai la réaction implique un gaz dans l’une des électrodes).
Alternativement, un pont salin ou une membrane sert à maintenir le contact ionique si les deux demi de cellules doivent être mesurées en différents électrolytes. Dans électrocatalyse hétérogène, ce type de cellule « deux compartiments » est souvent utilisé si la molécule de test à l’électrode de travail est également réactive à la contre-électrode. Cela arrive fréquemment que la contre-électrode généralement employée est de platine, qui est un catalyseur très actif de nombreuses réactions. Ici, les cellules dans un compartiment unique est utilisés, où tous les trois électrodes sont dans le même support.
Cette vidéo vous expliquera le processus de polissage d’une électrode de travail, préparer une encre de catalyseur, fixation de l’encre de catalyseur sur l’électrode de travail, préparer la cellule électrochimique et effectuer ensuite des mesures électrochimiques. Les mesures effectuées comprennent : voltampérométrie cyclique (CV), voltamétrie à balayage linéaire (LSV), chronopotentiométrie (CP) et la chronoampérométrie (CA).
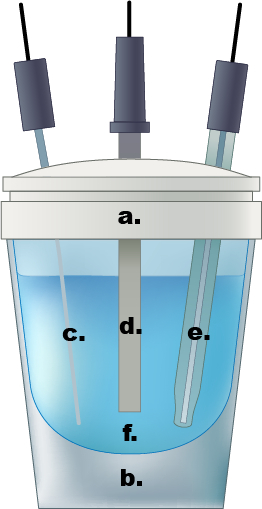
Figure 1. Un exemple d’une cellule électrochimique de compartiment unique. bouchon Teflon a.), b.) verre cellulaire, c.) PT fils contre-électrode, d.) électrode de travail, e.) Électrode de référence Ag/AgCl, f.) 0,5 solution d’électrolyte de l’acide sulfurique aqueux M.
Principles
Le potentiostat peut être utilisé pour appliquer une constante anodique ou cathodique potentiel à l’électrode de travail et de mesurer le courant anodique ou cathodique qui en résulte (chronoamperométrie) ou le potentiostat peut être exploités de façon via une boucle de rétroaction contrôle et appliquer un courant anodique ou cathodique constant avec le potentiel mesuré variant avec le temps de maintenir cela s’applique actuel (chronopotentiométrie). Sinon, espace potentiel peut être exploré avec le temps à l’aide de voltampérométrie cyclique ou voltamétrie à balayage linéaire pour mesurer le potentiel anodique et cathodique par rapport à une vitesse de balayage potentiel appliqué (la dérivée du potentiel en fonction du temps).
Dans toutes ces techniques, même pendant le travail galvanostatique, le potentiostat contrôle du potentiel appliqué et mesure le flux d’électrons de (à) l’électrode de travail à (de) la contre-électrode lorsque l’électrode de travail agit comme l’anode (cathode). Le potentiel appliqué est référencé contre l’électrode de référence, qui contient un système d’oxydoréduction (par exemple, une électrode de chlorure d’argent ou de l’électrode au calomel saturée) avec un potentiel connu et stable qui est interfacé avec la solution d’électrolyte via une fritté poreuse. En fonctionnement normal, le potentiostat dessine un courant négligeable mais non nuls, par le biais de l’électrode de référence ainsi qu’un potentiel exact peut être appliqué à l’électrode de travail. Alors que le potentiostat mesure le flux d’électrons ou de réaction de moitié à l’autre, la solution d’électrolyte termine le circuit en empêchant l’accumulation de la charge à l’anode ou la cathode.
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. catalyseur encre et préparation de l’électrode de travail
Consignes de sécurité : Métaux pris en charge sur le noir de carbone peuvent être aspirés dans une enceinte de hood ou équilibre de fumée jusqu'à ce qu’il soit sous forme de suspension que ces poudres sont des dangers de l’inhalation.
- À l’aide d’une balance ci-joint, peser 5 à 10 mg de catalyseur métal/noir de carbone et ajouter un flacon en verre avec un bouchon.
- À l’aide d’une micropipette, diluer le catalyseur avec de l’eau telle que la concentration finale est de 7,5 mg de catalyseur par mL d’eau.
- Tandis que la sonification, 100 µL de solution Nafion 117 / mL de l’eau est ajoutée à la suspension.
- L’encre doit être soniquée pendant au moins 10 min assurer la dispersion uniforme et mélange de l’appui de noir de carbone avec l’agent liant complet.
- Alors que l’encre est sonification, une électrode à disque 3 mm carbone vitreux Nettoyez et polie par le frottement dans un mouvement circulaire qui tournoie sur un tampon doux alumine recouverte de 0,05 solution d’alumine µm. Il puis rincer abondamment à l’eau pour enlever l’alumine.
- Ensuite, 7 µL d’encre est dégoutté sur une électrode à disque carbone vitreux brillant, orientés verticalement 3 mm. L’électrode de travail est ensuite séché à 80 ° c pendant 1 h si le catalyseur est stable à l’air ou évaporé sous un vide faible pendant 30 min si le catalyseur est sensible à air.
2. cellule électrochimique préparation
Consignes de sécurité : Gants, blouse et lunettes de sécurité doivent être portés en permanence, mais est surtout primordiale pour travailler avec la solution d’acide sulfurique. Si des gouttes de solution se renverse sur les poignets, il doit être lavé avec du savon et l’eau pendant 15 minutes. Pour les grands déversements, enlever les vêtements contaminés et l’utilisation de la douche oculaire ou douches doivent servir pendant 15 min, suivie d’une consultation médicale. Les fils électriques ne devraient pas être touchés une fois placé dans la cellule électrochimique.
- Une cellule de verre est remplie avec 10 mL de 0,5 M H2SO4 et dégazé pendant au moins 30 minutes avec un courant d’azote ultra haute pureté
- Les bouchons de téflon des cellules électrochimiques ont 3 ports pour l’électrode de travail contre-électrode et l’électrode de référence
- L’électrode de référence Ag/AgCl est retiré de sa solution de KCl 1 M, rincée avec l’eau distillée et ensuite placée dans la cellule.
- La contre-électrode de fil de platine platiné est rincée avec l’eau distillée et ensuite placée dans la cellule.
- L’électrode de travail séché est rincé à l’eau distillée et ensuite placée dans la cellule.
- Le potentiostat est activée.
- Le plomb de l’électrode blanche est relié à l’abord et connecté à l’électrode de référence.
- Le plomb de l’électrode rouge est ensuite connecté à l’électrode de compteur de fil de Pt.
- Le plomb de l’électrode verte est alors connecté à l’électrode de travail du métal/noir de carbone.
- Un petit ruisseau de purge2 N est laissé bouillonner continuellement dans l’électrolyte.
- Assurer aucune piste ne se touchent et qu’il n’y a pas de contact électrique direct entre les 3 électrodes autrement qu’avec les 0,5 M H2SO4 électrolyte.
3. analyse électrochimique
- Après avoir activé le potentiostat, effectuer au moins 20 conditionnement cycles entre 0 et 0,4 V vs RHE à 50 mV/s à l’aide de CV. Cela est possible en choisissant des CV en tant que technique et en entrant le potentiel supérieur et inférieur limite ainsi que la vitesse de balayage.
- Voltamétrie à balayage linéaire (LSV) est possible alors en choisissant LSV comme technique et en spécifiant un départ potentiel, un potentiel final et une vitesse de balayage. La vitesse de balayage pour LSV est généralement beaucoup moins que les CV, généralement 1 à 2 mV/s afin que les courants capacitifs deviennent beaucoup plus faibles que les courants dus aux réactions de surface faradique
- Chronoampérométrie (CA) s’effectue en choisissant CA ou « Courbe de i-t ampérométrique » comme une technique et en spécifiant le potentiel fixe ainsi que la durée de l’instrument devrait tenir l’électrode de travail comme ce potentiel fixe.
- Chronopotentiométrie (CP) est effectuée en choisissant CP comme technique. CP peut être effectuée par une série d’étapes actuelles lorsqu’un courant est spécifiée pour un certain laps de temps, suivie d’un nouveau courant pour une période de temps déterminée. Ces courants appliqués peuvent s’étendre sur des courants anodiques et cathodiques au sein de la même mesure de CP.
- Lorsque l’analyse électrochimique est terminé, éteignez le potentiostat.
- Déconnectez les câbles d’électrode et stockez-les dans un endroit sec loin des liquides pour prévenir la corrosion.
- Enlever l’électrode de référence et rincer abondamment avec de l’eau distillée. Puis retourner l’électrode de référence directement à sa solution de stockage de 1 M KCl. La pointe de cette électrode ne devrait jamais être autorisée à s’assèchent.
- Retirez la contre-électrode fils de Pt et rincer abondamment à l’eau distillée
- Enlever l’électrode de travail et rincer abondamment à l’eau distillée et ensuite utiliser un Kimwipe avec de l’acétone pour retirer facilement l’encre séchée de catalyseur de la surface de l’électrode de travail. Il est recommandé pour polir les électrodes immédiatement après utilisation.
- Désactiver la purge de2 N.
- Vider l’électrolyte utilisé dans un conteneur à déchets d’acide. Rincez le verre cellulaire et le cap de téflon abondamment avec de l’eau distillée.
Un potentiostat-galvanostat est le plus couramment utilisé l’instrument dans la caractérisation électrochimique et est utilisée pour comprendre l’effet des variations électriques sur une réaction chimique.
Un potentiostat-galvanostat est un instrument utilisé dans les systèmes électrochimiques. Il mesure actuelle à un potentiel appliqué en mode potentiostat, ou vice versa en mode galvanostat. Pour plus de simplicité, l’instrument est communément appelé un potentiostat.
Réactions d’oxydo-réduction, ou redox, se produisent à la surface de l’électrode et impliquant le transfert d’électrons. En particulier, la perte d’électrons dans une espèce chimique est le cas de l’oxydation, ou le gain d’électrons dans le cas de réduction. Cet événement d’oxydoréduction peut être induit par un potentiel appliqué, E, aussi appelé tension.
Cette vidéo fera la démonstration de l’ensemble vers le haut et les essais de rendement des électrochimiques à l’aide d’un potentiostat.
Dans la plupart des cas, les événements d’oxydo-réduction sont couplés à un potentiostat via une cellule de trois électrodes. La cellule de trois électrodes se compose d’une électrode de travail, comptoir ou électrode auxiliaire et électrode de référence. L’électrode de travail est où se produit la réaction d’intérêt et la contre-électrode sert à compléter le circuit électrique.
Un potentiel appliqué est évalué en fonction de l’électrode de référence, qui contient un système d’oxydoréduction avec un potentiel d’électrode connu et stable, les électrodes de référence E. Common sont l’électrode au calomel saturée et l’électrode à hydrogène réversible, qui sont utilisés à des fins d’étalonnage. L’électrode Ag/AgCl est couramment utilisé dans les tests électrochimiques et est interfacé avec la solution d’électrolyte via une fritté poreuse.
La cellule électrochimique est remplie d’une solution d’électrolyte de force ionique élevée, telle qu’une solution acide, alcaline ou sel. La solution d’électrolyte empêche l’accumulation de charge les électrodes.
Dans une expérience électrochimique, le potentielle, actuel, temps et des frais peuvent tous être manipulés ou mesuré par le potentiostat. Lorsque l’électrode de travail joue le rôle de la cathode, électrons découlent de la contre-électrode à l’électrode de travail. Charge positive ions, ou cations, écoulement vers la cathode. L’inverse est vrai lorsque l’électrode de travail agit comme l’anode. Chargé négativement les flux d’ions, ou anions, à l’anode.
En sélectionnant les paramètres manipulés et mesurées, un certain nombre de techniques de mesure est possible. Chronoampérométrie est une technique où une étape potentielle est appliquée à l’électrode de travail, et la variation de courante qui en résulte est mesurée en fonction du temps. Quand une étape potentielle est suffisante pour provoquer une réaction électrochimique à l’électrode de travail, les changements en cours. Cette technique peut être utilisée pour de nombreuses applications, telles que la détermination des coefficients de diffusion dans la cinétique de la réaction.
De même, chronopotentiométrie est une technique où une constante ou varié courant est appliqué, et le potentiel est mesuré en fonction du temps. Le courant appliqué provoque des espèces électroactives être oxydé ou réduit à une certaine vitesse. Cette technique est utilisée pour une variété d’applications, telles que la détermination de l’avancement de la réaction.
Voltamétrie mesure courant anodique et cathodique par rapport à un balayage de potentiel appliquée. Cette mesure porte sur l’ajout ou la suppression des électrons d’une espèce chimique lors de l’augmentation ou diminution du potentiel à un rythme constant. Voltamétrie cyclique, ou CV, est traité en détail séparément dans une autre vidéo de cette collection.
Maintenant que les bases de la potentiométrie ont été couverts, la préparation d’une cellule de trois électrodes et une électrode de travail avec un catalyseur lié surface sera démontrée en laboratoire. Dans cette démonstration, encre de catalyseur sera préparé et mesurée, qui se compose des nanoparticules platine dans un support de noir de carbone, avec un agent de liaison Nafion. Ce système est représentative de la pile à combustible actuel et de la recherche de la batterie.
Pour commencer, pèsent 7,5 mg de catalyseur métal/noir de carbone sous une hotte et ajoutez-le à un flacon en verre. Diluer le catalyseur avec 1 mL d’eau et ajouter 100 μL de 117 Nafion, puis Boucher le flacon.
Laisser agir le mélange sur la glace pendant au moins 10 min assurer la dispersion uniforme et mélange de l’appui de noir de carbone avec la Nafion complet. Alors que l’encre est sonification, préparer l’électrode de travail, qui est un disque de 3 mm carbone vitreux.
Nettoyer et polir l’électrode en frottant doucement avec un mouvement tourbillonnant, circulaire sur un tampon doux recouvert de solution d’alumine colloïdal 0,05 μm. Après le polissage, rincez l’électrode copieusement avec de l’eau déionisée pour enlever l’alumine.
Ensuite, 7 mL d’encre est dégoutté sur l’électrode de carbone vitreux brillant, orientées verticalement. Sécher l’électrode de travail sous vide à température ambiante. Puis séchez-le à 80 ° C pour une heure si les nanoparticules de catalyseur sont air stable.
Tout d’abord, remplir la cellule électrochimique de verre avec 10 mL de l’électrolyte. Chapeau la cellule électrochimique avec un plafond de téflon avec ouvertures pour les trois électrodes. Dé-gaz l’électrolyte pendant au moins 30 min à l’azote ultra haute pureté afin d’éliminer l’oxygène actifs en oxydoréduction. Permettre à l’azote à bouillonner légèrement tout au long de l’expérience.
Retirez l’électrode de référence Ag/AgCl de sa solution de stockage de NaCl de 3M. Rincez l’électrode avec de l’eau désionisée et placez-le dans la cellule électrochimique.
Ensuite, rincez l’électrode de compteur de fil de platine et l’électrode de travail séchées avec de l’eau désionisée et insérez-les dans la cellule. Veiller à ce que les électrodes ne se touchent pas. Allumez le potentiostat et connecter les fils sur les électrodes de référence et le compteur.
Effectuer au moins 20 cycles de conditionnement en exécutant des analyses de voltampérométrie cyclique entre le haut et le bas limites éventuelles à 50 mV par seconde. Cette étape garantit que les surfaces d’électrode sont entièrement hydratés.
Voltamétrie à balayage linéaire ou LSV, peut être exécuté en spécifiant les potentiels initiaux et finaux et la vitesse de balayage. La vitesse de balayage pour LSV est généralement inférieur à celui de CV. Il en résulte un complot potentiel contre courant avec les événements d’oxydation ou réduction visualisé comme des pics dans l’analyse. Dans ce cas, le perchlorate dans l’électrolyte a été réduit sur la surface du catalyseur dans l’analyse cathodique.
Pour effectuer la chronoampérométrie, sélectionnez-le comme la technique, puis spécifiez le potentiel fixe ainsi que le temps. Le résultat est un tracé de courant / temps. La décomposition initiale est due à une décharge capacitive, tandis que la portion de l’état d’équilibre est essentiellement une ligne droite. Chronoampérométrie est potentiostatique et donc après la décomposition asymptotique initiale des effets capacitif, le courant attribué aux réactions de surface peut être isolé.
Enfin, chronopotentiométrie est réalisée dans une série d’étapes actuelles, lorsqu’un courant est spécifiée pour un certain laps de temps. Chaque fois que les commutateurs actuels entre zéro et le travail actuel, il y a un changement asymptotique initial en potentiel, suivie d’un état stable. Après chaque cycle de marche/arrêt, le matériau stable catalyseur exige le même dépassement potentiel à conduire le courant spécifié.
Mesures électrochimiques avec un potentiostat sont largement utilisés dans l’analyse et de fabrication.
Électrochimie sert à analyser la liaison de molécules sondes aux électrodes. Dans cet exemple, électrodes ont été modelés dans des canaux microfluidiques et fonctionnalisées avec ADN bicaténaire unique. Lorsque l’ADN a été hybridé avec le brin de gratuit, le couple redox a été bloqué à la surface de l’électrode.
Hybridation de l’ADN a été ensuite mesurée en branchant les électrodes sur le potentiostat à l’aide de trois électrodes de la sonde.
Mesures d’impédance, une mesure de la résistance au courant, a montré que gratuit ADN concentration croissante a entraîné une augmentation impédance et augmente donc l’hybridation.
Prochains processus électrochimiques ont été utilisés pour surveiller et caractériser la croissance des biofilms sur une électrode. Pour ce faire, une cellule de trois électrodes a été Assemblée, avec l’électrolyte étant le bouillon de culture cellulaire.
La croissance du biofilm a été suivie à l’aide de chronoampérométrie, afin d’obtenir une mesure exacte et les conditions de culture reproductible.
Techniques électrochimiques peuvent également être utilisés dans la fabrication de couches minces et des couches sur la surface de l’électrode. Signaux électriques déclenchent des environnements localisés à la surface de l’électrode, qui peuvent induire l’auto-assemblage des matériaux.
Dans cet exemple, le dépôt des biomatériaux a effectué un dépôt électrolytique. Chitosan, un biopolysaccharide, subit une transition sol-gel à la surface de l’électrode, création d’un film.
Vous avez juste regardé introduction de Jupiter à la potentiométrie. Vous devez maintenant comprendre comment mettre en place une cellule de trois électrodes typique et effectuer des tests électrochimiques base.
Merci de regarder !
Subscription Required. Please recommend JoVE to your librarian.
Results
Cette procédure se traduira en chiffres contenant des parcelles du courant mesuré vs potentiel pour chacun des quatre techniques. Par convention de CV et LSV, les parcelles seront également produits dans le courant mesuré vs potentiel malgré la réalité que ce sont des techniques transitoires que mesurent le courants par rapport à la dérivée temporelle du potentiel.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
CV, LSV, CP et CA sont des techniques indispensables pour déterminer l’efficacité de nouveaux matériaux d’électrode pour les piles à combustible, électrolyseurs, batteries et supercapacités ainsi que pour développer les domaines tels que l’oxydation partielle sélective ou la réduction des produits chimiques. Ces méthodes permettent de déterminer les experiences de réactions sur les matériaux d’électrodes différentes par rapport à leur potentiel d’équilibre thermodynamique. Ces méthodes permettent en outre la capacité volumétrique ou gravimétrique des supercondensateurs à déterminer. De même, les taux de charge/décharge des électrodes de batteries ou supercondensateurs peuvent être déterminées avec ces techniques. Ces techniques permettent également la caractérisation de la stabilité électrochimique des matériaux à déterminer. Au-delà de ces techniques de base, des techniques plus avancées comprennent la combinaison des techniques potentiométriques avec méthodes in situ comme IR et spectrométrie de masse.
Subscription Required. Please recommend JoVE to your librarian.




