Summary
经典途径激活抗体和靶细胞裂解高潮。这架CH
Abstract
补体系统是一组蛋白质,当激活,导致靶细胞裂解,促进吞噬通过opsonisation。个人补体成分是可以量化的,但这不提供任何信息的途径的活动。这架CH
Protocol
制备的5倍Veronal缓冲液(VBS)
- 要准备Veronal缓冲液(VBS),3个单独的解决方案都需要做好准备。
- 准备通过溶解在蒸馏水350毫升NaCl和0.94gm钠巴比妥21.25gm溶液1。氯化钠和巴比妥钠终浓度分别为1.02M和13MM。
- 准备通过溶解在热蒸馏水125毫升巴比妥1.44gm溶液2。巴比妥最终浓度62.5mM。
- 准备通过溶解在蒸馏水100ml 氯化钙氯化镁2和4.41gm 20.33gm溶液3。 2氯化镁和氯化钙2终浓度分别是218万和440MM。
- 混合解决方案1和2,冷却到室温。
- 一旦合并的解决方案已经冷却,加1.25毫升解决方案3,使用1M盐酸调节pH值至7.3-7.5。
- 调整最终体积至500ml,用蒸馏水,准备了5倍原液。
- 为了准备1X的工作方案,用蒸馏水稀释股票1:5。
致敏的绵羊红细胞溶血
- 准备首先用VBS稀释1:50的溶血
- 至SRBC4毫升添加的VBS6毫升,轻轻颠倒混合
- 离心600克x5分钟
- 弃上清,另2次清洗细胞
- 最后一次洗涤后,离心900克x5分钟包细胞的细胞
- 弃上清,重悬细胞足够的VBS准备10%的解决方案,即细胞排列0.5毫升悬浮于5毫升的缓冲
- 纷飞不断滴状细胞加入同等体积的溶血素(兔抗绵羊红细胞抗体)
- 在30℃水浴中孵育30分钟
- 轻轻地混合细胞每15分钟
- Sensitised SRBC可存放过夜,4 ° C
CH 50检测
- 标签系列的管子,一式两份,每份1:8,1:16,1:32,1:64和1:128。
- 重复准备了一系列控制和VBS的每个测试血清两折系列稀释
- 在1:4(100毫升血清+300毫升VBS的),并开始样品转移到下一个标记管200毫升。
- 调匀未来稀释稀释和转移200毫升之间的一个新的枪头。
- 重复,直到所有的5个稀释。
- 丢弃从最终的1:128稀释200毫升。
- 将暂停致敏SRBC 200ml到所有的管子。
- 标签两个单独的管为空白 ,并添加致敏SRBC +200毫升VBS的200毫升。这些管子将测量的VBS的SRBC自发溶解。
- 标签为总裂解另外两个单独的管和致敏SRBC +200毫升蒸馏水添加200毫升。
- 轻轻混合所有的管子。
- 在37℃,在水浴中搅拌15分钟后30分钟。
- 在1500克离心5分钟,沉积物中的红细胞样本。
- 从每管转移上清百毫升以及一个96孔平底板。
- 添加蒸馏水100ml,以每口井。
- 阅读使用酶标仪在540nm处的吸光度的样品。
计算
- 计算每个样本的平均吸光度
- 从所有样本中减去空白吸光度(自发裂解)
- 为每个稀释使用下列公式计算%裂解:

- 剧情与横轴上的血清稀释的比例溶解(垂直轴)。
- 计算为50%的控制和测试血清(图2)溶血所需的稀释。
代表性的成果:
视频包括代表性的成果的一个例子。在实践中,对照血清在测试血清的同时还可以运行,并以同样的方式对待。如下(表1)是从测试的血清样本的样本数据。数据是根据5.3方程操纵。
| 样品 | 外径540 | 平均 | ||
| 空 | 0.042,0.044 | 0.043 | ||
| 共有裂解 | 0.183,0.183 | 0.183 | ||
| 稀释 | 外径540 | 平均 | 平均空白 | %裂解 |
| 1:8 | 0.200,0.219 | 0.210 | 0.168 | 116 |
| 1:16 | 0.179,0.173 | 0.176 | 0.134 | 93 |
| 1:32 | 0.134,0.110 | 0.122 | 0.08 | 55 |
| 1:64 | 0.053,0.066 | 0.059 | 0.017 | 12 |
| 1:128 | 0.044,0.045 | 0.045 | 0.003 | 2 |
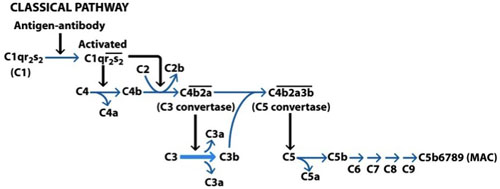
图1。激活经典补体途径激活经典途径是通过结合免疫球蛋白M(IgM)的免疫球蛋白- G(IgG)的目标细胞的表面上。的抗体的Fc片段结合补体C1q,C1R激活,而这又反过来激活另一个C1R分子一起激活两个C1s的分子。 C1s的切割公开为C2的结合位点,这也是裂解C4。 C4B和C2A结合,形成一个复杂的简称为C3转化。现在这种复杂的裂解C3形成C3a和C3b,其中一些与C3形成了C5的convertase convertase结合。现在这种复杂的行为对C5的,绑定到C6开始形成膜攻击复合物(MAC),由此产生C5b。 C5b6行为,C7,打开C8的行为,并最终C9形成最终的MAC。 (Goldsby 等 ,2003)。
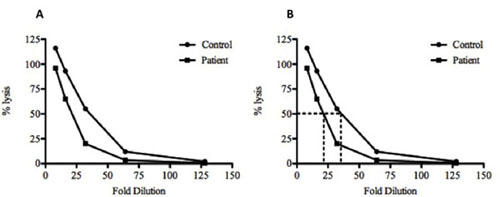
图2。绘制样本数据,计算控制和检测血清样本的CH50(A),绘制对稀释倍数计算的百分比(%)控制(•)和试验(+)血清样品的裂解。 (二)要计算50%的裂解,一条线是来自50%的价值,直到它与图线相交,然后绘制一条垂直线下来的稀释。在这个例子中,需要控制和21.6倍稀释的待测血清稀释35倍,达到50%溶解。这一数据表明,有少补测试血清中比对照,因为它需要较少的稀释前达到50%裂解。控制样本也显示> 100%,在1:8稀释溶解。这是最有可能是由于不完全溶解的SRBC蒸馏水和补体成分更高效裂解。
Subscription Required. Please recommend JoVE to your librarian.
Discussion
CH 50含量是受到很多干扰。有些SRBC的是比其他人更脆弱,导致自发溶血补体活性无关。兔抗体的亲和力很多很多,从生产厂家之一到另一个不同,这影响的SRBC结合的抗体量。此外,敏与在细胞与不同数量的抗体涂层的SRBC的抗体结果SRBC的过程。标本采集和存储是一个重要的潜在的错误来源。补体成分如补体C1q,C3,C4和C5是非常不稳定的,因此适当的样品处理是至关重要的。长时间暴露在高温将减少补体活性,并会产生补体成分的不活跃的片段。要尽可能的许多误差来源检测,关键是测试已知的CH值50的每一个对照血清进行检测时间和重现的接受值已知的血清对照。 ,以确定是否有SRBC和溶血素的不同批次之间的任何分歧的方法之一是对标准样品的血清多次测试新的测试材料,然后再确定是否有溶血的基础水平,或在CH值50任何变化对照血清。
Subscription Required. Please recommend JoVE to your librarian.
Acknowledgments
笔者想感谢劳拉马修斯小姐表演的技巧和摄影郑明牧羊犬。这个项目是由南澳大学,实验室医学程序。
Materials
| Name | Company | Catalog Number | Comments |
| Sheep red blood cells | CSL | 2490201 | Use at 1% final |
| Serum | Human serum | ||
| Rabbit Anti-Sheep Haemolytic serum (RBCs), Unconjugated | AbD Serotec | C12HSB | |
| 96 well flat bottom plate | Sarstedt Ltd | 83.1839 | |
| Veronal buffered saline | Use at 1x final | ||
| Waterbath | |||
| Plate reader | |||
| 37°C room/incubator |
References
- Goldsby, R. A., Kindt, T. J., Osborne, B. A., Kuby, J. Immunology. , W.H. Freeman. (2003).




