4.9 : Reações de Precipitação
Os sólidos iônicos podem ser solúveis ou não solúveis em água. Os sólidos iônicos solúveis em água dissolvem-se por decomposição ou dissociação em íons. As moléculas de água rodeiam os íons dissociados para formarem uma solução aquosa.
Os sólidos iônicos insolúveis em água permanecem não dissolvidos ou não dissociados em soluções aquosas. Se misturarmos soluções aquosas de dois compostos iônicos diferentes resultando numa reação química que produz um sólido iônico insolúvel denominado precipitado trata-se de uma reação de precipitação. O precipitado permanece não dissolvido e pode ser separado da solução por filtração.
O cloreto de sódio e o nitrato de prata são compostos iônicos solúveis em água. Uma solução aquosa de cloreto de sódio contém íons de sódio e íons de cloreto nas suas formas dissociadas. Da mesma forma, uma solução aquosa de nitrato de prata contém íons de prata dissociados e íons de nitrato.
Quando as duas soluções são misturadas, a solução resultante contém os quatro íons:os cátions de sódio e prata, bem como os aníons de cloreto e nitrato. Uma vez que os íons com cargas opostas são atraídos um pelo outro, o cátion de cada reagente pode emparelhar com o ânion do outro reagente para formar novos produtos iônicos. Assim, os cátions de sódio emparelham-se com os aníons de nitrato para formarem nitrato de sódio, e os cátions de prata combinam-se com os aníons de cloreto para formarem cloreto de prata.
A referência às regras de solubilidade permite-nos determinar se os produtos iônicos são solúveis ou não em água. De acordo com este guia, todos os sais de nitrato são solúveis em água sem exceção. A maioria dos sais de cloreto são solúveis em água, mas o sal de prata é uma exceção.
Portanto, o nitrato de sódio é um sal solúvel que permanece na solução como íons de sódio e íons de nitrato dissolvidos, enquanto que o cloreto de prata é um sal insolúvel que se precipita da solução. A equação molecular para esta reação de precipitação sugere que o cloreto de sódio aquoso reage com o nitrato de prata aquoso para formar nitrato de sódio aquoso e cloreto de prata sólido. Este é um exemplo de uma reação de metátese salina, que também é denominada de reação de duplo deslocamento.
A metátese salina é um processo químico em que os íons positivos e negativos de dois reagentes iônicos trocam de parceiros para formarem dois novos produtos iônicos. Nesta reação, os cátions de sódio e prata trocam de parceiros emparelhando com os aníons de nitrato e cloreto, respetivamente para formarem nitrato de sódio e cloreto de prata.
Em uma reação de precipitação, soluções aquosas de sais solúveis reagem para originar um composto iónico insolúvel – o precipitado. A reação ocorre quando iões opostamente carregados em solução superam a sua atração pela água e ligam-se entre si, formando um precipitado que se separa da solução. Como tais reações envolvem a troca de iões entre compostos iónicos em solução aquosa, são também referidas como reações de dupla deslocação, dupla substituição, de permuta, ou reações de metatese (Grego para “transpor”). Uma reação de precipitação é usada como técnica de análise para identificar iões metálicos em um composto e métodos gravimétricos para determinar a composição da matéria.
A medida em que uma substância pode ser dissolvida em água, ou em qualquer solvente, é expressa quantitativamente como a sua solubilidade, definida como a concentração máxima de uma substância que pode ser obtida em condições específicas. Diz-se que as substâncias com solubilidades relativamente grandes são solúveis. Uma substância precipita quando as condições da solução forem tais que a sua concentração excede a sua solubilidade. Diz-se que as substâncias com solubilidades relativamente baixas são insolúveis, e são estas as substâncias que rapidamente precipitam da solução.
Por exemplo, observa-se precipitação quando se misturam soluções de iodeto de potássio e nitrato de chumbo, resultando na formação de iodeto de chumbo sólido:

Esta observação é consistente com as diretrizes de solubilidade: O único composto insolúvel entre todos os envolvidos é o iodeto de chumbo, uma das excepções à solubilidade geral dos sais de iodeto.
A equação iónica líquida que representa esta reação é:
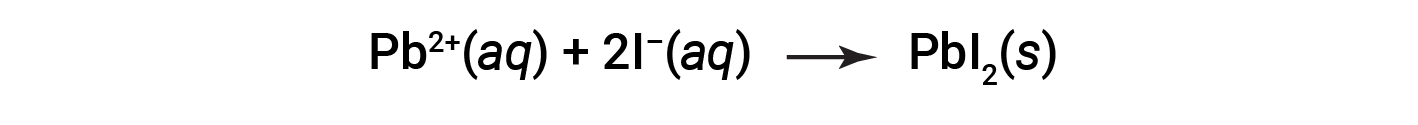
As diretrizes de solubilidade podem ser utilizadas para prever se irá ocorrer uma reação de precipitação quando se misturam soluções de compostos iónicos solúveis. Basta identificar todos os iões presentes na solução e, em seguida, considerar se o possível emparelhamento catião-anião pode resultar em um composto insolúvel.
Por exemplo, misturar soluções de nitrato de prata e fluoreto de sódio irá originar uma solução que contém iões Ag+, NO3−, Na+, e F−. Para além dos dois compostos iónicos originalmente presentes nas soluções, AgNO3 e NaF, dois compostos iónicos adicionais podem derivar deste conjunto de iões: NaNO3 e AgF. As diretrizes de solubilidade ditam que todos os sais de nitrato são solúveis, mas que AgF é uma das excepções à solubilidade geral dos sais de fluoreto. Prevê-se, portanto, a ocorrência de uma reação de precipitação, conforme descrito pelas seguintes equações:


Este texto é adaptado de OpenStax Chemistry 2e, Section 4.2: Classifying Chemical Reactions.
Os sólidos iônicos podem ser solúveis em água ou insolúveis em água. Os sólidos iônicos solúveis em água se dissolvem quebrando-se - ou dissociando-se - em íons. As moléculas de água então circundam os íons dissociados para formar uma solução aquosa. Os sólidos iônicos insolúveis em água permanecem não dissolvidos ou não dissociados em soluções aquosas.
Se a mistura de soluções aquosas de dois compostos iônicos diferentes resultar em uma reação química que produz um sólido iônico insolúvel - chamado precipitado - é uma reação de precipitação. O precipitado permanece indissolvido e pode ser separado da solução por filtração.
O cloreto de sódio e o nitrato de prata são compostos iônicos solúveis em água. Uma solução aquosa de cloreto de sódio contém íons sódio e íons cloreto em suas formas dissociadas. Da mesma forma, uma solução aquosa de nitrato de prata contém íons de prata dissociados e íons de nitrato.
Quando as duas soluções são misturadas, a solução resultante contém todos os quatro íons: os cátions de sódio e prata, bem como os ânions cloreto e nitrato.
Como os íons com cargas opostas são atraídos uns pelos outros, o cátion de cada reagente pode emparelhar com o ânion do outro reagente para formar novos produtos iônicos. Assim, os cátions de sódio se emparelham com ânions de nitrato para formar nitrato de sódio, e os cátions de prata se combinam com ânions cloreto para formar cloreto de prata.
Consultar as regras de solubilidade nos permite determinar se os produtos iônicos são solúveis em água ou insolúveis em água. De acordo com este guia, todos os sais de nitrato são solúveis em água, sem exceção. A maioria dos sais de cloreto é solúvel em água, mas o sal de prata é uma exceção.
Portanto, o nitrato de sódio é um sal solúvel que permanece na solução como íons de sódio dissolvidos e íons nitrato, enquanto o cloreto de prata é um sal insolúvel que precipita da solução.
A equação molecular para esta reação de precipitação sugere que o cloreto de sódio aquoso reage com o nitrato de prata aquoso para formar nitrato de sódio aquoso e cloreto de prata sólido.
Este é um exemplo de uma reação de metátese de sal, que também é chamada de reação de duplo deslocamento. A metátese de sal é um processo químico no qual os íons positivos e negativos de dois reagentes iônicos trocam parceiros para formar dois novos produtos iônicos.
Nesta reação, os cátions de sódio e prata trocam parceiros - emparelhando-se com ânions nitrato e cloreto, respectivamente - para formar nitrato de sódio e cloreto de prata.
From Chapter 4:

Now Playing
4.9 : Reações de Precipitação
Chemical Quantities and Aqueous Reactions
0 Views

4.1 : Reaction Stoichiometry
Chemical Quantities and Aqueous Reactions
0 Views

4.2 : Limiting Reactant
Chemical Quantities and Aqueous Reactions
0 Views

4.3 : Reaction Yield
Chemical Quantities and Aqueous Reactions
0 Views

4.4 : General Properties of Solutions
Chemical Quantities and Aqueous Reactions
0 Views

4.5 : Solution Concentration and Dilution
Chemical Quantities and Aqueous Reactions
0 Views

4.6 : Electrolyte and Nonelectrolyte Solutions
Chemical Quantities and Aqueous Reactions
0 Views

4.7 : Solubility of Ionic Compounds
Chemical Quantities and Aqueous Reactions
0 Views

4.8 : Chemical Reactions in Aqueous Solutions
Chemical Quantities and Aqueous Reactions
0 Views

4.10 : Oxidation-Reduction Reactions
Chemical Quantities and Aqueous Reactions
0 Views

4.11 : Oxidation Numbers
Chemical Quantities and Aqueous Reactions
0 Views

4.12 : Acids, Bases and Neutralization Reactions
Chemical Quantities and Aqueous Reactions
0 Views

4.13 : Synthesis and Decomposition Reactions
Chemical Quantities and Aqueous Reactions
0 Views