11.14 : Estruturas de Sólidos
Os sólidos são classificados como amorfos ou cristalinos com base na sua estrutura interna tridimensional. Sólidos amorfos como vidro de sílica fundido falta uma encomenda de arranjo interno das suas partículas constituintes, enquanto que os sólidos cristalinos como o quartzo têm as suas partículas constituintes dispostas numa repetição tridimensional padrão em todo o sólido. A estrutura de um sólido cristalino é representada por uma célula unitária, que é a menor unidade de repetição da estrutura cristalina que mantém a simetria da estrutura.
O conjunto padrão tridimensional é conhecido como um cristal de malha, que é composto de pontos de malha e vetores de malha. Os vetores da malha delineiam os bordos da célula da unidade, e os pontos de malha podem ser nos cantos, nas faces, ou no centro da célula da unidade. Os sistemas de malha são definidos pelas dimensões da célula de unidade.
Existem 7 tipos de sistemas de malha:cúbica, tetragonal, ortopédica, rombohedral, monoclínica, triclínico, e hexagonal. As posições dos átomos numa célula unitária não são necessariamente os mesmos que os pontos da malha. O padrão de átomos na célula da unidade, ou motivo, é frequentemente definida em termos de localização dos átomos relativo a um dado ponto da malha.
O número de átomos numa célula unitária reflete a eficiência do sólido, ou a quantidade do seu volume ocupados por átomos em vez do espaço entre eles. Um número mais elevado de átomos na célula da unidade corresponde geralmente a embalagem mais eficiente. Átomos atribuídos a uma célula unitária não podem ser totalmente contidos dentro da célula.
Uma maneira de contar estes átomos parciais é considerar cada átomo um canto como um oitavo de um átomo e cada átomo uma face como metade de um átomo. Em alternativa, se uma célula unitária tem um átomo em cada canto, um é atribuído à célula de unidade e as outras sete são ignoradas. Se uma célula unitária tiver um átomo em cada uma de duas faces, um é atribuído à célula de unidade e a outra é ignorada.
Sólidos nos quais os átomos, iões, ou moléculas estão dispostos em um padrão repetitivo definido são conhecidos como sólidos cristalinos. Metais e compostos iónicos formam normalmente sólidos cristalinos. Um sólido cristalino tem uma temperatura de fusão precisa porque cada átomo ou molécula do mesmo tipo é mantida no lugar com as mesmas forças ou energia. Sólidos amorfos ou sólidos não cristalinos (ou, às vezes, vidros) não possuem uma estrutura interna ordenada e estão dispostos aleatoriamente. Substâncias constituídas por moléculas grandes, ou uma mistura de moléculas cujos movimentos são mais restritos, formam muitas vezes sólidos amorfos. O material amorfo sofre amolecimento gradual, em uma gama de temperaturas, devido à não equivalência estrutural das moléculas. Quando um material amorfo é aquecido, as atrações intermoleculares mais fracas quebram primeiro. À medida que a temperatura aumenta, as atrações mais fortes são quebradas.
Célula Unitária
A estrutura de um sólido cristalino é melhor descrita pela sua unidade repetitiva mais simples, chamada de célula unitária. A célula unitária consiste em pontos reticulares que representam as localizações de átomos ou iões. Toda a estrutura consiste então nesta célula unitária que se repete em três dimensões, como ilustrado na Figura 1.
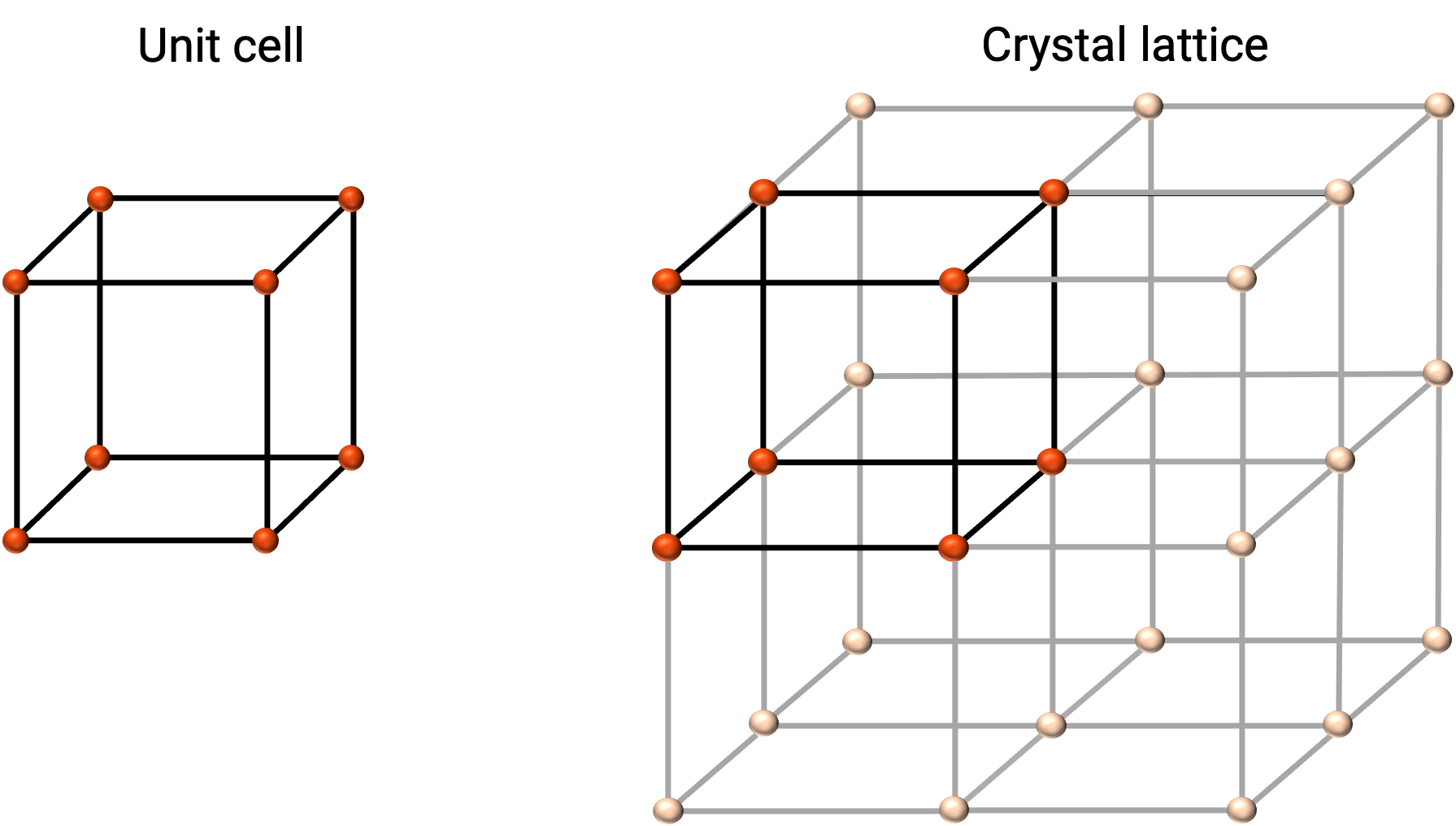
Figura 1. Célula unitária e retículo de cristal com pontos reticulares indicados a vermelho.
No geral, uma célula unitária é definida pelos comprimentos de três eixos (a, b e c) e pelos ângulos (α, β, e γ) entre eles, como mostra a Figura 2. Os eixos são definidos como sendo os comprimentos entre os pontos no espaço reticular.
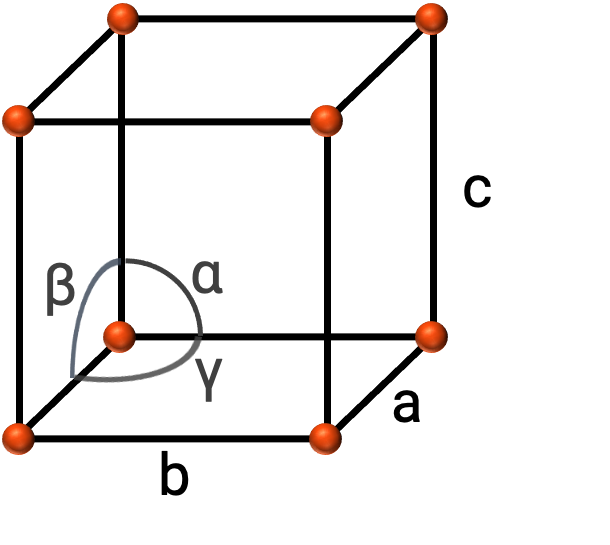
Figura 2. A célula unitária é definida pelos seus eixos (a, b, e c) e ângulos (α, β, e γ)
Existem sete sistemas reticulares diferentes, alguns dos quais têm mais de um tipo de malha, para um total de catorze células unitárias diferentes.
| Sistemas | Ângulos | Eixos |
| Cúbico | α = β = γ = 90° | a = b = c |
| Tetragonal | α = β = γ = 90° | a = b ≠ c |
| Ortorrômbico | α= β = γ = 90° | a ≠ b ≠ c |
| Monoclínico | α = γ = 90°; β ≠ 90° | a ≠ b ≠ c |
| Triclínico | α ≠ β ≠ γ ≠ 90° | a ≠ b ≠ c |
Este texto é adaptado de Openstax, Chemistry 2e, Section 10.6: Lattice Structures in Crystalline Solids.
Os sólidos são classificados como amorfos ou cristalinos com base em sua estrutura interna tridimensional.
Sólidos amorfos, como o vidro de sílica fundido, não possuem um arranjo interno ordenado de suas partículas constituintes, enquanto sólidos cristalinos, como o quartzo, têm suas partículas constituintes dispostas em um padrão tridimensional repetitivo em todo o sólido.
A estrutura de um sólido cristalino é representada por uma célula unitária, que é a menor unidade repetitiva da estrutura cristalina que retém a simetria da estrutura.
O padrão tridimensional geral é conhecido como rede cristalina, que é composta de pontos de rede e vetores de rede. Os vetores de rede delineiam as arestas da célula unitária, e os pontos de rede podem estar nos cantos, nas faces ou no centro da célula unitária.
Os sistemas de rede são definidos pelas dimensões da célula unitária. Existem 7 tipos de sistemas de rede: cúbico, tetragonal, ortorrômbico, romboédrico, monoclínico, triclínico e hexagonal.
As posições dos átomos em uma célula unitária não são necessariamente as mesmas que as dos pontos de rede. O padrão de átomos na célula unitária, ou motivo, é frequentemente definido em termos das localizações dos átomos em relação a um determinado ponto de rede.
O número de átomos em uma célula unitária reflete a eficiência de empacotamento do sólido, ou a quantidade de seu volume ocupada pelos átomos, em vez do espaço entre eles. Um número maior de átomos na célula unitária geralmente corresponde a um empacotamento mais eficiente.
Os átomos atribuídos a uma célula unitária podem não estar totalmente contidos na célula. Uma maneira de contar esses átomos parciais é considerar cada átomo em um canto como um oitavo de um átomo e cada átomo em uma face como metade de um átomo.
Alternativamente, se uma célula unitária tiver um átomo em cada canto, um será atribuído à célula unitária e os outros sete serão ignorados. Se uma célula unitária tiver um átomo em cada uma das duas faces, uma será atribuída à célula unitária e a outra será ignorada.
From Chapter 11:

Now Playing
11.14 : Estruturas de Sólidos
Liquids, Solids, and Intermolecular Forces
0 Views

11.1 : Molecular Comparison of Gases, Liquids, and Solids
Liquids, Solids, and Intermolecular Forces
0 Views

11.2 : Intermolecular vs Intramolecular Forces
Liquids, Solids, and Intermolecular Forces
0 Views

11.3 : Intermolecular Forces
Liquids, Solids, and Intermolecular Forces
0 Views

11.4 : Comparing Intermolecular Forces: Melting Point, Boiling Point, and Miscibility
Liquids, Solids, and Intermolecular Forces
0 Views

11.5 : Surface Tension, Capillary Action, and Viscosity
Liquids, Solids, and Intermolecular Forces
0 Views

11.6 : Phase Transitions
Liquids, Solids, and Intermolecular Forces
0 Views

11.7 : Phase Transitions: Vaporization and Condensation
Liquids, Solids, and Intermolecular Forces
0 Views

11.8 : Vapor Pressure
Liquids, Solids, and Intermolecular Forces
0 Views

11.9 : Clausius-Clapeyron Equation
Liquids, Solids, and Intermolecular Forces
0 Views

11.10 : Phase Transitions: Melting and Freezing
Liquids, Solids, and Intermolecular Forces
0 Views

11.11 : Phase Transitions: Sublimation and Deposition
Liquids, Solids, and Intermolecular Forces
0 Views

11.12 : Heating and Cooling Curves
Liquids, Solids, and Intermolecular Forces
0 Views

11.13 : Phase Diagrams
Liquids, Solids, and Intermolecular Forces
0 Views

11.15 : Molecular and Ionic Solids
Liquids, Solids, and Intermolecular Forces
0 Views
See More