Overview
Fonte: Laboratório de Jeff Salacup - Universidade de Massachusetts Amherst
O produto de uma extração de solvente orgânico, um extrato lipídeca total (TLE), é muitas vezes uma mistura complexa de centenas, se não milhares, de diferentes compostos. O pesquisador muitas vezes só está interessado em um punhado de compostos. Os compostos de interesse podem pertencer a uma das várias classes de compostos, como alkanes, cetonas, álcoois ou ácidos(Figura 1), e podem ser úteis para remover as classes compostas às quais não pertence, a fim de obter uma visão mais clara dos compostos que você está interessado. Por exemplo, um TLE pode conter 1.000 compostos, mas o proxy de temperatura da superfície do mar Uk'37 é baseado em apenas dois compostos (alkenones) e o proxy de temperatura da superfície do mar TEX86 é baseado em apenas quatro (tetraethers de glicerol dialkyl gliceol). Seria necessário que o pesquisador removesse o maior número de compostos em que não estão interessados. Isso torna menos provável que a análise instrumental dos compostos de juros (alkenones ou GDGTs) seja menos complicada por outros compostos ínteuos.
Em outros casos, uma técnica de purificação a montante pode ter produzido compostos que você deseja remover agora da amostra, como a produção de ácidos carboxílicos durante a saponificação em nosso vídeo anterior. Em ambos os casos acima, a técnica de purificação chamada cromatografia de coluna é muito útil.
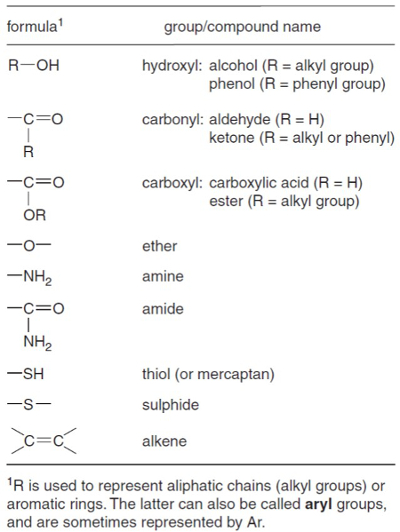
Figura 1. Grupos funcionais geoquimicamente importantes. De Killops e Killops1.
Principles
A cromatografia da coluna de gel de sílica é uma técnica de purificação que utiliza as diferentes associações de classes compostas discretas para uma fase sólida de sílica, um pó fino chamado gel. Uma pipeta pequena é carregada aproximadamente meio cheia com o gel(Figura 2). Esta coluna é então saturada com um solvente apolar, muitas vezes hexano. Uma amostra é então carregada na parte superior do gel na coluna, e uma série de solventes de crescente polaridade é transmitida sequencialmente através da amostra, a fim de separá-la em classes compostas separadas. A separação baseia-se na afinidade das diferentes classes compostas para a fase sólida ou para a fase do solvente. Os compostos polares se ligam mais fortemente à sílica e, portanto, levam mais solventes polares para serem lavados da coluna. Assim, utilizando uma coluna e uma amostra, essa amostra pode ser separada em várias frações; por exemplo, apolars (hidrocarbonetos), polares médios (cetonas e álcoois) e polares (ácidos e outros compostos funcionalizados).

Figura 2. Imagem de um rack feito sob medida que permite a purificação de até 12 amostras por vez.
A cromatografia da coluna é uma técnica flexível para purificar a complexa mistura de compostos encontrados em sedimentos. Misturas se separam à medida que se movem através da coluna e são coletadas em frações, cada uma contendo uma classe química diferente de compostos. Portanto, a cromatografia da coluna é frequentemente usada como um passo adicional de purificação após o isolamento inicial do composto desejado. Extratos orgânicos, como extratos lipídudos totais, podem ser misturas complexas de muitos compostos. Algumas técnicas de purificação, como a saponificação, introduzem compostos que podem danificar instrumentos analíticos e, portanto, devem ser removidos antes da análise. Este vídeo faz parte de uma série sobre extração lipídica, purificação e análise de sedimentos. Uma vez que um extrato lipídeca total é coletado de uma amostra sedimentar, a cromatografia da coluna é usada para purificar tanto alkenones quanto GDGTs, dependendo da análise desejada.
Na cromatografia da coluna, uma mistura de compostos químicos é carregada em uma fase estacionária sólida, como gel de sílica. Uma fase móvel como um solvente orgânico é então usada para eluto, ou remover, os compostos da coluna. A ordem em que os compostos são elucidos depende da força das interações dos compostos com o gel de sílica e com o eluente.
O eluato é coletado em frações, cada uma contendo compostos diferentes da mistura. Dependendo das propriedades dos compostos, um único solvente pode fornecer separação suficiente e elute todos os compostos de interesse. Caso contrário, vários solventes são usados para eluto cada composto de interesse por sua vez.
Compostos polares, que têm uma distribuição desigual de carga, adsorb fortemente para o gel de sílica polar, enquanto compostos apolar adsorb fracamente. Os solventes polares têm maior afinidade com o gel de sílica e, portanto, são eluentes mais poderosos do que solventes apolares. Assim, solventes apolares elute apenas compostos apolares, enquanto solventes polares elute tanto compostos apolares quanto polares.
Quando os compostos desejados são moderadamente polares, os compostos apolares devem ser lavados da coluna com um solvente apolar antes que um solvente polar seja usado. Para evitar a eluição de compostos altamente polares indesejados, como ácidos, um eluente polar não deve ter mais energia de eluição do que o necessário para o composto mais polar desejado.
Agora que você entende os princípios da cromatografia da coluna, vamos passar por um procedimento de purificação de biomarcadores lipídicos de um extrato lipídeca total pela cromatografia da coluna de gel de sílica.
Para remover contaminantes orgânicos, combustão borossilicato pipetas de vidro, frascos de vidro borossilicato e lã de vidro por 6 h a 550 °C. Uma vez que o vidro esteja pronto para uso, configure um rack para segurar pipetas e frascos. Obtenha lâmpadas pipetas, pinças limpas, espátula de laboratório, gel de sílica, hexano, diclorometano e metanol. Com pinças limpas, coloque um pequeno tufo de lã de vidro na boca de uma pipeta. Empurre suavemente a lã de vidro para o fundo da pipeta com a haste de outra pipeta para formar um plugue solto. Carregue cuidadosamente gel de sílica na pipeta até ficar meio cheio. Fixar a pipeta na parte vertical do rack. Fixar um frasco de vidro borossilicato de 4 mL abaixo da ponta da pipeta para coleta de lixo. Em outro frasco de vidro borossilicato, suspenda até 10 mg de amostra seca do processo de saponificação em hexano. Se a amostra grudar nas paredes do frasco, sonicar o frasco por 5 minutos. O procedimento de cromatografia já pode começar.
Para iniciar a cromatografia, lave a coluna de gel de sílica com 3 volumes de hexano para remover bolhas de ar e impurezas. Em seguida, substitua o frasco de resíduo por um frasco vazio para a fração apolar. Com uma pipeta de vidro, carregue a amostra na coluna e deixe a suspensão de molho no gel de sílica. Trabalhe rapidamente para que a coluna não seque durante o procedimento. Enxágüe o frasco de amostra duas vezes com pequenas porções de hexano e transfira cada enxágue para a coluna. Continue adicionando hexano à coluna até que o frasco de coleta esteja quase cheio. Deixe que toda a hexana termine de entrar no gel de sílica. Em seguida, troque o frasco preenchido com um frasco vazio pela fração média polar. Em seguida, enxágue o frasco de amostra com DCM e adicione-o à coluna 3 vezes. Continue adicionando DCM à coluna até que o frasco de coleta esteja quase cheio. Deixe o DCM terminar de mergulhar no gel de sílica e, em seguida, troque o frasco preenchido com um frasco vazio para a fração polar. Repita este processo com metanol.
Uma vez que o frasco esteja quase cheio, deixe o metanol terminar de escorrer no frasco e, em seguida, tampar todos os frascos. A fração polar média contém as alkenonas desejadas, enquanto os GDGTs estão na fração polar. Para amostras de alkenona particularmente sujas ou complexas, a fração média polar deve ser purificada ainda mais com adução de ureia, antes da análise.
A cromatografia da coluna é amplamente utilizada na química como técnica analítica e purificação.
Nanotubos de carbono, ou CNTs, são cada vez mais usados em muitas indústrias, mas há uma preocupação crescente de seus efeitos na saúde humana. Variar as propriedades das CNTs muda a forma como se comportam na água e no solo. Para investigar o quão bem a mídia porosa como areia e sujeira retêm CNTs, uma coluna foi preparada com solo poroso como fase estacionária. Primeiro, foram coletadas frações durante o carregamento da solução CNT na coluna para análise do transporte de CNTs pelo solo. Em seguida, as CNTs ainda adsorvidas ao solo foram elucidadas e as frações analisadas para a quantidade de CNTs que haviam permanecido no solo. Os resultados dão uma visão da relação entre a funcionalização superficial da CNT e seus mecanismos de transporte no ambiente.
A cromatografia da coluna pode ser operada em grandes e pequenas escalas e, portanto, é usada na concepção de sínteses para aplicações industriais. As sedas de aranha têm excelente resistência à tração e ductilidade, mas não podem ser colhidas em escala industrial. Seguindo a síntese de proteína de seda, as proteínas de seda recombinantes são purificadas pela cromatografia de afinidade, na qual a fase estacionária é projetada para prender apenas a molécula desejada. A lavagem e a elução completas concedem as frações de proteína pura necessárias para girar a seda de aranha em grandes escalas.
Muitas fases estacionárias estão disponíveis para cromatografia de coluna. Uma fase estacionária pode não ser adequada para todos os produtos potenciais de uma síntese com um amplo escopo substitutivo, como esta síntese de iodoaziridina. O produto bruto é misturado com várias fases estacionárias e decomposição avaliada pelo próton NMR. Como o Próton NMR é altamente sensível, muitas fases estacionárias podem ser rastreadas para decomposição do produto usando uma pequena quantidade de produto bruto. A cromatografia da coluna é então realizada com a fase estacionária ideal, permitindo a purificação de compostos novos e altamente reativos.
Você acabou de assistir a introdução de JoVE à cromatografia da coluna para a purificação de um extrato lipídedo total. O vídeo a seguir demonstrará como purificar ainda mais misturas complexas contendo alkenones.
Obrigado por assistir!
Subscription Required. Please recommend JoVE to your librarian.
Procedure
1. Instalação e Preparação de Materiais
- Obtenha um extrato lipídeco total (TLE) usando um método de extração de solvente (Sonication, Soxhlet ou Accelerated Solvent Extraction (ASE).
- Junte o seguinte: pipetas e lâmpadas de vidro borossilicato queimados, gel de sílica, hexano, diclorometano (DCM) e metanol.
- Esses materiais podem ser adquiridos de qualquer revendedor químico. Os reagentes devem ser puros e livres de hidrocarbonetos.
- Também obter lã de vidro queimada e frascos de vidro borossilicato de 4 mL.
- Certifique-se de ter um meio de apoiar a coluna e os frascos de coleta durante o procedimento. Por exemplo, um suporte com grampos e um rack vil. Muitos laboratórios projetaram racks feitos sob medida que possuem várias colunas e frascos de coleta(Figura 2). Isso permite que muitas colunas sejam executadas ao mesmo tempo.
2. Métodos
- Comece com a amostra seca em um frasco de 4 mL. Se a amostra pesa mais de ~ 10 mgs quando seca, pode precisar ser dividida antes de realizar os próximos passos, pois o gel de sílica só pode reagir com uma massa finita de matéria orgânica.
- Suspenda a amostra em uma pequena quantidade de hexano. Este é o primeiro e menos polar dos três solventes usados neste experimento.
- Se houver amostra presa no interior do frasco, sonicar as amostras por 5 minutos.
- Coloque uma pequena quantidade de lã de vidro no topo de uma pipeta usando um conjunto de pinças limpas. Empurre suavemente a lã de vidro para o fundo da pipeta, usando outra pipeta, para formar um plugue.
- Transfira cuidadosamente o gel de sílica para a pipeta até que esteja aproximadamente meio cheio.
- Coloque um frasco de coleta de resíduos de 4 mL sob a coluna.
- Mergulhe o gel de sílica na pipeta com 3 volumes de hexano. Isso condiciona a coluna, remove bolhas de ar e enxagua qualquer impureza do gel de sílica.
- Uma vez feita a lavagem final, remova o frasco de coleta de resíduos e substitua-o por um frasco para coletar a fração apolar.
- Transfira cuidadosamente toda a amostra em hexano para a coluna usando uma pipeta. Enxágüe o frasco de amostra mais duas vezes com pequenos volumes de hexano e transfira para a coluna. Deixe a hexana em que a amostra foi transferida para absorver completamente o gel de sílica. Em nenhum momento durante o procedimento o gel de sílica deve secar.
- Continue adicionando hexano ao topo da amostra até que o frasco de coleta abaixo da coluna esteja quase cheio (~4 mL).
- Deixe que todo o hexano entre no gel de sílica antes de começar com o próximo solvente.
- Coloque o frasco de coleta de polaridade média sob a coluna.
- Adicione DCM à parte superior da coluna até que o frasco de coleta esteja quase cheio. Novamente, permita que todo o DCM entre no frasco de coleta antes de iniciar o próximo solvente.
- Coloque o frasco de coleta polar sob a coluna.
- Adicione metanol ao topo da coluna até que a coleção vil esteja quase cheia.
A cromatografia da coluna é uma técnica flexível para purificar a complexa mistura de compostos encontrados em sedimentos. Misturas se separam à medida que se movem através da coluna e são coletadas em frações, cada uma contendo uma classe química diferente de compostos. Portanto, a cromatografia da coluna é frequentemente usada como um passo adicional de purificação após o isolamento inicial do composto desejado. Extratos orgânicos, como extratos lipídudos totais, podem ser misturas complexas de muitos compostos. Algumas técnicas de purificação, como a saponificação, introduzem compostos que podem danificar instrumentos analíticos e, portanto, devem ser removidos antes da análise. Este vídeo faz parte de uma série sobre extração lipídica, purificação e análise de sedimentos. Uma vez que um extrato lipídeca total é coletado de uma amostra sedimentar, a cromatografia da coluna é usada para purificar tanto alkenones quanto GDGTs, dependendo da análise desejada.
Na cromatografia da coluna, uma mistura de compostos químicos é carregada em uma fase estacionária sólida, como gel de sílica. Uma fase móvel como um solvente orgânico é então usada para eluto, ou remover, os compostos da coluna. A ordem em que os compostos são elucidos depende da força das interações dos compostos com o gel de sílica e com o eluente.
O eluato é coletado em frações, cada uma contendo compostos diferentes da mistura. Dependendo das propriedades dos compostos, um único solvente pode fornecer separação suficiente e elute todos os compostos de interesse. Caso contrário, vários solventes são usados para eluto cada composto de interesse por sua vez.
Compostos polares, que têm uma distribuição desigual de carga, adsorb fortemente para o gel de sílica polar, enquanto compostos apolar adsorb fracamente. Os solventes polares têm maior afinidade com o gel de sílica e, portanto, são eluentes mais poderosos do que solventes apolares. Assim, solventes apolares elute apenas compostos apolares, enquanto solventes polares elute tanto compostos apolares quanto polares.
Quando os compostos desejados são moderadamente polares, os compostos apolares devem ser lavados da coluna com um solvente apolar antes que um solvente polar seja usado. Para evitar a eluição de compostos altamente polares indesejados, como ácidos, um eluente polar não deve ter mais energia de eluição do que o necessário para o composto mais polar desejado.
Agora que você entende os princípios da cromatografia da coluna, vamos passar por um procedimento de purificação de biomarcadores lipídicos de um extrato lipídeca total pela cromatografia da coluna de gel de sílica.
Para remover contaminantes orgânicos, combustão borossilicato pipetas de vidro, frascos de vidro borossilicato e lã de vidro por 6 h a 550 °C. Uma vez que o vidro esteja pronto para uso, configure um rack para segurar pipetas e frascos. Obtenha lâmpadas pipetas, pinças limpas, espátula de laboratório, gel de sílica, hexano, diclorometano e metanol. Com pinças limpas, coloque um pequeno tufo de lã de vidro na boca de uma pipeta. Empurre suavemente a lã de vidro para o fundo da pipeta com a haste de outra pipeta para formar um plugue solto. Carregue cuidadosamente gel de sílica na pipeta até ficar meio cheio. Fixar a pipeta na parte vertical do rack. Fixar um frasco de vidro borossilicato de 4 mL abaixo da ponta da pipeta para coleta de lixo. Em outro frasco de vidro borossilicato, suspenda até 10 mg de amostra seca do processo de saponificação em hexano. Se a amostra grudar nas paredes do frasco, sonicar o frasco por 5 minutos. O procedimento de cromatografia já pode começar.
Para iniciar a cromatografia, lave a coluna de gel de sílica com 3 volumes de hexano para remover bolhas de ar e impurezas. Em seguida, substitua o frasco de resíduo por um frasco vazio para a fração apolar. Com uma pipeta de vidro, carregue a amostra na coluna e deixe a suspensão de molho no gel de sílica. Trabalhe rapidamente para que a coluna não seque durante o procedimento. Enxágüe o frasco de amostra duas vezes com pequenas porções de hexano e transfira cada enxágue para a coluna. Continue adicionando hexano à coluna até que o frasco de coleta esteja quase cheio. Deixe que toda a hexana termine de entrar no gel de sílica. Em seguida, troque o frasco preenchido com um frasco vazio pela fração média polar. Em seguida, enxágue o frasco de amostra com DCM e adicione-o à coluna 3 vezes. Continue adicionando DCM à coluna até que o frasco de coleta esteja quase cheio. Deixe o DCM terminar de mergulhar no gel de sílica e, em seguida, troque o frasco preenchido com um frasco vazio para a fração polar. Repita este processo com metanol.
Uma vez que o frasco esteja quase cheio, deixe o metanol terminar de escorrer no frasco e, em seguida, tampar todos os frascos. A fração polar média contém as alkenonas desejadas, enquanto os GDGTs estão na fração polar. Para amostras de alkenona particularmente sujas ou complexas, a fração média polar deve ser purificada ainda mais com adução de ureia, antes da análise.
A cromatografia da coluna é amplamente utilizada na química como técnica analítica e purificação.
Nanotubos de carbono, ou CNTs, são cada vez mais usados em muitas indústrias, mas há uma preocupação crescente de seus efeitos na saúde humana. Variar as propriedades das CNTs muda a forma como se comportam na água e no solo. Para investigar o quão bem a mídia porosa como areia e sujeira retêm CNTs, uma coluna foi preparada com solo poroso como fase estacionária. Primeiro, foram coletadas frações durante o carregamento da solução CNT na coluna para análise do transporte de CNTs pelo solo. Em seguida, as CNTs ainda adsorvidas ao solo foram elucidadas e as frações analisadas para a quantidade de CNTs que haviam permanecido no solo. Os resultados dão uma visão da relação entre a funcionalização superficial da CNT e seus mecanismos de transporte no ambiente.
A cromatografia da coluna pode ser operada em grandes e pequenas escalas e, portanto, é usada na concepção de sínteses para aplicações industriais. As sedas de aranha têm excelente resistência à tração e ductilidade, mas não podem ser colhidas em escala industrial. Seguindo a síntese de proteína de seda, as proteínas de seda recombinantes são purificadas pela cromatografia de afinidade, na qual a fase estacionária é projetada para prender apenas a molécula desejada. A lavagem e a elução completas concedem as frações de proteína pura necessárias para girar a seda de aranha em grandes escalas.
Muitas fases estacionárias estão disponíveis para cromatografia de coluna. Uma fase estacionária pode não ser adequada para todos os produtos potenciais de uma síntese com um amplo escopo substitutivo, como esta síntese de iodoaziridina. O produto bruto é misturado com várias fases estacionárias e decomposição avaliada pelo próton NMR. Como o Próton NMR é altamente sensível, muitas fases estacionárias podem ser rastreadas para decomposição do produto usando uma pequena quantidade de produto bruto. A cromatografia da coluna é então realizada com a fase estacionária ideal, permitindo a purificação de compostos novos e altamente reativos.
Você acabou de assistir a introdução de JoVE à cromatografia da coluna para a purificação de um extrato lipídedo total. O vídeo a seguir demonstrará como purificar ainda mais misturas complexas contendo alkenones.
Obrigado por assistir!
Subscription Required. Please recommend JoVE to your librarian.
Results
Esta técnica de purificação produz três frascos diferentes, cada um contendo uma classe composta diferente ou um grupo de classes compostas. A complexidade de qualquer amostra a ser analisada em um instrumento foi muito reduzida. Esse processo também remove compostos, como ácidos produzidos durante uma saponificação, que podem realmente grudar em partes dos instrumentos, devido à sua baixa volatilidade, o que diminuiria sua precisão, precisão e vida útil.
Subscription Required. Please recommend JoVE to your librarian.
Applications and Summary
Alkenones e GDGTs isoorenoidais são constituintes muito comuns de sedimentos marinhos e podem ser encontrados em todos os oceanos do mundo. Alkenonas estão sendo cada vez mais detectadas em sedimentos do lago, embora os organismos responsáveis por sua produção sejam diferentes do que no oceano, e assim a relação entre a razão Uk'37 e a temperatura da água (calibração) é diferente do oceano e até mesmo entre lagos separados. GDGTs isoorenoidais são encontrados em alguns lagos grandes e assim como alkenones, muitas vezes precisam de uma calibração local.
As alkenonas e GDGTs que estamos interessados em sair nas frações cetona e polar, respectivamente. Em sedimentos marinhos, muitas vezes analisamos tanto os proxies da temperatura da superfície do mar (SST) de uma amostra. Isso permite a construção de dois registros independentes de SST, que mostram a evolução da temperatura da água no local central ao longo do tempo. Essa comparação, chamada de abordagem multiproxy, muitas vezes destaca momentos em que os dois proxies concordam e os momentos em que não concordam. Este acordo ou discrepância em si contém informações. Se os dois proxies concordam, talvez os organismos produtores ocupassem o mesmo habitat de profundidade, ou talvez vivessem em profundidades separadas, mas uma coluna de água bem misturada levou à homogeneização vertical da temperatura (a água geralmente esfria com profundidade). Se os dois proxies discordam, pode ser que as duas populações viviam em profundidades separadas; um vivendo em águas quentes e rasas e outro em águas mais frias e profundas. Ou pode ser que os compostos foram produzidos em diferentes épocas do ano e assim refletir as temperaturas de diferentes estações. Essas questões são criadas pela análise de dois proxies diferentes da SST no mesmo local e destacam os cuidados que geoquímicos orgânicos e paleo-climatologistas precisam tomar ao interpretar seus dados.
Devido à alta estabilidade relativa dos hidrocarbonetos apolares, a fração apolar contém muitos compostos orgânicos interessantes. Alkanes são importantes constituintes da camada cerada externa de uma folha e são usados em registros de sedimentos por muitas razões. Seu comprimento médio da cadeia (número de átomos de carbono) contém informações sobre o domínio das plantas aquáticas versus terrestres, temperatura e precipitação. A razão isotópica de carbono em alcanos está relacionada com o tipo de planta C3 vs. C4 da planta que a produziu e a razão isotópica do hidrogênio está relacionada com a temperatura e precipitação local ao global. Steranes e hopanes também são encontrados na fração apolar. Estes biomarcadores são as versões geoestratésas de compostos bioativos como hopanoides e esteroides, que servem importantes papéis bioquímicos em prócarios e eucariotes, respectivamente.
A fração de polaridade média contém nossas alkenones. Alkenones são cetonas, que são importantes gravadores de temperaturas antigas da superfície através do proxy de temperatura da superfície do mar Uk'37. Algumas cetonas também vêm das mesmas ceras de folhas que os alcanos fazem, embora geralmente haja muito menos.
A fração polar contém ácidos carboxílicos, outro importante constituinte na cera de folha, que é ligeiramente menos específico e mais difícil de trabalhar do que alkanes (baixa volatilidade), mas pode, no entanto, relacionar algumas das mesmas informações. Tetraethers de glicerol de glicerol (GDGTs) estão na fração polar e são outro importante gravador de temperaturas antigas de água e ar.
Subscription Required. Please recommend JoVE to your librarian.
References
Killops, S. and Killops, V. Introduction to Organic Geochemistry. Blackwell Publishing, Malden, MA (2005).




