Summary
ここでは、温帯の自然条件下でのコロラドジャガイモ甲虫の冬眠を研究する方法と、冬に甲虫を採集する技術を紹介します。この方法により、冬眠のどの段階でも、さまざまな分析のために必要な数の越冬個体を得ることができます。
Abstract
温帯のジャガイモ Solanum tuberosum L.の主要な害虫の1つは、昆虫のコロラドジャガイモカブトムシ(CPB)です。CPBの免疫と疾患に関するほとんどの研究は、活発な摂食段階で実施されます。それにもかかわらず、これらのカブトムシはライフサイクルのほとんどを冬の休眠状態(冬眠)で過ごしますが、休息段階に関する研究は少ないです。この研究では、自然条件下でのCPB冬眠を調査する方法が開発され、テストされ、冬に十分な数の個体を収集する機会が提供されました。本稿では、CPBの生存率を評価し、冬眠のさまざまな段階にある感染性病原体を同定した。CPBによる死亡率は冬眠中に増加し、4月から5月にかけて最大値に達した。昆虫病原性真菌(Beauveria、 Isaria、 Lecanicillium)および細菌 Bacillus、Sphingobacterium、Peribacillus、Pseudomonas、および Serratia は、死んだ昆虫から分離されました。冬眠期間全体のカブトムシの生存率は61%でした。凍結または乾燥した甲虫は見つからず、提示された方法の成功を示しています。
Introduction
コロラド州のジャガイモのカブトムシLeptinotarsa decemlineata Say(CPB)は、ナス科植物、主にジャガイモSolanum tuberosum Lの重要な害虫です。この種の地理的範囲は1600万km2以上であり、常に拡大しています1。CPBは通性冬季休眠があり、温帯では冬眠が義務付けられています。休眠は短日日長によって誘発され、温度1によって調節される。成虫期には土に穴を掘って越冬します。緯度が上がるにつれて、冬眠期間が長くなります。温帯、特にその範囲の北方領土では、越冬は8月から9月までの5月から6月までの9か月間続きます(Noskovら、個人的な観察)。この期間中、CPBは、温帯の他の昆虫と同様に、不利な冬の条件にさらされ、耐寒性を高める必要があります。同時に、カブトムシが土壌と接触すると、さまざまな日和見微生物や病原性微生物による感染のリスクが高まります2。そのため、これらのカブトムシは冬眠中に一定レベルの免疫系活動を維持する必要があり、これもエネルギー的にコストがかかります。それにもかかわらず、昆虫が感染を生き延びたとしても、病気はその耐寒性を低下させる可能性があります3。低温がCPBの冬の死亡率の唯一の理由ではないことに注意する必要があります。酸素の欠乏も重要な役割を果たしており、条件によっては、冬の死亡率の主な要因となる可能性があります4,5。
CPBの冬季の自然死亡率は非常に高く、粘土質ローム土壌では100%に達することが知られています6。したがって、越冬はCPBライフサイクルにおいて最も重要な時期の1つです。それにもかかわらず、自然条件下でのCPB冬眠の生理機能、免疫系活性、生存率、およびその他のパラメータに関するデータはまだ限られています。休眠中およびコールドショックに応答するCPB成人の遺伝子発現の違いとさまざまな生理学的パラメーターに関する研究があります7,8,9,10,11,12;しかし、これらの分析は、主に、温度、湿度、および固有の病原体負荷の自然な変動のない実験室条件下での休眠または寒冷ストレスの誘発によって行われてきました。しかし、自然条件下で土壌から発掘して採取したこれらの甲虫の生理学に関する研究は重要です。1970年代から1980年代にかけて、自然条件下でのCPB越冬のさまざまな側面が活発に研究されました13,14,15,16,17,18。一方、これらの研究は、冬季の土壌からのCPB掘削を含みませんでした。また、CPBの冬眠を制御するための技術やケージの説明については、詳細には説明されていません。したがって、自然環境で越冬するCPBの生理機能の調査が必要である19。
この研究の目的は、自然条件下でCPB成虫の冬眠を制御する方法を開発し、テストすることでした。提案手法は、大陸性気候の野外条件下での冬眠中に、微生物学的、免疫学的、およびその他のアッセイのために所望の数のCPB個体を得ることを可能にします。この方法は、雪の下の土壌で越冬する他の昆虫種にも適用できます。
Subscription Required. Please recommend JoVE to your librarian.
Protocol
1.冬眠用ケージの説明
注:実験の目的に応じて、ケージの数は異なります。サンプリング日ごとに少なくとも3つのケージを使用してください。羽化するカブトムシの数を見積もるには、春まで土から取り出さない少なくとも3つの追加のケージを準備します。
- ケージは、25×25×40cm(L × W × H)のサイズの硬い木製フレームで作られたものを使用してください。
- ケージのフレームを作るには、厚さ2cm以上、幅4cm以上の木製スラットを使用します。
- ケージの内側を、5 mm×3 mm以下の開口部のサイズのステンレス鋼メッシュで覆います。木のホッチキスを使用してメッシュを固定します。
- ステンレスメッシュをホッチキスで底の外側に固定します。
- ケージの内側を密度60 g / m2の黒い合成ジオテキスタイルで裏打ちします。
注:ジオテキスタイルは、カブトムシの脱出を防ぐための追加のバリアとして機能します。活発に動く昆虫病原体や寄生虫に関連する実験には使用しないでください。 - 高さ約60cmの合成半透明の通気性生地のチューブをケージの上部にしっかりと取り付けます。
- ケージの底に2本の強力なロープを交差させて固定し、必要に応じて土から引き出します。
2.ケージの設置
- 土に40cmの深さの穴を掘り、中にケージを置きます。
- 穴に枯れ草や干し草を置きます。
- 干し草や枯れ草がケージの壁と土の間に来るようにケージを内側に置きます。
- 昆虫が集められたのと同じジャガイモ畑の土でケージを満たします。
- 防水温度および湿度データロガーをケージ内の必要な深さに設置します。
注意: どのメーカーのデータロガーでも使用でき、低温で動作できる必要があります。 - 甲虫の導入の3〜4週間前に各ケージ内にジャガイモの苗を植え、適度に水をやります。
- 合成繊維のチューブをケージの外側に取り付けられた素材の棒に垂直に固定します。
3. 越冬前の昆虫の飼育
- ジャガイモの植生の終わりに向かって無農薬のジャガイモ畑で成虫のカブトムシを手作業で集めます。
注:成虫のカブトムシは幼虫とは大きく異なり、縞模様の鞘翅が特徴ですが、幼虫は赤です。 - 集めたカブトムシを、昆虫に餌を与えるためのジャガイモのてっぺんが入った15〜20Lのプラスチックバケツ(バケツあたり最大200個)に入れてからケージに入れます。
- 通気性のある布でバケツを覆います。
注意: 昆虫をバケツに12時間以上保管しないでください。バケツの底にカブトムシが蓄積するのを防ぐために、十分な大きさのジャガイモの上部を使用してください。 - 合成繊維メッシュで覆われたジャガイモの植物に200個以下のCPB個体を配置します。
- ポテトトップスが消費されたら、水の入ったプラスチックの瓶にセットされた新しいものを追加し、その後毎日ポテトトップを交換します。
注意: 瓶に茎を固定するには、脱脂綿とパラフィルムを使用します。古い茎を取り除くときは、カブトムシがないか注意深くチェックしてください。 - すべてのカブトムシが越冬のために土に穴を掘ったら、棒から合成繊維のチューブをほどき、布を置きます。
4.冬季の昆虫採集
- ケージの表面の上の雪を取り除きます。
- 強力なシャベルで両側のケージを緩めます。
- ロープを使ってケージを土から引き出します。
- ケージをラボに持参します。
注:実験の目的によっては、冬眠中のカブトムシを分析前に不活性にする必要がある場合があります。この場合、カブトムシを土壌から分離する際の実験室の温度は、2~5°Cでなければなりません。 - 箱から土を少しずつ取り出し、大きな土を慎重に砕き、ピンセットでカブトムシを隔離します。
- 生きたカブトムシを死体から分離します。生きている健康なカブトムシは、周囲にコンパクトな土壌を作り、空気空洞(いわゆるクレードル)を形成するため、土壌から簡単に分離できます。真菌によって殺されたカブトムシは、ミイラ化しているか、表面に菌糸体が見えます。バクテリアで分解する昆虫は暗いです。
- ふるいを通して土をふるいにかけ、すべてのカブトムシが孤立し、損傷していないことを確認します。
- 真菌感染または細菌分解の症状のある死体は、将来の識別のために、個々の滅菌15 mL遠心チューブに入れます。
- 生きたカブトムシは、湿らせた綿球が入った密閉された換気容器で分析するまで、0〜2°Cの温度で冷蔵庫に保管してください。
5. 臓器・組織サンプルの調製
- 血リンパ液を採取するには、インスリン針を使用して鞘翅の下の腹部の外側部分に穿刺します。
注:越冬中は血リンパ液の量が大幅に減少し、この液体を採取することが困難になります。 - 腸を分離するには、ヘッドカプセルを切り取り、すべての内容物をリン酸緩衝液を含むペトリ皿に絞り出し、腸を分離し、脂肪とマルピーギ血管を浄化します。
- 前腸、中腸、後腸など、腸の目的の部分を分離します。
- 脂肪体を分離するには、腸を分離した後、他の組織から分離します。
注:単離された組織は、抗酸化酵素や解毒酵素の活性の測定(例:補足 図1)、免疫シグナル伝達経路遺伝子の調節の解析(例: 補足図2)、昆虫の腸内容物のメタバーコーディングなどに使用できます。
6.死体からの微生物の分離
- 昆虫病原性真菌を死体から分離するには、ミイラ化した昆虫を滅菌湿度チャンバーに入れます。
- カブトムシの内部内容物からの空中分生子(利用可能な場合)または菌核を使用して、0.4%乳酸を含むSabouraudデキストロース寒天にめっきします。
注意: 菌糸体と分生子を備えたカブトムシは、すぐにメッキに使用してください(湿度チャンバーに入れないでください)。 - 細菌分解の症状がある死体から細菌を分離します。
- カブトムシの頭を切り落とし、内部の内容物を絞り出し、チューブに集めて、バクテリアの培地(ルリア・ベルタニ寒天培地、エンド寒天培地、胆汁エスクリン寒天培地)にめっきします。
注:顕微鏡と分子学的方法を使用して、病原体の属と種を特定します。必要に応じて、他の寄生虫の存在についての分析を行うことができます。
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
以下の越冬CPBの結果は、土壌温度、生存率、感染性を示しています。
土壌温度のダイナミクス。
11月下旬から4月上旬にかけて、水深30cmのケージ内の氷点下の気温を記録しました(図1)。この期間の平均気温はマイナス3.3°C±0.1°C(標準誤差±平均)でした。最低気温は2月中旬のマイナス7.9°Cでした。
越冬CPBの生存。
昆虫の死亡率は冬眠中に見られ、羽化前の春に最大に達しました。当初のカブトムシ数は2000頭で、5月末までに1470頭が生き残った。冬眠中のカブトムシの生存率は61%でした(図2)。
越冬CPBの感染。
530匹のカブトムシの死骸を分析したところ、冬眠期間中、53%に細菌分解の症状があり、25%に真菌感染症の症状がありました(図3)。 Beauveria は、昆虫病原性真菌の孤立した培養物の中で優勢(45の分離株)でした。 Metarhizium、冬虫夏草 (=Isaria)、 およびLecanicillium ははるかに一般的ではありませんでした(それぞれ2つの分離株)。細菌分解の症状を呈した死体から分離された細菌(n=30)のうち、バチルス属、ス フィンゴバクテリウム属、ペリバチルス属、シュードモナス属、セラチア属、ラネ ラ属および グルタミシバクター 属に属する種が同定された(付表1)。

図1:地温の動態 水深30cmに設置された防水温度データロガーで測定した地温動。 この図の拡大版をご覧になるには、ここをクリックしてください。

図2:冬眠期間の違いによる越冬中のコロラドジャガイモ甲虫の生存率。 ケージを掘り出し、11月、1月、4月、5月に生き残ったカブトムシと死んだカブトムシを数えました。ひげは標準誤差を示します。 この図の拡大版をご覧になるには、ここをクリックしてください。

図3:越冬中のコロラドジャガイモ甲虫の死体における感染。 この図の拡大版をご覧になるには、ここをクリックしてください。
補足資料:以下の補足ファイルをダウンロードするには、ここをクリックしてください。
補足図1.冬眠中のCPBの中腸における非特異的エステラーゼの活性。 ひげは標準誤差を示します。異なる文字は、時点間の有意差を示します(Dunnの検定、P < 0.05)。
補足図2:冬眠中のCPBの腸および脂肪体における転写因子NFκB(IMD経路)の発現の変化。データは、8 月の時点に対する倍数の変化として表示されます。Rp4、Rp18、およびArf19を参照遺伝子として使用しました。 ひげは標準誤差を示します。
補足表1:冬眠中に死んだCPBから分離された細菌の16S rRNA(~800 bp)遺伝子配列の推定同定。
Subscription Required. Please recommend JoVE to your librarian.
Discussion
本研究は、CPBの越冬を研究するための提案手法により、異なる冬眠期間において十分な数の昆虫を獲得できることを示している。提示された技術の成功は、いくつかの独立した要因に依存しますが、その中で最も重要なのは気象条件です。雪の降らない寒い冬には、土がケージの奥深くまで凍ってしまうことがあります。この場合、すべてのカブトムシの死のリスクが大幅に上昇します18。カブトムシの生存は多くの要因の組み合わせに依存し、それは年ごとに大きく異なる可能性があります6。
実験では、冬季のケージ内の土壌温度はマイナス7.9°Cを下回りませんでした。 水深25cm以上の氷は観測されず、最も寒冷化が激しい時期(1月〜2月)でも土壌は緩いままであった。ほとんどのカブトムシは、各ケージの下部、30〜40 cmの深さに蓄積しました。カブトムシは、ケージの深さが深くなるほど深く穴を掘ったのかもしれません。一方、ケージの深さを増すと重量が増加し、特に冬場はケージを土から取り出すのが難しくなります。さらに、調査対象地域のジャガイモ畑での観察によると、CPBは越冬のために35cmより深く穴を掘ることはありません。この発見は、カブトムシが克服できない深さ30〜35 cmの粘土質土壌層によって説明できます。私たちの実験では、地平線上30cmの砂質ローム質の土壌を使用しました。これが、カブトムシが自然条件下よりも深く穴を掘ることができた理由でしょう。CPBが冬眠する深さは通常10〜25cmですが(参考文献 1)、これは地理的な地域によって異なる場合があります。例えば、米国北東部(ニュージャージー州)では、ほとんどの甲虫が水深10〜13cmで冬眠します(文献 13)。同様の越冬深度(≤15cm)の甲虫は、米国ウィスコンシン州でも記録されている18。ウラル山脈南部(ロシア)では、CPBが越冬のために巣穴を掘る深さは5〜30cmの範囲です(文献 20)。昆虫の生存率は、越冬深度の増加と必ずしも正の相関があるとは限らないことに注意すべきである1。実際、エストニア6での野外越冬実験では、CPBの生存率は水深50cmよりも水深30cmの方が高いことが示されました。著者らは、この発見は酸素不足によるものかもしれないと提唱している。米国ウィスコンシン州での野外実験でも同様のデータが得られており18、越冬したCPBの生存率(51.5%)は水深15-25cmで記録された。同時に、18、カブトムシの100%の死亡率が25〜35cmの深さで記録されました。温帯での実験には、生き残った甲虫の割合が高く、土壌凍結がケージの深さ全体に及ばなかったため、40cmの深さで十分であると考えています。積雪の存在は、土壌の冷却を弱めます。必要に応じて、ケージの表面より上の積雪の厚さを調整できます。
プロトコルのもう一つの重要な点は、少量の貯蔵栄養素のために、CPBの越冬の準備が不十分である可能性があることです。一部の成虫のCPBは、カブトムシが大量に土壌に穴を掘った後、土壌表面に残っていました。越冬の成功は蓄積された栄養素の量にも依存するため、十分な脂肪を蓄えられなかった可能性があります21。また、冬に生け簀を土から取り出すと、一部の甲虫は土表や表層付近で凍った状態になっていました。おそらく、これらは栄養失調、感染症、またはその他の有害な要因のために穴を掘るのに十分なエネルギーを持っていないカブトムシでした。Lashomb et al.13 は、CPBの越冬実験で、成虫の~15%が越冬のために土壌に穴を掘らなかったことを指摘しました。これらの著者は、その理由を論じなかった。いずれにせよ、カブトムシに十分な餌を与える必要があります。
研究の目的によっては、カブトムシを土壌から採取した後、冬眠状態に保つ必要がある場合があります。この目的のために、実験室の温度を涼しくし、カブトムシは土壌から抽出した後すぐに0〜2°Cの条件に置く必要があります。私たちの研究では、秋と春に、CPBは土壌から掘り出された後、ほぼ即座に自発運動活動を開始することが観察されました。このプロセスは、真冬にはるかにゆっくりと行われます。
この研究では、活発に動く昆虫病原体と寄生虫は考慮されていませんでした。CPBの蔓延に対する追加の障壁としてジオテキスタイルを使用しました。ジオテキスタイルは、活発に動く昆虫病原体(昆虫病原性線虫など)、捕食者、寄生虫の研究には使用しないでください。
CPBの免疫と疾患に関する研究は、主に活発な摂食期に行われることを指摘することが重要です。安静期はあまり調査されておらず、主に実験室条件下で検査されています。しかし、このような条件下では、自然飼育地で発生する温度・湿度・曝気の変動をシミュレーションすることは困難です。したがって、野外実験が好ましい22。異なる冬眠期間における野外でのCPB冬季死亡率の原因を特定するには、土壌から越冬する甲虫を発掘する必要があります。1970年代から1980年代にかけて、自然条件下でのCPB越冬に関する研究が盛んに行われました。これらの論文で述べられている方法は、主に春に羽化した個体を採集して数えること13、越冬前に昆虫病原性真菌14,15,16または昆虫病原性線虫15を使用することの有効性を評価し、春と秋に越冬した甲虫を土壌から採取して冬の自然死亡率を決定すること17である.同時に、これらの実験で使用されたケージのサイズと形状は、20×20 cmから90×90×90 cm(文献13)または180×60×30 cm(文献18)までさまざまでした。前述の研究は、冬に昆虫を採集する可能性を備えたCPB越冬の方法論を開発することを目的としていないことを指摘する必要があります。既存の方法とは異なり、本稿で紹介する手法では、積雪期における自然CPB個体群の調査が可能となる。
結論として、提案手法により、研究者は、昆虫の死亡率が比較的低く、低コストで、自然条件下で越冬するCPB個体数を得ることができます。CPB冬眠のさまざまな側面の調査は、基礎研究と応用の両方の観点から、この害虫の防除へのアプローチを改善するために不可欠です。この技術は、土壌で越冬する他の昆虫種にも適用できます。将来の研究者は、この方法を応用して、さまざまな昆虫種の一般的な生理学と生化学(越冬期の免疫を含む)を研究する可能性があります。さらに、この方法は、冬の死亡率に基づいて、関心のある害虫の豊富さを予測するために使用できます。
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
著者らは、競合する利害関係はないと宣言しています。
Acknowledgments
同僚のVladimir Shilo氏、Vera Morozovа氏、Ulyana Rotskaya氏、Olga Polenogova氏、Oksana Tomilova氏には、フィールドと実験手順の整理と実行に協力していただいたことに感謝します。
この研究は、ロシア科学財団(プロジェクト番号:22-14-00309)の支援を受けました。
Materials
| Name | Company | Catalog Number | Comments |
| Agar-agar bacteriological purified | diaGene | 1806.5000 | |
| Bile Esculin Agar | HiMedia | M972 | |
| Endo Agar | HiMedia | M029 | |
| Glucose monohydrate-D | PanReac Applichem | 143140.1000Φ | |
| Lactic acid | PanReac Applichem | 141034.1211 | |
| Luria-Bertani liquid medium | HiMedia | G009 | |
| 15 ml conical centrifuge tubes | Axygen | SCT-15ML-25-S | |
| Peptone | FBIS SRCAMB | M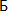 030/O61 030/O61 |
|
| Phosphate buffered saline | Medigen | PBS500 | |
| Temperatutre and humidity datalogger Ecklerk-M-11 | Relsib | Waterproof datalogger |
References
- Alyokhin, A., Benkovskaya, G., Udalov, M. Colorado potato beetle. Insect Pests of Potato. , Academic Press. 29-43 (2022).
- Alyokhin, A., Kryukov, V. Ecology of a potato field. Insect Pests of Potato. , Academic Press. 451-462 (2022).
- Lee Jr, R. E., Costanzo, J. P., Kaufman, P. E., Lee, M. R., Wyman, J. A. Ice-nucleating active bacteria reduce the cold-hardiness of the freeze-intolerant Colorado potato beetle (Coleoptera: Chrysomelidae). Journal of Economic Entomology. 87 (2), 377-381 (1994).
- Ushatinskaja, R. S. Diapause of insects and its modifications. Journal of General Biology. 34, In Russian 194-215 (1973).
- Zheng, X. L., et al. Effect of soil moisture on overwintering pupae in Spodopteraexigua (Lepidoptera: Noctuidae). Applied Entomology and Zoology. 48, 365-371 (2013).
- Hiiesaar, K., Metspalu, L., Jõudu, J., Jõgar, K. Over-wintering of the Colorado potato beetle (Leptinotarsa decemlineata Say) in field conditions and factors affecting its population density in Estonia. Agronomy Research. 4 (1), 21-30 (2006).
- Yocum, G. D., Rinehart, J. P., Chirumamilla-Chapara, A., Larson, M. L. Characterization of gene expression patterns during the initiation and maintenance phases of diapause in the Colorado potato beetle, Leptinotarsa decemlineata. Journal of Insect Physiology. 55 (1), 32-39 (2009).
- Yocum, G. D., Buckner, J. S., Fatland, C. L. A comparison of internal and external lipids of nondiapausing and diapause initiation phase adult Colorado potato beetles, Leptinotarsa decemlineata. Comparative Biochemistry and Physiology Part B: Biochemistry and Molecular Biology. 159 (3), 163-170 (2011).
- Nikonorov, Y. M., Syrtlanova, L. A., Kitaev, K. A., Benkovskaya, G. V. Transcription activity of genes involved in diapause regulation in the Colorado Potato beetle and its change under a fipronil impact. Russian Journal of Genetics: Applied Research. 8, 80-86 (2018).
- Govaere, L., et al. Transcriptome and proteome analyses to investigate the molecular underpinnings of cold response in the Colorado potato beetle, Leptinotarsa decemlineata. Cryobiology. 88, 54-63 (2019).
- Lehmann, P., Westberg, M., Tang, P., Lindström, L., Käkelä, R. The diapause lipidomes of three closely related beetle species reveal mechanisms for tolerating energetic and cold stress in high-latitude seasonal environments. Frontiers in Physiology. 11, 576617 (2020).
- Lebenzon, J. E., Torson, A. S., Sinclair, B. J. Diapause differentially modulates the transcriptomes of fat body and flight muscle in the Colorado potato beetle. Comparative Biochemistry and Physiology Part D: Genomics and Proteomics. 40, 100906 (2021).
- Lashomb, J. H., Ng, Y. S., Ghidiu, G., Green, E. Description of spring emergence by the Colorado potato beetle, Leptinotarsa decemlineata (Say) (Coleoptera: Chrysomelidae), in New Jersey. Environmental entomology. 13 (3), 907-910 (1984).
- Cantwell, G. E., Cantelo, W. W., Schroder, R. F. Effect of Beauveria bassiana on underground stages of the Colorado potato beetle, Leptinotarsa decemlineata (Coleoptera: Chrysomelidae). The Great Lakes Entomologist. 19 (2), 6 (1986).
- Fedorko, A., Bajan, C., Kmitowa, K., Wojciehowska, M. Effectiveness of the use of selected microorganisms to control the Colorado beetle during hibernation. Ecological Studies. 3 (2), 127-134 (1977).
- Gaugler, R., Costa, S. D., Lashomb, J. Stability and efficacy of Beauveria bassiana soil inoculations. Environmental Entomology. 18 (3), 412-417 (1989).
- Bajan, C., Kmitowa, K. Contribution of entomopathogenic fungi to the natural winter reduction of Colorado beetle adults. Polish Ecological Studies. 3 (2), 107-114 (1977).
- Milner, M., Kung, K. S., Wyman, J. A., Feldman, J., Nordheim, E. Enhancing overwintering mortality of Colorado potato beetle (Coleoptera: Chrysomelidae) by manipulating the temperature of its diapause habitat. Journal of Economic Entomology. 85 (5), 1701-1708 (1992).
- Doğan, C., et al. Characterization of calcium signaling proteins from the fat body of the Colorado Potato Beetle, Leptinotarsa decemlineata (Coleoptera: Chrysomelidae): Implications for diapause and lipid metabolism. Insect Biochemistry and Molecular Biology. 133, 103549 (2021).
- Benkovskaya, G. V., Udalov, M. B. Colorado potato beetle investigations in the south Urals. Nova Science Publishers. , (2011).
- Short, C. A., Hahn, D. A. Fat enough for the winter? Does nutritional status affect diapause. Journal of Insect Physiology. , 104488 (2023).
- McDonald, J. R., Bale, J. S., Walters, K. F. A. Low-temperature mortality and overwintering of the western flower thrips Frankliniella occidentalis (Thysanoptera: Thripidae). Bulletin of Entomological Research. 87 (5), 497-505 (1997).



