Summary
여기 선물이 집중 치료 단위, 즉 cefepime, meropenem, ciprofloxacin, moxifloxacin, linezolid, 및 piperacillin에서에서 자주 사용 되는 항생제의 정량화를 위한 탠덤 질량 분석 기반 프로토콜.
Abstract
특히 병원 항생제 관리 프로그램의 구현에 관한 많은 임상 시설에서 항생제의 치료 약물 모니터링에 대 한 늘어나는 수요를 있다.
현재 작업에서는 cefepime, meropenem, ciprofloxacin, moxifloxacin, linezolid, 및 일반적으로 사용 되는 piperacillin의 정량화에 대 한 다중-고성능 액체 크로마토그래피 탠덤의 질량 분석 (HPCL-MS/MS) 프로토콜 소개 집중 치료 단위에 항생제입니다. 메서드는 이전 유럽 약 기관의 지침에 따라 포괄적으로 검증 된다.
빠른 샘플 정리 후에 analytes는 4 분 이내 C8 역 상 HPLC 열에 분리 하 고 해당 안정 동위 원소 라는 내부 표준 여러 반응에 분무 이온화 (ESI +) 질량 분석에서 정량 시간 모니터링 (MRM)입니다. 제시 방법은 간단한 계측 균일 한 컬럼에 조건 설정, 임상 실험실에서 매일 하 고 강력한 항생제 치료 약물 모니터링에 대 한 허용을 사용 합니다. 보정 곡선 함으로써 민감한 박테리아 및 피크 농도 (C최대) bolus로 가져온 최소 억제 농도 (MIC) 가까이 항생제 금액을 포함 한 pharmacokinetic 농도 범위에 걸쳐 관리 식이요법입니다. 샘플 정리 하기 전에 혈 청 희석이 필요 없이 관리 항생제에 대 한 곡선 아래의 영역 여러 측정을 통해 얻어질 수 있다.
Introduction
항생제는 의학의 실천에 혁명을, 비록 심각한 세균 감염 병 적 상태 및 중요 한 질병1사망률의 주요 원인이 남아 있습니다. 이와 관련, 적절 한 복용량에 적합 한 조직과의 프롬프트 관리 질병 통제2최고 중요성 이다.
증거의 성장 몸은 넓 스펙트럼 항생제와 경험적 치료 환자 집단의 복잡도와 점점 더 문제가 되고있다 보여줍니다. 이것은 특히 집중 치료 단위 (ICU)에 대 한 사실 어디 키 pharmacokinetic (PK) 매개 변수의 엄청난 간 개별 다양성은 자주 관찰3,4. 따라서, 중 환자 실 환자 부족 치료 성공을5,6의 위험 치료 하위 레벨의 절박 한 위험이 있습니다. 그럼 다시, 환자는 심각한 부작용 없이 임상 혜택7에서 발생할 수 있는 항생제 농도 지나치게 높은 불필요 하 게 노출 된다. 항생제 오용 및 부족 한 먹이 지 보건8적 성장 위협 되 고 항생제 저항의 보급을 연료도 있습니다.
항생제의 사용을 개선 하 고 그들의 effectivenessas를 유지 하기 위해, 가능한 한 세계 보건 기구 20159에 항균 성 저항에 대 한 글로벌 행동 계획에 착수 했다. 항생제 관리 프로그램 구성 국가 공중 보건 전략10, 같은 시간에, 그리고 환자 치료11 의 품질을 크게 개선 임상을 돕고 신중한 항균 성 사용의 필수적인 초석 항생제 저항12감소. 항균 성 치료 약물의 응용 프로그램을 통해 개별 환자에서 투약 모니터링 (TDM)이 컨텍스트13주요 악기 이다.
날짜 하려면, 상용 TDM 분석 실험 glycopeptide 항생제와 aminoglycosides 사용할 수만 있습니다. 다른 클래스에서 물질의 정량화는 일반적으로 사내 방법 개발 또는 성가신 수 있는 유효성 검사를 해야 합니다. 그러므로, 선물이 자세히14그들의 임상 관련 농도 범위 내에서 중 환자 실에 가장 관련성이 높은 항생제의 정량화에 대 한 사용할 수 있는 강력한 질량 분석 기반 분석에 대 한 프로토콜. 메서드와 우리의 질량 분석 시설에 최근에 설립 이후로 루틴 중 환자 실에서 TDM에 대 한 적용 되었습니다. 절차 유니폼 샘플 정리, 질량 분석 기능을 갖춘 많은 시설에서 항생제 TDM의 신속한 구현을 위한 수 있도록 간단 하 고 단순 분석 설정을 사용 합니다.
여기에 설명 된 프로토콜은 cefepime, meropenem, ciprofloxacin, moxifloxacin, linezolid, 및 탠덤와 함께에서 동위 원소 희석 액체 크로마토그래피 (LC)를 사용 하 여 인간의 혈 청에 piperacillin의 정량화에 대 한 최적화 된 질량 분석 (MS/MS)입니다. 동위 원소 희석 LC-MS/MS 방법론에 대 한 안정 동위 원소 표시 된 화합물 (예, 혈 청) 특정 행렬에 대 한 관심의 샘플에 추가 됩니다. 동위 원소 분류 기준은 그들의 레이블 없는 대응, 즉 자연 분자 및 부모 이온-하-딸-이온 전환 되 나, 그들의 조각화 제품의 다른 분자 중량으로 관심의 분석에서에서 구분할 수 있습니다. 동위 원소 라는 화합물 그들의 레이블 없는 대응에 비해 거의 동일한 전반적인 물리 화학 행동으로, 그들은 MS/MS의 높은 수준으로 거의 매트릭스 독립적인 분석 정량화를 허용에 대 한 이상적인 내부 표준 정확도15. 요즘, 많은 안정 동위 원소 라는 내부 표준 작은 분자 정량화, 항균, TDM을 포함 하 여 사용할 수 있는 상업적으로 사용할 수 있습니다.
설명된 프로토콜에서 항생제 analytes 컬럼에 분리 분석 C8 알 킬 체인 길이 역 상 열 (100 m m x 2.1 m m, 3 µ m 입자 크기)으로 수행 됩니다. 방법 개발 하는 동안 모든 analytes에 대 한 내부 표준 정규화 된 매트릭스 요소 94.6%와 105.4%, ≤8.314의 변형 계수 했다.
Subscription Required. Please recommend JoVE to your librarian.
Protocol
참고: 메탄올 등 유기 용 매를 처리할 때 증기 두건에서 작동 하도록 추천 된다. 부피 측정 플라스 크에서 모든 버퍼 및 모바일 단계를 준비 합니다. 지정 하지 않으면, 솔루션 준비 후 최대 1 달 동안 실내 온도에 저장할 수 있습니다.
1. 교정기 및 품질 관리 샘플의 준비
참고: 재고 및 스파이크 솔루션의 준비에 대 한 해당 데이터 분석 시트 추가 파일에 제공 됩니다. 추적의 이유로 해당 열에는 제조 업체, 카탈로그 번호 및 각 항생제의 많은 수를 삽입 합니다. 4 ° C에서 냉장에서 모든 항생제를 녹이 고 작업 시간을 가능한 한 짧게 유지.
- 준비 물에 25% 메탄올 100 mL: 절대 메탄올 25 mL를 100 mL 부피 플라스 크 프리 필과 그것을 채울 최대 100 mL 증류수.
- 준비 물에 200 m m 초 산의 10 mL: HPLC 학년 물 9 mL와 10 mL 부피 플라스 크 프리 필 빙 초 산 (순도 99.5%, 17.4 M)의 115 µ L을 추가 하 고 증류수를 추가 최대 10 mL.
- 20 mM 아세트산과 물에서 25% 메탄올 25 mL를 준비: 수성 200 m m 초 산 솔루션의 2.5 mL와 25 mL 부피 플라스 크 프리 필 절대 메탄올의 6.25 mL을 추가 하 고 증류수와 25 mL를 플라스 크를 채우기.
- 전체 규모를 사용 하 여 열 초기 무게 추가 파일 에 설명 된 대로 15 mL 원뿔 튜브에 항생제의 적절 한 양의 무게를.
- Fluoroquinolones, ciprofloxacin, moxifloxacin 25% 메탄올-물 20 m m 초 산 등의 재고 솔루션을 준비 합니다. "마지막 볼륨" 열에 있는 추가 파일 에 설명 된 대로이 중된 수량을 해당 볼륨을 추가 합니다. 빠르게 2 분 및 강렬한 vortexing에 의해 초음파 목욕 fluoroquinolone 항생제 분해.
- Cefepime, meropenem, linezolid, 및 25% 메탄올-물에서 piperacillin의 재고 솔루션을 준비 합니다. 이렇게 하려면 열 마지막 볼륨 에 추가 파일 에 설명 된 대로 해당 볼륨이 수량을 추가 하 고 빠르게 강렬한 vortexing에 의해 항생제를 분해 합니다. 마지막 물질로 meropenem을 디졸브.
- 10 배 농축된 스파이크 해결책을 보충 파일 에 재고 솔루션의 해당 볼륨 차트에 설명 된 대로 모든 항생제의 재고 솔루션을 결합 합니다.
- 0-7 혈 청 교정기를 10 배로 집중된 스파이크 해결책의 1 개의 볼륨으로 마약 없는 혈 청의 9 볼륨 스파이크와 품질 제어 (QC) A-d. 예를 들어 10 mL 폴 리 프로필 렌 튜브에 혈 청의 4.5 ml 스파이크 해결책의 0.5 mL을 추가 하 고 50 rpm에서 롤러 믹서에 4 ° C에서 냉장에서 15 분 동안 품 어.
- 1.5 mL 폴 리 프로필 렌 튜브에 교정기 및 QCs 100 µ L aliquots를 생성 하는 반복적인 피 펫을 사용 합니다.
- 교정기, 품질 제어 및 항생제 재고 솔루션-80 ° C에서 최대 6 개월까지 저장 합니다.
- 각 항생제에 대 한 또한 단일 항생제의 1000 mg/L를 포함 하는 깔끔한 솔루션을 준비 합니다. (예를 들어, ciprofloxacin를 사용 하 여 25% 메탄올-물 20 m m 초 산을 포함 하 여에 대 한)는 적절 한 희석 액으로 해당 재고 솔루션을 희석.
참고: 깔끔한 항생제 솔루션은 악기 튜닝 필요만.
2입니다. 내부 표준 혼합의 준비
참고: 내부 표준 샘플 정리 동안 샘플에 추가 된 관심의 analytes의 동위 원소 표시 대응 됩니다. 내부 표준 레이블된 들을 거의 동일한 전반적인 물리 화학적 특성으로, 그들은 주어진된 샘플의 매트릭스 효과 대 한 보상.
- 10 mL 쉐이크 플라스 크를 절대 메탄올의 5 mL을 추가 하 여 물에 50% 메탄올 10 mL를 준비 하 고 그것을 채울 최대 10 mL 증류수.
- 물 20 m m 초 산을 포함 하 여 50% 메탄올 10 mL를 준비 합니다. 이렇게 하려면 10 mL 플라스 크에 200 m m 초 산의 1 mL를 추가 하 고 절대 메탄올의 5 mL을 추가 하 고 채워 최대 10 mL 증류수.
- 제조업체에서 제공 하는 튜브에 직접 1000 mg/L와 내부 표준 (IS)의 재고 솔루션을 생성 합니다. Cefepime-13C12D3 황산 증류수, meropenem D6, linezolid D3, 및 50% 메탄올-물 용액에서 piperacillin-D5 를 분해. Ciprofloxacin D8 50% 메탄올-물에 20 mM 아세테이트 및 moxifloxacin 염-13C1D3 20 mM 아세테이트와 증류수에 용 해.
- 오부 집중된 내부 표준 믹스를 1.5 mL 폴 리 프로필 렌 튜브에는 재고 솔루션을 결합 합니다. Cefepime-13C12D3의 meropenem D6, ciprofloxacin D8, moxifloxacin 염-13C1D3의 linezolid 2 µ L의 2 µ L의 1 µ L 10 µ L의 10 µ L을 추가 3, 및 piperacillin-D5 25% 메탄올-물 965 µ L의 10 µ L.
- 내부 표준 재고 솔루션 및 오부 집중된 IS 믹스-80 ° c.에 저장
3. 환자 샘플 저장
주: 혈 청 최대한 빨리 취득 하 고 냉동된 샘플의 콜드 체인 유지 됩니다 확인 하십시오.
- 전체 혈액 혈 청 컬렉션 튜브에 수집 합니다.
- 실 온에서 20-30 분 동안 혈액 응고를 하자.
- 10 분 2000 x g 에서 원심 분리 하 여 혈액에서 혈 청을 분리 합니다.
- 깨끗 한 폴 리 프로필 렌 튜브에는 상쾌한을 전송.
- 혈 청까지 저장할-80 ° C에서 6 개월까지 분석 이다. 또는-20 ° c.에 3 일까지 샘플을 저장하시오
4. 버퍼 크로마토그래피에 대 한 준비
- 준비 물에 1m 암모늄 편대, HPLC 학년 물 100 mL 쉐이크 플라스 크를 사용 하 여 100 mL에 암모늄 편대의 6.306 g을 분해. 4 ° c.에서 1 개월에 솔루션 저장
- 모바일 준비 단계는 [10mm 암모늄 편대 물 개미의 산 (99.9:0.1 v/v)]. HPLC 학년 물 약 500 mL와 함께 1000 mL 부피 플라스 크 프리 필, 포 름 산의 1 mL와 10 mL 1 M 염화 편대 솔루션의 추가 하 고 1000 mL를 HPLC 학년 물에 채워. 깨끗 한 유리병에 모바일 단계 A를 전송 및 HPLC 시스템에 연결. 실 온에서 2 주까지 모바일 단계를 저장 합니다.
- 깨끗 한 유리병에 모바일 단계 B. 전송 HPLC 급 절대 메탄올을 준비 하 고 HPLC 시스템에 연결.
- 바늘으로 사용 절대 메탄올 용 매를 세척 하 고 모바일 단계 B. 포함 된 유리 병에 해당 튜브를 연결
- 물개 및 메탄올-물-개미의 산 (7:92.9:0.1, v/v/v)의 제거 용 매를 생성 합니다. 약 500 mL 증류수와 1000 mL 부피 플라스 크 프리 필 절대 메탄올, 포 름 산의 1 mL의 70 mL을 추가 하 고 1000 mL에 증류수를 추가. 깨끗 한 유리병에 용 매를 전송 및 HPLC 시스템으로 연결.
참고: 다양 한 autosampler 시스템 사용 강한 그리고 약한 바늘 세척 용 매. 이러한 경우, 제조 업체의 권장 사항에 따라 세척 솔루션을 준비 합니다. 예를 들어 메탄올-물-isopropylic 알코올 (70:20:10, v/v/v) 강한 세척 및 물-메탄올 (95:5, v/v)와 약한 세척 할.
5. 악기 조정
참고:이 단계는 특정 질량 분 서 계에 방법의 설정에 대 한 수행 됩니다.
- 깔끔한 1000 mg/L 분석 및 내부 표준 솔루션 1시 10분 또는 검출기 신호 강도 따라 모바일 위상 A와 B (50: 50, v/v)의 혼합물에 1: 100 희석. Autotune 기능을 가진 질량 분석기를 조정 하거나 다음 부모 딸 이온 영상14에 대 한 수동 조정: cefepime (481.0 > 167.0/395.7), cefepime-13C12D3 (485.1 > 167.1 / 400.0) meropenem (384.1 > 114.0/141.0), meropenem D6 (390.1 > 114.0/147.2), ciprofloxacin (332.0 > 231.0/245.0), ciprofloxacin D8 (340.1 > 235.1/249.3), moxifloxacin (402.0 > 261.0/383.9), moxifloxacin-13 C1D3 (406.1 > 265.1/388.0), linezolid (338.0 > 235.0/296.0), linezolid D3 (341.1 > 235.1/297.1), piperacillin (518.0 > 143.0/358.9), piperacillin-D5 (523.1 > 142.8/364.1).
- Autotuning와 악기에 대 한 감지기를 통해 전압 및 MS 입구의 설정을 자동으로 조정 하려면 autotune 기능을 사용 합니다.
- 수동 조정, 악기 설정 및 조정 합니다 (예를 들어, 충돌 전압 충돌 에너지) 최적 (일반적으로 최대)까지 대 한 신호 강도 각 부모와 딸 이온 검출기에서 얻어진 다. 예를 들어 혼합 티를 연결 하 고 0.5 mL/min에서 모바일 위상 A와 B (50: 50, v/v)을 제공 하 고, 지속적으로 0.1 mL/min의 유량과 깔끔한 항생제 또는 내부 표준 달.
6. HPLC-MS/MS 설정
참고: 기능 질량 분 서 계, HPLC 시스템 (를 포함 하 여는 autosampler), 및 해당 소프트웨어의 제조업체에 따라 다릅니다. 질량 분 서 계 매개 변수 및 제조 업체의 권장 사항에 따라 세척 절차를 적응.
- 해당 질량 분석기 매개 변수 저장 'MS 조정 파일 '. 모든 analytes에 대 한 긍정적인 모드 (ESI +)에서 분무 이온화를 사용 합니다. 이온 소스 설정을 사용 하는 악기에 대 한 적응 (예를 들어, 1.5의 모 세관 전압 kV, 소스 온도 120 ° C의, desolvation 온도 400 ° C의, 600 L/h의 desolvation 가스 흐름 율, 0.1 V, RF 렌즈 전압 및 80 ms의 면만 시간).
- 분석 및 내부 표준 조정 매개 변수 (예를 들어, 모 세관 전압, 충돌 에너지)에 지정 된 'MS 파일 '.
- Autosampler 조건에 다음과 같이 설정 된 '입구 파일 ': 샘플 온도 10 ° C ± 5 ° C;의 한도 1 x 제거-세척-지우기와 600 µ L에서 세척 순서 제거할 볼륨 교체.
- 위에서 언급 한에서 '입구 파일 '설정, 흐름 속도 0.4 또는 0.5 mL/min, 4 분, 실행된 시간 345 바, 압력 높은 한도 및 제한 ± 30 ° C에 열 온도 5 ° c. 모바일 단계 A와 B의 용 매 이름을 추가 하 고 각각 7% B/93% a, 그들을 설정 합니다.
- 프로그램에서 크로마 그라디언트는 '입구 파일 ' 다음과 같습니다: 0.00-0.10 7% 모바일 단계 B/93% A, 0.11-0.60와 분 65% 모바일 단계 B/35% A, 0.61-2.10 분 7% 모바일 단계 B/93% A. 95% 모바일 단계 B/5% A, 2.11-4.00 분 분
참고: 추가 열 볼륨, 경 음악 플랫폼 및 USP < 621 > 크로마토그래피 지침16에 설명 된 대로 분석 보존 요인에 대 한 잡고 최대 볼륨을 계산 합니다.
7. 샘플 측정 마스터 파일
: 참고는 '샘플 측정 마스터 파일 ', 환자 샘플 지정, HPLC-MS/MS 분석 시작 되 고 데이터 평가 수행 됩니다. 낮은 및 높은 품질 제어 쌍을 포함 하 여 두 개의 별도 템플릿 파일 생성 됩니다; A와 C, 다른 한 QC 쌍 B와 D. QC 쌍을 포함 하는 하나의 서식 파일
- 만드는 새로운 '샘플 측정 마스터 파일 '. 위에서 언급 한 선택 'MS 조정 파일 ', 'MS 파일 ', '입구 파일' (6 절), 그들에 각 샘플 줄 고 15 µ L로 주입 볼륨을 지정 하 고.
- 오름차순, 교정기 0-7 및 품질 관리 (QC) 페어/C 또는 QC 쌍 동 "샘플 텍스트"를 추가 합니다.
- 샘플 형식을 지정 합니다. 품질 관리 쌍에 대 한 교정기 및 "QC"에 대 한 샘플 유형을 "표준"을 선택 합니다.
- 해당 교정기 및 품질 컨트롤 (스프레드시트, 농도 [µ g/mL] 칼 7-칼 0, QC/C 또는 빌딩 참조)에 대 한 각 항 생 물질의 농도 지정 합니다.
- 프로그램은 '데이터 평가 방법 '. 계측기 (5 절)을 튜닝 하는 동안 최적화 된 전환을 사용 합니다. 해당 동위 원소 분류 표준 (예를 들어, meropenem-meropenem D6) 각 항생제를 일치 합니다.
8. 샘플 정리 및 HPLC-MS/MS 분석
참고: 각 샘플 일괄 처리에 대 한 낮은 항생제 농도와 (QC/C 또는 QC 빌딩) 설정 짝된 품질 관리는 처리 및 분석. 다른 배치 사이 짝된 QC 샘플 대체 시퀀스에서 사용 되는 (하루에 1,예를 들어, 선택은 '샘플 측정 마스터 파일 ' 품질 관리를 포함 한 쌍/C; 2 일에 한 포함 한 QC 쌍 동 선택. 혈 청 샘플의 처리는 그림 1에 나와 있습니다.
- 준비 강수량 에이전트 10% 메 틸-tert-부 틸 에테르 메탄올 (10:90, v/v)에서 (예를 들면, 메 틸-tert의 2.5 mL와 함께 prefill 25 mL 부피 플라스 크-부 틸 에테르 절대 메탄올 25 mL를 채우는).
- C8 역 위상을 열 약 실에 넣으십시오. HPLC와 흐름의 방향에서 질량 분 서 계에 그것을 연결 합니다.
- 샘플 목록을 생성 합니다. 해당 열고 '샘플 측정 마스터 파일 ' 서식 파일 추가 목록에 처리할 의미 환자 샘플. 최대 20 환자 샘플의 그룹을 생성 하 고 해당 하는 품질 관리 쌍으로 그들을 측면.
- 젖은-프라임 HPCL 시스템 사용 하는 '입구 파일 ' 제어 소프트웨어: 단계로 50% 모바일 A/50% B, "젖은 총리" 기능을 설정 하 고 젖은-프라임 1 mL/min의 유량과 2 분.
- 주사기를 새로 고칩니다. 이렇게 하려면 제어 소프트웨어를 사용 하 여 600 µ L의 6 획을 실행 합니다.
- C8 역 위상 열 equilibrate 흐름은 설정 소프트웨어를 사용 하는 '입구 파일 ' 플러시 그것 7% 모바일 확인 0.5 mL/분의 유량을 사용 하 여 5 분의 최소 단계 B/93% A 30 ° c.의 열 온도
- 녹여 환자 샘플, 교정기 0-7의 한 약 수와 품질 관리 쌍 (어느 A / B 또는 C/D).
- 반복적인 피 펫으로 몇 초 동안 내부 표준 혼합의 25 µ L 100 µ L 교정기, QC 샘플, 또는 소용돌이 튜브 1.5 mL 폴 리 프로필 렌 튜브에 환자 혈 청에 추가 합니다.
- 벤치탑 통 (예를 들어, 1200 rpm)에 실 온에서 5 분을 위한 혼합물을 품 어.
- 반복적인 피 펫과 샘플 내부 표준 혼합 강 수 시 약의 150 µ L를 추가 합니다.
- 또, 소용돌이 몇 가지에 대 한 튜브 초 고 벤치탑 통 (예를 들어, 1200 rpm)에 실 온에서 5 분 동안 품 어.
- 4 ° c.에서 10 분 동안 탁상 원심 분리기에 20000 x g 에서 현 탁 액을 원심
- HPLC 학년 물 마이크로 삽입 유리 약 병을 사용 하 여 상쾌한 1: 3을 묽 게 하십시오 그리고 그것으로 가공된 샘플은 autosampler 로드.
- 수동으로 시작 하는 HPLC-MS/MS 분석는 '샘플 측정 제어 파일 '.
참고: 장기간된 저장을 위해 철저 하 게 단계 붕괴를 방지 하기 위해 [예를 들어, 0.5 mL/min 메탄올-물 (50: 50, v/v)] 제조업체의 추천에 따라 분석 열 플러시.

그림 1: 샘플 정리의 도식 대표. 높은 원심력에 단백질 강 수 밀도 펠 릿을 제공 하 고 그 단백질 강 수 완료 했다 명확한 표면에 뜨는, 나타내는. 전체 처리 시간은 샘플 정리, 컬럼에 분리 및 MS/MS 분석을 포함 하 여 약 30 분입니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
9. 품질 평가 및 정량화
- 샘플을 처리 하려면 해당 엽니다 '샘플 측정 제어 파일 ', 교정기, 품질 제어 및 환자 샘플을 선택 하 고 그들을 평가 '항생제 정량화 방법 '.
- 특정 분석에 대 한 봉우리 제대로 통합 여부를 확인 합니다. 각 교정기, QC, 그리고 환자 샘플에 대 한 봉우리를 검사 하 고 수동으로 reintegrate 그들 기준선에 필요한 경우.
- 보정 곡선을 연구 하 고 다음 품질 기준 충족 여부를 확인할: a) 선형성 전체 보정 범위, b)에 보정 계수 r2 > 0.995, c) 각 교정의 ± 15% 표준 편차는 공칭 값, 부 량 (LLOQ), ± 20%가 필요에의 한 제외.
- 위에서 언급 한 조건을 준수 하지 않은 교정 표준 거부 고 다시 회귀 분석을 포함 하 여 교정 곡선을 평가.
- 품질 제어를 공부 하 고는 편차는 공칭 값의 ± 15% 이내 여부 검사.
- 환자 샘플의 농도 높은 교정기의 농도 초과 하는 경우 1:5 (예, 혈 청의 100 µ L 플러스 증류수의 400 µ L) 샘플 정리 하기 전에 증류수와 샘플 최대 희석. 8.8-8.14 그 특정 샘플에 대 한 단계를 reperform 하 고 그것을 다시 처리.
Subscription Required. Please recommend JoVE to your librarian.
Representative Results
설명 된 프로토콜을 사용 하는 전형적인 크로마 그림 2에 묘사 된다. 현재 시스템에서 열 죽은 볼륨 ~0.22 mL와 ~0.08 mL와 함께 추가 열 볼륨 (인젝터, 배관, 및 커넥터 포함) 결정 했다 미국 약전 (USP) 크로마토그래피 지침16, 따라 주는 ~0.30 mL의 잡고 최대 볼륨입니다. 모든 analytes에 대 한 계산 된 보존 요인 했다 2.8 (cefepime)-대 (piperacillin)에 대 한 4.2.
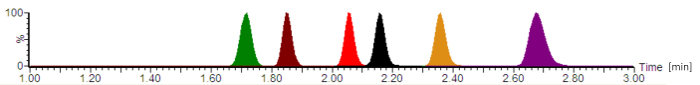
그림 2: 표준화 된 신호 농도와 전형적인 분석 크로마. 항생제는 다음과 같은 순서로 방출: cefepime (녹색), meropenem (갈색), ciprofloxacin (빨간색), moxifloxacin (검정), linezolid (오렌지), 및 piperacillin (자주색). 보존 회는 분에서 주어 집니다 그리고 실정이 피크 대칭성에 따라 모바일 단계, 흐름 율, 크로마토그래피 튜브 및 분석 열 나이의 정확한 구성. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
그림 3A 교정기 0-7을 포함 하 여 가공된 샘플에 대 한 샘플 차트 목록이 포함 되어 있습니다 ("0 Kalibrator"-"7 Kalibrator"), 품질 제어 및 주입 번호로 표시 된 환자 세라 (#); 샘플 식별 텍스트 (예제 텍스트); 측정된 농도 mg/l (하자마자); 샘플 형식으로 빈, 표준, 품질 관리, 또는 환자 샘플 (형식); mg/L (표준 광);에 교정기의 공칭 농도 분석 보존 시간 (RT); 응답을 분석/피크의 피크 면적의 비율입니다 (응답); 공칭 농도 값 ();에서 편차 유리병 위치 (유리병); 그리고 획득 시간 (Acq.Time). 키 매개 변수 사용 하는 정량화에 대 한 응답, 점차적으로 추가 된 동위 원소 라는 내부 표준의 일정 금액 분석 농도 증가 이다.
그림 3B 보정 곡선을 보여 줍니다. 결정 r2 의 계수는 회귀, > 0.995 이어야 한다. 다음과 같은 보정 모델은이 방법에 설명 된 모든 analytes에 대 한 사용: 유형 곡선 선형; = 출처 = 포함; 가중치 = 1 / x; 축 변환 = 없음. 주어진된 예제에서 보정 곡선 및 품질 제어 수행 모든 품질 기준: r2 > 0.995 보정 곡선 및 교정기 (를 포함 하 여는 LLOQ) 및 QC 샘플의 편차에 대 한 공칭 값의 ± 15% 이내입니다.
측정 된 부모 딸 이온 전환 (MRM) 보존 동시에 4 개의 봉우리를 보여주는 그림 3C에서 주어진: 두 위 봉우리 묘사 관심의 분석에 대 한 측정 하는 2 개의 전환, 낮은 두 봉우리는 해당 동위 원소 라는 내부 표준의 전환 품질 평가 대 한 분석 봉우리는 각각 보존 시간 창에서 시각적으로 확인 하 고 수동으로 필요한 경우 기준선에 reintegrated.
최소 억제 농도 (MIC) pharmacokinetic 노출 대상 pharmacokinetic pharmacodynamic (PK/KD) 비율13,17를 달성 하는 데 필요한 정의 항균 TDM의 중심 구성 요소입니다. 따라서, 대상 항생제 TDM 농도 원인 병원 체의 MIC에 관하여 표현 됩니다. 베타-락탐 항생제의 조치는 시간에 따라, 그들의 효 험 마이크 4 x-5를 초과 하는 치료 농도의 달성을 통해 최대화 x (fT > 마이크 x 4-5). 알 수 없는 전염 성 병원 체에 직면, 무료 (단백질 언바운드) piperacillin의 대상 여 물통 농도 범위는, 그러므로, 64 mg/L, 약 90 mg/L 총 piperacillin18에 해당.
첫 번째 환자 (샘플 #11) 수준이 만족 스러운 높은 혈 청 여 물통은 또한 문제 병원 균, 녹 농 균등에 대 한 충분 한 83.4 mg/L piperacillin의. 두 번째 환자 (샘플 #12)는 약 0.2 mg/L, 최저 캘 리브레이 터 (LLOQ) 아래의 농도가 있다. 아마도 환자 회복, 그리고 piperacillin의 중단 했다. 결과 "< 0.5 mg/L"은, 따라서, 병원 정보 시스템에 보고 됩니다. 세 번째 환자 (샘플 #13)만 5.3 mg/L의 분명 대부분의 병원 균에 대 한 충분 하지 않은 낮은 piperacillin 여 물통 농도 있습니다. 효과적인 항균 화학요법에 대 한 복용량은 의사에 의해 증가 되어야 합니다.
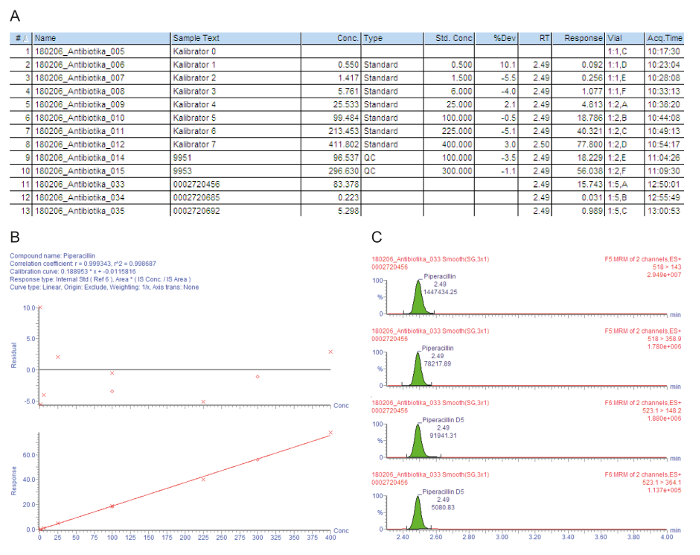
그림 3: 모범 품질 평가 및 분석 piperacillin에 대 한 정량화. 이 패널은 질량 분석 데이터 분석을 나타냅니다. (A)이이 패널 (표준, 샘플 #1-#8) 교정기, 품질 컨트롤 (품질 관리, 샘플 # 9와 #10), 그리고 환자 세라 (샘플 #11-#13)를 포함 하 여 샘플 목록 보여 줍니다. 교정기 0 없이 분석, 하지만 내부는 표준의 추가 함께 빈을 말합니다. 9951이 나타냅니다 QC B 9953 나타냅니다 QC 디 (B)이이 패널 piperacillin에 대 한 교정 곡선을 보여 줍니다. 위쪽 그래프에서 주어진 공칭 교정기 농도에서 백분율 편차 (y-축: 잔여), 낮은 그래프 선형 보정 범위를 보여 줍니다. (C)이이 패널 piperacillin와 해당 내부 표준 piperacillin-D5 환자 혈 청 샘플 # 12에 대 한 모니터링 (MRM) 여러 반응 시간을 표시 합니다. 2 부모 딸 이온 영상 그들의 보존 기간 및 해당 신호 강도 표시 됩니다. 이 그림의 더 큰 버전을 보려면 여기를 클릭 하십시오.
보충 파일. 이 파일을 다운로드 하려면 여기를 클릭 하십시오.
Subscription Required. Please recommend JoVE to your librarian.
Discussion
이 원고에 보고 하는 중 환자 실19, 즉 cefepime, meropenem, ciprofloxacin, moxifloxacin, linezolid, 자주 사용된 항생제의 정량화에 대 한 간단 하 고 강력한 탠덤 질량 분석 기반 방법에 대 한 프로토콜 및 piperacillin14. 스프레드시트 항생제 재고 솔루션, 교정기, 및 품질 컨트롤, 항생제의 순도 및 그들의 counterions의 분자량의 준비에 대 한 원고를 동반 한다. 항생제의 농도 오히려 높은, 그에 주어진 그들의 정량화 분석 관점에서 더 특정 도전 해야 합니다. 따라서, 우리는 확신이 프로토콜은 다양 한 MS 경 음악 플랫폼에 적용 됩니다. 방법 전송, 사용자가 추가 열 량을 계량 하는 격려 된다 및 그들의 컬럼에 시스템의 그라데이션 시작 맞게 막히는 볼륨 따라16시간. 방법 설정 하는 동안 시스템도 이어지기 위해 평가 되어야 한다 하 고 높은 항생제 농도가 높은 교정기 및 환자 샘플 후 빈 샘플을 주입 해야 합니다 필요한 경우. 사용자가 또한 너무 많은 이온 탠덤 질량 분석기를 입력 하는 경우 발생 하는 검출기 채도의 가능성을 고려해 야 합니다. 샘플 정리 / 튠 대상 분석 (예를 들어, 최적의 전압 설정을 다운 그레이드)의 동안 높은 실정이 희석 작은 주입 양으로 관련 검출기 채도 제거할 수 있습니다.
다른 방법에 반대 교정 범위는 피크 농도 (c최대) bolus 행정부와 가져온 감염 병원 체의 MIC에 가까운 농도의 두 부 량을 수 있습니다. 높은 C최대-성인은 FDA 약물 안전 데이터베이스에 다음과 같이 해당 전문 정보 시트에 보고 됩니다 값: cefepime20163.9 mg/L, meropenem21112 mg/L, ciprofloxacin22 4.6 mg/L , moxifloxacin234.1 mg/L, linezolid24, 21.2 mg/L 및 298 mg/L piperacillin25. 항생제 농도 모니터링 환자의 혈액 순환에 관련 된 병원 체의 자화 율에 복용량 조정 있지만 곡선 아래 pharmacokinetic 지역으로 여러 혈액 샘플링을 통해 또한 얻어질 수 있다는 주어진 프로토콜입니다.
많은 항생제 (특히 베타-락탐 meropenem)는 한 번 해산 화학적으로 안정. 이 프로토콜의 가장 중요 한 단계는, 그러므로, 재고 솔루션, 교정기, 및 차가운 조건26,27아래 품질 컨트롤의 준비 합니다. 그 존경에서는, 또한 가능한 한 빨리 환자 샘플을 동결 필수적 이다. 혈 청 스토리지-80 ° C에서26권장 되지만 샘플 보기 수도 있습니다 우리의 안정성 실험 (여 물 수준)에 항생제 농도의 어떤 뜻깊은 감소 없이-20 ° C에서 3 일 저장.
(예를 들어, 캘 리브레이 터 3와) 환자 샘플의 각 HPLC-MS/MS 분석 전에 시스템 적합성 테스트를 수행 하는 것이 좋습니다. 일반적으로, 시스템 적합성 시험 LC-MS/MS 시스템의 반복성을 확인 하 고 있는지 그것은 또한 할 수 분석에 대 한 적절 한 사용 됩니다. 따라서, 예를 들면, 감소 신호 강렬에 의해 발생, 유기 용 매와 청소는 요구 하는 MS 스윕 원추형의 오염. 깨끗 하 게 유지 MS 소스, 크로마토그래피 열, 질량 분석기를 도달 하기 전에 낭비에 모바일 위상의 부분 "분석 무료" 지시 후 divert 밸브를 소개 수 있습니다. 다른 한편으로, 압력의 전반적인 증가 열 시간이 지남에 막힘을 나타낼 수 있습니다. 열을 높이기 위해 장 수 사용 비용 효율적인 precolumn 필터는 추천. 압력 여전히 문제가 계속 되 면 0.4 mL/min의 유량은이 프로토콜에서 크로마 그라데이션으로 사용할 수 있습니다.
이 기술은의 작은 한계는 샘플 정리에 대 한 세 가지 별도 수동 단계 필요, 약 30 분의 총 처리 시간에 따른 강 수 에이전트에 동위 원소 라는 내부 표준 추가 저장할 수 있습니다 일부 처리 시간입니다. 그러나,이 높은 샘플 처리량 속도 이루어져야만 한다 고 강 수와 에이전트 또한 내부 기준으로 (예를 들어,-20 ° C에서), 추위에 저장 되 고 체 외에서 높은 온도에서 저하.
설명된 프로토콜 표준 1.5 mL 폴 리 프로필 렌 튜브에 처리 하는 샘플에 대 한 개발 되었습니다. 더 높은 처리량 속도 항생제 TDM 필요 해야, 절차 진공 매니폴드와 적절 한 원심 분리기 삽입 또는 필터 플레이트를 사용 하 여 멀티 잘 플레이트 형식으로 업그레이드할 수 있습니다.
Subscription Required. Please recommend JoVE to your librarian.
Disclosures
저자는 공개 없다.
Acknowledgments
저자에 대 한 그의 제시 방법 수립 박사 Schütze 감사 하 고 귀중 한 입력에 대 한 박사 Zoller 적절 한 보정 범위에 관한. 저자는 또한 질량 분석 시설 기술 직원을 인정합니다.
Materials
| Name | Company | Catalog Number | Comments |
| cefepime hydrochloride | Sigma-Aldrich | 1097636 | USP Reference Standard |
| meropenem trihydrate | Sigma-Aldrich | Y0001252 | EP Reference Standard |
| ciprofloxacin | Sigma-Aldrich | 17850 | |
| moxifloxacin hydrochloride | Sigma-Aldrich | SML1581 | |
| linezolid | Toronto Research Chemicals | L466500 | |
| piperacillin sodium salt | Sigma-Aldrich | 93129 | |
| cefepime-13C12D3 sulfate | Alsachim | C1297 | Isotope labelled internal standard for cefepime |
| meropenem-D6 | Toronto Research Chemicals | M225617 | Isotope labelled internal standard for meropenem |
| ciprofloxacin-D8 | Toronto Research Chemicals | C482501 | Isotope labelled internal standard for ciprofloxacin |
| moxifloxacin-13C1D3 hydrochloride | Toronto Research Chemicals | M745003 | Isotope labelled internal standard for moxifloxacin |
| linezolid-D3 | Toronto Research Chemicals | L466502 | Isotope labelled internal standard for linezolid |
| piperacillin-D5 | Toronto Research Chemicals | P479952 | Isotope labelled internal standard for piperacillin |
| methanol | JT Baker | 8402 | |
| HPLC grade water | JT Baker | 4218 | |
| formic acid | Biosolve | 6914132 | |
| acetic acid | Biosolve | 1070501 | |
| ammonium formate | Sigma-Aldrich | 70221-25G-F | |
| tert-Butyl methyl ether | Merck | 101845 | |
| Fortis 3 μm C8 100 * 2.1 mm | Fortis | F08-020503 | |
| Ti-PEEK-encased Prifilter (2 μm) | Chromsystems | 15011 | |
| 2795 Alliance HPLC system | Waters | 176000491 | |
| Quattro micro API Tandem Quadrupole System | Waters | 720000338 | |
| QuanLynx 4.1 software | Waters | / | Data evaluation software provided by the mass spectrometer manufacturer |
| Supplemental File | Stock Solutions |
References
- Fleischmann, C., et al. Assessment of Global Incidence and Mortality of Hospital-treated Sepsis. Current Estimates and Limitations. American Journal of Respiratory and Critical Care Medicine. 193 (3), 259-272 (2016).
- Dellinger, R. P., et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012. Intensive Care Medicine. 39 (2), 165-228 (2013).
- Lodise, T. P., Drusano, G. L. Pharmacokinetics and pharmacodynamics: optimal antimicrobial therapy in the intensive care unit. Critical Care Clinics. 27 (1), 1-18 (2011).
- Macedo, R. S., Onita, J. H., Wille, M. P., Furtado, G. H. Pharmacokinetics and pharmacodynamics of antimicrobial drugs in intensive care unit patients. Shock. 39, Suppl 1. 24-28 (2013).
- Petersson, J., Giske, C. G., Eliasson, E. Standard dosing of piperacillin and meropenem fail to achieve adequate plasma concentrations in ICU patients. Acta Anaesthesiologica Scandinavica. 60 (10), 1425-1436 (2016).
- Abdul-Aziz, M. H., Lipman, J., Mouton, J. W., Hope, W. W., Roberts, J. A. Applying pharmacokinetic/pharmacodynamic principles in critically ill patients: optimizing efficacy and reducing resistance development. Seminars in Respiratory and Critical Care Medicine. 36 (1), 136-153 (2015).
- Imani, S., Buscher, H., Marriott, D., Gentili, S., Sandaradura, I. Too much of a good thing: a retrospective study of beta-lactam concentration-toxicity relationships. Journal of Antimicrobial Chemotherapy. 72 (10), 2891-2897 (2017).
- Ventola, C. L. The antibiotic resistance crisis: part 1: causes and threats. Pharmacy & Therapeutics. 40 (4), 277-283 (2015).
- World Health Organization. Global Action Plan on Antimicrobial Resistance. , Available from: http://www.who.int/antimicrobial-resistance/global-action-plan/en (2015).
- Pulcini, C. Antibiotic stewardship: update and perspectives. Clinical Microbiology and Infection. 23 (11), 791-792 (2017).
- Cairns, K. A., et al. The impact of a multidisciplinary antimicrobial stewardship team on the timeliness of antimicrobial therapy in patients with positive blood cultures: a randomized controlled trial. Journal of Antimicrobial Chemotherapy. 71 (11), 3276-3283 (2016).
- Baur, D., et al. Effect of antibiotic stewardship on the incidence of infection and colonisation with antibiotic-resistant bacteria and Clostridium difficile infection: a systematic review and meta-analysis. Lancet Infectious Diseases. 17 (9), 990-1001 (2017).
- Roberts, J. A., Norris, R., Paterson, D. L., Martin, J. H. Therapeutic drug monitoring of antimicrobials. British Journal of Clinical Pharmacology. 73 (1), 27-36 (2012).
- Paal, M., Zoller, M., Schuster, C., Vogeser, M., Schutze, G. Simultaneous quantification of cefepime, meropenem, ciprofloxacin, moxifloxacin, linezolid and piperacillin in human serum using an isotope-dilution HPLC-MS/MS method. Journal of Pharmaceutical and Biomedical Analysis. 152, 102-110 (2018).
- Vogeser, M., Seger, C. Pitfalls associated with the use of liquid chromatography-tandem mass spectrometry in the clinical laboratory. Clinical Chemistry. 56 (8), 1234-1244 (2010).
- United States Pharmacopeia and National Formulary. Chapter <621>. CHROMATOGRAPHY (USP 37-NF 32 S1). , United Book Press, Inc. Baltimore, MD. 6376-6385 (2014).
- Wong, G., Sime, F. B., Lipman, J., Roberts, J. A. How do we use therapeutic drug monitoring to improve outcomes from severe infections in critically ill patients? BMC Infectious Diseases. 14, 288 (2014).
- EUCAST: European Committee on Antimicrobial Susceptibility Testing. Information on clinical breakpoint tables. , Available from: http://www.eucast.org/clinical_breakpoints/ (2017).
- Surveillance der Antibiotika-anwendung und der bakteriellen Resistenzen auf Intensivstationen. SARI information for antibiotic consumption 2016 of all intensive care units participating at SARI. , Available from: http://sari.eu-burden.info/auswertung/down/AD-ZEIT.pdf (2016).
- Cefepime hydrochloride: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2016/050679s040lbl.pdf (2016).
- Meropenem: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2008/050706s022lbl.pdf (2006).
- Ciprofloxacin hydrochloride: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2016/019537s086lbl.pdf (2016).
- Moxifloxacin hydrochloride: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2010/021277s038lbl.pdf (2010).
- Linezolid: Highlights of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2012/021130s028lbl.pdf (2011).
- Piperacillin and Tazobactam: Highlighs of prescribing information. , Available from: https://www.accessdata.fda.gov/drugsatfda_docs/Label/2017/050684s88s89s90_050750s37s38s39lbl.pdf (2017).
- Zander, J., et al. Effects of biobanking conditions on six antibiotic substances in human serum assessed by a novel evaluation protocol. Clinical Chemistry and Laboratory. 54 (2), 265-274 (2016).
- Zander, J., et al. Quantification of piperacillin, tazobactam, cefepime, meropenem, ciprofloxacin and linezolid in serum using an isotope dilution UHPLC-MS/MS method with semi-automated sample preparation. Clinical Chemistry and Laboratory. 53 (5), 781-791 (2015).



