FIM Imaging en FIMtrack: Twee nieuwe instrumenten die High-throughput en Rendabele Locomotion Analyse
Summary
FIM is een nieuwe, voordelige beeldvormingssysteem om kleine bewegende objecten zoals C. bijhouden elegans, planaria of Drosophila larven. De begeleidende FIMTrack programma is ontworpen om snelle en efficiënte data-analyse te leveren. Samen vormen deze tools kunnen high-throughput analyse van gedragskenmerken.
Abstract
De analyse van neuronale netwerk functie vereist een betrouwbare meting van gedragskenmerken. Aangezien het gedrag van vrij bewegende dieren variabele in zekere mate, veel dieren moeten worden geanalyseerd om statistisch significante gegevens te verkrijgen. Dit vereist op zijn beurt een computerondersteund geautomatiseerde kwantificering van de motoriek patronen. Om een hoog contrast van bijna doorschijnend en kleine bewegende objecten te verkrijgen, een nieuwe beeldvormingstechniek op basis van gefrustreerde totale interne reflectie genoemd FIM werd ontwikkeld. In deze opstelling worden de dieren alleen verlicht met infrarood licht op de zeer specifieke positie van het contact met het onderliggende kruipen oppervlak. Deze methode resulteert in een zeer hoog contrast. Vervolgens worden deze contrastrijke beelden verwerkt met behulp van gevestigde contour volgen algoritmen. Op basis hiervan ontwikkelden we de FIMTrack software, waarvan een aantal functies die nodig extract kwantitatief beschrijven een grote verscheidenheid van voortbewegingkenmerken. Tijdens de ontwikkeling van deze software pakket, we onze inspanningen gericht op een open source architectuur waardoor de eenvoudige toevoeging van verdere modules. Het programma werkt platformonafhankelijk en gaat vergezeld van een intuïtieve GUI die de gebruiker door middel van data-analyse. Alle motoriek parameter waarden worden gegeven in de vorm van csv-bestanden waardoor verdere data-analyses. Bovendien a Resultaten Viewer geïntegreerd in de tracking software biedt de mogelijkheid om interactief te beoordelen het uitgangsniveau, zoals nodig kunnen zijn tijdens stimulus integratie. De kracht van FIM en FIMTrack wordt aangetoond door het bestuderen van de beweging van de Drosophila larven.
Introduction
De meeste dieren de mogelijkheid om te bewegen in een zeer geavanceerde gecontroleerde manier. Om de genetische basis onderliggende motoriek controle te ontcijferen is het verplicht om verschillende gedragspatronen kwantitatief te beoordelen. In dit opzicht kan Drosophila dienen als een ideaal model. Tracking van vrij vliegen Drosophila is verleidelijk 1-4 maar kruipen van Drosophila larven gebeurt in twee dimensies bij relatief lage snelheid en kan dus eenvoudig worden gecontroleerd. Camera-gebaseerde opstellingen in combinatie met de juiste belichting worden gebruikt om beelden 5 verwerven. Beide incident of doorgelaten licht wordt gebruikt in gedragsexperimenten 6,7. Echter, als gevolg van de semi-doorschijnend lichaam van de larven en mogelijke licht reflecties van de kruipende oppervlak getrouwe wijze vastleggen van larvale bewegingen kan een uitdaging zijn. Om dergelijke problemen te overwinnen, hebben sommige complexe methoden ontwikkeld. Onlangs werd donker veld verlichting geïntroduceerd op de voorgrond / achtergrond cont verbeterenrast 8. Als alternatief voor cameragebaseerde opname, lens minder optische beeldvorming en-sensorloze on-chip acquisitietechnieken geïntroduceerd 9-11.
Verschillende opsporingsprogramma's zijn onlangs geïntroduceerd, waaronder de handel verkrijgbare software 12 en maatwerkoplossingen. Voorbeelden voor high-throughput opsporingsprogramma's zijn de Multi Worm Tracker (MWT) 13 en Multianimal Gait En Track (Magat) 8. Beide hebben met elkaar gemeen, dat meerdere dieren kunnen worden bijgehouden in een enkele open-veld arena zodat botsende dieren leiden tot meerdere nieuwe dier identiteiten. Om deze beperking te omzeilen, werd een multi-well setup geïntroduceerd scheiden van 12 dieren in de individuele putten 14. Nauwkeurige kwantificering van beweging van afzonderlijke individuen kan worden bereikt door een beweegbare tracking-fase in combinatie met een microscoop 15. Al deze methoden zijn ofwel kosteninefficiënte, onvoldoende reoplossing of te tijdrovend voor high throughput fenotypering.
Om de bovengenoemde beperkingen te overwinnen, ontwikkelden we FIM (FTIR-based Imaging Method) op basis van gefrustreerde totale interne reflectie (FTIR) 16 (Figuur 1). Deze nieuwe imaging benadering biedt een ongekend hoog contrast en maakt zelfs multi-color opname van kruipende dieren 16. Het onderliggende principe van deze handige en effectieve methode is eenvoudig. Een acrylglas plaat wordt overspoeld met licht (bijvoorbeeld 875 nm infrarood). Vanwege de verschillende brekingsindices van acrylglas en lucht, wordt het licht volledig weerspiegeld in het glas / lucht grens. Geen verwarming van het acrylglas wordt opgemerkt 16. Alleen als objecten met een hogere brekingsindex raken de lichte tafel, kan het licht voert deze objecten. Indien de dieren het oppervlak raken, wordt licht gereflecteerd en kan worden opgenomen uit hieronder (figuur 1). Bijgevolg alleen contactgebied van de dieren verschijnt als een lichtpuntje, die een gedetailleerde beeldvorming mogelijk maakt met een totale zwarte achtergrond. Zo FIM-imaging maakt het mogelijk om perfect films voor computer vision algoritmes opnemen. De eenvoudige en robuuste gebruik van FIM brengt nu gedetailleerde hoge doorvoer analyse van complexe dierlijk gedrag in bereik en kan worden gebruikt voor het bestuderen van informatieverwerking: bijvoorbeeld reukzin 8, 16; vision 17 of thermosensation 18.
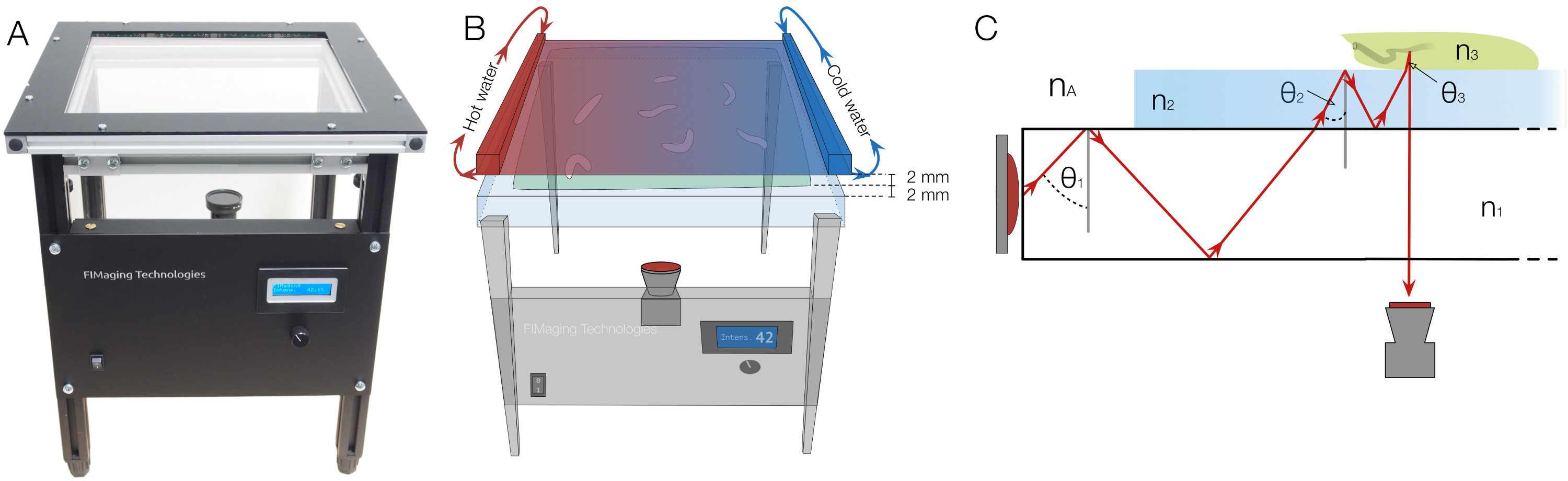
Figuur 1. FIM setup met warmte-stimulus-integratie en de onderliggende fysische principes. (A) De FIM setup. Lichtintensiteit kan op het voorpaneel worden geregeld. (B) Om een warmte stimulans te leveren, een zwart gelakte aluminium plaat, perfusie met warm en koud water aan beide zijden, wordt geplaatst 2 mm boven de agar oppervlak datzelf is 2 mm dik. De gradiënt is gevestigd op het vuur radiator plaat en de agar door de temperatuurverschillen (C) Het natuurkundige principe van gefrustreerde totale interne reflectie. Een acrylglas plaat wordt verlicht door infrarood licht. θ 1, θ 2, en θ 3 geven de lichtreflectie hoeken. n A, n 1, n 2 en n 3 duiden de brekingsindex van lucht, acrylglas, agar en de larve respectievelijk en voldoen aan de ongelijkheid n A <n 1 <n 2 <n 3. Door breking, verandert de reflectiehoek tijdens de overgang. Als de hoek onder de kritische hoek, wordt het licht niet meer terug te vinden, kan door de lagen en kunnen worden vastgelegd van onderen. Klik hier om een grotere versie van deze afbeelding te bekijken.
De spectrum processen die kunnen worden geanalyseerd door FIM breed. Zonder verdere aanpassingen kunnen FIM beeldvorming worden gebruikt om alle larvale stadia van Drosophila (Figuur 5B) monitor of kan worden gebruikt om de voetafdrukken van volwassen Drosophila 19 volgen. Ook de banen van C. elegans of de beweging van planarian platwormen kan eenvoudig worden opgenomen (Figuur 5C). Zelfs de analyse van schimmel Schimmeldraad of wortel haar groei lijkt haalbaar 19. In de huidige FIM opstart, worden 4 x 16 infrarood licht emitterende diodes (IR LEDs) geïntegreerd in een 32 x 32 cm 2 acrylglas plaat, genaamd de tabel volgen (figuur 1). De intensiteit van de IR-LED's wordt aangepast afhankelijk van het gewicht van de voorwerpen op de tracking tafel, die gemakkelijk kunnen worden uitgevoerd door een microcontroller verbonden met het circuit via pulsbreedtemodulatie (PWM). Levert FIM zeer contrastrijke beelden over een breed scala van verlichting intensiteiten. Belangrijker is dat het genteert uitstekende resultaten bij al lage totale infrarood irridation.
Een camera met een infrarood filter onder het volgen tabel, die de integratie van extra stimuli laat in de opstelling geplaatst. Warmte stimuli kan gemakkelijk door een warmte radiator plaat worden toegepast en licht stimuli worden door een LCD-projector toegepast. Ook geurstoffen kunnen in verlopen worden opgenomen door eenvoudige deksels 8. Voor warmte gradiënt experimenten wordt de warmte radiator plaat doorbloed met warm en koud water aan beide zijden respectievelijk geplaatst 2 mm boven de larven (Figuur 1B).
Het produceren van een hoog contrast, hoge kwaliteit films opent de mogelijkheid voor geavanceerde computer gebaseerde beeldanalyse, waardoor implementeerden we de FIMTrack software om een grote reeks van functies uit beelden te extraheren (Figuur 2). Eerste zes primaire functies gedefinieerd van de contour van het dier (Figuur 3A). Deze functies bieden de basislijnvoor verdere berekening zes secundaire functies die de dieren vorm en zijn in bepaalde stimuli op een bepaald tijdstip (Figuur 3B). Momenteel zijn negen tertiaire kenmerken berekend dat integreren temporele aspecten en daarmee karakteriseren de voortbeweging van het dier tezamen met de primaire en secundaire kenmerken (figuur 3C).
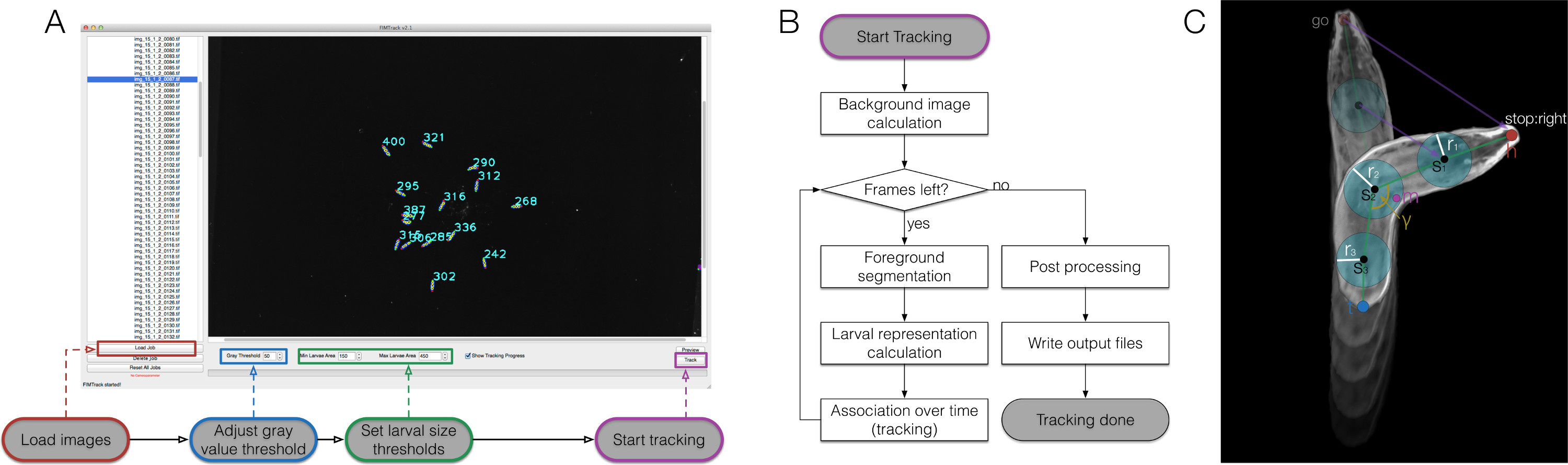
Figuur 2. FIMTrack overzicht, algoritmische workflow en larvale vertegenwoordiging. (A) Hoe FIMTrack gebruiken. De afbeeldingen worden geladen. Grijswaarde drempel en larvale drempels definiëren van enkele larven moeten worden ingesteld. De larvale moet gelegen zijn op [min-size, max-size]. Tracking wordt gestart door de gemarkeerde knop. (B) Tracking workflow. Na de start knop wordt geklikt, de achtergrondafbeelding is calculated (minimale intensiteiten in de tijd). Zolang er frames verlaten, worden de larven gesegmenteerd op basis van de grijsdrempelwaarde en de min- en max-drempelwaarde. Voor alle segmentaties de larvale representaties berekend (te vergelijken (C)). Elk nieuw model is gekoppeld aan een bepaald traject als een geldig nummer beschikbaar is. Als het laatste frame is bereikt, wordt de laatste hand nabewerking gedaan, gevolgd door de output genereren. (C) Larvale vertegenwoordiging. Het dier bestaat uit een kop en een staart punt (h en t). Tussen deze punten een willekeurig oneven aantal wervelkolom punten s kan ik worden ingesteld met een straal r i. Bovendien, het centrum van de massa m en het hoofdlichaam buighoek γ berekend. Verschillende motion gerelateerde parameters worden geschetst door paarse lijnen. Klik hier om een grotere versie van deze afbeelding te bekijken.

Figuur 3. Kenmerken berekend door FIMTrack. (A) Primaire functies op basis van de contour van de dieren. (B) Secundaire functies, op basis van de primaire functies. (C) Tertiaire functies, op basis van de primaire functies in opeenvolgende frames en extra ingangen Klik hier om een grotere versie van deze foto figuur.
Protocol
Representative Results
Discussion
In Behavioral Neuroscience is het verplicht om kwantitatief te ontcijferen complexe gedragskenmerken. Zo moet grote aantallen individuen worden waargenomen bij hoge resolutie en geautomatiseerde procedures nodig voor statistische analyse. Hier wordt FIM beeldvorming beschreven, een nieuw, eenvoudig en robuust imaging opstelling, waarbij de middelen om voortbeweging van een groot aantal dieren daarop bepaalt. De werkzaamheid van de FIM beeldvormende opstelling werd getest met Drosophila larven, planarian platwormen en C. elegans wormen. De FIM technologie intrinsiek hoog contrast zelfs interne structuren van de dieren, zoals de hersenen, de luchtpijp, de darm of de bijmaag detecteren. Belangrijk is dat deze interne structuren robuust geïdentificeerd zodat ze kunnen dienen om de oriëntatie van het dier 19 automatisch te identificeren.
De kwaliteit van de films kunnen worden beïnvloed door overmatige hoeveelheid water op het oppervlak kruipen. Aldus is het essentieel omcontrole van de vochtigheid van de agar. Te oud agar of te veel water aan de oppervlakte kunnen artefacten veroorzaken. Ook ervoor zorgen dat er geen luchtbellen zijn opgenomen in het kruipen oppervlak. In het algemeen een goed voorbereide agaroppervlak laat opnemen van films om 4 uur.
Als gevolg van de onderliggende fysische principes FIM beeldvorming genereert bijna ruisvrij beeldopnamen, wat resulteert in een superieure beeldkwaliteit. Dit op zijn beurt faciliteert daaropvolgende computer gebaseerde beeldanalyse en zorgt voor een hoge doorvoersnelheid. Echter, wordt de methodiek beperkt tot het analyseren van dieren die rechtstreeks contact opnemen met de agar oppervlak. De tracking software wordt uitgedaagd door dieren die een donut vorm. Hoewel een binaire indicator erkent de donut vorm, kan een verkeerde wervelkolom worden berekend.
Door de modulaire opbouw van de tracking tafel dual en triple kleur beeldvorming is in handbereik. Bovendien kunnen extra prikkels (licht, geurstoffen, elektrische of mechanische stimuli) gemakkelijk delivered van boven. Het FIMTrack programma dat is ontworpen om de kracht van FIM beeldvorming overeenkomen kan eenvoudig worden vastgesteld om Drosophila larven, C. volgen elegans of planarians. Zo en vanwege de eenvoudige en goedkope constructie (zie http://FIM.uni-muenster.de), FIM beeldvorming haalbaar is voor een brede waaier van biomedische toepassingen en in het bijzonder maakt dringend high throughput studies nodig.
Disclosures
The authors have nothing to disclose.
Acknowledgements
We zijn dankbaar voor S. Thomas die dit project heeft geïnitieerd, J. Hermann en U. Burgbacher voor hulp bij de bouw van de FIM setup. Dit werk werd gefinancierd door de DFG (SFB 629 B6).
Materials
| Name of the Material/Equipment | Source | Catalog Number | Comments |
| FIM setup | Custom | details for construction or purchase of setups is available upon request | |
| Acrylic glass plate | Custom | Additional for agar pouring | |
| Heat radiator plate | Custom | Aluminum plate (paintet in matt black) perfusable on opposing sites with adjustable mounting | |
| Water calorifier/cooling pumps and hoses | Custom | based on GE healthcare MultiTempIII (No.: 18-1102-78) and Dr Bruno Lange GmBH (Typ: LTG013) | |
| Standard Camera (4 MP) | Basler | acA2040-25gm | Camera defaultly used for the FIM setup |
| Test Camera (1.4 MP) | QImaging | 1394 firewire (01- QIC-F-M-12 MONO) | Camera used for comparison |
| Test Camera (0.8 MP) | Point Grey | Dragonfly 2 (DR2-13S2M/C-CS) | Camera used for comparison |
| Test Camera (0.3 MP) | Sony | PS Eye USB2.0 camera | Camera used for comparison |
| Computer | Custom | equipped with at least i5 Intel processor or better, 16 GB RAM and sufficient HDD storage space [>1TB] | |
| Standard Fly food | Custom | ||
| Standard Fly vials 135 ml | Sarstedt AG&Co, Nümbrecht, Germany | 78,895 | |
| Petri dishes 9cm | Sarstedt AG&Co, Nümbrecht, Germany | 821,473 | |
| Ultrapure deionized water | Merck Millipore, Darmstadt, Germany | Synergy | |
| NaCl | Carl Roth GmbH, Karlsruhe, Germany | 3957.2 | |
| Food grade agar | AppliChem GmbH, Darmstadt, Germany | A0917,5000 | |
| Paintbrush (small and large) | Milan | Aquarell 310 Size 0 and 2 | |
| Pyrometer | Trotec | BP20 |
References
- Maimon, G., Straw, A. D., Dickinson, M. H. A Simple Vision-Based Algorithm for Decision Making in Flying Drosophila. Current Biology. 18 (6), 464-470 (2008).
- Frye, M. A., Dickinson, M. H. Closing the loop between neurobiology and flight behavior in Drosophila. Current opinion in neurobiology. 14 (6), 729-736 (2004).
- Fry, S. N. The Aerodynamics of Free-Flight Maneuvers in Drosophila. Science. 300 (5618), 495-498 (2003).
- Risse, B., Berh, D., Tao, J., Jiang, X., Klette, R., Klämbt, C. Comparison of two 3D tracking paradigms for freely flying insects. EURASIP Journal on Image and Video Processing. 2013 (1), 57 (2013).
- Yilmaz, A., Javed, O., Shah, M. Object tracking: A Survey. ACM Computing Surveys. 38 (4), (2006).
- Pistori, H., et al. Mice and larvae tracking using a particle filter with an auto-adjustable observation model. Pattern Recognition Letters. 31 (4), 337-346 (2010).
- Ramot, D., Johnson, B. E., Berry, T. L., Carnell, L., Goodman, M. B. The Parallel Worm Tracker: a platform for measuring average speed and drug-induced paralysis in nematodes. PloS one. 3 (5), e2208 (2008).
- Gershow, M., et al. Controlling airborne cues to study small animal navigation. Nature Methods. 9 (3), 290-296 (2012).
- Cui, X., et al. Lensless high-resolution on-chip optofluidic microscopes for Caenorhabditis elegans and cell imaging. Proceedings of the National Academy of Sciences of the United States of America. 105 (31), 10670-10675 (2008).
- Heng, X., et al. Optofluidic Microscopy – a Method for Implementing a High Resolution Optical Microscope on a Chip. Lab on a chip. 6 (10), 1274-1276 (2006).
- Liu, P., Martin, R. J., Dong, L. Micro-electro-fluidic grids for nematodes: a lens-less, image-sensor-less approach for on-chip tracking of nematode locomotion. Lab on a chip. 13 (4), 650-661 (2013).
- Spink, A. J., Tegelenbosch, R. A., Buma, M. O., Noldus, L. P. The EthoVision video tracking system–a tool for behavioral phenotyping of transgenic mice. Physiology. 73 (5), 731-744 (2001).
- Swierczek, N. A., Giles, A. C., Rankin, C. H., Kerr, R. A. High-throughput behavioral analysis in C. elegans. Nature methods. 8 (7), 592-598 (2011).
- Yu, C. -. C. J., Raizen, D. M., Fang-Yen, C. Multi-well imaging of development and behavior in Caenorhabditis elegans. Journal of neuroscience methods. 223, 35-39 (2014).
- Wang, S. J., Wang, Z. -. W. Track-A-Worm, An Open-Source System for Quantitative Assessment of C. elegans Locomotory and Bending Behavior. PloS one. 8 (7), e69653 (2013).
- Gomez-Marin, A., Stephens, G. J., Louis, M. Active sampling and decision making in Drosophila chemotaxis. Nature communications. 2, 441 (2011).
- Kane, E. A., et al. Sensorimotor structure of Drosophila larva phototaxis. Proc. Natl. Acad. Sci. U.S.A. 110 (40), E3868-E3877 (2013).
- Luo, L., et al. Navigational decision making in Drosophila thermotaxis. Journal of Neuroscience. 30 (12), 4261-4272 (2010).
- Risse, B., Thomas, S., Otto, N., Löpmeier, T., Valkov, D., Jiang, X., Klämbt, C. FIM, a Novel FTIR-Based Imaging Method for High Throughput Locomotion Analysis. PLoS one. 8 (1), e53963 (2013).
- Risse, B., Otto, N., Jiang, X., Klämbt, C. Quantifying subtle locomotion phenotypes of Drosophila larvae using internal structures based on FIM images. Comput Biol Med. 14, (2014).

