FIM Imaging und FIMtrack: Zwei neuer Instrumente, die Hochdurchsatz und Kosteneffektiv Locomotion Analyse
Summary
FIM ist ein neuartiger, kostengünstiger Imaging-System entwickelt, um kleine, bewegliche Objekte, wie C. verfolgen elegans, Planarien oder Drosophila-Larven. Die begleitende FIMTrack Programm wurde entwickelt, um eine schnelle und effiziente Datenanalyse zu liefern. Zusammen bieten diese Tools ermöglichen Hochdurchsatz-Analyse von Verhaltensmerkmalen.
Abstract
Die Analyse der neuronalen Netzwerkfunktion erfordert eine zuverlässige Messung der Verhaltensmerkmale. Da das Verhalten von frei umherlaufenden Tieren variabel ist, um einem gewissen Grad haben viele Tiere analysiert, um statistisch signifikante Daten zu erhalten. Dies wiederum erfordert eine computergestützte automatische Quantifizierung von Bewegungsmustern. Um Bilder mit hohem Kontrast von fast durchsichtig und kleine bewegte Objekte zu erhalten, wurde ein neuartiges bildgebendes Verfahren auf Basis von frustrierten Totalreflexion genannt FIM entwickelt. In dieser Konfiguration werden die Tiere nur mit Infrarotlicht an der sehr spezifischen Lage der Kontakt mit der darunter kriechen Fläche beleuchtet. Diese Methode führt zu einem sehr kontrastreiche Bilder. Anschließend werden diese Bilder mit hohem Kontrast mit etablierten Konturverfolgungsalgorithmen verarbeitet. Die FIMTrack Software, die eine Anzahl von Merkmalen benötigt extrahieren quantitativ zu beschreiben eine große Vielzahl von Bewegungs dient auf dieser Basis haben wirEigenschaften. Bei der Entwicklung dieser Software-Paket, konzentrieren wir unsere Bemühungen auf einem Open Source-Architektur ermöglicht die einfache Zugabe von weiteren Modulen. Das Programm arbeitet plattformunabhängig und wird durch eine intuitive Benutzeroberfläche, die den Benutzer über die Datenanalyse begleitet. Alle Bewegungsparameterwerte werden in Form von csv-Dateien die eine weitere Datenanalysen gegeben. Darüber hinaus bietet ein Ergebnisviewer in die Tracking-Software integriert die Möglichkeit, interaktiv überprüfen und stellen Sie den Ausgangs, wie man während der Stimulus-Integration erforderlich sein. Die Macht der FIM und FIMTrack wird durch das Studium der Fortbewegung von Drosophila-Larven zeigte.
Introduction
Die meisten Tiere besitzen die Fähigkeit, in einem hochentwickelten und kontrollierte Weise zu bewegen. Um die genetischen Grundlagen zugrunde liegenden Bewegungssteuerung zu entschlüsseln ist es zwingend notwendig die quantitative Erfassung unterschiedlicher Verhaltensmuster. In dieser Hinsicht kann Drosophila als ideales Vorbild dienen. Tracking der frei fliegenden Drosophila tantalizing 1-4 aber kriecht von Drosophila-Larven erfolgt in zwei Dimensionen bei relativ niedriger Geschwindigkeit und kann somit leicht kontrolliert werden. Kamerabasierte Setups in Kombination mit geeigneten Beleuchtung verwendet werden, um Bilder zu 5 zu erwerben. Sowohl Auf- oder Durchlicht wird in Verhaltensexperimenten 6,7 eingesetzt. Allerdings kann aufgrund der semi-transluzente Körper der Larven und mögliche Lichtreflexionen des kriechenden Oberfläche treue Aufzeichnung von Larven Bewegungen schwierig sein. Um diese Probleme zu überwinden, haben einige komplexe Methoden entwickelt worden. Vor kurzem wurde der Dunkelfeldbeleuchtung eingeführt, um die Vorder- / Hintergrund cont verbessernrast 8. Als Alternative zum kamerabasierten Aufzeichnungslinsen weniger optischen Bildgebung und bildsensorlosen chipAkquisitionsTechniken eingeführt worden 9-11.
Mehrere Tracking-Programme haben vor kurzem eingeführt, darunter handelsübliche Software 12 und kundenspezifische Lösungen. Beispiele für die Hochdurchsatz-Tracking-Programme sind die Multi Worm Tracker (MWT) 13 und Multianimal Gang und Track (Magát) 8. Beide haben gemeinsam, dass mehrere Tiere in einem einzigen Freiflächen-Arena verfolgt werden, so dass kollidierende Tieren führen, mehrere neue Tier Identitäten. Um diese Einschränkung zu überwinden, wurde eine Multi-Well-Aufbau eingeführt Trenn 12 Tiere in einzelne Vertiefungen 14. Präzise Quantifizierung der Fortbewegung von einzelnen Personen können durch die Verwendung eines beweglichen Verfolgungsstufe in Kombination mit einem Mikroskop 15 erreicht werden. Jedoch sind alle diese Ansätze entweder Kosten ineffizient, keine ausreichende WiederLösung oder zu zeitaufwendig für die Hochdurchsatz-Phänotypisierung.
Um die oben genannten Beschränkungen zu überwinden, die wir entwickelt haben FIM (FTIR-basierten Imaging-Verfahren), basierend auf frustrierte Totalreflexion (FTIR) 16 (Abbildung 1). Diese neuen bildgebenden Ansatz bietet einen beispiellosen hohen Kontrast und erlaubt sogar Mehrfarbaufzeichnung der kriechenden Tiere 16. Das zugrunde liegende Prinzip dieses handliche und effektive Methode ist einfach. Eine Acrylglasplatte ist lichtdurchflutet (zB 875 nm Infrarot). Wegen der unterschiedlichen Brechungsindices von Acrylglas und Luft, wird das Licht vollständig an der Glas / Luft-Grenze reflektiert wird. Keine Erwärmung der Acrylglas wird bemerkt 16. Nur dann, wenn Objekte mit einem höheren Brechungsindex berühren Sie die lichtdurchfluteten Tabelle können leuchten geben diese Objekte. Wenn die Tiere die Oberfläche berühren, wird das Licht reflektiert und von unten (Figur 1) erfasst werden. Folglich wird nur der KontaktBereich der Tiere erscheint als heller Fleck, der detaillierte Bildgebung mit einer Gesamt schwarzem Hintergrund ermöglicht. So erlaubt FIM-Bildgebung, um perfekte filme für Computer Vision Algorithmen erfassen. Die einfache und robuste Anwendung von FIM bringt nun detaillierte Hochdurchsatzanalyse von komplexen Verhalten der Tiere in Reichweite und kann für das Studium der Informationsverarbeitung eingesetzt werden: zB Geruchssinn 8, 16; Vision 17 oder thermosensation 18.
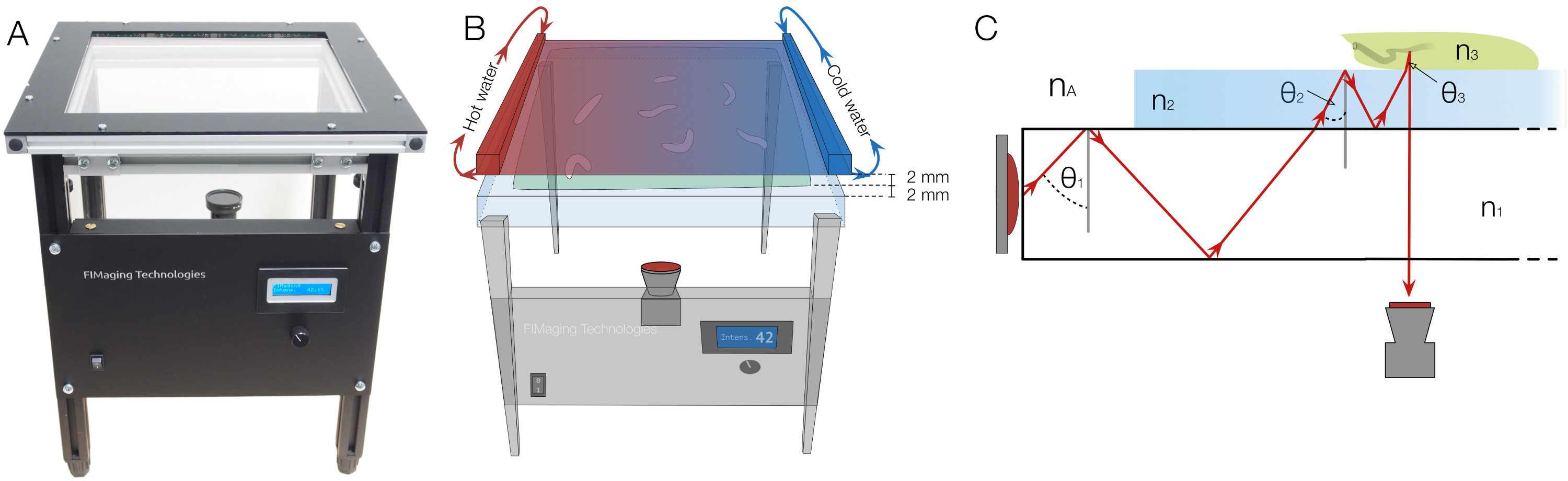
Abbildung 1. FIM-Setup mit Hitzereiz Integration und die zugrunde liegenden physikalischen Prinzipien. (A) Die FIM-Setup. Beleuchtungsstärke können am vorderen Bedienfeld geregelt werden. (B) Um einen Hitzereiz liefern, malte eine schwarze Aluminium-Platte, mit heißem und kaltem Wasser durchströmt auf beiden Seiten wird 2 mm über der Agar-Oberfläche platziert dieselbst ist 2 mm dick. Die Steigung ist auf dem Wärmestrahler Platte und der Agar durch die Temperaturunterschiede festgestellt (C) Das physikalische Prinzip der gestörten Totalreflexion:. Eine Acrylglasplatte wird mit Infrarotlicht beleuchtet. θ 1, θ 2 und θ 3 die Lichtreflexionswinkel. n A, n 1, n 2 und n 3 bezeichnen die Brechungsindizes von Luft, Acrylglas, Agar und Larven jeweils und erfüllen die Ungleichung n A <n 1 <n 2 <n 3. Aufgrund der Brechung ändert beim Übergang der Reflexionswinkel. Wenn der Winkel unterhalb des kritischen Winkels ist, wird das Licht nicht mehr reflektiert, können durch die Schichten hindurchtreten und von unten erfasst werden. Bitte klicken Sie hier, um eine größere Version dieses Bild anzuzeigen.
Die spectrum von Prozessen, die von der FIM analysiert werden können, ist breit. Ohne weitere Einstellungen können FIM Bildgebung verwendet werden, um alle Larvenstadien von Drosophila (5B) zu überwachen oder kann verwendet werden, um die Fußspuren der Erwachsenen folgen Drosophila 19. Ebenso sind die Trajektorien C. elegans oder die Bewegung der Planarie Plattwürmer leicht aufgenommen werden (5C). Auch die Analyse der Pilzhyphen oder Wurzelhaarwachstum möglich erscheint 19. In unserem aktuellen FIM Setup werden 4 x 16 Infrarot-Leuchtdioden (IR-LEDs) in eine 32 x 32 cm 2 Acrylglasplatte integriert, die so genannte Tracking-Tabelle (Abbildung 1). Die Intensität der IR-LEDs wird abhängig von dem Gewicht der Gegenstände auf dem Verfolgungstabelle, die leicht von einem Mikroregler mit der Schaltung über eine Pulsweitenmodulation (PWM) verbunden erfolgen kann eingestellt. FIM ergibt sehr kontrastreiche Bilder über einen weiten Bereich von Beleuchtungsstärken. Wichtiger ist, es genriert hervorragende Ergebnisse bei insgesamt bereits niedrigen Infrarot irridation.
Eine Kamera mit einem Infrarot-Filter ist unterhalb der Verfolgungstabelle, die die Integration von zusätzlichen Impulse in das Setup ermöglicht platziert. Wärmereize kann durch einen Wärmestrahlerplatte aufgebracht werden und Lichtreize werden durch ein LCD-Projektor verwendet. Auch Duftstoffe können in Gradienten mit einfachen Deckeln 8 enthalten sein. Für Wärmegradienten Experimenten wurde die Wärmestrahlerplatte wird mit warmem und kaltem Wasser auf beiden Seiten jeweils perfundiert und platziert 2 mm oberhalb der Larven (1B).
Die Erzeugung von hochauflösenden, qualitativ hochwertige Filme eröffnet die Möglichkeit für anspruchsvolle computergestützte Bildanalyse, damit wir die FIMTrack Software implementiert, um eine große Palette an Funktionen aus Bildern zu extrahieren (Abbildung 2). Ersten sechs Primärmerkmale wurden aus der Kontur des Tieres (3A) definiert ist. Diese Funktionen bieten die Grundliniezur weiteren Berechnung der sechs Sekundärmerkmale, die die Tiere Form und seine Position auf bestimmte Reize zu einem gegebenen Zeitpunkt (Figur 3B), beschreiben. Derzeit sind neun tertiären Merkmale berechnet, die Integration sind zeitliche Aspekte und so prägen die Fortbewegung der Tiere zusammen mit den primären und sekundären Funktionen (3C).
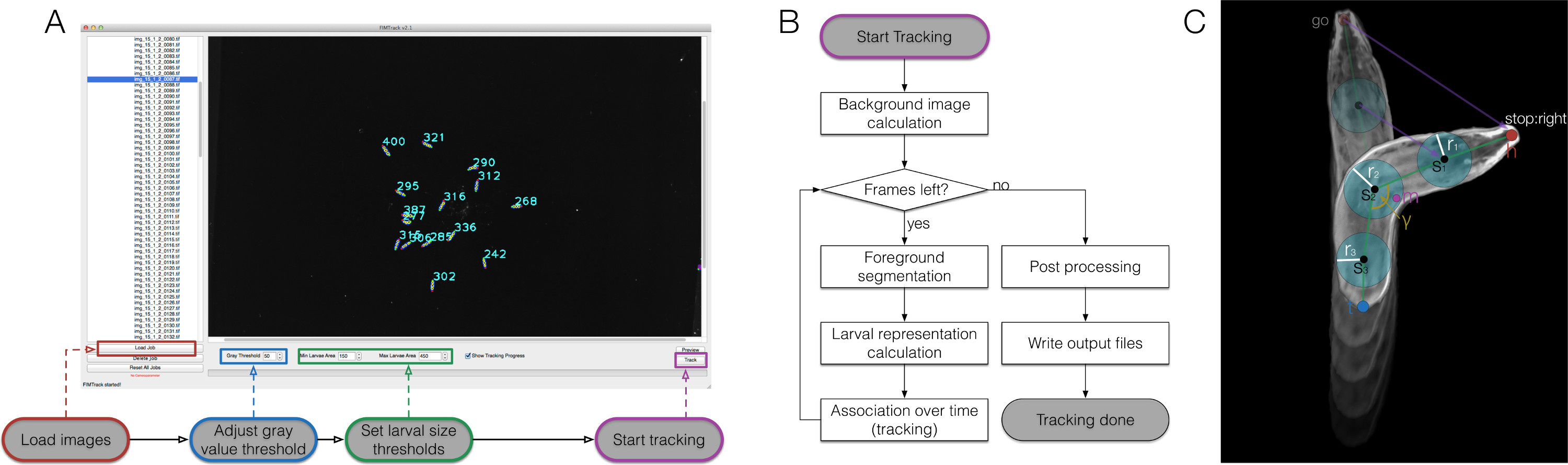
Abbildung 2. FIMTrack Übersicht, algorithmische Workflow und Larven Darstellung. (A) Wie FIMTrack verwenden. Die Bilder werden geladen. Grauwertschwelle und Larvengrößenschwellen zu definieren einzelne Larven müssen eingestellt werden. Die Larvenbereich muss in [min-Größe, max-size] sein. Tracking wird durch die hervorgehobene Schaltfläche (B) Tracking-Workflow gestartet.. Nachdem der Start-Taste angeklickt wird, wird das Hintergrundbild calculated (minimale Intensität über die Zeit). Solange gibt es Rahmen links werden die Larven auf der Grundlage der Grauschwelle und die Min- und Max-Größenschwelle segmentiert. Für alle Segmentierungen die Larvendarstellungen berechnet werden (im Vergleich zu (C)). Jedes neue Modell ist mit einer gegebenen Flugbahn verbunden, wenn eine gültige Strecke verfügbar ist. Wenn das letzte Bild erreicht ist, wird in Kürze Nachbearbeitung fertig durch die Ausgabe Generation gefolgt. (C) Larven Darstellung. Das Tier aus einem Kopf und einem Schwanz Punkt (h und t). Zwischen diesen Punkten eine beliebige ungerade Anzahl an Rückgrat Punkte s kann ich mit einem Radius r i eingestellt werden. Darüber hinaus ist die Mitte der Masse m und der Hauptkörper Biegewinkel γ berechnet. Mehrere Bewegung relevante Parameter sind durch violette Linien skizziert. Bitte klicken Sie hier, um eine größere Version dieses Bild anzuzeigen.

Abbildung 3. Merkmale von FIMTrack berechnet. (A) Die wichtigsten Merkmale auf der Grundlage der Kontur der Tiere. (B) Sekundäre Funktionen, basierend auf dem primären Funktionen. (C) Tertiäre Funktionen, basierend auf dem primären Funktionen in aufeinanderfolgenden Rahmen und zusätzliche Eingänge Bitte klicken Sie hier, um eine größere Version davon zu sehen Figur.
Protocol
Representative Results
Discussion
In Behavioral Neuroscience ist es zwingend erforderlich, um quantitativ zu entziffern komplexe Verhaltensmerkmale. So muss eine große Zahl von Personen mit hoher Auflösung beobachtet und automatisiert werden Verfahren für die statistische Analyse erforderlich. Hier wird FIM Bildgebung beschrieben, eine neuartige, einfache und robuste Bildaufbau, die die Mittel zur Fortbewegung von einer Vielzahl von Tieren Überwachung bietet. Die Wirksamkeit der FIM Imaging-Setup wurde mit Drosophila-Larven, Planarien Plattwürmer und C getestet elegans Würmer. Die FIM-Technologie bietet eigen hohen Kontrast, auch die internen Strukturen der Tiere, wie das Gehirn, Luftröhre, des Darms oder der Drüsen erkennen. Wichtig ist, dass diese inneren Strukturen robust identifiziert, so dass sie dazu dienen können, um die Ausrichtung des Tieres 19 automatisch zu identifizieren.
Die Qualität der Filme können durch zu viel Wasser auf der Oberfläche kriechen beeinflusst werden. So wichtig, ist esKontrolle der Feuchtigkeit des Agar. Zu alt Agar oder zu viel Wasser auf der Oberfläche kann Artefakte verursachen. Ebenso ist sicherzustellen, dass keine Luftblasen in der Krabbeloberfläche enthalten. Im Allgemeinen ist eine gut vorbereitete Agar-Oberfläche ermöglicht die Aufnahme von Filmen 4 Stunden.
Aufgrund der zugrunde liegenden physikalischen Prinzipien FIM-Bildgebung erzeugt nahezu rauschfreie Bildaufnahmen, was eine hervorragende Bildqualität. Dies wiederum erleichtert das nachfolgende computerbasierte Bildanalyse und ermöglicht einen hohen Durchsatz. Jedoch ist die Methode der Analyse Tiere, die direkt an die Agaroberfläche beschränkt. Die Tracking-Software wird von Tieren Bildung einer Ringform in Frage gestellt. Obwohl eine binäre Anzeige erkennt die Donut-Form, kann eine falsche Wirbelsäule berechnet werden.
Durch den modularen Aufbau der Verfolgungstabelle Dual- und Triple-Farbabbildung ist in Reichweite. Darüber hinaus können zusätzliche Reize (Licht, Geruchsstoffe, elektrische oder mechanische Reize) leicht delvon oben ivered. Die FIMTrack Programm entwickelt, um die Macht der FIM Bild passen einfach angenommen, um Drosophila-Larven, C. verfolgen elegans oder Planarien. Daher und aufgrund seiner einfachen und billigen Aufbau (siehe http://FIM.uni-muenster.de), FIM-Bildgebung möglich für eine breite Palette von biomedizinischen Anwendungen und insbesondere ermöglicht dringend benötigten hohen Durchsatzstudien.
Offenlegungen
The authors have nothing to disclose.
Acknowledgements
Wir sind für die Hilfe beim Bau des FIM-Setup dankbar, S. Thomas, die dieses Projekt ins Leben gerufen hat, J. Hermann und U. Burgbacher. Diese Arbeit wurde von der DFG (SFB 629 B6) finanziert.
Materials
| Name of the Material/Equipment | Source | Catalog Number | Comments |
| FIM setup | Custom | details for construction or purchase of setups is available upon request | |
| Acrylic glass plate | Custom | Additional for agar pouring | |
| Heat radiator plate | Custom | Aluminum plate (paintet in matt black) perfusable on opposing sites with adjustable mounting | |
| Water calorifier/cooling pumps and hoses | Custom | based on GE healthcare MultiTempIII (No.: 18-1102-78) and Dr Bruno Lange GmBH (Typ: LTG013) | |
| Standard Camera (4 MP) | Basler | acA2040-25gm | Camera defaultly used for the FIM setup |
| Test Camera (1.4 MP) | QImaging | 1394 firewire (01- QIC-F-M-12 MONO) | Camera used for comparison |
| Test Camera (0.8 MP) | Point Grey | Dragonfly 2 (DR2-13S2M/C-CS) | Camera used for comparison |
| Test Camera (0.3 MP) | Sony | PS Eye USB2.0 camera | Camera used for comparison |
| Computer | Custom | equipped with at least i5 Intel processor or better, 16 GB RAM and sufficient HDD storage space [>1TB] | |
| Standard Fly food | Custom | ||
| Standard Fly vials 135 ml | Sarstedt AG&Co, Nümbrecht, Germany | 78,895 | |
| Petri dishes 9cm | Sarstedt AG&Co, Nümbrecht, Germany | 821,473 | |
| Ultrapure deionized water | Merck Millipore, Darmstadt, Germany | Synergy | |
| NaCl | Carl Roth GmbH, Karlsruhe, Germany | 3957.2 | |
| Food grade agar | AppliChem GmbH, Darmstadt, Germany | A0917,5000 | |
| Paintbrush (small and large) | Milan | Aquarell 310 Size 0 and 2 | |
| Pyrometer | Trotec | BP20 |
Referenzen
- Maimon, G., Straw, A. D., Dickinson, M. H. A Simple Vision-Based Algorithm for Decision Making in Flying Drosophila. Current Biology. 18 (6), 464-470 (2008).
- Frye, M. A., Dickinson, M. H. Closing the loop between neurobiology and flight behavior in Drosophila. Current opinion in neurobiology. 14 (6), 729-736 (2004).
- Fry, S. N. The Aerodynamics of Free-Flight Maneuvers in Drosophila. Science. 300 (5618), 495-498 (2003).
- Risse, B., Berh, D., Tao, J., Jiang, X., Klette, R., Klämbt, C. Comparison of two 3D tracking paradigms for freely flying insects. EURASIP Journal on Image and Video Processing. 2013 (1), 57 (2013).
- Yilmaz, A., Javed, O., Shah, M. Object tracking: A Survey. ACM Computing Surveys. 38 (4), (2006).
- Pistori, H., et al. Mice and larvae tracking using a particle filter with an auto-adjustable observation model. Pattern Recognition Letters. 31 (4), 337-346 (2010).
- Ramot, D., Johnson, B. E., Berry, T. L., Carnell, L., Goodman, M. B. The Parallel Worm Tracker: a platform for measuring average speed and drug-induced paralysis in nematodes. PloS one. 3 (5), e2208 (2008).
- Gershow, M., et al. Controlling airborne cues to study small animal navigation. Nature Methods. 9 (3), 290-296 (2012).
- Cui, X., et al. Lensless high-resolution on-chip optofluidic microscopes for Caenorhabditis elegans and cell imaging. Proceedings of the National Academy of Sciences of the United States of America. 105 (31), 10670-10675 (2008).
- Heng, X., et al. Optofluidic Microscopy – a Method for Implementing a High Resolution Optical Microscope on a Chip. Lab on a chip. 6 (10), 1274-1276 (2006).
- Liu, P., Martin, R. J., Dong, L. Micro-electro-fluidic grids for nematodes: a lens-less, image-sensor-less approach for on-chip tracking of nematode locomotion. Lab on a chip. 13 (4), 650-661 (2013).
- Spink, A. J., Tegelenbosch, R. A., Buma, M. O., Noldus, L. P. The EthoVision video tracking system–a tool for behavioral phenotyping of transgenic mice. Physiology. 73 (5), 731-744 (2001).
- Swierczek, N. A., Giles, A. C., Rankin, C. H., Kerr, R. A. High-throughput behavioral analysis in C. elegans. Nature methods. 8 (7), 592-598 (2011).
- Yu, C. -. C. J., Raizen, D. M., Fang-Yen, C. Multi-well imaging of development and behavior in Caenorhabditis elegans. Journal of neuroscience methods. 223, 35-39 (2014).
- Wang, S. J., Wang, Z. -. W. Track-A-Worm, An Open-Source System for Quantitative Assessment of C. elegans Locomotory and Bending Behavior. PloS one. 8 (7), e69653 (2013).
- Gomez-Marin, A., Stephens, G. J., Louis, M. Active sampling and decision making in Drosophila chemotaxis. Nature communications. 2, 441 (2011).
- Kane, E. A., et al. Sensorimotor structure of Drosophila larva phototaxis. Proc. Natl. Acad. Sci. U.S.A. 110 (40), E3868-E3877 (2013).
- Luo, L., et al. Navigational decision making in Drosophila thermotaxis. Journal of Neuroscience. 30 (12), 4261-4272 (2010).
- Risse, B., Thomas, S., Otto, N., Löpmeier, T., Valkov, D., Jiang, X., Klämbt, C. FIM, a Novel FTIR-Based Imaging Method for High Throughput Locomotion Analysis. PLoS one. 8 (1), e53963 (2013).
- Risse, B., Otto, N., Jiang, X., Klämbt, C. Quantifying subtle locomotion phenotypes of Drosophila larvae using internal structures based on FIM images. Comput Biol Med. 14, (2014).

