FIM Imaging and FIMtrack: Duas novas ferramentas que permitam de alta capacidade e Análise de Custo Efetivo Locomotion
Summary
FIM é um sistema novo, o custo de imagem eficaz projetado para monitorar pequenos objetos em movimento, como C. elegans, planaria ou larvas de Drosophila. O programa acompanha FIMTrack foi projetado para oferecer análise de dados rápida e eficiente. Juntas, essas ferramentas permitem a análise de alto rendimento de traços comportamentais.
Abstract
A análise da função rede neuronal requer uma medição confiável de traços comportamentais. Uma vez que o comportamento dos animais que se deslocam livremente é variável até um certo grau, muitos animais têm de ser analisados, para se obter dados estatisticamente significativos. Este, por sua vez, exige um computador assistida quantificação automática de padrões de locomoção. Para obter imagens de alto contraste de objetos que se movem quase translúcidas e pequenos, foi desenvolvida uma nova técnica de imagem baseada na reflexão interna total frustrada chamado FIM. Nesta configuração, os animais são apenas iluminado com luz infravermelha na posição muito específica de contato com a superfície crawling subjacente. Esta metodologia resulta em imagens de contraste muito alto. Posteriormente, estas imagens de alto contraste são processados usando algoritmos de rastreamento de contorno estabelecidas. Com base nisto, foi desenvolvido o software FIMTrack, que serve para extrair uma série de recursos necessários para descrever, quantitativamente uma grande variedade de locomoçãocaracterísticas. Durante o desenvolvimento deste pacote de software, nós nos concentramos nossos esforços em uma arquitetura de código aberto que permite a fácil adição de novos módulos. O programa funciona independente de plataforma e é acompanhada por uma interface gráfica intuitiva guiando o usuário através de análise de dados. Todos os valores de parâmetros de locomoção são dadas em forma de arquivos CSV que permitam uma maior análise dos dados. Além disso, um visualizador de resultados integrados no software de rastreamento fornece a oportunidade de rever de forma interativa e ajustar a saída, pois pode ser necessária durante a integração de estímulo. O poder de FIM e FIMTrack é demonstrada pelo estudo da locomoção de larvas de Drosophila.
Introduction
A maioria dos animais têm a capacidade de se mover de uma maneira altamente controlada e sofisticado. Para decifrar a base genética subjacente controle de locomoção é obrigatório para avaliar quantitativamente diferentes padrões comportamentais. A este respeito, Drosophila pode servir como um modelo ideal. Rastreamento de voar livremente Drosophila é tentadora 1-4, mas o rastreamento de larvas de Drosophila ocorre em duas dimensões em velocidade relativamente baixa e pode, assim, ser monitorada facilmente. Setups baseado em câmera combinadas com uma iluminação adequada são usados para adquirir imagens 5. Ambos incidente ou luz transmitida é empregado em experimentos comportamentais 6,7. No entanto, devido ao corpo semi-translúcido das larvas e possíveis reflexos de luz do rastejando superfície fiel registro dos movimentos larval pode ser um desafio. Para superar esses problemas, alguns métodos complexos foram criadas. Recentemente, iluminação de campo escuro foi introduzido para aumentar o primeiro plano / fundo contrast 8. Como uma alternativa à gravação à base da câmara, imagiologia óptica da lente e menos de sensor de imagem inferior-on-chip técnicas de aquisição ter sido introduzida 9-11.
Vários programas de monitoramento foram introduzidos recentemente, incluindo o software de 12 e personalizadas soluções disponíveis no mercado. Exemplos de programas de rastreamento de alto rendimento são o Rastreador Worm multi (MWT) 13 e Multianimal marcha e Track (Magat) 8. Ambos têm em comum, que vários animais podem ser rastreados em uma única arena de campo aberto para que os animais que colidem levar a várias novas identidades animais. Para superar essa limitação, uma configuração multi-bem foi introduzido separando 12 animais em poços individuais 14. A quantificação precisa de locomoção dos indivíduos isolados pode ser conseguido usando uma fase móvel de seguimento em combinação com um microscópio 15. No entanto, todas estas abordagens são ineficientes, quer custo, falta de re suficientesolução ou muito demorado em alta fenotipagem rendimento.
Para superar as limitações acima referidas, temos desenvolvido FIM (Método de imagem baseado no FTIR) baseado em reflexão interna total frustrada (FTIR) 16 (Figura 1). Esta nova abordagem de imagem fornece uma alto contraste sem precedentes e até mesmo permite a gravação multi-color de bichos rastejantes, 16. O princípio subjacente a este método prático e eficaz é fácil. Uma placa de vidro acrílico é inundado de luz (por exemplo, 875 nm infravermelho). Devido a diferentes índices de refracção de vidro acrílico e ar, a luz é totalmente reflectida no limite de vidro / ar. Sem aquecimento do vidro acrílico é anotado 16. Só no caso de objetos com maior índice de refração tocar a mesa inundado de luz, pode acender inserir esses objetos. Se os animais toque na superfície, a luz é reflectida e podem ser capturados a partir de baixo (Figura 1). Em consequência, só o contactoárea dos animais aparece como um ponto brilhante, que permite imagens detalhadas com um fundo preto global. Assim, FIM-imaging permite gravar filmes perfeitos para algoritmos de visão computacional. O uso simples e robusto de FIM agora traz análise de alto rendimento detalhada do comportamento animal complexo em alcance e pode ser usado para o estudo do processamento de informação: por exemplo, o olfato 8, 16; visão 17 ou thermosensation 18.
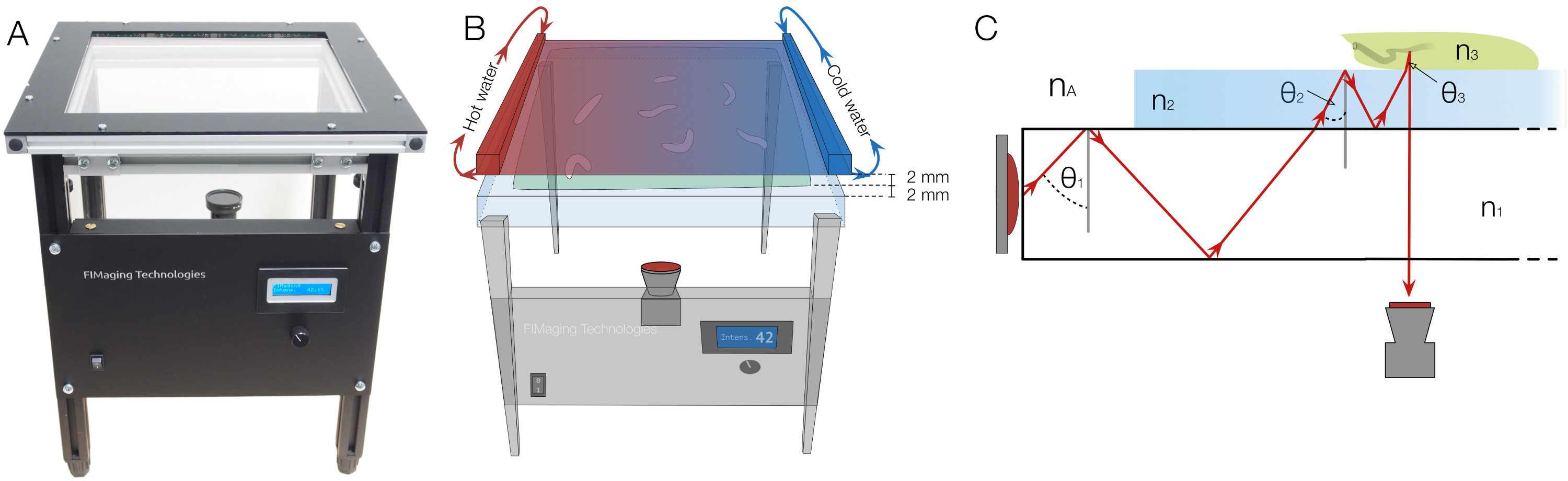
Figura 1. Configuração FIM com a integração de calor de estímulo e os princípios físicos subjacentes. (A) A configuração FIM. Intensidade de iluminação pode ser regulado no painel frontal. (B) para entregar um estímulo térmico, um pintado de preto placa de alumínio, perfundidos com água quente e fria em ambos os lados, é colocado 2 mm acima da superfície do ágar queem si é de 2 mm de espessura. O gradiente é estabelecida na placa radiador de calor e o agar pelas diferenças de temperatura (C) O princípio físico da reflexão interna total frustrada:. Uma placa de vidro acrílico é iluminado por luz infravermelha. θ 1, θ 2 e θ 3 indicam os ângulos de reflexão de luz. n A, n 1, n 2 e n 3 denotar os índices de refracção do ar, vidro acrílico, o agar e a larva respectivamente e cumprir a desigualdade n A <1 n <n2 <n3. Devido à refração, o ângulo de reflexão muda durante a transição. Se o ângulo é inferior ao ângulo crítico, a luz não é mais refletida, pode passar através das camadas e pode ser capturado a partir de baixo. Por favor, clique aqui para ver uma versão maior desta figura.
A spectrum de processos que podem ser analisadas por FIM é ampla. Sem quaisquer outros ajustes, a imagem latente FIM pode ser usado para monitorar todos os estágios larvais de Drosophila (Figura 5B) ou pode ser usado para acompanhar os pés-impressões de adulto Drosophila 19. Da mesma forma, as trajetórias de C. elegans ou o movimento de vermes chatos planarian pode ser facilmente registada (Figura 5C). Mesmo a análise dos fungos hypha ou raiz do cabelo crescimento parece viável 19. Em nossa configuração atual FIM, 4 x 16 diodos emissores de luz infravermelha (IR- LEDs) são integrados em um cm 2 placa de vidro acrílico 32 x 32, chamada de tabela de rastreamento (Figura 1). A intensidade do IR-LED é ajustada em função do peso dos objectos na mesa de acompanhamento, os quais podem ser facilmente realizados por um micro controlador do circuito da via modulação de largura de impulso (PWM). FIM produz imagens muito alto contraste em uma ampla gama de intensidades de iluminação. Importante, generados resultados excelentes a já baixa irridation infravermelho geral.
Uma câmera com um filtro infravermelho é colocado abaixo da tabela de rastreamento, que permite a integração de estímulos adicionais para a instalação. Estímulos de calor pode ser facilmente aplicado por uma chapa de radiador de calor e estímulos luminosos são aplicados por um projector LCD. Também odorants pode estar contido em gradientes por tampas simples 8. Para as experiências de gradiente de calor, a placa do radiador de calor é submetido a perfusão com água quente e fria sobre ambos os lados, respectivamente, e colocado de 2 mm acima do larvas (Figura 1B).
A geração de alto contraste, filmes de alta qualidade abre a possibilidade para sofisticado baseado em computador de análise de imagem, portanto, foi implantado o software FIMTrack para extrair um grande conjunto de recursos a partir de imagens (Figura 2). Primeiros seis características primárias foram definidas a partir do contorno do animal (Figura 3A). Esses recursos fornecem a linha de basepara posterior cálculo de seis características secundárias que descrevem a forma de animais e a sua posição em certos estímulos num dado ponto de tempo (Figura 3B). Atualmente, nove características terciárias são calculados que estão integrando aspectos temporais e, portanto, caracterizar a locomoção do animal, juntamente com as características primárias e secundárias (Figura 3C).
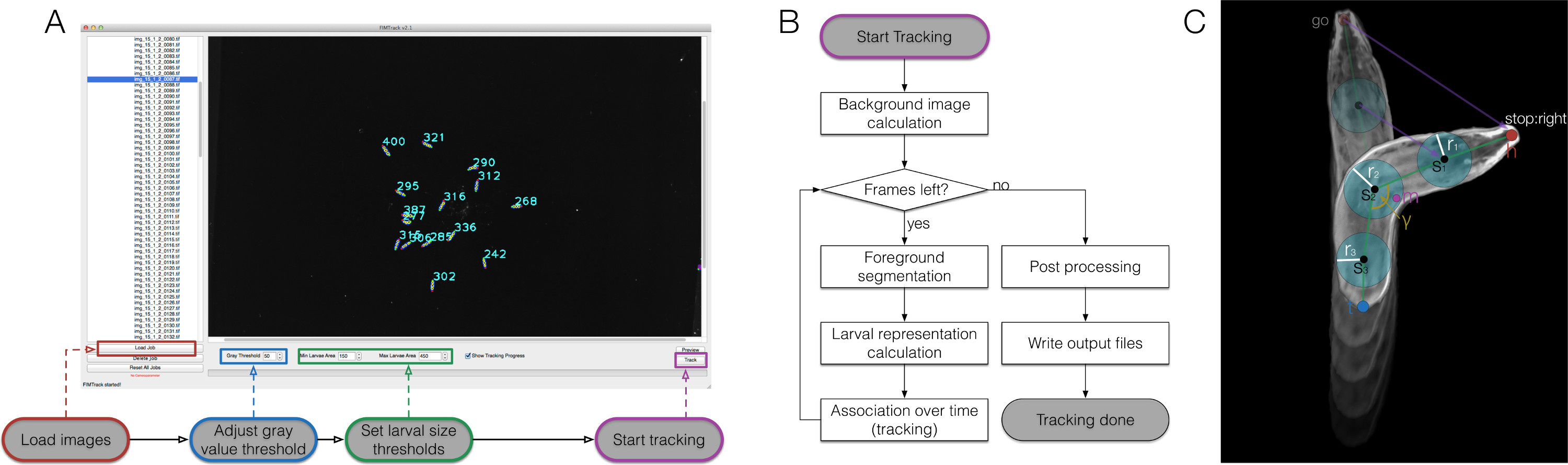
Figura 2. Visão FIMTrack, workflow algorítmica e representação larval. (A) Como usar FIMTrack. As imagens são carregadas. Limiar Gray e limiares de larvas que definem único larvas deve ser definido. A área de larvas devem ser apresentados em [-tamanho min, de tamanho max]. Rastreamento é iniciado pelo botão realçado. Workflow (B) Rastreamento. Após o botão de partida é clicado, a imagem de fundo é calculated (intensidades mínimas ao longo do tempo). Enquanto existem quadros à esquerda, as larvas são segmentados com base no limiar de cinzento e o limite máximo de mineração e de tamanho. Para todas as segmentações as representações de larvas são calculadas (compare a (C)). Cada novo modelo está associado a uma determinada trajectória, se uma faixa válida está disponível. Se o último quadro for atingido, a finalizar o processamento pós é feito seguindo-se a geração de saída. (C) representação larval. O animal é constituído por uma cabeça e uma cauda ponto (h e t). Entre esses pontos um número ímpar arbitrário de pontos da coluna s i pode ser definido com um raio r i. Além disso, o centro de massa m e o corpo principal de flexão γ ângulo são calculados. Vários parâmetros de movimento relacionados são esboçados por linhas roxas. Por favor, clique aqui para ver uma versão maior desta figura.

Figura 3. Características calculados pelo FIMTrack. (A) recursos primários com base no contorno dos animais. (B) Características secundárias, com base em recursos primários. (C) características terciárias, com base em recursos primários em quadros consecutivos e insumos adicionais Por favor, clique aqui para ver uma versão maior desta figura.
Protocol
Representative Results
Discussion
Em neurociência comportamental é obrigatório para decifrar quantitativamente traços comportamentais complexas. Procedimentos Assim, um grande número de indivíduos devem ser observadas em alta resolução e automatizados são necessários para a análise estatística. Aqui, a imagem latente FIM é descrito, um romance, configuração simples e robusta de imagem, que fornece os meios para acompanhar a locomoção de uma grande variedade de animais. A eficácia da estrutura de imagem MIF foi testado utilizando larvas de Drosophila, e vermes chatos planarian C. vermes elegans. A tecnologia FIM fornece intrinsecamente elevado contraste para detectar mesmo as estruturas internas de animais, tais como o cérebro, traqueia, o intestino ou o proventrículos. É importante notar que estas estruturas internas forem rigorosamente identificado de modo que eles podem servir para identificar automaticamente a orientação do animal 19.
A qualidade dos filmes pode ser influenciada por uma quantidade excessiva de água na superfície do rastreamento. Assim, é críticocontrolar a humidade do agar. Água agar ou muito velho demais na superfície pode causar artefatos. Da mesma forma, garantir que não há bolhas de ar estão incluídas na superfície de rastreamento. Em geral, uma superfície de agar bem preparados permite a gravação de filmes durante 4 h.
Devido aos princípios físicos subjacentes imaging FIM gera quase ruído gravações de imagens gratuitos, resultando em uma excelente qualidade de imagem. Este, por sua vez facilita a posterior análise de imagem baseada em computador e permite alto rendimento. No entanto, a metodologia é restrita a analisar animais que contactam directamente a superfície do ágar. O software de rastreamento é desafiado por animais que formam uma forma de donut. Apesar de um indicador binário reconhece a forma de rosca, uma espinha errado pode ser calculado.
Devido à construção modular da tabela de controle dual e triple imagens a cores está ao alcance. Além disso, outros estímulos (luz, Fragrância, estímulos elétricos ou mecânicos), pode facilmente ser delivered a partir de cima. O programa FIMTrack projetado para combinar o poder da imagem FIM podem ser facilmente adotadas para controlar larvas de Drosophila, C. elegans ou planárias. Assim, e devido à sua construção simples e barata (ver http://FIM.uni-muenster.de), imagiologia FIM é viável para uma grande variedade de aplicações biomédicas e, em particular, permite urgentemente necessários estudos de alta produtividade.
Offenlegungen
The authors have nothing to disclose.
Acknowledgements
Somos gratos a S. Tomé, que deu início a este projeto, J. Hermann e U. Burgbacher para ajudar na construção da instalação FIM. Este trabalho foi financiado pelo DFG (SFB 629 B6).
Materials
| Name of the Material/Equipment | Source | Catalog Number | Comments |
| FIM setup | Custom | details for construction or purchase of setups is available upon request | |
| Acrylic glass plate | Custom | Additional for agar pouring | |
| Heat radiator plate | Custom | Aluminum plate (paintet in matt black) perfusable on opposing sites with adjustable mounting | |
| Water calorifier/cooling pumps and hoses | Custom | based on GE healthcare MultiTempIII (No.: 18-1102-78) and Dr Bruno Lange GmBH (Typ: LTG013) | |
| Standard Camera (4 MP) | Basler | acA2040-25gm | Camera defaultly used for the FIM setup |
| Test Camera (1.4 MP) | QImaging | 1394 firewire (01- QIC-F-M-12 MONO) | Camera used for comparison |
| Test Camera (0.8 MP) | Point Grey | Dragonfly 2 (DR2-13S2M/C-CS) | Camera used for comparison |
| Test Camera (0.3 MP) | Sony | PS Eye USB2.0 camera | Camera used for comparison |
| Computer | Custom | equipped with at least i5 Intel processor or better, 16 GB RAM and sufficient HDD storage space [>1TB] | |
| Standard Fly food | Custom | ||
| Standard Fly vials 135 ml | Sarstedt AG&Co, Nümbrecht, Germany | 78,895 | |
| Petri dishes 9cm | Sarstedt AG&Co, Nümbrecht, Germany | 821,473 | |
| Ultrapure deionized water | Merck Millipore, Darmstadt, Germany | Synergy | |
| NaCl | Carl Roth GmbH, Karlsruhe, Germany | 3957.2 | |
| Food grade agar | AppliChem GmbH, Darmstadt, Germany | A0917,5000 | |
| Paintbrush (small and large) | Milan | Aquarell 310 Size 0 and 2 | |
| Pyrometer | Trotec | BP20 |
Referenzen
- Maimon, G., Straw, A. D., Dickinson, M. H. A Simple Vision-Based Algorithm for Decision Making in Flying Drosophila. Current Biology. 18 (6), 464-470 (2008).
- Frye, M. A., Dickinson, M. H. Closing the loop between neurobiology and flight behavior in Drosophila. Current opinion in neurobiology. 14 (6), 729-736 (2004).
- Fry, S. N. The Aerodynamics of Free-Flight Maneuvers in Drosophila. Science. 300 (5618), 495-498 (2003).
- Risse, B., Berh, D., Tao, J., Jiang, X., Klette, R., Klämbt, C. Comparison of two 3D tracking paradigms for freely flying insects. EURASIP Journal on Image and Video Processing. 2013 (1), 57 (2013).
- Yilmaz, A., Javed, O., Shah, M. Object tracking: A Survey. ACM Computing Surveys. 38 (4), (2006).
- Pistori, H., et al. Mice and larvae tracking using a particle filter with an auto-adjustable observation model. Pattern Recognition Letters. 31 (4), 337-346 (2010).
- Ramot, D., Johnson, B. E., Berry, T. L., Carnell, L., Goodman, M. B. The Parallel Worm Tracker: a platform for measuring average speed and drug-induced paralysis in nematodes. PloS one. 3 (5), e2208 (2008).
- Gershow, M., et al. Controlling airborne cues to study small animal navigation. Nature Methods. 9 (3), 290-296 (2012).
- Cui, X., et al. Lensless high-resolution on-chip optofluidic microscopes for Caenorhabditis elegans and cell imaging. Proceedings of the National Academy of Sciences of the United States of America. 105 (31), 10670-10675 (2008).
- Heng, X., et al. Optofluidic Microscopy – a Method for Implementing a High Resolution Optical Microscope on a Chip. Lab on a chip. 6 (10), 1274-1276 (2006).
- Liu, P., Martin, R. J., Dong, L. Micro-electro-fluidic grids for nematodes: a lens-less, image-sensor-less approach for on-chip tracking of nematode locomotion. Lab on a chip. 13 (4), 650-661 (2013).
- Spink, A. J., Tegelenbosch, R. A., Buma, M. O., Noldus, L. P. The EthoVision video tracking system–a tool for behavioral phenotyping of transgenic mice. Physiology. 73 (5), 731-744 (2001).
- Swierczek, N. A., Giles, A. C., Rankin, C. H., Kerr, R. A. High-throughput behavioral analysis in C. elegans. Nature methods. 8 (7), 592-598 (2011).
- Yu, C. -. C. J., Raizen, D. M., Fang-Yen, C. Multi-well imaging of development and behavior in Caenorhabditis elegans. Journal of neuroscience methods. 223, 35-39 (2014).
- Wang, S. J., Wang, Z. -. W. Track-A-Worm, An Open-Source System for Quantitative Assessment of C. elegans Locomotory and Bending Behavior. PloS one. 8 (7), e69653 (2013).
- Gomez-Marin, A., Stephens, G. J., Louis, M. Active sampling and decision making in Drosophila chemotaxis. Nature communications. 2, 441 (2011).
- Kane, E. A., et al. Sensorimotor structure of Drosophila larva phototaxis. Proc. Natl. Acad. Sci. U.S.A. 110 (40), E3868-E3877 (2013).
- Luo, L., et al. Navigational decision making in Drosophila thermotaxis. Journal of Neuroscience. 30 (12), 4261-4272 (2010).
- Risse, B., Thomas, S., Otto, N., Löpmeier, T., Valkov, D., Jiang, X., Klämbt, C. FIM, a Novel FTIR-Based Imaging Method for High Throughput Locomotion Analysis. PLoS one. 8 (1), e53963 (2013).
- Risse, B., Otto, N., Jiang, X., Klämbt, C. Quantifying subtle locomotion phenotypes of Drosophila larvae using internal structures based on FIM images. Comput Biol Med. 14, (2014).

