1.8:
Medição: Unidades Derivadas
1.8:
Medição: Unidades Derivadas
O Sistema Internacional de Unidades ou sistema SI, por acordo internacional, tem unidades de medição fixas para sete propriedades fundamentais: comprimento, massa, tempo, temperatura, corrente elétrica, quantidade de substância, e luminosidade. Estas são chamadas unidades SI base.
As unidades de medição derivadas da combinação matemática de unidades SI base são chamadas unidades derivadas do SI. Por exemplo, a relação entre a unidade SI para a distância (metro; m) e a unidade SI para o tempo (segundo; s) fornece a unidade derivada do SI para a velocidade (metro por segundo; m/s). Outra forma comum de expressar a velocidade de um objecto é usar milhas por hora (milhas/hora). As milhas por hora também são consideradas uma unidade derivada, mesmo que as unidades base não sejam unidades SI. No geral, qualquer unidade derivada é uma combinação de outras unidades.
Unidades Derivadas: Volume e Densidade
Volume é a medição da quantidade de espaço ocupado por um objeto. A unidade de comprimento define a unidade de volume.
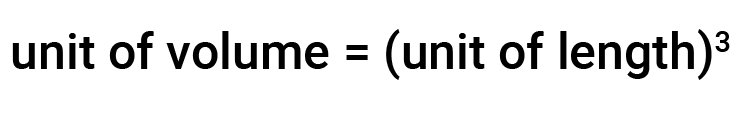
A unidade de volume derivada do SI é um metro cúbico (m3), um cubo com um comprimento entre arestas de exactamente um metro. Para dispensar um metro cúbico de água, poderíamos construir uma caixa cúbica com comprimentos de exatamente um metro entre arestas. Esta caixa teria um metro cúbico de água ou qualquer outra substância.
Outras unidades de volume comuns são o decímetro cúbico (dm3) e o centímetro cúbico (cm3). Um cubo com comprimentos entre arestas de exactamente um decímetro (ou 10 cm) contém um volume de um decímetro cúbico (1 dm3 ou 1000 cm3). Um litro (L) é o nome mais comum para o decímetro cúbico. Um litro é igual a 1000 mililitros e um mililitro é igual a 1 centímetro cúbico.
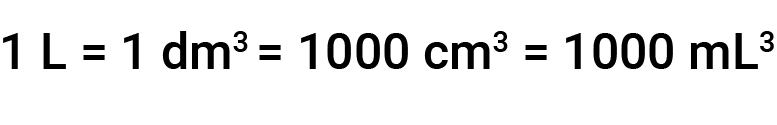
A densidade de uma substância é a razão entre a massa da substância e o seu volume
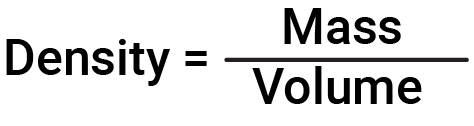
Assim, as unidades de densidade são definidas pelas unidades de massa e comprimento (volume = comprimento3). Como a unidade SI de massa é o quilograma (kg) e de volume é o metro cúbico (m3), a unidade de derivada do SI de densidade é o quilograma por metro cúbico (kg/m3).
Outra unidade comum, gramas por centímetro cúbico (g/cm3), é frequentemente utilizada para as densidades de sólidos e líquidos, e gramas por litro (g/L) para gases.
Propriedades Extensivas e Intensivas da Matéria
Uma unidade de medição expressa a magnitude de uma quantidade física usada para definir uma propriedade física da matéria. As propriedades físicas podem ser extensivas ou intensivas. Se a propriedade depende da quantidade de matéria presente, é uma propriedade extensiva. As propriedades extensivas incluem massa, peso, e volume. Por exemplo, um litro de leite tem uma massa maior do que uma chávena de leite. O valor de uma propriedade extensiva é diretamente proporcional à quantidade de matéria em questão. Pelo contrário, se a propriedade não depender da quantidade de matéria presente, é uma propriedade intensiva. A temperatura é um exemplo de uma propriedade intensiva. Se um litro de leite e uma chávena de leite estiverem a 20 °C, a temperatura permanece a 20 °C quando combinados. Considere outro exemplo para compreender as propriedades distintas mas relacionadas entre o calor e a temperatura. Uma gota de óleo de cozinha quente que espirre para o seu braço provoca um breve desconforto pequeno, enquanto que um pote de óleo quente produz queimaduras graves. Tanto a gota como o pote de óleo estão à mesma temperatura (uma propriedade intensiva), mas o pote de óleo contém muito mais calor (propriedade extensiva).
Este texto é adaptado de Openstax, Chemistry 2e, Section 1.3: Physical and Chemical Properties and Openstax, Chemistry 2e, Section 1.4: Measurements.
