10.1:
过渡金属的性质
10.1:
过渡金属的性质
过渡金属被定义为部分填充 d 轨道的元素。 如图 1 所示,第 3 – 12 组中的 d 块元素是过渡元素。 f 块元素 (也称为内部过渡金属 (镧系元素和锕系元素)) 也符合此标准,因为 d 轨道在 f 轨道之前被部分占用。
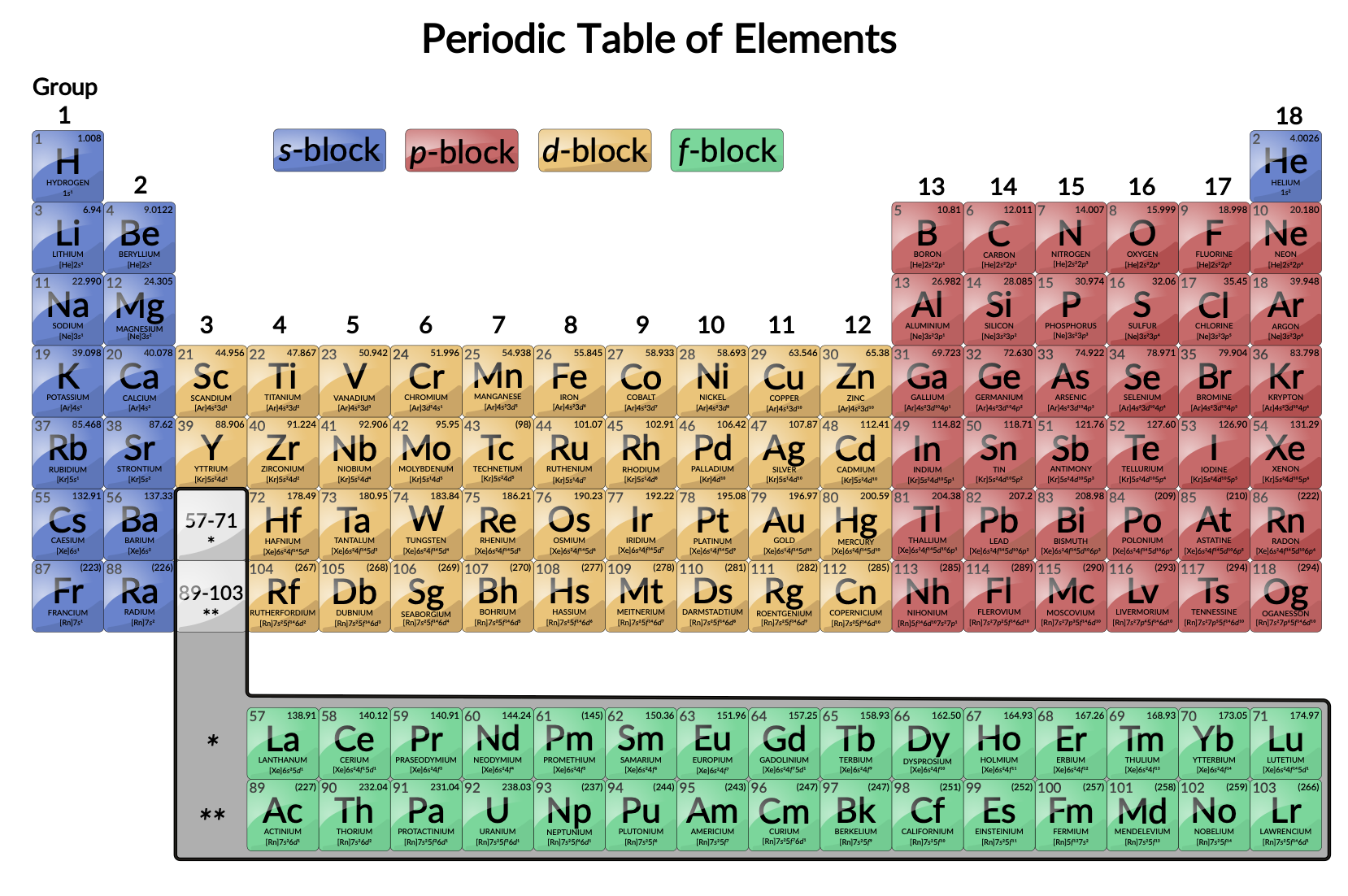
图 1 :元素周期表。 过渡金属位于元素周期表的第 3 – 11 组中。 内部过渡金属位于表格主体下方的两行中。
d 块元素分为第一个过渡序列 (元素 SC 至 Cu) ,第二个过渡序列 (元素 Y 至 Ag) 和第三个过渡序列 (元素 La 和元素 HF 至 Au)。 AC 的锕是第四个转换系列的第一个成员,该系列还包括通过 RG 的射频。
f 块元素是构成镧系元素系列 (或类固醇系列) 的元素 CE 至 LU ,以及构成锕系元素系列 (或类固醇系列) 的元素 Th 至 LR。 由于兰坦的行为与镧系元素元素非常相似,因此被视为镧系元素元素,即使其电子配置使其成为第三个变换序列的第一个成员。 同样,锕的行为意味着它是锕系元素系列的一部分,尽管其电子配置使它成为第四个转换系列的第一个成员。
过渡元素与其他金属有许多性质。 它们几乎都是坚硬的,高熔化的固体,能很好地进行热电操作。 它们容易形成合金并失去电子以形成稳定阳离子。 此外,过渡金属形成了多种稳定的配位化合物,其中中心金属原子或离子充当路易斯酸并接受一对或多对电子。 许多不同的分子和离子都可以将孤对捐赠给金属中心,作为路易斯碱。
过渡元素的性质
过渡金属表现出多种化学行为。 一些过渡金属是强还原剂,而另一些则具有极低的还原活性。 例如,镧系元素均形成稳定的 3+ 水阳离子。 此类氧化物的驱动力类似于碱性地金属 (如 BE 或 mg) ,形成 BE2+ 和 Mg2+。 另一方面,铂金和金等材料的还原潜力要高得多。 它们抗氧化的能力使它们成为制造电路和珠宝的有用材料。
较轻的 d 块元素 (如 CR3+ , Fe3+ 和 CO2+) 的离子形成了在水中稳定的彩色化合物离子。 但是,在这些离子 (Mo3+ , Ru3+ 和 IR2+) 正下方的时段内的离子不稳定,并容易与来自空气的氧气发生反应。 由较重的 d 块元素形成的大多数简单,水稳定的离子是氧离子,如 MoO42− 和 ReO4−。
钌,镉,铑,铱,钯, 铂是铂金金属。 它们很难形成水中稳定的简单阳离子,与第二和第三个过渡系列中的早期元素不同,它们不会形成稳定的氧合离子。
d 块和 f 块元素都与非金属反应以形成二进制化合物;通常需要加热。 这些元素与卤素反应,形成多种卤素,氧化状态范围为 +1 至 +6。 加热时,氧气会与所有过渡元件发生反应,但钯,铂,银和金除外。 这些后金属的氧化物可以使用其他反应物形成,但在加热后会分解。 除铜外, F 块元素,第 3 组元素和第一个过渡系列元素与酸的水溶液反应,形成氢气和相应盐的溶液。
过渡金属可以形成具有广泛氧化状态的化合物。 第一个过渡系列元素的一些观察到的氧化状态显示在表格 1 中。 在第一个过渡系列中从左向右移动,常见氧化状态的数量首先增加到最大值,然后减少到表格的中间。 表格中的值是典型值;还有其他已知值,可以合成新的附加值。 例如, 2014 年,研究人员成功地合成了铱的新氧化状态 (+9)。
| 21 Sc | 22 Ti | 23 V | 24 Cr | 25 Mn | 26 Fe | 27 Co | 28 Ni | 29 Cu | 30 Zn |
| +1 | |||||||||
| +2 | +2 | +2 | +2 | +2 | +2 | +2 | +2 | ||
| +3 | +3 | +3 | +3 | +3 | +3 | +3 | +3 | +3 | |
| +4 | +4 | +4 | +4 | ||||||
| +5 | |||||||||
| +6. | +6. | +6. | |||||||
| +7. |
表格 1. 第一个过渡系列的过渡金属可形成不同氧化状态的化合物。
对于通过锰 (第一个过渡系列的前半部分) 进行的钠元素,最高的氧化状态相当于其价壳的 s 和 d 轨道中所有电子的损耗。 例如,钛 (IV) 离子是在钛原子失去两个 3D 和两个 4S 电子时形成的。 这些最高氧化状态是最稳定的钠,钛和钒形式。 但是,在我们继续执行系列时,无法继续从金属中移除所有价电子。 据了解,铁在 +2 到 +6 之间形成氧化状态,铁 (II) 和铁 (III) 是最常见的。 第一个过渡系列的大多数元素形成的离子电荷为 2+ 或 3+ ,在水中稳定,尽管该系列早期成员的离子可以很容易地被空气氧化。
第二和第三个过渡序列的元素在氧化程度较高的状态下通常比第一个序列的元素更稳定。 一般来说,原子半径会向下增加一组,这会导致第二和第三系列的离子大于第一系列的离子。 从离核更远的轨道中取出电子比取出靠近核的电子更容易。 例如, 6 类成员钼和钨在水溶液中的氧化状态大多限于 +6。 铬是该组中最轻的成员,在水中形成稳定的 CR3+ 离子,在没有空气的情况下, CR2+ 离子的稳定性较差。 铬氧化状态最高的硫化物是 Cr2S3 ,其中含有 CR3+ 离子。 钼和钨形成硫化物,金属在其中氧化状态为 +4 和 +6。
过渡金属展示的性质种类繁多,这是由于它们的价壳体复杂。 与通常观察到一种氧化状态的大多数主要金属不同,过渡金属的价壳层结构意味着它们通常发生在几种不同的稳定氧化状态中。 此外,这些元素中的电子离子对可以与可见电磁频谱中光子的吸收相对应,从而产生彩色化合物。 由于这些行为,过渡金属表现出丰富而迷人的化学特性。
