11.17:
Metalik Katılar
11.17:
Metalik Katılar
Bakır, alüminyum ve demir kristalleri gibi metalik katılar, metal atomlarından oluşur. Metalik kristallerin yapısı genellikle, yerelleştirilmiş elektronların bir “denizi” içinde atom çekirdeğinin tekdüze bir dağılımı olarak tanımlanır. Böyle bir metalik katı içindeki atomlar, birçok kullanışlı ve çeşitli kütle özelliklerine yol açan, metalik bağ olarak bilinen benzersiz bir kuvvet tarafından bir arada tutulur.
Tüm metalik katılar, yüksek termal ve elektriksel iletkenlik, metalik parlaklık ve işlenebilirlik sergiler. Birçoğu çok sert ve oldukça güçlü. Dövülebilirlikleri nedeniyle (basınç veya çekiçleme altında deforme olma yetenekleri) kırılmazlar ve bu nedenle yararlı inşaat malzemeleri yaparlar. Metallerin erime noktaları çok çeşitlidir. Cıva, oda sıcaklığında sıvı haldedir ve alkali metaller 200 °C’nin altında erir. Çeşitli geçiş sonrası metaller de düşük erime noktalarına sahipken, geçiş metalleri 1000 °C’nin üzerindeki sıcaklıklarda erir. Bu farklılıklar, metaller arasındaki metalik bağın güçlerindeki farklılıkları yansıtır.
Metalik Katıların Özellikleri
Kristal yapıları nedeniyle metalik katılar, yapı ile ilişkili birkaç benzersiz özellik sergiler ve aşağıdaki tabloda tablo halinde verilmiştir.
| Katının Tipi | Parçacıkların Tipi | Etkileşimlerin tipi | Özellikler | Örnekler |
| Metalik | Elektropozitif elementlerinatomları | Metalik bağlar | parlak, dövülebilir, sünek, ısı ve elektriği iyi iletir, değişken sertlik ve erime sıcaklığı | Cu, Fe, Ti, Pb, U |
Metalik Katıların Kristal Yapısı: Yakın paketleme
Özdeş atomlardan oluşan katılar iki tür düzenlemeye sahip olabilir: kare veya kapalı paket (Şekil 1). Yakın paketleme atomlar arasındaki toplam çekiciliği maksimize ettiğinden ve toplam moleküller arası enerjiyi en aza indirdiğinden, çoğu metaldeki atomlar bu şekilde paketlenir.

Şekil 1. Kare ve paketli düzenleme.
Basit metalik kristal yapılarda en yakın iki tür paket bulduk: altıgen en yakın istifleme (HCP) ve en yakın kübik istifleme (CCP). Her ikisi de altıgen olarak düzenlenmiş atomların tekrar eden katmanlarından oluşur. Her iki tipte de birinci katman (A) üzerine ikinci bir katman (B) yerleştirilir, böylece ikinci katmandaki her bir atom birinci katmandaki üç atomla temas halinde olur. Üçüncü katman, iki yoldan biriyle konumlandırılır.
HCP’de, üçüncü katmandaki atomlar birinci katmandaki atomların hemen üzerindedir (yani üçüncü katman aynı zamanda bir tip A’dır) ve istifleme, alternatif tip A ve tip B kapalı paketli katmanlardan (yani ABABAB⋯) oluşur ( Şekil 2a).
CCP’de, üçüncü katmandaki atomlar, ilk iki katmandan hiçbirindeki atomların üzerinde değildir (yani, üçüncü katman C tipidir) ve yığın, alternatif tip A, tip B ve tip C kapalı paketli katmanlardan oluşur ( yani, ABCABCABC⋯) (Şekil 2b). Kübik yüz merkezli (FCC) ve CCP düzenlemeleri, hacmin% 74’ünü kaplayan, atomların kompakt bir şekilde paketlendiği aynı yapılardır.
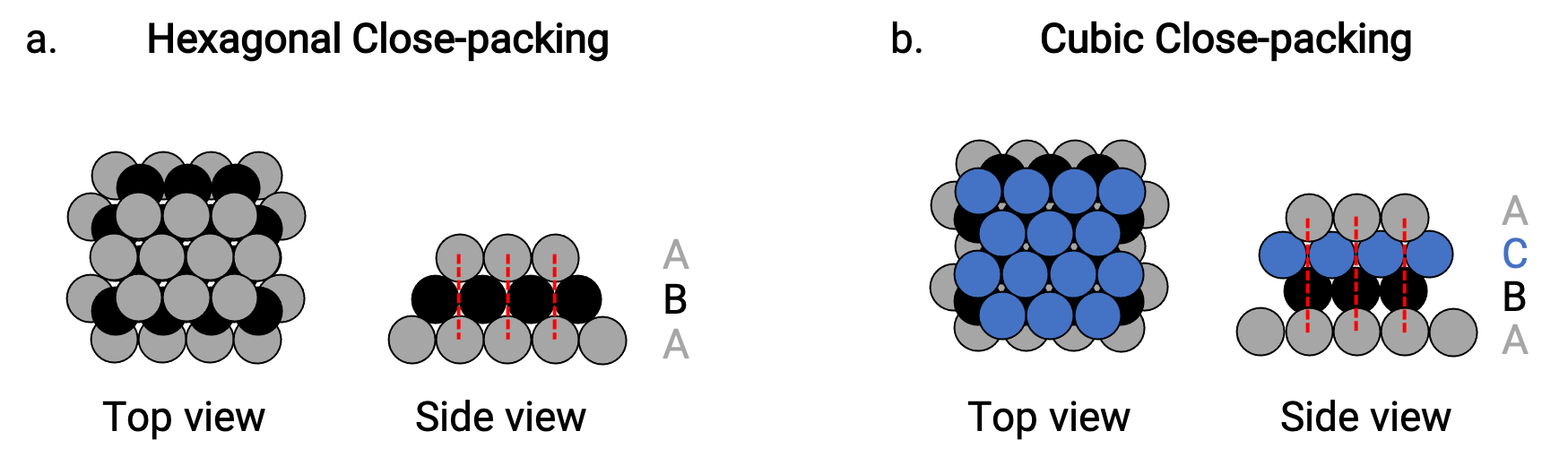
Şekil 2. (a) Altıgen kapalı paketleme, iki alternatif katmandan oluşur (ABABAB…). (b) Kübik yakın paketleme, üç alternatif katmandan oluşur (ABCABCABC…).
Her iki tür paketlemede de, her atom kendi katmanında altı atomla, üstteki katmanda üç ve aşağıdaki katmanda üç atomla temas eder. Böylelikle her atom yakın komşularına 12 dokunur ve bu nedenle koordinasyon numarası 12’dir.
Tüm metallerin yaklaşık üçte ikisi koordinasyon sayıları 12 olan en yakın paketlenmiş dizilerde kristalleşir. Bir HCP yapısında kristalleşen metaller arasında Cd, Co, Li, Mg, Na ve Zn bulunur ve bir CCP yapısında kristalleşen metaller Ag içerir. Al, Ca, Cu, Ni, Pb ve Pt.
Bu metin bu kaynaktan uyarlanmıştırOpenstax, Chemistry 2e, Sections 10.5 The Solid State of Matter, and 10.6 Lattice Structures in Crystalline Solids.
