11.17:
금속성 고체
11.17:
금속성 고체
구리, 알루미늄 및 철의 결정과 같은 금속 고체는 금속 원자에 의해 형성됩니다. 금속 결정의 구조는 종종 탈지역화된 전자의 “바다”내에서 원자 핵의 균일한 분포로 묘사된다. 이러한 금속 고체 내의 원자는 많은 유용하고 다양한 벌크 특성을 야기 금속 결합으로 알려진 독특한 힘에 의해 함께 개최됩니다.
모든 금속 고체는 높은 열 및 전기 전도도, 금속 광택 및 가단성을 나타낸다. 많은 사람들이 매우 어렵고 매우 강하다. 때문에 그들의 가단성 (압력이나 망치로 변형 할 수있는 능력), 그들은 산산조각하지 않고, 따라서, 유용한 건축 자재를합니다. 금속의 융점은 매우 다양합니다. 수은은 실온에서 액체이며, 알칼리 금속은 200 °C 이하로 녹습니다. 여러 전이 후 금속은 또한 낮은 융점을 가지고, 전환 금속은 1000 ° C 이상의 온도에서 용융 하는 반면. 이러한 차이는 금속 간의 금속 결합의 강점의 차이를 반영합니다.
금속 고형물의 특성
결정구조로 인해 금속 고체는 구조와 관련된 고유한 특성을 거의 나타내지 않으며 다음 표에 표로 세타게 되었습니다.
| 솔리드 타입 | 파티클 유형 | 어트랙션유형 | 속성 | 예제 |
| 금속 | 전기 양성 원소의 원자 | 금속 채권 | 광택, 가단성, 연성, 열과 전기를 잘 전도, 가변 경도 및 용융 온도 | Cu, Fe, Ti, Pb, U |
금속 고형물의 크리스탈 구조: 밀착 포장
동일한 원자로 만들어진 고체는 정사각형 또는 밀착 포장된 두 가지 유형의 배열을 가질 수 있습니다(그림 1). 밀착 포장은 원자 사이의 전반적인 매력을 극대화하고 총 분자 간 에너지를 최소화하기 때문에 대부분의 금속의 원자는 이러한 방식으로 포장됩니다.

그림 1. 스퀘어 vs 밀착 배열.
우리는 간단한 금속 결정 구조에서 가장 가까운 포장의 두 가지 유형을 찾을 수 있습니다 : 육각형 가장 가까운 포장 (HCP), 및 입방 가장 가까운 포장 (CCP). 둘 다 육각형 배열 원자의 반복 층으로 구성되어 있습니다. 두 유형 모두에서 두 번째 레이어(B)는 제1 층(A)에 배치되어 두 번째 레이어의 각 원자가 첫 번째 레이어의 세 원자와 접촉하게 됩니다. 세 번째 레이어는 두 가지 방법 중 하나로 배치됩니다.
HCP에서 제3층의 원자는 제1층(즉, 제3층은 A형)에서 원자 바로 위에 있으며, 스태킹은 교대형 A형과 B형 클로즈로 포장된 레이어(즉, ABABAB⋯)(도 2a)로 구성된다.
CCP에서, 제3층의 원자는 처음 두 층 중 하나에서 원자(즉, 제3층은 C형)의 원자 를 초과하지 않으며, 스태킹은 교대형 A, 유형 B 및 C 클로즈라이닝 층(즉, ABCABCABC⋯)으로구성된다. 입방 얼굴 중심(FCC) 및 CCP 배열은 실제로 원자의 컴팩트 한 포장과 동일한 구조입니다, 차지 74% 볼륨.
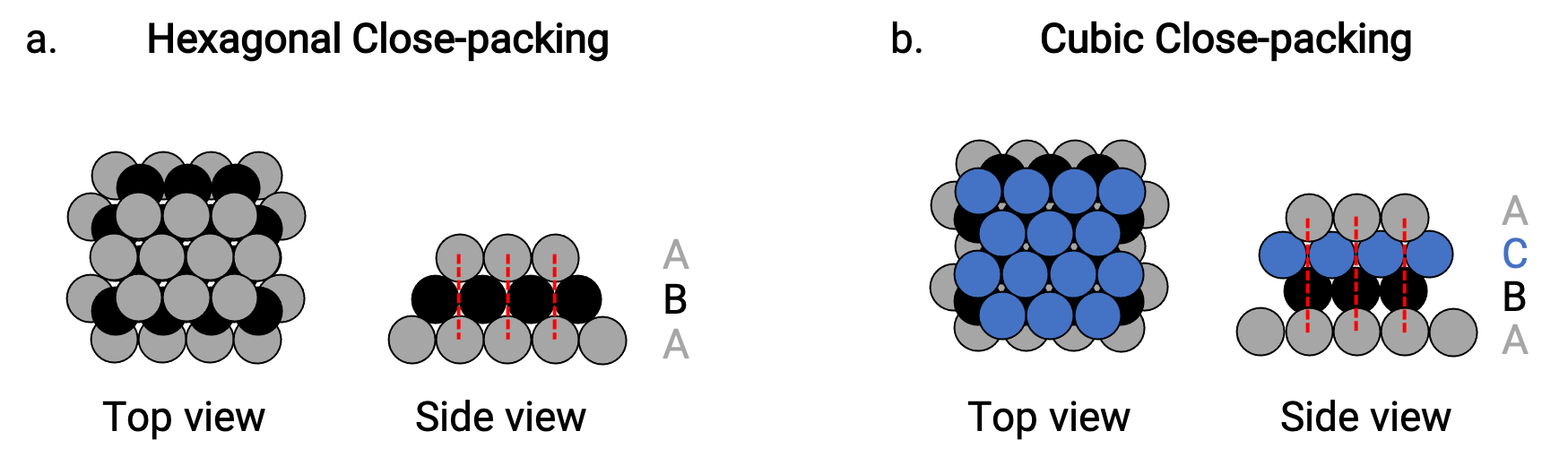
그림 2. (a)육각형 밀착형 밀착식은 두 개의 교대층(ABABAB…)으로 구성된다. (b)입방 클로즈 패킹은 세 개의 교대 층으로 구성됩니다 (ABCABCABC…).
두 유형의 패킹에서 각 원자는 자체 레이어에 6개의 원자, 위의 레이어에 3개, 아래 레이어에 3개의 원자를 접촉합니다. 따라서 각 원자는 이웃 근처의 12에 닿기 때문에 조정 번호가 12입니다.
모든 금속의 약 3분의 2가 12의 조정 번호로 가장 가까운 포장 배열에서 결정화됩니다. HCP 구조에서 결정화되는 금속에는 Cd, Co, Li, Mg, Na 및 Zn 및 CCP 구조에서 결정화되는 금속에는 Ag, Al, Ca, Cu, Ni, Pb 및 Pt가 포함됩니다.
이 텍스트는 Openstax, 화학 2e, 섹션 10.5 물질의 고체 상태,크리스탈 솔리드의 10.6 격자 구조에서 적용되었습니다.
