17.6:
吉布斯自由能
A subscription to JoVE is required to view this content. Sign in or start your free trial.
JoVE Core
Chemistry
Gibbs Free Energy
热力学第二定律指出,对于所有自发 过程,体系的熵-系统熵 与环境熵之 和-都会增加。虽然可以从标准摩尔熵 计算出系统熵,但环境熵却更难 计算或测量。因此,约西亚·威拉德·吉布斯 定义了 一个新热力学函数,它允许自发性仅通过 系统的熵和焓来确定,而不是 通过环境来确定。回想一下,在恒温恒压 条件下,环境的ΔS 等于 系统的负ΔH 除以 温度 T,这一项可以 代入表示第二定律的方程。当两边都乘以负 T 时,方程现在变成负 T 乘以 体系的ΔS 等于系统的ΔH 减去 T 乘以系统的ΔS。方程右侧的热力学 函数-焓和熵-都完全 依赖于系统。因为焓和熵都是状态函数,所以可以将一个新状态函数定义为负 T 乘以 体系的熵。这个新项叫做吉布斯自由能,用字母 G 表示。ΔG 方程引出了一个新 自发反应判据。焓变和 温度的熵变之差必须小于零。ΔG 也称为化学势,因为它类似于系统的 机械势能。就像球总是向下滚动。来降低它的势能一样,化学反应也会 继续进行来降低它的化学势。因此,在恒定温度和压力下,如果系统的自由能减少-即,ΔG 小于零-那么,这个反应会自发进行。相反,如果系统的自由能增加,ΔG 大于零,这个反应 将不会自发进行。如果ΔG 等于零,反应物和生成物 将处于平衡状态。
17.6:
吉布斯自由能
使用热力学第二定律来确定流程是否是自发的一个挑战是,它需要测量系统的熵变化和周围环境的熵变化。 十九世纪末,美国数学家乔西亚 · 威拉德 · 吉布斯推出了一种替代方法,该方法涉及仅以系统性质定义的新型热动力学属性。 这个新的属性被称为吉布斯自由能 (G) (或简称自由能) ,它在系统焓和熵中定义如下:
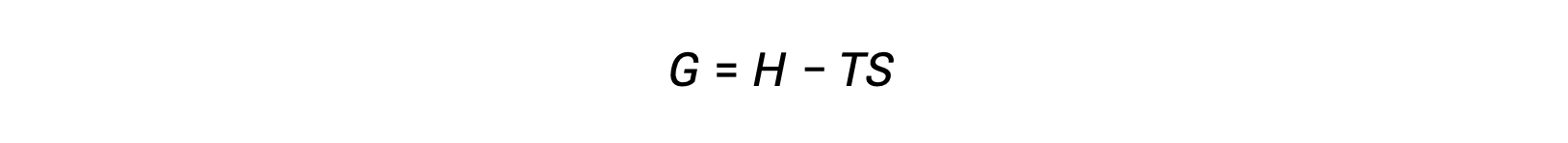
自由能是一种状态函数,在恒定的温度和压力下,自由能变化 (ΔG) 可以表示如下:
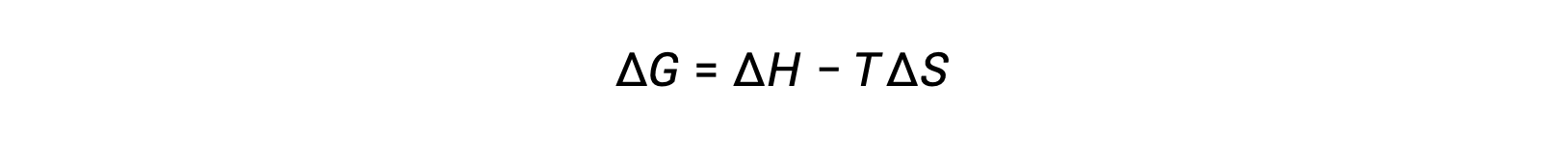
可以通过调用先前派生的第二个定律表达式来理解此系统属性与进程自发性之间的关系:
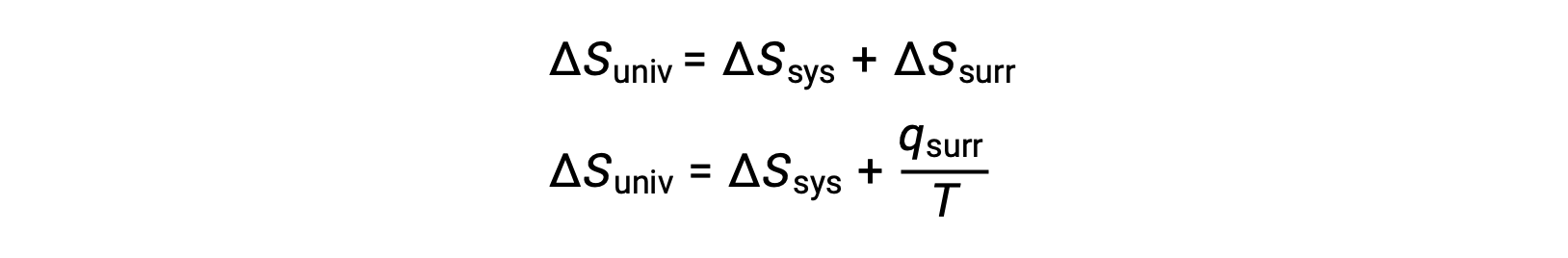
第一个定律要求 qsurr = −Qsys ,在恒压条件下 Qsys = ΔH ,因此该表达式可以改写为:
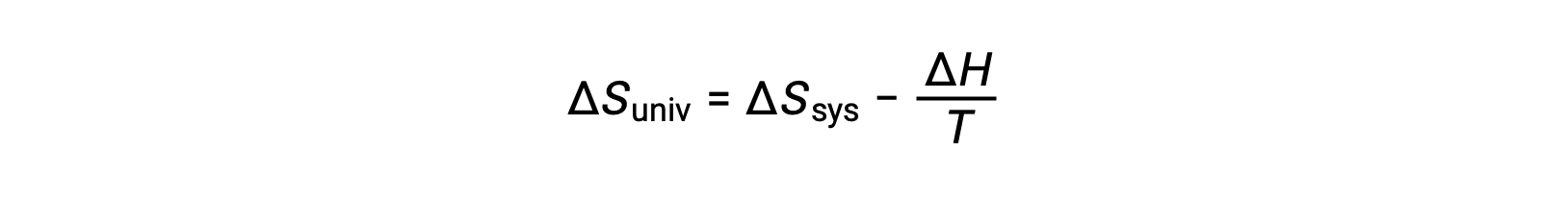
将该方程的两侧乘以 −T 并重新排列将产生以下结果:
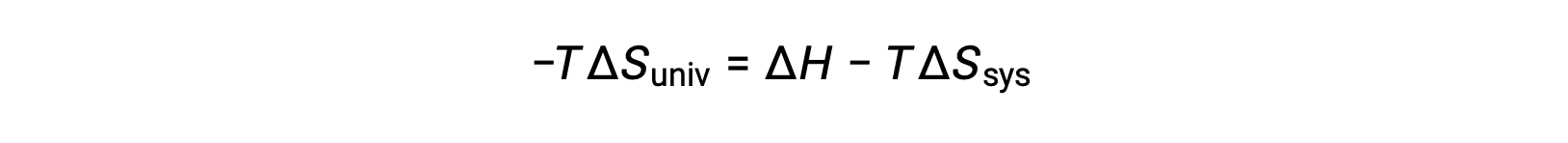
为了简单起见,可以省略下标“ sys ”,表达式将变为
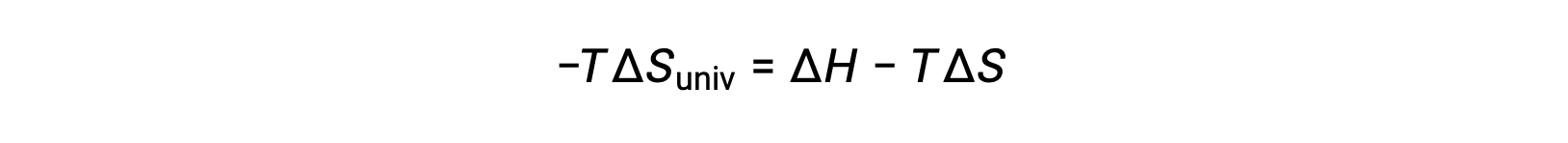
将此方程与上一个用于自由能更改的 进行比较时,将显示以下关系:
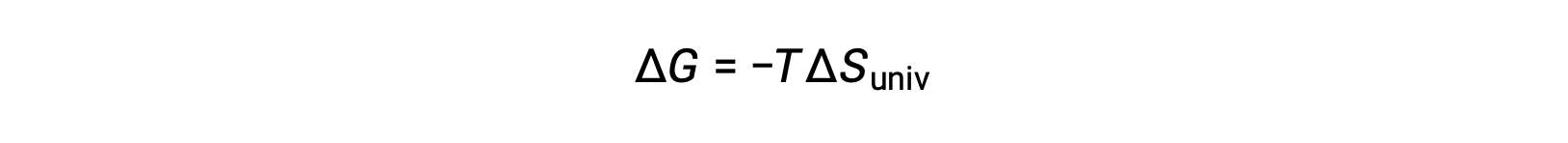
因此,自由能变化是一个可靠的过程自发性指标,因为它与先前确定的自发性指标 ΔSuniv 直接相关。
如果 ΔSuniv > 0 , ΔG < 0 ,则反应是自发的。
如果 ΔSuniv < 0 , ΔG > 0 且反应是非自发性的。
如果 ΔSuniv = 0 , ΔG = 0 且反应处于平衡状态。
本文改编自 Openstax, 化学 2e, 第16.4 章:自由能。
