Controlled Cortical Impact Model for Traumatic Brain Injury
Summary
Traumatic brain injuries (TBIs) remain a serious health problem. Using the controlled cortical impact surgery model, research on the effects of TBI and possible treatment methods may be performed.
Abstract
Every year over a million Americans suffer a traumatic brain injury (TBI). Combined with the incidence of TBIs worldwide, the physical, emotional, social, and economical effects are staggering. Therefore, further research into the effects of TBI and effective treatments is necessary. The controlled cortical impact (CCI) model induces traumatic brain injuries ranging from mild to severe. This method uses a rigid impactor to deliver mechanical energy to an intact dura exposed following a craniectomy. Impact is made under precise parameters at a set velocity to achieve a pre-determined deformation depth. Although other TBI models, such as weight drop and fluid percussion, exist, CCI is more accurate, easier to control, and most importantly, produces traumatic brain injuries similar to those seen in humans. However, no TBI model is currently able to reproduce pathological changes identical to those seen in human patients. The CCI model allows investigation into the short-term and long-term effects of TBI, such as neuronal death, memory deficits, and cerebral edema, as well as potential therapeutic treatments for TBI.
Introduction
Traumatic brain injury (TBI) is defined as an alteration in brain function, or other evidence of brain pathology, caused by an external force1. TBIs remain a serious health problem throughout the world, particularly in the United States. According to the Centers for Disease Control and Prevention, at least 1.7 million TBIs occur annually in the United States resulting in 30.5% of all injury-related deaths. In 2000, the direct medical costs and indirect costs of TBIs totaled an estimated $76.5 billion in the United States alone. Although technological and therapeutic advancements in preceding decades have improved the quality and length of life for those suffering from TBIs, no effective pharmaceutical or preventative treatments currently exist. Due to the complexity and wide-reaching effects of TBIs, including tissue lesions, cell death, and axon degeneration, no two injuries are identical; thus, no current TBI model for animals accurately reproduces all aspects of TBI as seen in humans. However, animal models do provide the ability to produce nearly identical injuries necessary to investigate various effects of TBI with the hope of further understanding the clinical manifestations of TBIs.
The controlled cortical impact (CCI) model uses an impact system to deliver physical impact to the exposed dura of an animal. It induces TBIs ranging from mild to severe similar to those experienced by humans. This injury was first characterized in the ferret2 and was later adapted for use in the rat3,4, mouse5-7, and sheep8. Since the first characterization, the site of injury has been placed both over the midline2,9 and the lateral cortex10. CCI provides an easy and accurate method of investigating the effects and potential treatments for TBIs.
In addition to the CCI model, the fluid percussion and weight drop models are commonly used to produce TBIs. However, these models present limitations, including less control over injury parameters, producing histopathalogical changes not seen in human TBIs, and greater incidence of accidental death in mice3,5,10. The blast wave model is also used to produce TBIs. Although the blast wave model does not reproduce the histopathalogical changes seen following a mechanical impact, this model does accurately produce TBIs experienced particularly by military personnel11. The controlled cortical impact model is easy to control due to the precise control over deformation parameters such as time, velocity, and depth of impact5. Such accuracy makes replicating nearly identical injuries across an entire group of animals more feasible. Most importantly, CCI reproduces TBIs with features seen in human TBIs12. However, there is no single animal model that is entirely successful in reproducing the complete spectrum of pathological changes observed after TBI. Further research is necessary to fully reveal the acute and chronic changes that occur after TBI.
Two types of injuries occur following a TBI: primary and secondary injuries. The primary injury occurs at the moment of impact and is not sensitive to therapeutic treatments; however, the secondary injuries that persist after the initial injury are subject to treatments13. The controlled cortical impact model produces the primary injury, thus allowing researchers to investigate the effects of TBI and potential therapeutic treatments for the potentially long-lasting effects of secondary injuries. Areas of potential research using the CCI model include neuronal death, cerebral edema, neurogenesis, vascular effects, histopathalogical changes, and memory deficits and more3,13-16.
Protocol
Animal Care
Male C57 BL/6 mice were group-housed and kept in a 12/12 hr light/dark cycle with free to access to food and water ad libitum. The animals used in this protocol were 10-12 weeks old. All procedures were performed under protocols approved by Indiana University’s Animal Care and Use Committee.
1. Surgical Preparation
- Anesthetize the mouse using a Ketamine/xylazine mixture (87.7 mg/ml Ketamine and 12.3 mg/ml Xylazine) and administer (1 ml/kg) via IP injection.
- Shave the head of the mouse between the ears.
- Apply a petroleum-based jelly to the eyes of the mouse to prevent drying out during surgery.
- Clean the shaven area with 10% iodine. Then use 70% ethanol to clean off the iodine.
- Fix the mouse head in the stereotactic frame using the ear bars and bite plate. Ensure the brain is stable.
2. Craniectomy
- Make a longitudinal incision in the middle of the head with scissors. Use a hemostat to hold skin off to the left side.
- Use a cotton-tipped applicator to remove the blood and tissue on the bone to expose the skull. Allow exposed skull to dry for 1 min.
- Use forceps to apply pressure and ensure that the skull remains immobile. Identify anatomical landmarks Lambda (caudal aspect) and Bregma (frontal aspect). Draw a circle in the center of Lambda and Bregma with a 4 mm diameter and 0.5 mm away from the midline.
- Use a drill to cut along the marked circle. Gently blow bone dust away. Do not drill completely through the bone to prevent damaging the dura mater.
- Use forceps to remove bone and expose the dura mater.
3. Impaction
The impact system includes a control box to set impact parameters, an actuator to perform the impaction, and a stereotactic frame to secure the actuator and mouse head for impact.
- Pre-set the velocity of the actuator to 3 m/sec before surgery.
- Pre-set different deformation depth to induce different injury severities. Deformation depths of 0.0-0.2 mm, 0.5-1.0 mm, and 1.2-2.0 mm would result in mild, moderate, and severe TBIs, respectively. This protocol explained how to achieve a moderately severe brain injury with a deformation depth of 1 mm by using a velocity of 3 m/sec.
- Attach the actuator to the holder in the stereotactic frame and use the micromanipulators moving it to secure the round, flat tip of the actuator (3 mm diameter) in the center of the open skull area. Then adjust the tip at an angle parallel to the surface of impact site.
- Establish the zero point by moving down the actuator in the extending model until the tip touches the surface of the impact site. Then set the Z channel on the stereotactic control panel to zero.
- Retract the impactor tip while simultaneously moving the actuator down 1 mm.
- Hit the impact button to strike the injury site and achieve a deformation depth of 1 mm.
4. Injury Site Closure
- Use cotton-tipped applicators to remove any blood following impact, but do not touch the injury area.
- Place mouse on a warm pad to maintain body temperature.
- Once bleeding has stopped, suture the wound closed. Put the animal back into the clean cage and allow it to recover from the surgery overnight on the warm pad.
- Administer Buprenorphine 0.05-0.10 mg/kg SQ every 8-12 hr for 2 days after surgery.
Representative Results
The controlled cortical impact model produces TBIs ranging in severity from mild to severe. Post-impact the amount of cranial swelling, bleeding, and cranial distortion at the impact site will reveal the injury severity resulting from the speed and deformation depth parameters. Mild TBIs result in cranial swelling at the impact site and slight bleeding due to the limited dura breach. A moderate TBI exhibits cranial swelling and increased bleeding due to dura breach upon impaction (Figure 1). The difference between a moderate and severe TBI may be difficult to distinguish until visualized on fixed tissues using a microscope (Figure 2); however, a severe TBI may occasionally display amplified distortion and cranial swelling post-impact. The CCI model may be used to determine the effects of multiple aspects of TBIs, including tissue deformation (Figure 2), neuronal death, and histopathalogical changes.

Figure 1. Controlled cortical impact model for moderate traumatic brain injury. The procedure for controlled cortical impact is illustrated in this figure. A) The mouse head was stably fixed on the stereotactic frame with ear bar and mouth bits. B) The left skull was exposed and 4 mm circle was drawn in the center of bregma and lambda. C) The bone was removed by the drilling to generate a window for impact. D) The actuator was attached on the stereotactic frame and the zero point on Z-axis was set up. E) The brain tissue was distorted and caused bleeding with impact. F) The bleeding stopped several minutes after impact and the blood was removed by cotton applicator. Click here to view larger image.
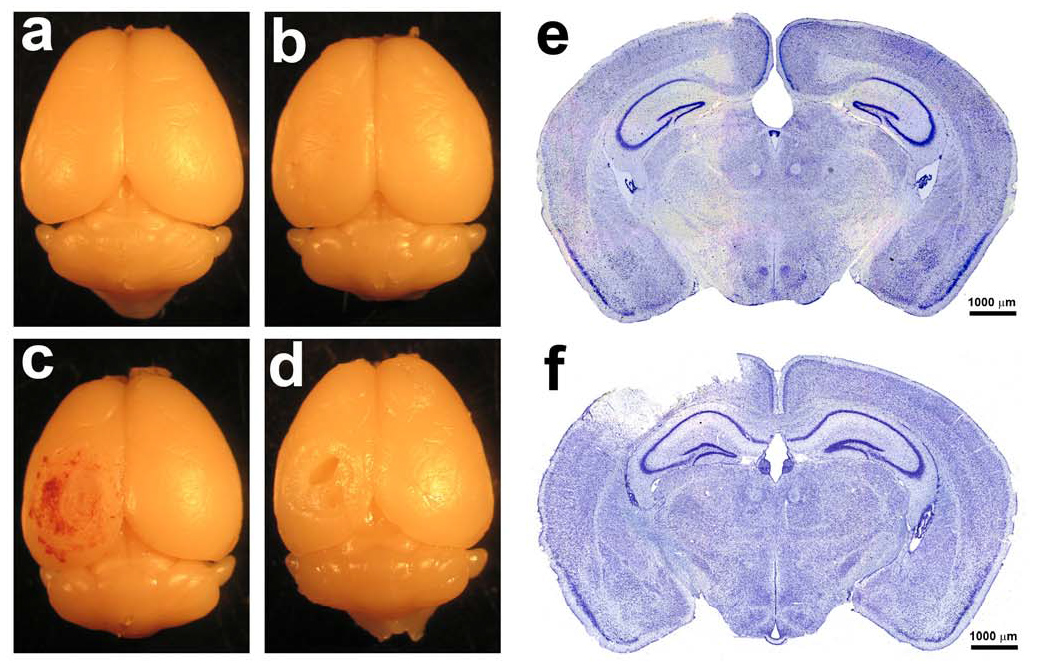
Figure 2. Histology for Moderate Traumatic Brain Injuries. A) A naïve 10-12 week old mouse brain was removed. B) A 10-12 week old mouse brain was used as a sham control. C) The brain of a 10-12 week old mouse was removed 24 hr after a moderate TBI using the CCI model. D) The brain of a 10-12 week old mouse was removed 6 weeks after a moderate TBI using the CCI model. An indention in the brain tissue is evident at the site of impact. E) Nissl staining was performed on a sham control 10-12 week old mouse brain to show the normal histology. F) Nissl staining was performed on a 10-12 week old mouse brain that had received a moderate TBI using the CCI model. A cavity is visible extending deep into the cortex. Click here to view larger image.
Discussion
The most critical steps for successfully generating consistent TBIs using an electronic magnet impact system to cause a CCI are: 1) stably fixing the mouse head in the stereotactic frame; 2) generating the same size of bone window between mice and removing the bone without damaging the dura under it during craniectomy; 3) correctly positioning the impact tip in the center of the open area and establishing the zero point before impacting.
A mouse head must be fixed in the stereotactic frame very tightly before impact. Loose fixation will generate large variations in injury level. To ensure fixation is stable, use forceps to apply pressure on the skull once the mouse head is fixed in the stereotactic frame and confirm that the skull remains immobile. Take precautionary measures to avoid infection of the exposed skull. After exposing the skull, move to the most difficult part of the controlled cortical impact surgery: drilling a circular cut into the skull without damaging the dura mater underneath.
The optimum size of drill bit tip is 0.5 mm. The suitable speed is 10,000-20,000 rpm; however, using a higher speed can facilitate drilling a better bone window. Drilling will generate heat that can damage the brain, particularly in young mice whose bone and dura are attached. To prevent damaging the brain, apply saline to the skull surface while drilling. Applying saline will make it necessary to use a dissecting microscope in order to see the drilled circle. When mice mature, a space develops between the bone and dura, thus the effect of heat generated by drilling would produce a minimal impact.
While drilling, move the drill bit slowly and constantly along a circular path. Otherwise, the bit may move off the line or go directly through the bone and damage the brain tissue. Gently touch the bone window using forceps to inspect the drilling. If the skull bone easily moves up and down, move the fine tip of the forceps into the space between the bone and the dura. Then lift up to remove the whole bone, thus creating the window. Do not lift bone from one side to another, because doing so may hurt the brain tissue. Making identically sized bone windows is critical for generating consistent brain injuries. Due to intracranial pressure, the brain will bulge out of the open area once the bone is removed, thus causing minor brain deformation. If the bone window size varies, the level of brain deformation will be different, being similar to the brain surface curve in the impact site. The bone was not repositioned over the impact site following surgery since it was smaller than the bone window. Doing so would cause the bone to adhere directly to the brain tissue. Applying glue to seal the bone window might result in increased intracranial pressure. Examining an impact site 3 weeks after a CCI surgery a new membrane was found covering the brain tissue with no brain tissue growth outside of the impact site. No known histological changes occur due to a lack of bone covering.
The electronic magnet impact system is exceedingly stable and can precisely control the velocity and deformation depth. However, due to the design, the coil connected to the impact tip can shift while striking and result in a shift of impact site. This is the major cause of inconsistent injuries, barring no other complications. Despite the possibility for shifting the impact site, the controlled cortical impact method remains more precise and easier to control compared to the fluid percussion and weight drop methods, thus making CCI a preferred method for investigating the short-term and long-term effects of TBIs, as well as possible therapeutic treatments. Although important for TBI research, removing a portion of the skull prior to impact limits the clinical relevance of the CCI model.
The protocol above describes the procedure to produce a moderate TBI in a mouse. The impact site may range from 1-6 mm in diameter depending on the animal and severity of injury desired. Although the protocol stated the impact tip was 3 mm in diameter, a 4 mm in diameter craniectomy was performed in order to prevent accidentally striking bone. In addition to altering the size of the impact site, the speed of the impactor and depth of deformation may be adjusted to reach the severity needed.
Disclosures
The authors have nothing to disclose.
Acknowledgements
This work was supported by funding from the Indiana Spinal Cord & Brain Injury Research Grants (SCBI 200-12), the Ralph W. and Grace M. Showalter Research Award, Indiana University Biological Research Grant, NIH grants RR025761 and 1R21NS072631-01A.
Materials
| Povidone-iodine 7.5% | Purdue product L.P. | Surgical scrub | |
| Cotton tipped applicators | Henry Schein | 100-6015 | Remove blood and debris |
| scissor | Fine Science Tools | 14084-08 | Surgery |
| forcept | Fine Science Tools | 11293-00 | Surgery |
| hemostat | Fine Science Tools | 13021-12 | Surgery |
| Rechargeable Cordless Micro Drill | Stoelting | 58610 | Combine with Burrs for generating the bone window |
| Burrs for Micro Drill | Fine Science Tools | 19007-05 | |
| Suture monofilament | Ethicon | G697 | Suture |
| tert-Amyl alcohol | Sigma | 152463-250ML | Making 2.5% Avertin |
| 2,2,2-Tribromoethanol | Sigma | T48402-25G | Making 2.5% Avertin |
References
- Menon, D. K., Schwab, K., et al. Position statement: definition of traumatic brain injury. Arch Phys Med Rehabil. 91 (11), 1637-1640 (2010).
- Lighthall, J. W., Dixon, C. E., et al. Experimental models of brain injury. J Neurotrauma. 6 (2), 83-97 (1989).
- Dixon, C. E., Clfton, G. L., et al. A controlled cortical impact model of traumatic brain injury in the rat. J Neurosci Methods. 39 (3), 253-262 (1991).
- Scheff, S. W., Baldwin, S. A., et al. Morris water maze deficits in rats following traumatic brain injury: lateral controlled cortical impact. J Neurotrauma. 14 (9), 615-627 (1997).
- Smith, D. H., Soares, H. D., et al. A model of parasagittal controlled cortical impact in the mouse: cognitive and histopathologic effects. J Neurotrauma. 12 (2), 169-178 (1995).
- Hannay, H. J., Feldman, Z., et al. Validation of a controlled cortical impact model of head injury in mice. J Neurotrauma. 16 (11), 1103-1114 (1999).
- Natale, J. E., Ahmed, F., et al. Gene expression profile changes are commonly modulated across models and species after traumatic brain injury. J Neurotrauma. 20 (10), 907-927 (2003).
- Anderson, R. W., Brown, C. J., et al. Impact mechanics and axonal injury in a sheep model. J Neurotrauma. 20 (10), 961-974 (2003).
- Lighthall, J. W. Controlled cortical impact: a new experimental brain injury model. J Neurotrauma. 5 (1), 1-15 (1988).
- Chen, S., Pickard, J. D., et al. Time course of cellular pathology after controlled cortical impact injury. Exp Neurol. 182 (1), 87-102 (2003).
- Long, J. B., Bentley, T. L., et al. Blast overpressure in rats: recreating a battlefield injury in the laboratory. J Neurotrauma. 26 (6), 827-840 (2009).
- Clark, R. S., Schiding, J. K., et al. Neutrophil accumulation after traumatic brain injury in rats: comparison of weight drop and controlled cortical impact models. J Neurotrauma. 11 (5), 499-506 (1994).
- Werner, C., Engelhard, K. Pathophysiology of traumatic brain injury. Br J Anaesth. 99 (1), 4-9 (2007).
- Colicos, M. A., Dixon, C. E., et al. Delayed, selective neuronal death following experimental cortical impact injury in rats: possible role in memory deficits. Brain Res. 739 (1-2), 111-119 (1996).
- Raghavendra Rao, V. L., Dogan, A., et al. Traumatic brain injury leads to increased expression of peripheral-type benzodiazepine receptors, neuronal death, and activation of astrocytes and microglia in rat thalamus. Exp Neurol. 161 (1), 102-114 (2000).
- Gao, X., Chen, J. Moderate traumatic brain injury promotes neural precursor proliferation without increasing neurogenesis in the adult hippocampus. Exp Neurol. 239, 38-48 (2013).

