Mapeo cuantitativo de la deformación de un aneurisma de la aorta abdominal
English
Share
Overview
Fuente: Hannah L. Cebull1, Arvin H. Soepriatna1, John J. Boyle2 y Craig J. Goergen1
1 Weldon School of Biomedical Engineering, Universidad Purdue, West Lafayette, Indiana
2 Ingeniería Mecánica y Ciencia de los Materiales, Universidad de Washington en St. Louis, St Louis, Missouri
El comportamiento mecánico de los tejidos blandos, como los vasos sanguíneos, la piel, los tendones y otros órganos, está fuertemente influenciado por su composición de elastina y colágeno, que proporcionan elasticidad y fuerza. La orientación de la fibra de estas proteínas depende del tipo de tejido blando y puede variar desde una sola dirección preferida hasta intrincadas redes malladas, que pueden alterarse en el tejido enfermo. Por lo tanto, los tejidos blandos a menudo se comportan anisotrópicamente a nivel celular y de órganos, creando una necesidad de caracterización tridimensional. Desarrollar un método para estimar de forma fiable los campos de deformación unitaria dentro de tejidos o estructuras biológicas complejas es importante para caracterizar y comprender mecánicamente la enfermedad. La tensión representa cómo el tejido blando se deforma relativamente con el tiempo, y se puede describir matemáticamente a través de varias estimaciones.
La adquisición de datos de imagen a lo largo del tiempo permite estimar la deformación y la tensión. Sin embargo, todas las modalidades de imágenes médicas contienen cierta cantidad de ruido, lo que aumenta la dificultad de estimar con precisión la tensión in vivo. La técnica descrita aquí supera con éxito estos problemas mediante el uso de un método de estimación de deformación directa (DDE) para calcular campos de deformación unitaria 3D que varían espacialmente a partir de datos de imagen volumétrica.
Los métodos actuales de estimación de deformación unitaria incluyen correlación de imágenes digitales (DIC) y correlación de volumen digital. Desafortunadamente, DIC sólo puede estimar con precisión la tensión de un plano 2D, limitando severamente la aplicación de este método. Si bien son útiles, los métodos 2D como DIC tienen dificultadpara cuantificar la tensión en regiones que se someten a deformación 3D. Esto se debe a que el movimiento fuera del plano crea errores de deformación. La correlación de volumen digital es un método más aplicable que divide los datos de volumen inicialen regiones y encuentra la región más similar del volumen deformado, lo que reduce el error fuera del plano. Sin embargo, este método demuestra ser sensible al ruido y requiere suposiciones sobre las propiedades mecánicas del material.
La técnica que se muestra aquí elimina estos problemas mediante el uso de un método DDE, por lo que es muy útil en el análisis de datos de imágenes médicas. Además, es robusta a cepa alta o localizada. Aquí describimos la adquisición de datos de ultrasonido 4D cerrados y volumétricos, su conversión en un formato analizable y el uso de un código Matlab personalizado para estimar la deformación 3D y las cepas de Green-Lagrange correspondientes, un parámetro que describe mejor las grandes deformaciones. El tensor de cepa Green-Lagrange se implementa en muchos métodos de estimación de deformación unitaria 3D porque permite calcular F a partir de un ajuste de mínimos cuadrados (LSF) de los desplazamientos. La ecuación siguiente representa el tensor de cepa Green-Lagrange, E, donde F y I representan el gradiente de deformación y el tensor de identidad de segundo orden, respectivamente.
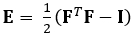 (1)
(1)
Principles
Procedure
Results
Using the procedure described above, 4D ultrasound of an angiotensin II-induced suprarenal dissecting abdominal aortic aneurysm (AAA) of a mouse was acquired. Multiple short-axis EKV video loops were acquired along the aorta and combined to create 4D data, as shown in Figure 1. This data was then converted into a MAT file using a custom code, which was then analyzed in a 3D strain calculation code using a warping function. After optimizing the parameters of the code for a specific data set, a representative, long-axis view with corresponding strain values was produced as well as a 3D slice visualization plot with an overlaid strain color map (Figure 2). This DDE technique and strain data highlight the heterogeneous spatial variations in strain, particularly when a thrombus is present. These results can then be correlated with vessel structure to determine the relationship between in vivo deformation and aneurysm composition.

Figure 1: ECG-gated kilohertz visualization (EKV) loops of the aorta are acquired from manually inputted starting and ending locations, following a step size of 0.2 mm.

Figure 2: 4D high frequency ultrasound data of a murine dissecting abdominal aortic aneurysm represented at systole (A) with principal strain fields estimated and overlaid (B) (Scalebar = 5 mm). Long- and short-axis views representing both aneurysmal and healthy regions corresponding principal strain over one cardiac cycle (systole: t= 0.4) (C, D). These data show relatively high strain levels in healthy regions and reduced strain values within the dissecting aneurysm.
Applications and Summary
Localized in vivo mechanical characterization is an important part of understanding the growth and remodeling of biological tissues. Compared to existing approaches, the strain quantification procedure described here uses an improved method of accurately calculating 3D strain through optimally warping the undeformed image before cross-correlation. This method does not use any material assumptions in determining strains within tissue volumes. Unfortunately, the strain estimation is reliable only down to a kernel size of 15x15x15 voxels when using ultrasound data, suggesting that this DDE approach may not detect subtle features within a strain field. Despite this limitation, it remains an important tool for investigating mechanical responses, diagnosing pathology, and improving disease models.
Many areas of research beyond aortic aneurysms can benefit from this strain measurement tool. Cardiac strain can also be easily quantified using this method. Because the myocardium undergoes 3D deformation during the cardiac cycle, quantifying strain in three dimensions is integral to reliably characterizing the dynamics of this tissue. Reliable strain data is especially important when tracking disease progression in animal models.
3D strain analysis can also be applied to intestinal ultrasound imaging. Mechanical characterization of intestinal tissue is most commonly conducted in vitro. However, this is not always a true representation of the actual behavior of the intestines in vivo because of effects from surrounding structures. As an example of clinically translating this approach, calculating the strain from images of intestinal fibrosis due to abnormal luminal pressure could provide early detection of problematic areas that require surgical intervention.
Beyond the larger scale applications, this method can also be applied to the cellular level by using higher resolution imaging techniques, such as confocal microscopy. Characterizing the extracellular matrix is important for understanding how cells communicate. Much research has been conducted on the biochemical characterization, but understanding how communication can be conducted through mechanical responses requires an understanding of deformation and strain. Bulk strain is not beneficial because there is no way to determine the origin of the deformation change. Applying a high-resolution DDE approach could directly reveal how the extracellular matrix responds to mechanical changes.
ACKNOWLEDGEMENTS
We would like to acknowledge John Boyle, Guy Genin, and Stavros Thomopoulos for the contribution of the DDE custom Matlab code capable of directly estimating Lagrange-Green strain.
Transcript
Three-dimensional strain imaging is used to estimate deformation of soft tissues over time and understand disease. The mechanical behavior of soft tissues, such as skin, blood vessels, tendons, and other organs, is strongly influenced by their extracellular composition, which can become altered from aging and disease. Within complex biological tissues, it is important to characterize these changes, which can significantly affect the mechanical and functional properties of an organ.
Quantitative strain mapping uses volumetric image data and a direct deformation estimation method to calculate the spatially varying three-dimensional strain fields. This video will illustrate the principles of strain mapping, demonstrate how quantitative strain mapping is used to estimate strain fields within complex biological tissues, and discuss other applications.
Biological tissues are strongly influenced by the composition and orientation of elastin and collagen. The protein elastin is a highly elastic component of tissues that continually stretch and contract, such as blood vessels and the lungs. Collagen is the most abundant protein in the body, and is assembled from individual triple-helical polymers that are bundled into larger fibers that provide structural integrity to tissues ranging from skin to bones.
The orientation of these proteins ranges from aligned fibers to fibrous mesh networks, which affects the mechanical properties of the tissue. Strain is a measure of the relative deformation of soft tissues over time, and can be used to visualize injury and disease. It is described and mapped using mathematical estimations.
To map strain in complex organs, such as the heart, four-dimensional ultrasound data, which provides high resolution, spatial, and temporal information, can be used. Then the direct deformation estimation method, or DDE, is applied to the data. A code is used to estimate the 3D deformation and corresponding Green-Lagrange strains using the following equation.
The Green-Lagrange strain tensor depends on the deformation gradient tensor and the second order identity tensor. Deformation gradient tensors are traditionally estimated from displacement fields. In the DDE method, a warping function is optimized to be directly analogous to the deformation tensor. The warping function depends on both spatial position and the warping parameter. The calculation of deformation is directly incorporated into the warping function. The first nine elements represent the deformation gradient tensor.
This method is used to estimate both large and localized deformations in soft tissues. Now that we understand the principles of strain mapping, let’s now see how strain mapping is performed to detect aortic aneurysms in mice.
To begin setup, open the Vivo 2100 software and connect the laptop to the ultrasound system. Make sure the physiological monitoring unit is on to measure heart rate and temperature. Then initialize the 3D motor stage.
Install the ultrasound transducer and ensure that all proper connections are made. Next, anesthetize the animal that will be imaged using 3% isoflurane in a knock-down chamber. Once the mouse is anesthetized, move it to the heated stage and secure a nose cone to deliver 1-2% isoflurane. Apply ophthalmic ointment to the eyes and secure the paws to the stage electrodes to monitor the animal’s respiration and heart rate. Then insert a rectal temperature probe. Apply depilatory cream to remove hair from the area of interest, and then apply a generous amount of warm ultrasound gel to the depilated area.
To start the image acquisition, first, open the imaging window and select B mode. Then lower the transducer onto the animal and use the x and y-axis knobs on the stage to locate the area of interest. Monitor the respiratory rate to make sure it does not decrease substantially. Position the transducer in the middle of the region of interest. Then approximate the distance required to cover the entire region of interest.
Enter these dimensions in the MATLAB code and choose a step size of 0.08 millimeters. Make sure the animal’s heart and respiratory rates are stable, then run the MATLAB code.
After image acquisition, export the data as raw XML files and convert them into MAT files. Make sure to input the number of frames, step size, and output resolution. Then re-sample the matrix in through-plane.
Import the new MAT file into the 3D strain analysis code. It may be necessary to rescale the file to reduce the computation time. Then, input the region to be analyzed. Approximate the number of pixels in a two-dimensional slice of the tracked feature and select the mesh template either as a simple box or manually chosen polygons. Choose the optimal pixel number for the mesh size. Compute the Jacobians and the gradients. Repeat for each region. Then apply the warping function.
Next, using Cartesian deformations calculated from DDE, determine the eigenvalues and eigenvectors of the deformation. Then, select the slices that you want to plot strain values for by scrolling through the long axis, sort axis, and coronal axis views.
Press Select Manifold for Analysis. Then use the cursor to place markers along the aortic wall, including the thrombus, aneurysm, and healthy parts of the aorta. Repeat for all views. Finally, use color mapping to plot the results of the strain field over the region of interest.
Let us have a close look at the example of an angiotensin II-induced suprarenal dissecting abdominal aortic aneurysm acquired from a mouse. First, multiple short axis ECG-gated kilohertz visualization loops are obtained at a given step size along the aorta and combined to create 4D data.
After performing 3D strain calculation using an optimized warping function, the 3D slice visualization plot of the infrarenal aorta is obtained. The color map of principal green strain is overlaid to highlight regions of heterogeneous aortic wall strain. In addition, long axis and short axis views reveal heterogeneous spatial variations in strain, particularly when a thrombus is present.
Corresponding strain plots show higher strain values in healthy regions of the aorta in the long axis, while the aneurysmal region shows decreased strain in the short axis.
Accurate quantitative strain visualization using direct deformation estimation is a useful tool used in various biomedical applications.
For instance, cardiac strain can be quantified. During the cardiac cycle, the myocardium undergoes 3D deformation. Quantifying strain in three dimensions is integral to reliably characterizing the dynamics of this tissue over time. This is useful in tracking disease progression in animal models.
Another application is in the characterization of intestinal tissue. In vivo imaging of the intestines is challenging because of the effects from surrounding structures. However, calculating strain from images of intestinal fibrosis could be particularly useful to provide early detection of problematic areas that require surgical intervention.
At a much smaller scale, this DDE method is also applied to the cellular level by using higher resolution imaging techniques such as confocal microscopy. It serves, for example, in the characterization of extracellular matrix to understand how cells communicate under mechanical changes.
You’ve just watched JoVE’s introduction to quantitative strain visualization. You should now understand how to measure three-dimensional strain in biological tissues and how that is used in early disease detection. Thanks for watching!
