16.6:
Calcoli di titolazione: acido forte - base forte
16.6:
Calcoli di titolazione: acido forte - base forte
Calcolo del pH per le soluzioni di titolazione: acido forte / base forte
Viene effettuata una titolazione per 25,00 mL di 0,100 M HCl (acido forte) con 0,100 M di una forte base NaOH. Il pH a diversi volumi di soluzione di base aggiunta può essere calcolato come segue:
(a) Volume titolazione = 0 mL. Il pH della soluzione è dovuto alla ionizzazione acida dell’HCl. Poiché si tratta di un acido forte, la ionizzazione è completa e la molarità degli ioni di idronio è di 0,100 M. Il pH della soluzione è quindi:

(b) Volume di titolazione = 12,50 mL. Poiché il campione acido e il titolazione di base sono sia monoprotici che ugualmente concentrati, questa aggiunta di titolazione comporta meno di una quantità stechiometrica di base, e quindi viene completamente consumata per reazione con l’acido in eccesso nel campione. La concentrazione di acido rimanente viene calcolata sottraendo la quantità consumata dalla quantità iniziale e quindi dividendo per il volume della soluzione:
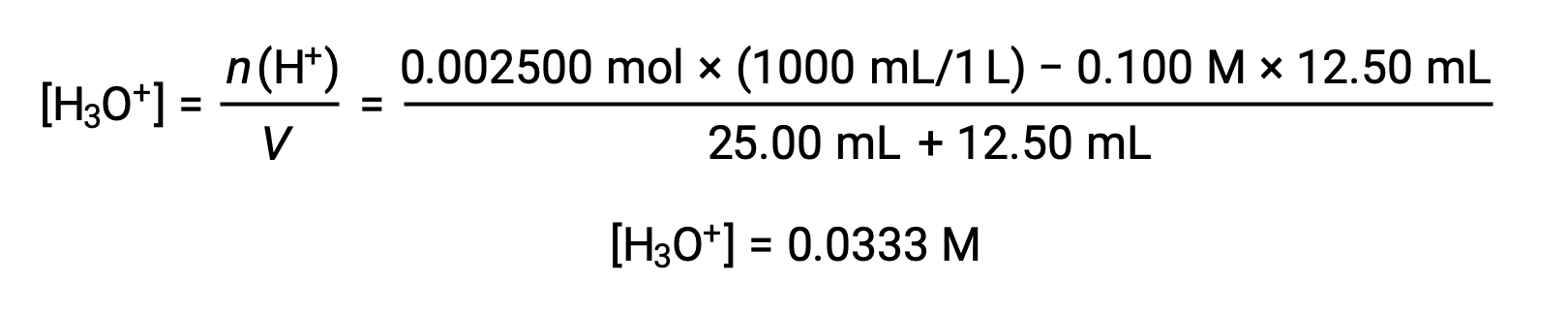
(e) Volume di titolazione = 25,00 mL. Questa aggiunta titolazione comporta una quantità stechiometrica di base (il punto di equivalenza), e quindi solo i prodotti della reazione di neutralizzazione sono in soluzione (acqua e NaCl). Né la catione né l’anione di questo sale subiscono ionizzazione acido-base; l’unico processo che genera ioni di idronio è l’autoprotolisi dell’acqua. La soluzione è neutra, con un pH = 7,00.
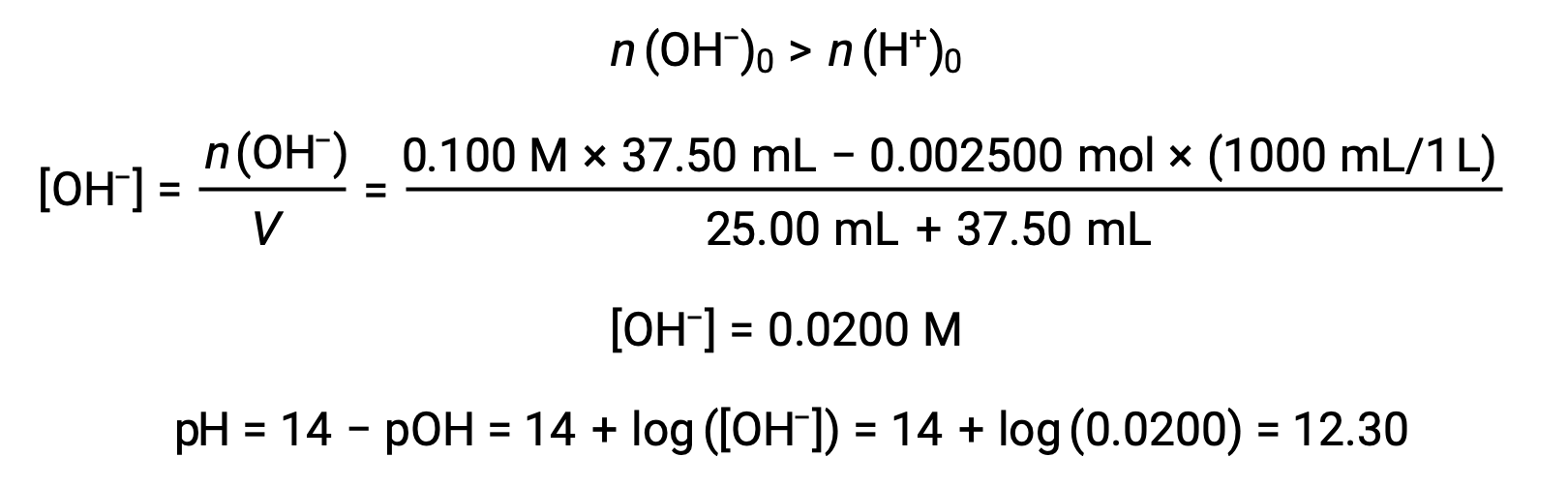
(d) Volume del titolazione = 37,50 mL. Ciò comporta l’aggiunta di titolazione superiore al punto di equivalenza. Il pH della soluzione viene quindi calcolato utilizzando la concentrazione di ioni idrossido:
Questo testo è adattato da Openstax, Chimica 2e, Sezione 14.7: Titolazioni acido-base.
